脾窦岸细胞血管瘤伴地中海贫血一例
2024-05-07杨丹萍王盛锦田大广
杨丹萍,王盛锦,田大广
昆明医科大学第二附属医院,云南 昆明 650101,1.肝胆外科,2.胃肠外科
脾窦岸细胞血管瘤(littoral cell angioma,LCA)是由Falk等最早于1991年报道并命名,是一种临床上罕见的脾脏良性肿瘤[1]。文献报道其起源于脾血窦特殊的窦岸细胞,具有内皮细胞和组织细胞双重分化特征[2]。临床上大多数患者无明显症状,在体检时发现异常,少数可出现左上腹痛、脾功能亢进等表现。本例患者出现肝脏肿大、脾脏肿大、贫血、出血、感染等脾功能亢进的表现。LCA诊断主要依靠组织病理学检查,仅依靠临床表现和影像学表现,很难将其与其他脾脏良性或恶性肿瘤鉴别开来。本例患者LCA伴地中海贫血,尚不清楚二者之间是否有关联,现报道如下。
病例
患者男性,32岁,因“乏力1个月、腹泻7 d”于2021年3月9日入院,5年前体检时发现脾肿大,偶有牙龈出血、鼻出血,无腹痛、腹胀、呕血、便血。查体:腹部平坦,腹部无压痛、反跳痛,脾脏中度肿大。实验室检查:血小板73×109/L,红细胞2.90×1012/L,血红蛋白48 g/L,总蛋白51.0 g/L,白蛋白33.6 g/L。地中海贫血基因检测示CD17和βE突变。影像学检查可见肝脏、脾脏明显肿大,多个脏器受压变形,脾脏血管增粗,见图1。患者入院后红细胞、血小板进一步降低,白细胞升高,肝功能、凝血功能异常,请血液科会诊,行相关检查后诊断为脾肿大、肝肿大、地中海贫血,给予输血、输液等对症支持治疗。但因肿大的脾脏压迫胰腺和肾脏以及脾脏占位性质未明,于2021年3月10日行开腹全脾切除术。术后病理:肿瘤由大小不一,互相吻合或网的血管腔组成,表面覆有单层内皮细胞,见图2。免疫组化:CD21(+),CD8(+),SMA(+),CD31(血管+),CD3(+),CD20(+),Ki-67(20%),VIM(+),CD34(+)。术后诊断为LCA伴髓外造血。患者术后9 d顺利出院,术后1个月影像学检查未见明显异常,随访至2023年11月,恢复良好。
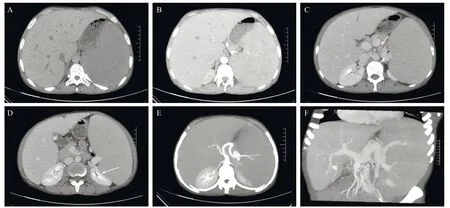
图1 LCA伴地中海贫血患者的上腹部CT平扫+增强扫描

图2 LCA伴地中海贫血患者的脾脏大体标本和病理图片
讨论
LCA的病因尚不清楚,但最近有研究认为,硫唑嘌呤等免疫抑制剂或生物活性TNF-α引起的免疫异常可能与LCA的发生有关[3-4]。各年龄段均可发生LCA,以50岁居多,男女比例在5∶3左右[5]。目前研究认为,LCA是一种良性肿瘤,原发于脾脏,但不排除潜在恶性的可能性,且有研究表明,LCA患者可并发恶性肿瘤如肝癌、胰腺癌、结直肠癌、肾癌等[2]。本例患者LCA与地中海贫血并发,尚不清楚二者之间的联系。
影像学检查对LCA的诊断具有重要价值,大多数LCA以脾弥漫性多发性结节状病灶为特征,极少数表现为孤立性单发结节。CT在鉴别脾脏肿瘤病变性质、血供、与周围器官的联系等方面具有较大的优势,是目前最有价值的影像学诊断方法之一。本例患者的CT示肝脏、脾脏明显肿大,胰尾部受压移位,左肾受压变形。增强扫描肝脏未见异常强化灶,脾脏内可见多发类圆形低密度影,未见强化。脾动脉明显增粗迂曲,门静脉主干增宽、脾静脉增粗迂曲。LCA的MRI成像取决于窦岸细胞内吞噬沉积的含铁血黄素,表现为T1 加权成像显示低信号,T2加权成像强度不定,诊断不具有特异性。本例患者MRI示脾脏明显增大,其内见多发小斑片状长T1、稍长及短T2 信号影;肝脏、脾脏明显增大,肝脏、胰腺、脾脏信号异常,考虑铁沉积,脾脏多发小结节。
组织病理学检查是目前诊断LCA最有价值的检查,也是确诊的主要手段。大体标本见脾体积增大,切面灰红、质软,有单个或多个结节。组织学特征是病变由类似脾血窦的吻合血管组成,通常伴有乳头状或囊性扩张,其中有两种细胞类型,两种细胞均缺乏异型性,且免疫组化表现不同。一类与正常脾脏窦岸细胞形态非常相似,排列在乳头状扩张的表面,体积较小,具有内皮细胞特性,免疫组化示细胞CD31(+)、FVⅢ(+)、CD34(-);另一类组织细胞体积更大,常与管腔分离,免疫组化示CD68(+)。在光镜下,肿瘤组织位于边界清晰的灰质中,肿瘤内部见相通的窦道,周围是纤维细胞基质,窦道表面覆有单层内皮样细胞。
LCA临床上需要与脾血管瘤、脾错构瘤、血管肉瘤、脾窦岸细胞血管肉瘤等进行鉴别,仅靠影像学难以区分,尚需病理组织学检查结果。脾血管瘤是最常见的脾脏良性肿瘤,可分为毛细血管瘤及海绵状血管瘤两种类型,常呈膨隆或裂隙状,内层为平坦的内皮细胞,在各发育时期的管腔中易形成微血栓,常有内皮分子标志物CD31、CD34 及FVⅢRAg等。其影像学特征为“快进慢出的向心性强化”,也就是在动脉期,从瘤缘到中心不均匀强化,再到门脉期和延缓期进一步增强的向心强化[6-8]。血管肉瘤大体病理可发现在脾脏实质中有大量的紫红色小结节,常伴有出血、坏死和囊性变[9],表现为迷宫状血管腔,内衬为多形性和上皮性纺锤形结构,内皮细胞异常,常表现为核分裂,肿瘤细胞沿血管壁呈巢状或乳头状发展。硬化性血管瘤样结节转化是一种特有的脾脏红髓非肿瘤性病变,树枝状的纤维分割对诊断具有一定的价值。CD34、CD31和CD8联合应用能鉴别病灶内三种不同的血管,其三种血管成分及多个模糊结节是鉴别本病的重要依据[10]。窦岸细胞血管肉瘤病理组织见血管吻合,内皮细胞呈片状增生,常伴出血坏死及核分裂。与LCA相比,窦岸细胞血管肉瘤中CD8、CD34呈阳性,而CD21、FVⅢ RAg呈阴性,Ki-67增殖指数更高[5]。脾错构瘤是一种罕见的良性血管增生性病变,由无组织的窦状通道组成,内衬有丰满或扁平的内皮细胞,其特征在于衬里细胞的CD8阳性的免疫表型。
目前LCA的治疗方法以外科手术为主,可采用腹腔镜/开腹全脾切除。对于病灶范围较小、单个病灶较小的单一病灶,在全面评估后,可施行脾部分切除术。近年来,腹腔镜下脾切除已成为LCA的主要治疗方法。本例患者因“乏力1 个月、腹泻7 d”入院,影像学检查提示巨脾且多个脏器受压变形,行开腹全脾切除术,术后复查受压迫脏器已无明显异常;患者入院时血细胞分析示重度贫血,地中海贫血基因检测示CD17和βE突变,住院期间严密监测血象的同时给予输血治疗,但患者血红蛋白等指标升高并不明显,行脾脏切除术后患者血红蛋白短期内快速恢复。术后7 d复查血常规,提示红细胞较前升高、血红蛋白指标恢复至轻度贫血状态,凝血功能指标较前好转,患者术后恢复良好。综合既往文献报道的病例分析,LCA患者的血象可表现为正常、白细胞和血红蛋白降低或三系减低等多种形式;但血红蛋白异常的患者仅报道了相关检验指标,忽略了患者的贫血类型、贫血程度,也未进一步探讨贫血类型是否与该疾病相关。LCA患者多种血象表现是否可以反映疾病进程,有待后续更多研究论证。
