SMILE与FS-LASIK对纠正高度近视患者视力的效果分析
2024-05-06贾刘才侯真真
贾刘才,侯真真
(济源尖峰眼科医院 眼科,河南 济源 459000)
据相关报道显示,高度近视可引发严重视功能受损,我国近年来高度近视的发生率居高不下,且多发于青少年[1]。目前,多数高度近视患者通过屈光手术来对视力进行矫正,由于在眼球全部屈光系统中角膜屈光力的占比较高,角膜屈光手术在临床上被广泛应用,飞秒激光的出现标志着角膜屈光手术的进步[2]。飞秒激光小切口角膜基质透镜取出术(SMILE)、飞秒激光辅助准分子激光角膜原位磨镶术(FS-LASIK)属于目前临床上应用较为广泛的两种术式,其中FS-LASIK已经取代了机械刀制瓣的LASIK手术,其临床疗效已获得认可[3]。SMILE属于一种较为新型的角膜屈光矫正手术,该手术主要是指采用飞秒激光做一个基质透镜,之后再将透镜取出,可使角膜相关并发症的发生率下降[4]。鉴于此,本研究回顾性分析了2020年10月至2023年10月济源尖峰眼科医院屈光科矫正的120例(230眼)高度近视患者的临床资料,将其按照手术方式的不同分为两组,重点探讨了SMILE与FS-LASIK应用于高度近视患者中的临床效果,以期为临床治疗提供参考。
1 资料与方法
1.1 一般资料
对2020年10月至2023年10月济源尖峰眼科医院屈光科矫正的120例(230眼)高度近视患者的临床资料进行回顾性分析,按照手术方法的不同将所有患者分为SMILE组60例(117眼)和FS-LASIK组60例(113眼)。其中SMILE组患者中男37例,女23例;年龄18~41岁,平均(25.02±5.14)岁;等效球镜-6.20~-9.50 D,平均(-7.45±0.75)D;左眼59只,右眼58只;角膜中央厚度510~605 μm,平均(548.21±24.67)μm。FS-LASIK组患者中男38例,女22例;年龄18~40岁,平均(25.95±5.20)岁;等效球镜-6.25~-10.75 D,平均(-7.70±0.80)D;左眼57只,右眼56只;角膜中央厚度505~607 μm,平均(540.35±24.75)μm。将两组患者性别、年龄、等效球镜等进行比较,差异无统计学意义(P>0.05),具有可比性。
纳入标准:符合角膜屈光手术适应证;无手术禁忌证;拟行SMILE或FS-LASIK手术者等。排除标准:伴有眼部活动炎症者;既往有精神病史者;伴有影响术后恢复的眼部疾患者。
1.2 手术方法
两组患者均在术前对裸眼视力、最佳矫正视力等进行检查,术前采用0.9%氯化钠溶液对结膜囊进行冲洗,对眼部及周围皮肤常规消毒,并进行表面麻醉。SMILE组行SMILE治疗,录入术眼手术数据,设置合适的参数包括能量、角膜帽厚度、透镜直径等,表面麻醉后开睑器撑开术眼,告知患者盯住上方固视灯,定位准确后启动负压将眼球吸引固定,采用飞秒激光对角膜基质按照顺序进行扫描,结束后,分离透镜的前表面、后表面,将角膜基质透镜取出,冲洗角膜微切口,术后第2天采用0.1%氟米龙滴眼液、0.5%左氧氟沙星滴眼液、0.1%玻璃酸钠滴眼液滴眼。FS-LASIK组患者行FS-LASIK治疗,术前进行常规消毒及表面麻醉,录入术眼手术数据,在飞秒机器下,开睑器撑开术眼,告知患者盯住上方固视灯,定位准确后启动负压将眼球吸引固定,采用飞秒激光对角膜瓣进行扫描制作,移动治疗床至准分子激光设备下,在显微镜观察下,分离角膜瓣,精准对位启动眼球追踪定位系统,采用准分子激光对角膜基质层进行切削,将残留碎屑冲洗后将角膜瓣复位。
1.3 观察指标
①将两组患者术前、术后1周、1个月、3个月、6个月裸眼视力(LogMAR)进行对比,采用国际标准视力表对两组患者进行测量,将结果转化为LogMAR视力。②将两组患者术前、术后1周、1个月、3个月、6个月客观视觉质量指标进行对比,指标有客观散射指数值(OSI)、调制传递函数截止频率(MTF cut-off值)及斯特列尔比值(SR),每个指标均于检测3次后取平均值。③对比两组患者术前、术后1个月、3个月泪膜稳定性,包括泪膜破裂时间(BUT)、泪液分泌功能(SIt)。④将两组患者术后并发症发生情况进行对比,包括干眼症、感染、眼压升高、单眼复视等。
1.4 统计学方法
应用SPSS 24.0软件行统计学分析,计量资料以均数±标准差()表示,采用t检验,多时间点计量资料比较采用重复测量方差分析;计数资料以百分率(%)表示,采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者LogMAR值比较
术后1周、1个月、3个月、6个月两组患者LogMAR值均比术前下降,且SMILE组患者术后1周、1个月LogMAR值比FS-LASIK组低,差异有统计学意义(均P<0.05),见表1。
表1 两组患者LogMAR值比较 ()

表1 两组患者LogMAR值比较 ()
注:1)与术前比较,P<0.05;2)与术后1周比较,P<0.05;3)与术后1个月比较,P<0.05。
2.2 两组患者客观视觉质量指标比较
术后1周、1个月两组患者OSI均比术前高,且SMILE组比FS-LASIK组低;术后1周、1个月两组患者MTF cut-off值均比术前下降(均P<0.05),但组间比较,差异均无统计学意义(均P>0.05),见表2。
表2 两组患者客观视觉质量指标比较 ()

表2 两组患者客观视觉质量指标比较 ()
注:1)与术前比较,P<0.05;2)与术后1周比较,P<0.05;3)与术后1个月比较,P<0.05。
2.3 两组患者泪膜稳定性指标比较
术后1个月、3个月两组患者BUT、SIt均呈先下降后上升趋势,且术后3个月SMILE组患者BUT、SIt比FS-LASIK组高,差异有统计学意义(均P<0.05),见表3。
表3 两组患者泪膜稳定性指标比较 ()

表3 两组患者泪膜稳定性指标比较 ()
注:1)与术前比较,P<0.05,2)与术后1个月比较,P<0.05。
2.4 两组患者并发症发生情况比较
SMILE组患者并发症总发生率比FS-LASIK组低,差异有统计学意义(χ2=10.198,P=0.001),见表4。
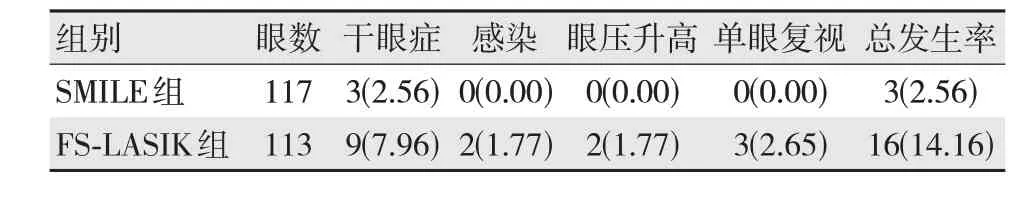
表4 两组患者并发症发生情况比较 [n(%)]
3 讨论
临床上对于高度近视的发病机制尚不明确,临床多认为其发生原因与遗传以及用眼习惯、饮食等相关[5]。目前,越来越多的高度近视患者选择通过屈光手术来对视力进行矫正,而如何选择合适的手术方式是临床重点关注的内容。
飞秒激光在角膜屈光手术中应用可迅速对角膜组织进行分离,准确切割,且可防止对周围正常组织造成损伤[6]。随着飞秒激光被广泛应用,SMILE与FS-LASIK也越来越受临床医生和高度近视患者的青睐。FS-LASIK指的是运用飞秒激光对角膜瓣进行制作,并对角膜组织切削,可有效提升手术的精准性,同时可减少相关并发症的发生[7]。SMILE则属于近年来新发展起来的一种手术方式,该手术主要是指运用飞秒激光将角膜基质进行切割,并做一个基质透镜,采用微创的方式再将其取出,从而使角膜的屈光力下降,该手术整个过程由飞秒激光完成且不需要做角膜瓣,充分体现了微创的特点[8-9]。本研究中,术后1周、1个月、3个月、6个月两组患者LogMAR值均比术前下降,且SMILE组患者术后1周、1个月LogMAR值比FS-LASIK组低,表明高度近视患者采用两种手术方式均可有助于视力的恢复,而SMILE组患者的视力恢复效果比FS-LASIK组好,这一研究结果与王红霞等[10]的基本相符,这是由于相较于FS-LASIK,高度近视患者采用SMILE治疗可减轻对角膜神经的损伤,从而有助于患者术后视力的恢复[11]。OSI数值越高,则散射程度越严重;MTF cut-off值的数值越大,则表明患者的视觉质量越高;SR指的是在同一瞳孔直径下,有无像差光强度之比,该指标数值的高低与光学质量呈正比[12]。本研究中将两组患者客观视觉质量指标进行对比发现,术后1周、1个月两组患者OSI均比术前高,且SMILE组比FS-LASIK组低;术后1周、1个月两组患者MTF cut-off值均比术前下降,但组间比较均差异无统计学意义,其可能原因在于相较于FS-LASIK,SMILE更有助于高度近视患者视觉质量的提高,这是由于采用该手术方法对患者的神经损伤较轻,患者术后炎性因子水平下降明显[13]。本研究中对两组患者手术前后泪膜稳定性指标进行对比发现,术后1个月、3个月两组患者BUT、SIt均呈先下降后上升趋势,且术后3个月SMILE组患者BUT、SIt比FSLASIK组高,表明相较于FS-LASIK,SMILE应用于高度近视患者中,可有效维持泪膜稳定性,同时减轻干眼症症状,这是由于FS-LASIK操作过程中需制作角膜瓣,而在激光切削的过程中,角膜中的传入性感觉神经纤维被切割,可造成角膜上皮的营养受到影响,最终导致术后干眼的出现[14];而SMILE操作过程中则不需要制作角膜瓣,因此可有效预防患者术后出现干眼,泪膜稳定性更佳[15]。本研究中对两组患者并发症总发生率进行对比得出,SMILE组患者并发症总发生率比FSLASIK组低,证实了相较于FS-LASIK,SMILE应用于高度近视患者中,具有较高的安全性,究其原因在于SMILE在操作过程中保留了较多的角膜神经纤维,对角膜敏感性的影响较小,从而可有效减少术后干眼症的发生[16]。
综上所述,SMILE与FS-LASIK均可有效矫正高度近视患者的视力水平,相较于FS-LASIK,SMILE更有助于患者视力与视觉质量的恢复,且可有效维持泪膜稳定性,降低术后并发症发生率,值得临床推广。
