缝线引导下穿透性Schlemm管成形术联合超声乳化术治疗原发性开角型青光眼
2024-04-28陈丽娜孙露丹
陈丽娜,靳 琳,孙露丹
0 引言
原发性开角型青光眼( primary open angle glaucoma,POAG)是一类以房角开放、多因素眼压增高导致视神经损伤和视野缺损为主要表现的不可逆致盲性眼病,好发于40-80岁人群[1],根据视野MD值(平均缺损)分为早期(>-6 dB),中期(-6--12 dB)和晚期(<-12 dB)。POAG治疗方法有药物、激光和手术。眼压不能控制或者视神经进行性损害,需要手术治疗。传统经典小梁切除术是治疗POAG的主要术式,它是依赖外滤过的青光眼手术,其降眼压效果确切,国外研究报道术后6 mo小梁切除术的条件成功率为72%-91%[2],但随着时间推移成功率会发生降低,术后3 a小梁切除术的成功率为54%-65%[3]。因外滤过手术存在瘢痕化及滤过泡相关并发症等问题,青光眼专家一直追求一种不依赖外滤过,重回自然生理通道的一种手术方式,近些年微创青光眼手术(minimally invasive glaucoma surgery,MIGS)已经成为青光眼手术的重要组成部分。MIGS安全性高、操作相对简单、恢复快、减少术后抗青光眼药物、有效降低眼压的特点[4],根据手术操作入路方式分为内路和外路手术。本研究中缝线引导下穿透性Schlemm管成形术是一种外入路的微创手术,2020年引进我院,本研究对我院就诊的晚期POAG合并白内障患者,根据手术方式不同,分为小梁切除术联合超声乳化人工晶状体植入组和缝线引导下穿透性Schlemm管成形术联合超声乳化人工晶状体植入组,分析比较两种手术方式降眼压、视力、成功率、并发症情况,评估其疗效及安全性。
1 对象和方法
1.1对象回顾性病例对照研究。收集2021-06/2022-06在我院住院手术治疗的晚期POAG合并白内障患者53例53眼,年龄55-88岁,其中26眼行小梁切除术联合超声乳化人工晶状体植入(A组),27眼行缝线引导下穿透性Schlemm管成形术联合超声乳化人工晶状体植入(B组)。纳入标准:(1)符合POAG诊断标准;(2)合并白内障并符合手术指征;(3)MD值<-12 dB;(4)至少完成术后6 mo随访。排除标准:(1)继发性开角型青光眼;(2)眼部有手术和激光病史;(3)合并眼部活动性炎症;(4)严重身心疾病,无法耐受手术。本研究经大连市第三人民医院伦理委员会审核批准,符合《赫尔辛基宣言》准则。所有患者均知情同意并签署知情同意书。
1.2方法
1.2.1术前检查所有患者术前均由同一位技师进行详细的眼部检查:包括最佳矫正视力(BCVA)、非接触眼压计检查IOP、前房角镜、视野、光学相干断层成像(optical coherence tomography, OCT)、扫描激光检眼镜(scanning laser ophthalmoscopy,SLO)、超声生物显微镜(ultrasonic biological microscope,UBM)、裂隙灯、眼底检查。视力检查采用国际标准视力表并转换为最小分辩角的对数(logarithm of minimum angle of resolution,LogMAR)视力进行统计学分析。
1.2.2A组手术方法奥布卡因滴眼液点术眼3次,上方结膜下注射利多卡因0.2 mL,沿角膜缘打开10∶30-1∶00结膜,电凝止血,做以穹窿为基底的4 mm×5 mm的浅层巩膜瓣,厚约1/2巩膜厚度,巩膜瓣下放置丝裂霉素棉片2 mg/mL,2-4 min,约100 mL生理盐水冲洗巩膜瓣下及结膜瓣下。3∶00位角膜缘侧切口,注入黏弹剂,10∶00位做2.8 mm角膜主切口,环形撕囊,水分离和水分层,超声乳化,注吸皮质,植入人工晶状体,注吸黏弹剂,卡巴胆碱缩瞳,水密切口。12∶00位置剪除透明角膜巩膜组织,并做周边虹膜切除,缝合巩膜瓣。10-0的尼龙线缝合结膜瓣。
1.2.3B组手术方法奥布卡因滴眼液点术眼3次,上方结膜下注射利多卡因0.2 mL,沿角膜缘打开10∶30-1∶00结膜,电凝止血,做以穹窿为基底的4 mm×5 mm的浅层巩膜瓣,厚约1/2巩膜厚度,3∶00位角膜缘侧切口,注入黏弹剂,10∶00位做2.8 mm角膜主切口,环形撕囊,水分离和水分层,超声乳化,注吸皮质,植入人工晶状体,注吸黏弹剂,卡巴胆碱缩瞳,水密切口。在浅层巩膜瓣下做约2 mm×2 mm大小深层巩膜瓣,厚度90%,向前剥离至Schlemm管并切除Schlemm管外壁及深层巩膜瓣,5-0聚丙烯缝线头端用烧烙器烧烙一圆头,插入Schlemm管一端,顺着Schlemm管走行360度。从对侧断端穿出。将1根9-0马尼线结扎于缝线圆头后,回退5-0聚丙烯缝线,完全退出后,缝线被留置在Schlemm管内并结扎。然后剪除Schlemm管前部及部分透明角膜巩膜组织,并做周边虹膜切除,紧密缝合巩膜瓣。10-0的尼龙线缝合结膜瓣。
两组患者手术均由同一术者完成。术后均予以醋酸泼尼松龙滴眼液每天4次,加替沙星滴眼液每天4次,普拉洛芬滴眼液点眼每天4次,持续4 wk。
1.2.4随访与观察指标所有患者随访至少6 mo,记录术中及术后并发症。记录A组术后滤过泡维护(按摩、针拨、注射5-FU)的数量。术后1 d和1 wk查BCVA和眼压,术后1、3、6 mo患者行BCVA、眼压、UBM检查。观察指标包括眼压、抗青光眼药物数量、手术成功率及手术并发症。随访期间记录一过性高眼压发生眼数及发生时间。术后眼压超过21 mmHg且在3 mo内眼压可恢复到正常范围定义为术后一过性高眼压[5-6]。
疗效标准:完全成功:末次随访时间未使用任何降眼压药物眼压≤21 mmHg;条件成功:使用降眼压药物的情况下眼压≤21 mmHg;失败:局部使用最大耐受降眼压药水眼压仍高于21 mmHg。
统计学分析:所有数据均使用SPSS 25.0统计学软件进行分析。计数资料采用百分比表示,采用卡方检验或卡方校正公式;等级资料采用Mann-WhitneyU非参数秩和检验。符合正态分布的计量资料以均数±标准差表示, 重复测量数据采用重复测量方差分析,两两时间点比较采用Bonferroni法检验(以P<0.017为差异有统计学意义),两组间比较采用独立样本t检验,手术前后比较采用配对样本t检验;不符合正态分布的计量资料以M(P25,P75)表示,采用独立样本Mann-WhitneyU非参数秩和检验比较。以P<0.05为差异有统计学意义。
2 结果
2.1两组患者术前一般资料比较本研究纳入晚期POAG合并白内障患者53例53眼,根据手术方式分为两组:小梁切除术联合超声乳化人工晶状体植入(A组,26例26眼),缝线引导下穿透性Schlemm管成形术联合超声乳化人工晶状体植入(B组,27例27眼)。两组患者术前性别构成比、年龄、眼压、BCVA、白内障核硬度、局部使用抗青光眼药物数量比较,差异均无统计学意义(P>0.05),见表1。
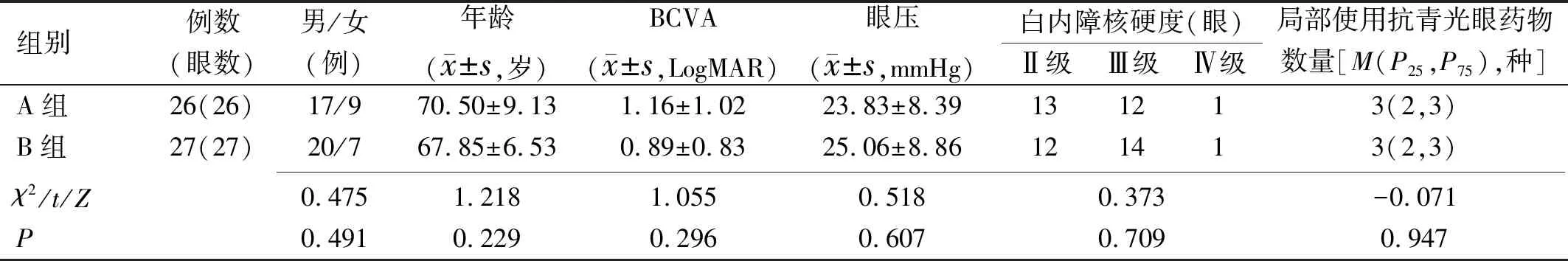
表1 两组患者术前一般资料比较
2.2两组患者手术前后眼压比较两组患者手术前后眼压组间和交互作用比较差异均无统计学意义(F组间=0.237,P组间=0.631;F交互=1.961,P交互=0.133);时间比较差异有统计学意义(F时间=7.375,P时间<0.001)。两组患者术后1 wk,1、3、6 mo眼压较术前均明显降低,差异均有统计学意义(P<0.017)。B组术后3、6 mo眼压均低于术后1 wk,差异均有统计学意义(P<0.017),见表2。

表2 两组患者手术前后眼压比较
2.3两组患者术后各个时间点眼压与术前差值比较两组患者术后各个时间点眼压与术前差值比较组间和时间比较差异均无统计学意义(F组间=0.468,P组间=0.500;F时间=0.22,P时间=0.882),交互作用差异有统计学意义(F交互=4.408,P交互=0.014),见表3。

表3 两组患者术后各个时间点眼压与术前差值比较
2.4两组患者手术前后BCVA比较两组患者手术前后BCVA 比较差异均无统计学意义(P>0.05),两组间患者术后6 mo BCVA比较差异无统计学意义(P>0.05),见表4。

表4 两组患者手术前后BCVA比较
2.5两组患者手术前后使用抗青光眼药物数量比较两组患者手术前后使用抗青光眼药物数量比较差异均有统计学意义(P<0.001),术后6 mo两组患者使用抗青光眼药物数量比较差异无统计学意义(P=0.209),见表5。
2.6两组患者手术成功率比较术后6 mo两组患者手术成功率比较差异无统计学意义(Z=0.448,P=0.654),见表6。
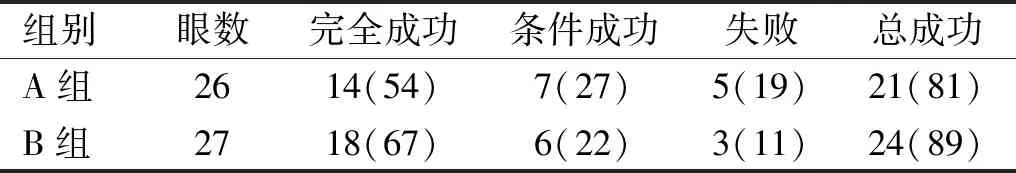
表6 两组患者手术成功率比较 眼(%)
2.7两组患者术后并发症比较两组患者术后前房出血比较差异有统计学意义(P<0.01),出血均在2 wk内吸收。两组患者浅前房和脉络膜脱离比较差异无统计学意义(P>0.05),B组患者中10眼出现一过性高眼压,发生率为37%,出现在术后2-6 wk,见表7。两组患者均未出现脉络膜爆发出血、眼内炎、恶性青光眼等严重并发症。

表7 两组患者术后并发症比较 眼(%)
2.8两组患者术后滤过泡护理情况A组术后6 mo内滤过泡护理共15眼(58%),其中术后按摩10眼,注射5-FU联合滤过泡分离5眼。B组无需滤过泡护理。
3 讨论
POAG发病机制尚不明确,其房角开放,小梁网异常,Schlemm管本身管径变窄、萎缩导致近端阻力增加可能是眼压增高的主要原因[7-8]。对于晚期POAG主要采用手术治疗,根据房水引流途径分为三种手术方式:内引流、外引流、抑制房水生成手术。小梁切除术是一种外引流手术,挽救无数青光眼患者的视功能,但其术后滤过泡带来的相关眼表影响和繁琐护理给青光眼患者和医生带来很大的负担,而且术后的并发症较多,如浅前房、脉络膜脱离、脉络膜上腔出血和角膜内皮失代偿等。21世纪以来,更符合眼自身生理结构的微创青光眼手术方法不断涌现,微创青光眼手术的手术量在中国逐年递增,微创、非滤过泡依赖理念成为新的手术发展趋势。
Schlemm管成形术是由Lewis等在Schlemm管切开术的基础上改良而成,是一种非滤过泡依赖的青光眼内引流手术[9-10]。多项研究显示,Schlemm 管成形术在开角型青光眼的治疗中降眼压效果良好[11-12]。穿透性Schlemm管成形术(penetrating canaloplasty,PCP)将Schlemm管成形术与小梁切除术手术技术相结合,从外路打开Schlemm管并通过切除局部小梁网(或深层角巩膜缘组织)和周边虹膜实现前房与Schlemm管直接沟通[13],可不受房角形态制约,也不受角膜混浊的影响,既适用于开角型青光眼,也适用于闭角型青光眼[14-15]。PCP手术在PACG患者中显示出理想的短期降眼压效果(6 mo),平均降眼压幅度为59%,手术的条件成功率和完全成功率分别为95%和90%[14],手术过程中需要iTrack导管指示穿行Schlemm管,其价格昂贵,一次性耗材,增加患者的经济负担,在基层医院广泛开展有一定困难。本研究利用5-0聚丙烯缝线代替微导管,5-0聚丙烯缝线直径100 μm, Schlemm管直径300-500 μm,可容纳3-4根5-0聚丙烯缝线,只要能准确定位Schlemm管,虽然没有指示灯指引,穿行成功率可达95%以上。目前国内还没有缝线引导穿透性Schlemm管成形术治疗原发性开角型青光眼的报道,因为缝线没有指示灯,难度较导管大一些,需要一定的学习曲线,本研究分析总结缝线是否穿入Schlemm管内几点经验:(1)缝线入前房前会发现瞳孔轻微变形。在穿行过程中时刻观察瞳孔,提早判断迷路,避免缝线入前房导致出血。(2)患者疼痛感。患者疼痛明显可能穿入脉络膜上腔,穿入Schlemm管内患者有轻度胀痛或者无感觉。(3)缝线穿行的阻力。无助力时可能迷路到脉络上腔或前房。穿行早期阻力小,后期阻力增加,如果Schlemm管塌陷,会出现5-0缝线弯曲情况,如果很难穿过,需从另一端穿入。(4)返血情况。缝线进入Schlemm管内会看见返血,缝线穿出前返血会增多。
本研究收集53例53眼晚期POAG合并白内障患者,与复合式小梁切除术比较,缝线引导穿透性Schlemm管成形术能够安全有效降低眼压。两组术后1 wk,1、3、6 mo眼压均与术前比较明显降低,差异均有统计学意义(P<0.05)。术后各个观察时间点两组患者眼压比较差异均无统计学意义,术后1 wk,1 mo B组的眼压均值高于A组,可能是A组早期有外滤过而显现眼压更低,到术后3、6 mo B组的平均眼压均低于A组,可能A组的外滤过逐渐形成瘢痕导致,而B组是依赖于内滤过,随时间推移内滤过逐渐启动,后期它的降眼压效果才体现出来。表3中可见两组患者术后各时间点眼压与术前差值比较无明显差异(P>0.05),但是P值逐渐变小,猜测如果术后1 a比较两组眼压,可能两组之间会有差异,B组低于A组,B组的手术方式可能优于A组,本研究还在继续跟踪患者,观察更远期的临床效果,希望能进一步指导临床,术后6 mo两组患者BCVA比较无明显差异,抗青光眼药物数量比较差异无统计学意义。随访6 mo,A组手术完全成功率为54%,条件成功率为27%,总成功率是81%,B组手术完全成功率为67%,条件成功率22%,总成功率是89%,两组成功率比较无统计学意义(P>0.05)。
本研究中随访期间两组患者均未出现脉络膜爆发出血、眼内炎、恶性青光眼等严重并发症。主要的并发症有前房出血、浅前房、脉络膜脱离和一过性高眼压。B组前房出血率达93%,明显高于A组,原因主要有两方面:(1)静脉系统血液回流。手术中穿通Schlemm管过程中可能存在内壁微撕裂,巩膜上静脉血倒流入前房,与360小梁切开比较出血量少很多,没有出现满贯血情况。(2)虹膜根切口处有9-0缝线结扎,其有一定张力,可能压迫虹膜导致出血量多一些。所有出血2 wk内均可以吸收,B组因术后早期出血较A组多,BCVA不如A组,患者会有些抱怨,经过耐心解释均能理解,术后6 mo两组患者BCVA比较无明显差异(P>0.05)。A组有9眼出现浅前房,发生率35%,高于与文献报道的传统小梁切除术后早期浅前房的发生率(22%)[16],B组有5眼出现浅前房,低于A组,PCP手术不依赖外滤过手术,原则上巩膜瓣可以紧密缝合,本研究病例均是晚期青光眼,术者缝合巩膜瓣时未紧密缝合,目的是让早期有些外滤过,眼压能降得低一些,但是这样会不会影响Schlemm管再通和一过性高眼压出现时间的推迟目前尚无科学依据。两组患者浅前房和脉络膜脱离经过散瞳消炎治疗均治愈。
A组术后15 d结膜缝线拆除后因眼压高指导患者按摩10眼,术后1 mo结膜下注射5-FU联合滤过泡分离5眼。B组无按摩和滤过泡分离。由此可见B组手术方式无术后滤过泡护理,也不存在滤过泡带来的相关并发症,例如:眼干、眼磨、滤过泡漏和滤过泡感染等,减少了患者和医生的负担。B组患者中10眼出现一过性高眼压,发生率为37%,出现在术后2-6 wk。这种高眼压的发病机制目前尚不清楚,可能和出血、炎症、黏弹剂残留、术后激素药水使用有关系[17]。梁远波教授团队认为一过性高眼压是启动Schlemm 管内引流通路,堵塞的再通和重塑的过程。B组患者均未出现后弹力层脱离和角膜水肿,缝线引导穿透性Schlemm管成形术用9-0缝线扩张Schlemm管,但是没有用黏弹剂扩张Schlemm管,不存在因黏弹剂使用过量导致后弹力层脱离,同时因没有黏弹剂扩张Schlemm管,是否会降低手术成功率,目前没有明确的数据支持。
本研究的局限性在于病例数不多且随访时间较短,今后的研究中我们将进一步收集病例,延长随访时间,观察缝线引导下穿透性Schlemm管成形术的长期疗效。
综上所述,本研究结果表明缝线引导下穿透性Schlemm管成形术联合超声乳化人工晶状体植入术与复合式小梁切除术联合超声乳化人工晶状体植入术疗效相当,并发症少,无需行滤过泡分离、按摩、注射抗代谢药物等治疗,简化术后护理流程。该手术采用缝线代替微导管,无需昂贵的设备和耗材,大大降低患者就医成本,可让广大青光眼患者受益。
