固液态均荧光发射的四苯乙烯基衍生物的合成
2024-04-27李素婉陈茂文刘森坤张灯青
李 曼, 李素婉, 陈茂文, 刘森坤, 江 背, 张灯青
(东华大学 化学与化工学院,上海 201620)
传统有机荧光材料在稀溶液中具有发射强度高、响应速度快和精度高等优点,但在聚集态时刚性分子平面易发生π-π堆积或形成激基复合物耗散能量,表现为ACQ现象[1-4],限制了其在固态下的应用。2001年,唐本忠课题组[5]报道了一种特殊的AIE分子,在溶液中其激发态能量以分子内旋转运动形式耗散,而当分子聚集时,由于旋转受限而发射出强的荧光[6-8]。 AIE分子的出现有效解决了由于ACQ效应引起的应用限制。萘酰亚胺(NI)类分子是应用最为广泛的ACQ荧光团之一,在溶液中强荧光发射,聚集态下荧光淬灭[9]。四苯乙烯(TPE)及其衍生物是目前AIE荧光分子中的代表性化合物,在聚集态下强发射,而溶液中不发射,显示出特征的聚集诱导发射特性。2019年,YU等[10]将四苯基乙烯和萘二甲酰亚胺结合在一起合成了新型共聚物,其在溶液、聚集态均保持较好的发光性能,且在不同的极性环境中表现出敏感荧光发射行为。因此,通过共价键将萘酰亚胺和四苯乙烯分子结合到同一分子中,可以构建具有ACQ与AIE性质的荧光材料,实现了分子在固液态下均发光[11-12],拓宽了荧光材料在不同场景下的应用。
本文设计合成了含有萘酰亚胺的化合物3作为ACQ分子和含有2个炔吡啶四苯乙烯的化合物7作为AIE分子,通过酰胺缩合进行共价连接,溶液中萘酰亚胺的大共轭刚性平面结构表现出良好的荧光效率,而在聚集或固态下四苯乙烯表现出优异的聚集发光性能,实现单分子在溶液、固态下均可荧光发射。白光材料在显示与照明等光学电子器件中具有十分重要的意义[13-15],尤其是单分子白光材料[16],可以克服由2个以上的荧光分子组成的系统中出现的相分离、颜色老化、易降解以及重现性低等缺点,目前关于单分子白光的报道仍然较少。本文报道的供体-受体型TPE-NI二联体化合物8,其合成路线如图1所示,在三氟乙酸的调控下能实现白光发射,CIE色坐标为(0.33, 0.32)。

图1 化合物8的合成路线
1 实验部分
1.1 仪器与试剂
TU-1901 spectrophotometer型紫外分光光度计; Horiba Fluoro Max+spectrofluorometer型荧光分光光度计; Bruker Model Avance DMX(400 MHz)型核磁共振仪(CDCl3为溶剂,TMS为内标); Agilent LC-MS 6120型液质联用仪。
化合物1[17]、2[17]、4[18]和5[19]分别按文献方法合成。其余所用试剂均为光学纯、分析纯。
1.2 合成
(1) 化合物3的合成
向50 mL二颈烧瓶中加入化合物2(442 mg, 1.000 mmol),混合溶剂(三氟乙酸 ∶二氯甲烷=1 ∶3,V∶V)16 mL,反应12 h, TLC监测反应,反应结束后减压蒸馏除去溶剂,加入碳酸氢钾溶液,调pH=8,二氯甲烷萃取,干燥称重,得到328 mg黄绿色固体化合物3,产率96%;1H NMR(400 MHz, CDCl3)δ:8.63(d,J=7.3 Hz, 1H), 8.58(d,J=8.2 Hz, 1H), 8.48(d,J=7.9 Hz, 1H), 7.78~7.70(m, 1H), 7.54(d,J=7.9 Hz, 1H), 4.27(t,J=6.6 Hz, 2H), 3.20~3.14(m, 2H), 3.07(t,J=6.6 Hz, 2H), 1.83(dt,J=13.3 Hz, 6.6 Hz, 1H), 1.70(dd,J=15.0 Hz, 7.2 Hz, 2H), 1.00(d,J=6.6 Hz, 6H);13C NMR(101 MHz, CDCl3)δ:164.2, 145.4, 131.1, 130.7, 130.0, 129.2, 127.6, 126.4, 122.3, 118.8, 42.9, 40.4, 37.0, 30.2, 27.6, 22.2。
(2) 化合物6的合成
化合物6利用Suzuki偶联方法合成。氩气保护下,向50 mL二颈烧瓶中依次加入化合物4(399 mg, 0.780 mmol)、化合物5(100 mg, 0.260 mmol)、四三苯基膦钯(30 mg, 0.026 mmol)、 1 mL 2 mol/L的K2CO3水溶液,再加入15 mL冷冻除氧的THF-PhMe混合溶剂(2 ∶1,V∶V), 80 ℃搅拌48 h。反应结束后旋除溶剂,残余物经硅胶柱层析(洗脱剂:二氯甲烷 ∶甲醇=20 ∶1,V∶V)提纯得到浅黄色固体169 mg,产率65%;1H NMR(400 MHz, CDCl3)δ:8.60(d,J=5.3 Hz, 4H), 8.17(s, 2H), 7.90(s, 1H), 7.44(m, 9H), 7.33(d,J=8.0 Hz, 4H), 7.18~7.02(m, 28H), 3.95(s, 3H);13C NMR(101 MHz, CDCl3)δ:166.9, 149.7, 144.9, 143.2, 142.9, 142.5, 141.3, 139.4, 138.0, 132.1, 132.1, 132.0, 131.6, 131.5, 131.4, 131.3, 128.5, 127.9, 126.9, 126.8, 126.5, 125.5, 120.0, 94.3, 87.0, 52.3; LC-MS(EI)m/z:calad for C74H50N2O2{[M+H+]}999.3906, found 999.3953。
(3) 化合物7的合成
向50 mL的二颈烧瓶中依次加入6(500 mg, 0.500 mmol)、氢氧化钠(240 mg, 6.000 mmol)、混合溶剂(四氢呋喃 ∶甲醇 ∶水=1 ∶1∶1,V∶V∶V)15 mL, 80 ℃反应过夜,旋除溶剂,加入2 mol/L的稀盐酸,调溶液pH=6,萃取干燥得到黄色固体490 mg,产率99%;1H NMR(400 MHz, CDCl3)δ:8.62(s, 4H), 8.22(s, 2H), 7.93(s, 1H), 7.54~7.40(m, 9H), 7.33(d,J=8.0 Hz, 4H), 7.18~6.94(m, 28H);13C NMR(101 MHz, CDCl3)δ:145.1, 143.3, 139.4, 138.3, 132.3, 131.9, 131.6, 131.4, 127.9, 127.2, 126.9, 126.6, 125.8, 119.8, 94.9, 86.8; LC-MS(EI)m/z:calad for C73H49N2O2{[M+H+]}985.3789, found 985.3798。
(4) 化合物8的合成
氩气保护下,将化合物7(99 mg, 0.100 mmol)、 2-(7-偶氮苯并三氮唑)-N,N,N′,N′-四甲基脲六氟磷酸酯(HATU)(58 mg, 0.150 mmol)和N,N-二异丙基乙胺(DIPEA)(0.2 mL, 0.150 mmol)依次加入50 mL二颈烧瓶中,加入10 mL二氯甲烷,室温搅拌1 h,再加入化合物3(35 mg, 0.100 mmol),室温反应6 h, TLC监测反应,反应完成后萃取,干燥有机相,残余物经硅胶柱层析(洗脱剂:二氯甲烷 ∶甲醇=20 ∶1,V∶V)纯化,得到浅黄色粉末化合物840 mg,产率30%,1H NMR和13C NMR谱图如图2~3所示;1H NMR(400 MHz, CDCl3)δ:8.51(s, 1H), 8.47(d,J=7.9 Hz, 4H), 8.33(d,J=7.9 Hz, 1H), 7.77(s, 2H), 7.71(s, 1H), 7.45(s, 1H), 7.32(d,J=8.1 Hz, 4H), 7.25(d,J=8.3 Hz, 8H), 7.18(s, 2H), 7.09~6.96(m, 29H), 4.48(s, 2H), 3.80(s, 2H), 3.04(s, 2H), 1.71(d,J=6.7 Hz, 2H), 1.25(s, 1H), 0.89(d,J=6.5 Hz, 6H);13C NMR(101 MHz, CDCl3)δ:167.62, 164.83, 149.69, 146.62, 145.03, 143.28, 142.80, 142.44, 141.28, 139.43, 138.34, 135.50, 131.89, 131.62, 131.36, 130.65, 129.54, 127.91, 126.93, 126.55, 124.47, 119.96, 87.01, 40.73, 39.23, 37.05, 29.72, 27.68, 22.28; LC-MS(EI)m/z:calad for C92H69N4O3S{[M+H+]}1309.5085, found 1309.5085。

δ

δ
2 结果与讨论
2.1 光谱分析
图4(a)中前体7作为具有AIE特性的分子与前体3相比,在1,4-二氧六环中荧光强度非常弱。图4(b~c)分别为化合物8在319 nm和390 nm激发下,在不同溶剂中的发射光谱。在氯仿、二氯甲烷等溶剂中,荧光强度较弱;随着溶剂极性增大,在乙酸乙酯、1,4-二氧六环中的荧光显著增强;在强极性溶剂DMF、 DMSO中荧光强度再次降低,这可能是由于分子内萘环与取代基以单键相连,高极性溶剂中分子旋转形成扭曲的分子内电荷转移(TICT),导致荧光降低[20]。以1,4-二氧六环为例,化合物8在390 nm激发的荧光强度为319 nm激发的荧光强度的5.5倍,如图4(d)所示。

λ/nm
2.2 聚集诱导发光(AIE)分析
化合物8在1,4-二氧六环中溶解性很好,但不溶于水,以水作为不良溶剂研究其AIE性质,荧光变化如图5所示。化合物8在纯1,4-二氧六环(Dio)溶液中发射蓝色荧光,量子产率为17.1%,在Dio溶液中化合物8的刚性萘酰亚胺倾向于以辐射跃迁方式发出荧光,而四苯乙烯可发生分子内运动以非辐射跃迁方式消耗能量无发光能力。随着化合物8的1,4-二氧六环溶液中水含量的不断增加,分子发生一定程度聚集形成π-π堆积复合体。此时化合物8的ACQ性质可能占据主导地位,能量以非辐射跃迁形式消耗,荧光强度降低,fw=40%时荧光量子产率为9.0%。继续增加水含量,化合物8表现出四苯乙烯的AIE性质,聚集程度增强,分子内运动受限从而以辐射跃迁形式发出荧光,因此荧光随水含量增加而急剧增强。fw=60%时,荧光强度最大,荧光量子产率为22.6%。fw进一步增大时,荧光强度逐渐降低,这可能是由于分子随机堆积形成了低发射性的聚集体[21]。
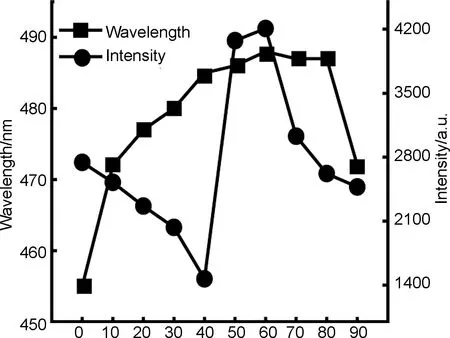
Water fraction/%(体积分数)
2.3 三氟乙酸调控的白光发射分析
由于化合物8含有2个末端吡啶,可以和酸反应生成吡啶盐,因而向化合物8的氯仿溶液中滴加三氟乙酸,溶液荧光颜色逐渐从蓝色经白色过渡到橙红色,荧光光谱如图6(a)所示。随着酸的不断加入,吡啶质子化,吸电子能力增强,分子内TICT效应增强,发射光谱红移。而450 nm附近属于萘酰亚胺,发射所受影响较小,因此荧光变化不明显。图6(b)中,当三氟乙酸含量为1.05 eq时,化合物8的氯仿溶液呈现白光发射,CIE色坐标为(0.33, 0.32)。

λ/nm
本文成功合成了一种固液态均可发射荧光的二联体化合物8,同时具有四苯乙烯结构和萘酰亚胺结构,兼具ACQ与AIE特性。ACQ特性分子前体化合物3中引入烷基硫醚,增强了该部分的共轭强度,赋予了化合物8在不同溶剂中荧光变化的可能性。AIE特性分子前体化合物7使化合物8在聚集态下有22.6%的荧光量子产率,并引入吡啶分子作为酸响应功能基团。化合物8在不同溶剂中的发光行为以及ACQ-AIE转换行为表明其在1,4-二氧六环中具有较好的荧光发射。在1,4-二氧六环/水体系中,随着水含量的不断增加,化合物8的荧光发射强度先降低后增强最后再降低,对应了ACQ行为向AIE行为转变。此外,在氯仿中,通过吡啶质子化调节分子内TICT效应实现了单分子白光发射。
