纳米氧化钨对序批式反应器活性污泥脱氮性能和胞外聚合物的影响*
2024-04-26边少晨储意轩宋亚丽方程冉
边少晨 邱 程 汪 华# 储意轩 郑 磊 宋亚丽 方程冉
(1.浙江科技大学土木与建筑工程学院,浙江 杭州 310023;2.浙江工业大学土木工程学院,浙江 杭州 310023)
金属氧化物纳米颗粒(NPs)具有比表面积大、吸附能力良好、催化作用强和选择性高等特点[1],已成为目前应用最广泛的一类纳米材料。金属氧化物NPs可以随生活污水以及生产废水进入污水处理厂。已有研究采用模型估算了污水处理厂污泥中的一些金属氧化物NPs浓度,其浓度高达毫克每千克级,甚至超过200 mg/kg[2]。金属氧化物NPs对活性污泥微生物具有潜在的毒性,可能对污水生物处理系统性能产生一定的影响。MA等[3]的研究表明,60 mg/L Fe3O4NPs对化学需氧量(COD)的去除有轻微抑制作用,而对氨氮的去除无明显影响。但有研究发现,经100 mg/L ZnO NPs作用后,序批式反应器(SBR)系统中的COD去除率没有明显变化[4]。ZHENG等[5]研究发现50 mg/L Al2O3NPs会抑制硝化和反硝化过程中相关功能酶的活性。上述研究表明,金属氧化物NPs种类不同,对系统产生的影响也有所区别。
胞外聚合物(EPS)是活性污泥的重要组成部分,主要由微生物分泌的多糖(PS)、蛋白质(PN)和少量核酸等大分子构成[6]。EPS呈动态双层结构,主要包括松散结合型EPS(LB-EPS)和紧密结合型EPS(TB-EPS),EPS能够影响活性污泥的絮凝、沉降和脱水性能[7]883,还可以保护污泥内部微生物免受外界污染物如重金属和化学品的影响[8]。EPS含量及组成对金属氧化物NPs的胁迫会产生响应。有研究发现50 mg/L CuO NPs可以促进LB-EPS的产生,并主要增加EPS中PS的产量[9]68。25 mg/L CeO2NPs可以促进生物膜产生更多的TB-EPS[10]93。但是,李维等[11]研究发现50 mg/L ZnO NPs能降低EPS中的PN和PS含量。
氧化钨(WO3)NPs是一种典型的金属氧化物NPs[12],广泛应用于半导体、气体传感器以及涂料生产等领域[13],已成为发展最迅速的一种纳米材料[14]。 WO3NPs的广泛应用使得其在制造、运输、利用和处置过程中可能会排放到污水处理系统。此外,WO3NPs是一种高效的光催化剂,可用于降解有机污染物,也有可能应用于污水处理[15]。因此有必要分析WO3NPs对污水生物处理系统的潜在影响。然而目前尚未发现WO3NPs对污水生物处理系统性能以及活性污泥EPS组成影响的相关报道。本研究采用SBR,以WO3NPs为研究对象,基于污泥中的金属氧化物NPs浓度,并考虑获取WO3NPs对活性污泥性能胁迫信息的需要以及其他突发情况(比如意外泄漏)等[16],选择较高浓度(10 mg/L和100 mg/L)的WO3NPs,研究WO3NPs对活性污泥系统脱氮性能和EPS组成的影响。同时,利用傅立叶红外光谱(FTIR)分析WO3NPs与EPS相互作用过程中EPS表面官能团的变化。研究结果可以为WO3NPs对污水处理系统的潜在风险评估提供一定的科学依据。
1 材料与方法
1.1 WO3 NPs与污水
WO3NPs购于某冶金材料有限公司,粒径约为50 nm。本试验SBR的进水为浙江科技大学学生宿舍西和公寓(位于杭州)生活污水,每天进行配水并且适当添加碳、氮、磷源,维持进水COD、氨氮和总磷分别在400、60、6 mg/L左右。进水COD由醋酸钠和无水葡萄糖配制,氨氮由碳酸氢铵配制,总磷由磷酸二氢钾配制。接种污泥取自绍兴某污水处理厂二沉池。
1.2 SBR的建立与运行
SBR底端进水,上端设置取水口,有效容积为2.5 L。反应器一个循环为7.5 h,分别由5 min进水阶段,60 min缺氧阶段,180 min好氧阶段,120 min缺氧阶段,20 min沉淀阶段,5 min出水阶段和60 min闲置阶段组成。反应器水力停留时间(HRT)为16 h,污泥停留时间(SRT)约为21 d。反应器混合液悬浮固体(MLSS)为(3 500±500) mg/L,进水pH维持在7.8左右。缺氧反应阶段溶解氧低于0.5 mg/L,好氧反应阶段溶解氧高于5 mg/L。反应器进出水通过电子计时器控制的蠕动泵完成。首先对污泥进行驯化,当所有反应器出水水质指标达到稳定后开始试验。试验分为两个阶段。第一阶段为0~30 d,设置2个处理:(1)CK10为对照组,不添加WO3NPs;(2)WO10处理组,添加10 mg/L的WO3NPs。第二阶段为30~60 d,设置2个处理:(1)CK100为对照组,不添加WO3NPs;(2)WO100处理组,添加100 mg/L的WO3NPs。每2天检测一次出水COD、氨氮、硝酸盐氮和亚硝酸盐氮的浓度,每个阶段结束时分析EPS含量。所有处理均重复3次。
1.3 EPS的提取与分析
LB-EPS和TB-EPS采用热萃取法提取[17]。EPS样品通过0.45 μm滤膜过滤后放入4 ℃冰箱内保存。采用蒽酮/硫酸法测定EPS中的PS[18]。EPS中的PN采用BCA蛋白试剂盒(上海生工)测定。
LB-EPS和TB-EPS溶液在-80 ℃冻干后,使用FTIR仪(Nicolet IS 5)对冻干粉进行分析。PN二级结构信息通过进一步分析酰胺Ⅰ区(1 600~1 700 cm-1)光谱来获取。首先采用九点Savitzky-Golay导数函数获得原始酰胺Ⅰ区光谱的二阶导数[19],然后,根据二阶导数光谱进一步对酰胺Ⅰ区进行反卷积,最后使用PEAKFIT V4.12曲线拟合软件对原始光谱进行量化。
1.4 其他分析方法
水样COD、氨氮、硝酸盐氮和亚硝酸盐氮、MLSS、混合液可挥发性悬浮固体(MLVSS)测定方法参照文献[20]。比氨氧化速率(SAOR)、比亚硝酸盐氧化速率(SNOR)、比亚硝酸盐还原速率(SNIRR)和比硝酸盐还原速率(SNRR)参考文献[3]进行测定。
1.5 数据分析
采用SPSS 26.0进行T检验来分析添加WO3NPs的影响,显著性水平设为p<0.05。
2 结果与讨论
2.1 SBR出水水质和氮转换速率
反应器整个运行期间对COD的平均去除率都在91.52%以上,表明WO3NPs对SBR中COD的处理效率几乎没有影响,这与WANG等[21]研究结果一致。WO10处理组的各项出水指标整体趋势无显著变化(见图1),说明10 mg/L WO3NPs对SBR的脱氮性能没有影响。WO100处理组的出水氨氮浓度相比对照组无显著差异。相比于对照组,WO100处理组的出水硝酸盐氮浓度在40、44 d增加,随后恢复,从52 d又开始升高并持续至60 d。这表明当WO3NPs增加到100 mg/L时,反应器内硝酸盐氮的去除开始受到抑制,然后恢复,但是随着WO3NPs不断加入,最终导致出水硝酸盐氮的积累。WO100处理组的出水亚硝酸盐氮浓度显著高于对照组。出水硝酸盐氮和亚硝酸盐氮浓度的变化表明100 mg/L WO3NPs会影响活性污泥的反硝化过程。

注:第一、第二阶段的CK出水分别对应CK10、CK100出水,第一、第二阶段的WO3出水分别对应WO10处理组、WO100处理组出水。
不同阶段氮转换速率(以每小时每克MLSS转化的氮质量计)如表1所示。WO10和WO100处理组的活性污泥SAOR相比于对照组分别降低了6.79%和23.08%,这说明WO3NPs会抑制氨氧化过程。ZHENG等[22]研究发现氨氧化细菌的生长速度缓慢,并且对各种污染物例如NPs较为敏感。已有研究表明高浓度的金属氧化物NPs会导致NPs吸附在氨氧化细菌细胞表面,影响细胞的正常生理功能,降低氨氧化细菌丰度,进而抑制氨氧化过程[23]。本研究中发现虽然WO3NPs抑制了SAOR,但并没有对出水氨氮浓度产生显著影响,这可能是因为SBR好氧阶段时间较长[24],同时氨氮进水浓度不高。WO10和WO100处理组的SNOR均无显著变化。WO10处理组的SNRR相较于对照组无显著变化,SNIRR则显著增加,而WO100处理组的SNRR和SNIRR相比于对照组分别下降了20.78%和43.04%,表明高浓度的WO3NPs会抑制活性污泥的反硝化过程,最终导致了出水中硝酸盐氮和亚硝酸盐氮的积累。ZHENG等[25]发现高浓度(50 mg/L)SiO2NPs会使硝酸盐还原酶(NAR)和亚硝酸盐还原酶(NIR)的酶活性降低,最终导致出水硝酸盐氮的积累,这与本研究结果类似。WANG等[26]同样发现高浓度(60 mg/L)ZnO NPs会抑制活性污泥的NAR和NIR,从而进一步影响反硝化过程。

表1 氮转换速率变化Table 1 Variation of nitrogen conversion rates mg/(g·h)
2.2 污泥EPS含量及组成
如图2(a)所示,EPS总量(以每克MLVSS中的EPS质量计)随WO3NPs浓度的增加而增加,与对照组相比,WO10处理组的EPS总量没有显著变化。但WO100处理组的EPS总量显著高于对照组。进一步分析EPS中TB-EPS和LB-EPS含量发现,WO10处理组的TB-EPS和LB-EPS的含量没有显著变化,但WO100处理组的LB-EPS含量增加了63.05%,而TB-EPS有增加的趋势,但差异不显著。已有研究报道了一些金属氧化物NPs可以促进EPS的产生[10]93,[27]349。EPS是活性污泥抵抗有毒物质侵害的重要屏障[7]883。活性污泥通过产生更多的EPS来延缓NPs与污泥内细菌的接触,从而增强自身的抵抗力。随着WO3NPs浓度的增加,作为对NPs的保护应激反应,活性污泥会产生更多的EPS。EPS呈动态双层结构,LB-EPS位于外层,而TB-EPS附着在活性污泥微生物细胞壁上[28]。外层的LB-EPS可能是与WO3NPs接触和相互作用的主要表面,延缓了NPs进入到TB-EPS和细胞内部的时间,这可能是LB-EPS的变化远大于TB-EPS的原因[9]68。

注:WO10-TB表示WO10处理组TB-EPS,其余类推,表2同。
图2(b)显示了不同浓度WO3NPs 处理下活性污泥LB-EPS和TB-EPS主要组分的变化。WO10处理组的LB-EPS和TB-EPS中PN和PS含量相比于对照组没有显著变化。WO100处理组的LB-EPS和TB-EPS中的PN含量同样没有显著变化,但LB-EPS中的PS含量和TB-EPS中的PS含量显著增加。HOU等[9]68研究也发现暴露于50 mg/L CuO NPs条件下EPS中PS含量显著增加。这可能与活性污泥应对高浓度NPs的防御机制有关,PS可以增加NPs的水合直径并促进其聚集[27]350,而团聚的NPs相较于分散的NPs毒性更小。随着WO3NPs浓度增加,活性污泥通过产生更多的PS,进而抵抗WO3NPs的毒性。
2.3 EPS的FTIR分析
图3为WO3NPs影响下污泥EPS的FTIR图谱。3 300 cm-1附近较宽的吸收峰是—OH 伸缩振动导致的。1 650 cm-1附近的吸收峰则是由酰胺基团C=O拉伸振动而形成。此外,1 404 cm-1附近的吸收峰主要来自羧基中C=O的伸缩振动,1 080 cm-1附近的吸收峰来自C—O—C的伸缩振动,指纹区(小于1 000 cm-1)中的一些峰则表明了磷酸或含硫官能团的存在。如图3所示,WO10处理组的LB-EPS图谱中—OH和酰胺基团C=O的吸收峰发生了偏移,C—O—C的吸收峰峰强增加。而WO10处理组的TB-EPS光谱则几乎没有变化。WO100处理组的LB-EPS图谱则发生了较大的变化,—OH吸收峰发生了偏移,且峰强增加;酰胺基团C=O的吸收峰也发生了偏移,羧基中C=O和C—O—C吸收峰峰强则都增加。WO100处理组的TB-EPS图谱变化较小,—OH吸收峰发生了偏移,酰胺基团C=O的吸收峰峰强增加。上述结果表明EPS中的—OH、C=O和C—O—C等官能团可能与WO3NPs发生了相互作用。
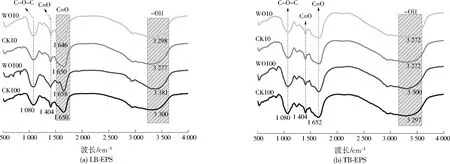
图3 FTIR图谱Fig.3 FTIR spectra
EPS有许多吸附位点,如PN中的芳香族、脂肪族以及碳水化合物中的疏水区[7]887, 可以吸附WO3NPs,并可能与NPs发生复杂相互作用进而对EPS表面官能团产生影响。外层LB-EPS具有松散多孔结构,为吸附WO3NPs提供了足够的结合位点[29],内层TB-EPS由于LB-EPS的保护作用,受到WO3NPs的影响较小,因此TB-EPS图谱变化小。MU等[30]的研究同样证实EPS中不同的官能团参与了金属氧化物NPs与活性污泥间的相互作用。
2.4 EPS的PN二级结构
有研究表明 PN在EPS吸附NPs过程中可能起着重要的作用[31]。因此通过二阶导数分析和曲线拟合程序将EPS的FTIR酰胺Ⅰ区(1 600~1 700 cm-1)分解为组分峰,从而得到更详细的WO3NPs作用下EPS PN二级结构信息[32]。EPS中的PN二级结构可分为:聚合链(1 610~1 625 cm-1)、β-折叠(1 630~1 640 cm-1)、无规则卷曲(1 640~1 645 cm-1)、α-螺旋(1 648~1 657 cm-1)、3-反螺旋(1 659~1 666 cm-1)和反平行式β-折叠(1 680~1 695 cm-1)。各二级结构的相对丰度(各二级结构峰面积在总峰面积中的占比)如表2所示。所有EPS在酰胺Ⅰ区中螺旋结构(α-螺旋+3-反螺旋)的相对丰度均高于其他二级结构,这与之前关于活性污泥EPS中PN二级结构组成的研究一致[33]。WO10 处理组的LB-EPS中聚合链和α-螺旋的相对丰度均高于对照组,β-折叠的相对丰度则减少。WO10处理组的TB-EPS变化很小,这与FTIR结果一致。WO100处理组的LB-EPS中α-螺旋的相对丰度增加,β-折叠和无规则卷曲的相对丰度降低,WO100处理组的TB-EPS中α-螺旋的相对丰度增加,无规则卷曲的相对丰度则降低。上述结果表明,EPS样品中PN二级结构组成有较大的差异,这可能是它们与WO3NPs相互作用的结果。已有研究表明聚合链和α-螺旋结构可以增强活性污泥的吸附、聚集和絮凝作用,而无规则卷曲则起相反作用[34]。WO3NPs处理的EPS中聚合链和α-螺旋相对丰度的上升可能会增强EPS对NPs的吸附作用。此外,低水平的α-螺旋和高水平的β-折叠或无规则卷曲可能会导致污泥结构松散,不利于污泥的絮凝性能提升[35]。与对照组相比,WO3NPs影响下EPS中α-螺旋/(β-折叠+无规则卷曲)高于对照组,这说明了EPS结构变得更紧密,絮凝沉降能力更好。WANG等[36]同样发现Fe3O4NPs会增加EPS中α-螺旋/(β-折叠+无规则卷曲)的值,从而增强了污泥的絮凝能力。

表2 WO3 NPs影响下PN二级结构变化Table 2 Change of secondary structure of PN under the influence of WO3 NPs
3 结 论
(1) 10 mg/L WO3NPs对SBR脱氮性能没有影响,而100 mg/L WO3NPs抑制了反硝化过程中硝酸盐还原和亚硝酸盐还原这两个过程,最终导致出水的硝酸盐氮与亚硝酸盐氮的积累,从而影响脱氮过程。
(2) 10 mg/L WO3NPs对活性污泥的EPS总量无显著性影响,而100 mg/L WO3NPs使活性污泥LB-EPS含量和EPS中PS含量显著增加。这可能是活性污泥应对高浓度WO3NPs的防御机制。
(3) FTIR分析显示10 mg/L WO3NPs仅对LB-EPS中官能团有影响,而在100 mg/L WO3NPs影响下,LB-EPS和TB-EPS两者的官能团都发生了不同程度的变化。参与EPS和WO3NPs相互作用的官能团主要有—OH、C=O以及C—O—C等。此外,对FTIR图谱的酰胺Ⅰ区(1 600~1 700 cm-1)进一步分析发现,WO3NPs改变了EPS中PN二级结构组成,增加了α-螺旋/(β-折叠+无规则卷曲)值,促进活性污泥絮凝。
