岩藻黄质通过AKT/mTOR途径调节糖酵解代谢促进人急性淋巴细胞白血病细胞凋亡的作用研究
2024-04-17叶松霖金炫安杜昊霏王家诚金旭东徐博怀丁浩淼
叶松霖 金炫安 杜昊霏 王家诚 金旭东 徐博怀 丁浩淼,*
(1浙江万里学院生物与环境学院,浙江 宁波 315100;2宁波大学附属第一医院,浙江 宁波 315000)
急性白血病(acute leukemia,AL)是起源于造血干细胞的恶性克隆性疾病,又分为急性淋巴细胞白血病(acute lymphoblastic leukemia,ALL)和急性髓细胞白血病(acute myeloid leukemia,AML)。ALL是儿童最常见的恶性肿瘤[1-3],复发率高,缓解率低,长期生存率低,且发病率逐年上升[4]。目前ALL的主要治疗方法是化疗,而多种药物联合和个体化治疗提高了ALL患者的5年生存率[5],但一些患者对这些治疗反应不佳,因此需要一种对患者副作用小的新型抗肿瘤物质。已有研究表明,来自植物、真菌、海洋生物和微生物的天然活性成分具有抗肿瘤和免疫调节作用,且副作用小[6]。因此,研究海洋生物中活性成分的抗肿瘤作用对预防和治疗ALL具有重要意义。
能量代谢的异常改变是肿瘤细胞的一个突出特征,其特征是倾向于将有氧糖酵解作为能量生成的主要手段[7]。研究表明,抑制肿瘤糖酵解途径可有效阻碍肿瘤细胞增殖,甚至诱导肿瘤细胞死亡[8]。此外,研究证实,蛋白激酶B(protein kinase B,AKT)/哺乳动物雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)通路可以促进参与糖酵解通路的关键酶的表达,导致肿瘤细胞对葡萄糖的摄取增强和糖酵解活性失调[9]。这种现象有助于增加能量供应,促进肿瘤生长,控制肿瘤细胞增殖[10]。上述发现为AKT/mTOR信号通路与糖酵解代谢之间的显著关联提供了有力的证据。因此,靶向AKT/mTOR信号通路控制的糖酵解途径,减少对肿瘤细胞的能量供应,可能成为一种治疗ALL的有前景的方法。
羊栖菜(Sargassumfusiforme)是一种褐藻门马尾藻科(Sargassaceae)的植物,在中国和日本作为药物治疗疾病已有数千年的历史[11]。研究表明,马尾藻属植物提取物具有多种作用,包括抗肿瘤、抗疲劳、抗辐射、抗病毒、抗衰老和免疫调节特性[12-13]。岩藻黄质是羊栖菜的主要活性成分。大量研究表明,岩藻黄质能够通过阻滞细胞周期、抑制DNA合成和促进细胞凋亡来阻止肿瘤细胞增殖。值得注意的是,岩藻黄质对多种癌症有显著的抑制作用,包括肺癌、肝癌、乳腺癌、胃癌和宫颈癌[14]。在Bae等[15]的研究中,岩藻黄质部分减弱了参与糖酵解和线粒体呼吸的基因表达的变化,这些基因包括己糖激酶、过氧化物酶体增殖物激活受体γ辅激活因子1β和丙酮酸脱氢酶激酶3。然而,目前关于岩藻黄质对ALL的特异性调控作用的信息很少。因此,本研究以急性淋巴细胞白血病CEM/C1细胞为研究对象,通过观察岩藻黄质对CEM/C1细胞的凋亡、细胞周期的应答差异及其相关糖酵解指标的变化,探究岩藻黄质抗白血病的机制,以期为岩藻黄质(图1)应用在ALL的预防和治疗提供理论依据。

图1 羊栖菜中岩藻黄质的化学结构Fig.1 Chemical structure of fucoxanthin isolated from Sargassum fusiforme
1 材料与方法
1.1 材料与试剂
急性淋巴细胞白血病CEM/C1细胞购自于上海中科院细胞库;RPMI-1640、胎牛血清购自杭州四季青公司;二甲基亚砜(dimethyl sulfoxide,DMSO)、3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴盐[3-(4,5-Dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide,MTT]、磷酸酶抑制剂、苯甲磺酰氟(phenyl methane sulfonyl fluoride,PMSF)、蛋白酶抑制剂购自诺维森生物科技有限公司;Bicinchoninic Acid Assay(BCA)蛋白定量试剂盒购自上海联祖生物科技有限公司;Annexin V-FITC/PI细胞凋亡试剂盒、碘化丙啶/核糖核酸酶(PI/Rnase)细胞周期试剂盒购自美国BD公司;EasyScript®One-Step gDNA Removal and cDNA Synthesis SuperMix反转录试剂盒、TransStart®Green qPCR SuperMix试剂盒购自北京全式金生物有限公司;AKT抗体、phospho-AKT抗体、m-TOR抗体、phospho-mTOR抗体、己糖激酶(hexokinases,HK)抗体、丙酮酸激酶(pyruvate kinase,PKM)抗体、甘油醛-3-磷酸脱氢酶(glyceraldehyde-3-phosphate dehydrogenase,GAPDH)抗体、辣根过氧化物酶(horseradish peroxidase,HRP)标记羊抗兔二抗购自武汉爱博泰克生物科技有限公司。
岩藻黄质由浙江万里学院提供,提取于羊栖菜,纯度>95%[高效液相色谱法(high performance liquid chromatography,HPLC)测定]。
1.2 仪器与设备
Series Ⅱ Water Jacket恒温CO2培养箱,美国Thermo公司;FACSVerse流式细胞仪,美国BD公司;TI-DH荧光倒置显微镜,日本Nikon公司;SpectraMax190连续波长多功能酶标仪,美国MD公司;Clinx凝胶成像仪,上海勤翔科学仪器有限公司。
1.3 试验方法
1.3.1 细胞培养 CEM/C1细胞接种于装有适量RPMI-1640培养基(10%胎牛血清、100 U·mL-1青霉素和100 μg·mL-1链霉素)的细胞培养瓶中,并将其置于37 ℃以及5% CO2浓度的细胞培养箱中培养[14]。
1.3.2 岩藻黄质对CEM/C1细胞活力的影响 取对数生长期CEM/C1细胞,以每孔5×104个接种于96孔板。试验分为药物组、对照组(不含药物)和空白组(仅加入空白培养基)。孵育24 h后,药物组加入不同浓度梯度的岩藻黄质(0、1、2、3、4、5、6、7、8、9、10 μg·mL-1),对照组加入等量培养基。每种剂量制备6个重复孔。进一步孵育0、8、16和24 h后,每孔加入10 μL MTT溶液。随后,细胞继续孵育4 h,使用酶标仪测定570 nm处的吸光度(A)值。
1.3.3 岩藻黄质对CEM/C1细胞凋亡的影响 取对数生长期CEM/C1细胞,以每孔5×104细胞密度接种于12孔培养板,培养24 h后分别加入0、2.5、5、7.5 μg·mL-1的岩藻黄质作用24 h,收集细胞并重新悬浮于100 μL的孵育液中。在上述细胞悬液中分别加入5 μL annexin V-FITC染色液和5 μL碘化丙啶染色液,室温避光孵育15 min后进行检测。流式细胞术检测细胞凋亡,并计算早期凋亡细胞和晚期凋亡细胞的比例。
1.3.4 岩藻黄质对CEM/C1细胞周期的影响 取对数生长期CEM/C1细胞,以每孔1×105细胞密度接种于6孔培养板中培养24 h。加入岩藻黄质(0、2.5、5和7.5 μg·mL-1)作用24 h,用冷磷酸盐缓冲盐水(phosphate buffered solution,PBS)连续洗涤细胞2次,加入1 mL 70%乙醇在4 ℃下固定18 h。PBS洗涤2次后加入0.5 mL PI/Rnase染料溶液,并在室温下静置20 min,采用流式细胞术分析各组细胞周期分布。
1.3.5 岩藻黄质对CEM/C1细胞葡萄糖摄取、ATP生成和乳酸生成的影响 取对数生长期CEM/C1细胞,以每孔1×105细胞密度接种于6孔培养板中培养24 h。岩藻黄质处理后收集细胞,少量细胞悬液使用细胞计数仪测定细胞计数。通过测量特定波长的吸光度来评估葡萄糖消耗、ATP生成和乳酸生成。应用酶标仪分别在555、570和340 nm测定葡萄糖摄取、乳酸和ATP生成的吸光值,并计算葡萄糖消耗、ATP生成和乳酸生成。
1.3.6 岩藻黄质对CEM/C1细胞HK和PK活性的影响 取对数生长期CEM/C1细胞,以每孔1×105细胞密度接种于6孔培养板中培养24 h。用岩藻黄质处理后收集细胞,少量细胞悬液用细胞计数仪测定细胞计数。应用酶标仪在340 nm处测定吸光值,计算HK和PK的酶活性。
1.3.7 岩藻黄质对CEM/C1细胞AKT/mTOR信号通路及糖酵解相关基因表达的影响 取对数生长期CEM/C1细胞,以每孔1×105细胞密度接种于6孔培养板中培养24 h。用TRIzol法提取细胞总RNA,并将RNA溶解于25 μL DEPC水中,NanoDrop分光光度计测定RNA浓度。按照逆转录试剂盒提供的说明书进行cDNA合成,逆转录体系为10 μL:PrimeScript Buffer RT Enzyme Mix 1.0 μL、RT Primer Mix 1.0 μL、5× PrimeScript Buffer 2 (for Real time) 4.0 μL、Rnase Free dH2O 4.0 μL。程序为:37 ℃反应15 min,85 ℃反应5 s。PCR循环条件为95 ℃预变性30 s,95 ℃变性5 s,60 ℃退火30 s,共循环40次。实时荧光定量PCR反应(quantitative real-time PCR,qRT-PCR)中使用的扩增引物序列见表1。
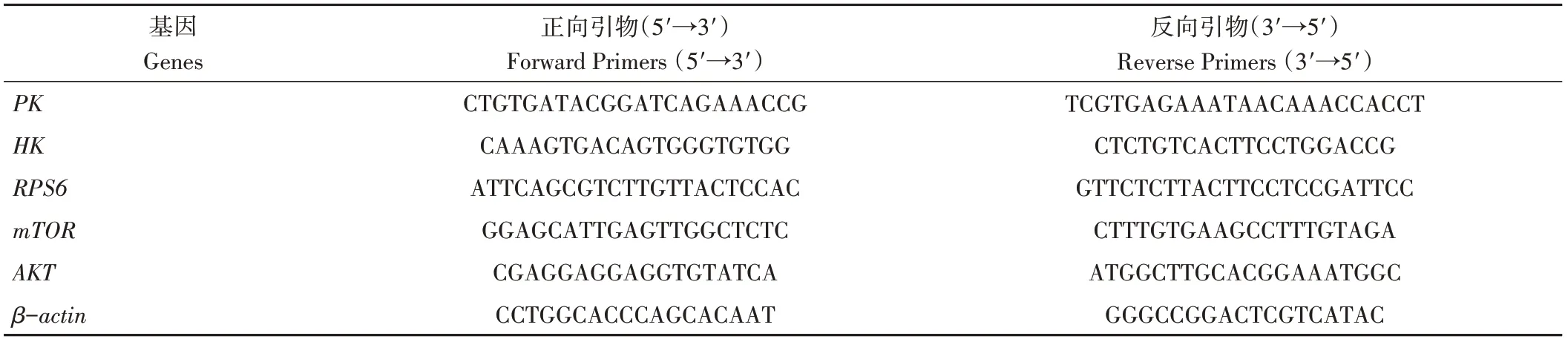
表1 引物序列Table 1 Primer sequences
1.3.8 岩藻黄质对CEM/C1细胞AKT/mTOR信号通路及糖酵解相关蛋白表达的影响 取对数生长期CEM/C1细胞,以每孔1×105细胞密度接种于6孔培养板中培养24 h。岩藻黄质处理后收集细胞,每管加入150 μL含磷酸酶抑制剂和蛋白酶抑制剂的RIPA裂解物,提取细胞蛋白。离心和收集上清液后,使用Bradford方法测定蛋白浓度并归一化。通过十二烷基硫酸钠-聚丙烯酰胺凝胶电泳对总量为30 μg的蛋白质样品进行分离。分离后将蛋白转移至NC膜上,并用5%脱脂牛奶溶液封闭2 h。将抗体AKT(1∶100 0)、mTOR(1∶100 0)、p-AKT(1∶100 0)、p-mTOR(1∶100 0)、HK(1∶100 0)、PKM(1∶100 0)和GAPDH(1∶200 0)孵育过夜。TBST缓冲液洗涤3次,每次10 min,在室温下与二抗孵育2 h。TBST缓冲液洗涤3次后加入ECL化学发光试剂,使用Tanon 4800 Multi成像系统分析蛋白表达水平。
1.3.9 分子对接 采用ChemDraw 19.0软件绘制岩藻黄质化学结构式,进一步应用Chem3D 14.0软件将其进行能量最小化处理。在蛋白质数据库(protein data bank,PDB,https://www.Rcsb.Org/)检索AKT蛋白(PDB ID:3MVH),保存为pdb格式,通过Pymol 2.5.2对蛋白结构删除水分子、去除修饰配体,再使用AutoDock Tools 1.5.7将岩藻黄质和AKT蛋白转换为pdbqt格式,并进行分子对接[16]。通过LigPlus 2.5.5分析配体与蛋白的氢键、疏水作用力等。
1.4 数据处理
各组数据以均值±标准差表示,采用SPSS 14.0中ANOVA模块对试验数据进行方差分析,P<0.05代表差异具有统计学意义,各组试验至少重复3次。
2 结果与分析
2.1 岩藻黄质对CEM/C1细胞活力的影响
采用MTT法检测岩藻黄质对CEM/C1细胞的细胞毒性作用,结果如图2所示。与对照组比较,不同浓度(0、1、2、3、4、5、6、7、8、9、10 μg·mL-1)的岩藻黄质处理CEM/C1细胞8、16、24 h后,细胞活力均降低,呈时间和剂量依赖性。当岩藻黄质浓度低于3 μg·mL-1作用8、16 h时,细胞活力高于90%。3 μg·mL-1的岩藻黄质作用24 h后,细胞活力明显受到抑制。作用24 h后,随着岩藻黄质浓度的增加,细胞活力呈剂量依赖性下降,其IC50值为6.48 μg·mL-1。根据试验结果,选择2.5、5.0、7.5 μg·mL-1的剂量进行岩藻黄质处理,处理时间为24 h。

图2 岩藻黄质对CEM/C1细胞活力的影响Fig.2 Effect of Fucoxanthin on the viability of CEM/C1 cells
2.2 岩藻黄质对CEM/C1细胞早期和晚期凋亡的影响
如图3-A所示,对照组CEM/C1细胞凋亡率为10.92%。当岩藻黄质浓度为2.5 μg·mL-1时,CEM/C1细胞的凋亡率增加至14.69%;当浓度为5 μg·mL-1时,CEM/C1细胞的凋亡率明显升高至25.20%;随着岩藻黄质浓度的升高,CEM/C1细胞的凋亡率持续升高,在浓度为7.5 μg·mL-1时达到39.90%。如图3-B~D所示,随着岩藻黄质浓度的增加,CEM/C1细胞的凋亡率、早期凋亡率和晚期凋亡率均增加。这些结果表明,岩藻黄质能有效地促进CEM/C1细胞的凋亡,与MTT试验结果相符合。
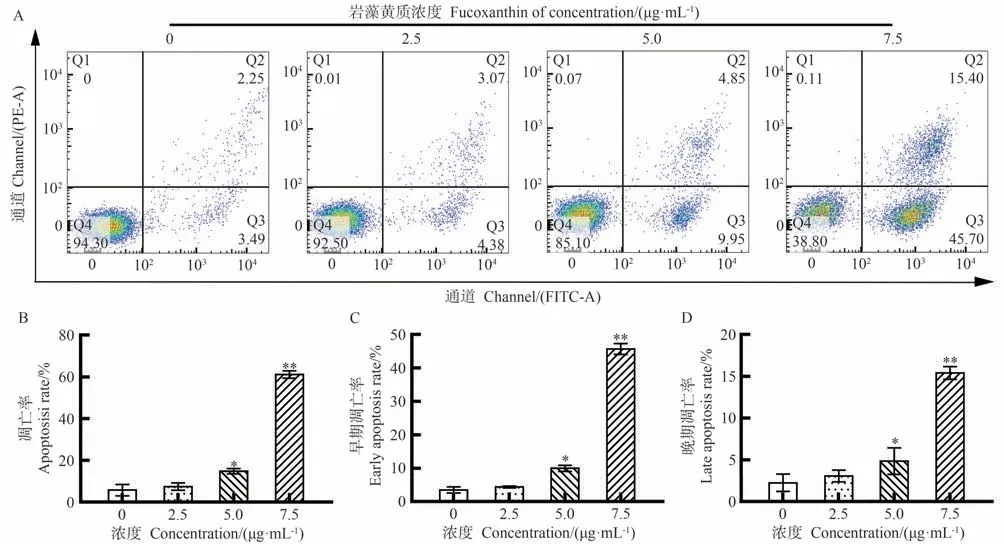
图3 岩藻黄质对CEM/C1细胞凋亡率的影响Fig.3 Effects of Fucoxanthin on apoptosis of CEM/C1 cells
2.3 岩藻黄质对CEM/C1细胞周期的影响
如图4-A所示,岩藻黄质将CEM/C1细胞周期阻滞于S期。如图4-B~D所示,当岩藻黄质浓度高于5 μg·mL-1时处于S期的CEM/C1细胞数量显著或极显著增加(P<0.05),当岩藻黄质浓度高于7.5 μg·mL-1时G1期和G2期细胞比例极显著降低(P<0.01)。在7.5 μg·mL-1岩藻黄质浓度下,CEM/C1细胞处于S期的细胞比例高达64.52%。

图4 岩藻黄质对CEM/C1细胞周期的影响Fig.4 Effect of fucoxanthin on CEM/C1 cell cycle
2.4 岩藻黄质对CEM/C1细胞的葡萄糖摄取、乳酸生成和ATP生成的影响
与对照组相比,当岩藻黄质浓度高于2.5 μg·mL-1时岩藻黄质显著或极显著抑制CEM/C1细胞的葡萄糖摄取、ATP生成和乳酸生成(P<0.05、P<0.01),呈剂量依赖性(图5-A~C)。该结果为岩藻黄质参与CEM/C1细胞糖酵解途径的调节作用提供了有力证据。

图5 岩藻黄质对CEM/C1细胞葡萄糖摄取、乳酸生成量以及ATP生成量的影响Fig.5 Effect of Fucoxanthin on glucose uptake,lactate production and ATP production in CEM/C1 cells
2.5 岩藻黄质对CEM/C1细胞中糖酵解相关酶的表达和活性的影响
岩藻黄质对CEM/C1细胞中糖酵解相关酶活性的影响如图6所示。随着岩藻黄质浓度升高,HK和PK的活性逐渐降低。与对照组相比,2.5 μg·mL-1岩藻黄质处理24 h后,HK和PK的活性均显著降低(P<0.05)。此外,岩藻黄质对HK和PK活性的抑制作用呈剂量依赖性。这些结果表明,岩藻黄质能够有效抑制CEM/C1细胞中糖酵解相关酶的活性。

图6 岩藻黄质对CEM/C1细胞HK、PK活性的影响Fig.6 Effect of Fucoxanthin on activities of HK and PK in CEM/C1 cells
2.6 岩藻黄质对CEM/C1细胞中AKT/mTOR信号通路激活及糖酵解相关基因表达的影响
采用qRT-PCR检测CEM/C1细胞中凋亡相关基因的mRNA水平,结果见图7-A、B。抗凋亡基因AKT、mTOR随岩藻黄质浓度的增加无明显变化(P>0.05)。由图7-C、D可知,与对照组相比,5 μg·mL-1以上岩藻黄质处理组中糖酵解相关酶HK基因表达水平显著或极显著降低(P<0.05、P<0.01),2.5 μg·mL-1以上岩藻黄质处理组中糖酵解相关酶PKM的基因表达水平显著或极显著降低(P<0.05、P<0.01),说明岩藻黄质可以抑制糖酵解相关酶基因的表达。

图7 岩藻黄质对CEM/C1细胞中AKT/mTOR 信号通路和糖酵解相关基因表达的影响Fig.7 Effect of Fucoxanthin on expressions of AKT/mTOR signaling pathway and glycolysis-related genes in CEM/C1 cells
2.7 岩藻黄质对CEM/C1细胞中AKT/mTOR信号通路激活及糖酵解相关蛋白表达的影响
为进一步探索岩藻黄质调控CEM/C1细胞糖酵解的机制,试验检测了糖酵解相关蛋白的表达。蛋白AKT和mTOR的相对表达量随岩藻黄质浓度的增加无明显变化(图8-B、D);当岩藻黄质浓度为7.5 μg·mL-1时,p-AKT蛋白的相对表达量极显著降低(P<0.01,图8-C);当岩藻黄质浓度为7.5 μg·mL-1时,p-mTOR蛋白的相对表达水平极显著降低(P<0.01,图8-E)。上述结果表明,岩藻黄质抑制了CEM/C1细胞中AKT/mTOR信号通路的激活。当岩藻黄质浓度为5 μg·mL-1时,糖酵解相关蛋白HK的相对表达量显著降低(P<0.05,图8-F)。如图8-G所示,当岩藻黄质浓度为2.5 μg·mL-1时,糖酵解相关蛋白PKM的相对表达水平显著降低(P<0.05),表明岩藻黄质可通过AKT/mTOR信号级联调控CEM/C1细胞的糖酵解通路。

图8 岩藻黄质对CEM/C1细胞中AKT/mTOR 信号通路和糖酵解相关蛋白表达的影响Fig.8 Effect of Fucoxanthin on expressions of AKT/mTOR signaling pathway and glycolysis-related proteins in CEM/C1 cells
2.8 分子对接验证
为了进步一探索岩藻黄质与目标蛋白之间的关系,试验进行了岩藻黄质与AKT的分子对接模拟。通过Pymol 2.1软件对岩藻黄质-AKT蛋白进行可视化,得到强制模式,可以清晰看到结合位点上相互作用的氨基酸残基。分子对接结果如图9显示,岩藻黄质与AKT蛋白之间的结合能小于-5.01 kcal·mol-1,与mTOR蛋白之间的结合能小于-5.53 kcal·mol-1,表明结合效率较高。AKT上的关键活性位点残基主要包括LEU295、GLY294、SER7以及AGR4等,mTOR的关键活性位点残基主要包含GLN1627、HIS2401以及ILE2398等。此外,岩藻黄质可以与氢键距离较短的残基形成强氢键(约1.9 Å),使岩藻黄质与AKT和mTOR蛋白形成稳定的复合物。

图9 岩藻黄质与AKT以及mTOR蛋白的分子对接结果Fig.9 Molecular docking results of Fucoxanthin with AKT and mTOR protein
3 讨论
由于缺乏有效的治疗方法,癌症已成为第二大死亡原因[17]。严重的副作用和化疗耐药性是限制当前化疗的主要问题[18],而天然物质因具有较少的副作用和更强的药理学特性,成为制药行业的宝贵资源[19]。目前岩藻黄质的最主要来源依旧是海藻[20],其因具有抗氧化、抗炎、抗肿瘤、减肥等药理作用,已成为药物研究与开发的热点之一[21-23]。本研究通过MMT试验发现,岩藻黄质对CEM/C1细胞的活性表现出时间和剂量依赖性的抑制作用,说明岩藻黄质可以降低急性淋巴白血病细胞活力。岩藻黄质是一种新型潜在抗癌药物,可以通过多种途径抑制肿瘤发展。Calabrone等[24]发现岩藻黄质具有抑制前列腺癌细胞生长和阻碍内皮细胞形成血管网络的能力。Wang等[25]观察到岩藻黄质有效抑制炎症因子诱导的细胞粘附分子(cell adhesion molecules,CAMs)的表达,从而减少MCF-7细胞与内皮细胞之间的粘附。此外,岩藻黄质还可以提高非小细胞肺癌对吉非替尼敏感性从而达到抗肿瘤的作用[26]。目前系统研究岩藻黄质促进急性淋巴白血病细胞凋亡作用的报道较少,本研究流式细胞术结果显示,岩藻黄质在CEM/C1细胞中诱导凋亡并将细胞周期阻滞于S期。Fang等[27]证明了岩藻黄质能够阻滞非小细胞肺癌细胞周期在G0/G1期从而抑制其增殖、迁移和侵袭。这与本研究结果不同,说明岩藻黄质促进CEM/C1细胞凋亡的机制尚不清楚,因此在后续研究中进行了进一步探索。
通过无氧糖酵解和增加的葡萄糖摄取是肿瘤组织葡萄糖代谢的重要特征。虽然氧化磷酸化在产生净ATP方面效率高于无氧糖酵解,但无氧糖酵解能快速提供能量,从而满足肿瘤细胞快速增殖的能量需求[28]。治疗癌症的有效方法之一是抑制肿瘤细胞的能量代谢,但仍然面临巨大挑战。Qi等[29]发现,电刺激诱导线粒体功能障碍,阻碍电子传递链和糖酵解途径,导致能量供应危机和癌细胞死亡。此外,肿瘤细胞通过增加葡萄糖摄取来促进糖酵解途径。本研究发现岩藻黄质能够显著减少CEM/C1细胞的葡萄糖摄取、ATP生成和乳酸产生。低水平的糖酵解难以为肿瘤细胞的无限增殖提供能量,而这个过程中产生的中间产物也成为遏制肿瘤生长的因素。糖酵解途径中关键酶的表达水平或活性的增加是肿瘤细胞异常活动的主要原因之一[30]。本研究发现岩藻黄质能够降低HK酶活性和HK蛋白的表达水平,HK催化己糖第六位羟基的磷酸化反应,是糖酵解的第一步,在各种癌症中呈异常表达[31]。Li等[32]发现,microRNA-let-7b-5p(let-7b-5p)通过与HK2 mRNA的3'非翻译区相互作用,对HK2的表达产生抑制作用。通过抑制HK2介导的无氧糖酵解,let-7b-5p有效限制了乳腺肿瘤的生长和转移,在体外和体内试验中都得到证实,这与本研究结果一致。与此同时,在不同浓度的岩藻黄质干预后,CEM/C1细胞中糖酵解相关蛋白PK的表达水平显著降低,PK酶活力也显著降低。PK酶是糖酵解过程中的主要限速酶之一,临床发现在髓性白血病人血清中PK总活性明显增高,这种酶在宫颈癌、淋巴肉瘤和髓性白血病等肿瘤的进展中起着关键作用[33]。综上所述,岩藻黄质可以通过抑制糖酵解途径,阻断肿瘤细胞能量供应,诱导细胞周期阻滞,从而有效促进肿瘤细胞的凋亡。
研究发现,AKT/mTOR信号通路是细胞过程中细胞对环境信号反应的重要调节因子,可以控制细胞的糖酵解代谢。AKT可以通过提高葡萄糖转运体的膜转位和表达,以及通过磷酸化糖酵解关键的酶来调节糖酵解的进程,因此AKT也是肿瘤细胞糖酵解表型的重要推动因子[34]。磷酸化的磷脂酰肌醇-3-激酶可以激活AKT,磷酸化的AKT是mTOR信号通路的重要上游调控者,mTOR在细胞内存在两种不同的蛋白复合物分别为mTORC1和mTORC2。研究报道,mTORC1主要由mTOR、mLST8和Raptor组成,是调节糖酵解过程的核心蛋白复合物[35]。本研究的结果表明,岩藻黄质能够降低CEM/C1细胞中AKT/mTOR通路中p-AKT和p-mTOR蛋白的表达水平。Triptolide(TP)的治疗显示出显著的剂量和时间依赖性抑制ICC细胞的增殖和糖酵解。随后的分析揭示了TP通过靶向AKT/mTOR信号通路对ICC细胞糖酵解的抑制作用[36],与本研究结果一致。明加雄[37]证明了海带提取物岩藻黄质可以一直肺癌转移,其作用机制可能与调控PI3K/AKT/NFκB信号通路,抑制人肺癌细胞的上皮-间质转化有关。因此,本研究认为岩藻黄质可能通过AKT/mTOR信号通路对CEM/C1细胞的糖酵解途径产生调节作用。为了进一步阐明岩藻黄质对AKT和mTOR蛋白的作用机制,通过分子对接模拟发现,岩藻黄质与AKT和mTOR蛋白具有较强的结合能力,因岩藻黄质与AKT和mTOR蛋白残基形成较强相互作用的氢键,而氢键距离较短,故使络合物之间能够稳定结合。
4 结论
岩藻黄质可能通过抑制AKT/mTOR信号通路阻断肿瘤细胞糖酵解,降低肿瘤细胞能量供应,并将CEM/C1细胞周期阻滞于S期,从而促进CEM/C1细胞凋亡。需进一步进行体内试验探讨岩藻黄质的作用机制,为开发岩藻黄质作为急性淋巴细胞白血病的潜在治疗剂提供科学依据。
