高选择性部分氧化催化剂Au-Pd/TiO2-SiO2的设计合成与苯甲醇部分氧化反应
2024-04-12吴萍萍舒洁王悦张永辉赵联明白鹏
吴萍萍 舒洁 王悦 张永辉 赵联明 白鹏

摘要 :贵金属纳米催化剂在苯甲醇部分氧化制备苯甲醛过程中具有较高的反应活性,产物苯甲醛选择性较低。采用一锅法制备TiO 2改性的Au-Pd/TiO 2-SiO 2纳米合金催化剂并用于苯甲醇部分氧化反应。对催化剂结构表征关联反应进行评价。结果表明:少量TiO 2的引入会改善贵金属纳米颗粒在载体表面的分散度,调变了金钯合金表面的电子结构,提高反应活性,并显著提高载体表面Lewis酸位的数量,从而大幅提高苯甲醛选择性;大量TiO 2的引入会导致金钯合金程度降低,产生大量的Bronsted酸位,使得反应活性和产物选择性都大幅降低。
关键词 :贵金属纳米催化剂; 部分氧化; 表面酸性; 助剂效应
中图分类号 :O 646.7 文献标志码 :A
引用格式 :吴萍萍,舒洁,王悦,等.高选择性部分氧化催化剂Au-Pd/TiO 2-SiO 2的设计合成与苯甲醇部分氧化反应[J].中国石油大学学报(自然科学版),2024,48(1):189-196.
WU Pingping, SHU Jie, WANG Yue, et al. Design and synthesis of Au-Pd/TiO 2-SiO 2 catalyst with high selectivity for partial oxidation of benzyl alcohol[J]. Journal of China University of Petroleum(Edition of Natural Science),2024,48(1):189-196.
Design and synthesis of Au-Pd/TiO 2-SiO 2 catalyst with high selectivity for partial oxidation of benzyl alcohol
WU Pingping 1, SHU Jie 1, WANG Yue 1, ZHANG Yonghui 1, ZHAO Lianming 2, BAI Peng 1
(1.School of Chemistry and Chemical Engineering in China University of Petroleum (East China), Qingdao 266580, China;
2.School of Material Science and Engineering in China University of Petroleum (East China), Qingdao 266580, China)
Abstract : Noble metal nanoparticle catalysts exhibit high catalytic activity in the partial oxidation of benzyl alcohol to benzaldehyde. However, the selectivity of benzaldehyde is low. TiO 2 modified Au-Pd/TiO 2-SiO 2 nano alloy catalysts were prepared by a one pot method and applied for benzyl alcohol partial oxidation. It is found that the introduction of a small amount of TiO 2 increases the metal dispersion on the support surface, and modifies the electronic structure of the Au-Pd alloy surface, and improves the reaction activity. Also, the number of Lewis acid sites on the support surface are increased, which improves benzaldehyde selectivity. However, the introduction of a large amount of TiO 2 destroys the alloying of Au-Pd and produces a large number of Bronsted acid sites, which greatly reduces the reaction activity and product selectivity.
Keywords : noble metal nano-catalyst; partial oxidation; surface acidity; promoter effect
苯甲醇部分氧化反應产物苯甲醛是一种重要的有机化工原料 [1-2] 。传统的苯甲醛制备方法有氯化苄水解法 [3] 和甲苯氧化法 [4] 。苯甲醇液相氧化制苯甲醛越来越引起人们的重视,其中高效催化剂的设计至关重要。江勤等 [5-7] 发现负载型贵金属纳米催化剂在苯甲醇部分氧化反应中表现出良好的活性。Verma等 [8] 采用浸渍法将纳米金负载到不同形貌的二氧化钛载体上,发现纳米棒状催化剂上苯甲醛的产率达到33%,优化反应条件后产率可以提升到55%。Hou等 [9] 以聚乙烯吡咯烷酮(PVP)为保护剂制备金、钯和金钯合金纳米催化剂,其中金钯合金纳米催化剂对苯甲醇具有良好的催化活性,当金钯物质的量比为1∶3时,催化剂对苯甲醇氧化反应效果最佳,证明金与钯之间存在协同效应。Wu等 [10] 研究发现当金钯物质的量比为1∶3时,二氧化硅负载的Au-Pd双金属催化剂上苯甲醇转化率大于95%,但苯甲醛选择性较差(约为60%)。在苯酚加氢制备环己酮过程中,催化剂上的Lewis酸(L酸)性位和C O基团之间的酸碱相互作用可以阻止生成的环己酮进一步氢化,从而提高了环己酮的选择性 [11] 。Pineda [12-13] 等发现苯甲醛的选择性与催化剂表面的L酸位数量成正比 [13] 。TiO 2作为催化剂 [14] 或催化剂载体在光催化领域应用广泛,TiO 2负载的Au-Pd纳米催化剂在光催化氧化中表现出较好的催化剂活性 [6] ,同时TiO 2的引入可以调变Pd/SiO 2催化剂表面性质 [15] 。笔者以TiO 2为助剂,设计一种富L酸位的负载型Au-Pd催化剂,通过一锅法合成TiO 2修饰的负载型Au-Pd/TiO 2-SiO 2催化剂用于苯甲醇部分氧化反应,探究TiO 2含量对催化剂结构性能的影响,关联苯甲醇氧化反应结果,研究TiO 2改性对催化剂催化苯甲醇部分氧化反应的影响机制。
1 试 验
1.1 试验试剂
乙醇、硅酸四乙酯、钛酸四乙酯,国药集团化学试剂有限公司;氯化钯、(3-巯基丙基)三甲氧基硅烷(MPTMS)、氯金酸,阿拉丁试剂有限公司。
1.2 催化剂的制备
通过一锅法制备TiO 2改性的Au-Pd/TiO 2-SiO 2催化剂。取一定量的硅酸四乙酯(TEOS)和钛酸四乙酯(TEOT)室温下混合搅拌均匀并放入0 ℃冰浴中,向混合液中滴加一定量的25% TEAOH和去离子水(滴加时间未0.5~1 h)并搅拌反应1 h。将反应混合物转移到油浴中升温至80 ℃加热1~2 h,然后升温至90 ℃回流搅拌18 h。后依次加入少量的MPTMS,一定量的0.02 mol/L PdCl 2溶液和0.02 mol/L的HAuCl 4溶液,继续回流搅拌6 h。反应所得混合物在170 ℃下晶化8 h,抽滤洗涤后,在110 ℃下干燥过夜,所得固体粉末在马弗炉中以2 ℃/min 升温速率升温至500 ℃煅烧5 h,待催化剂冷却至室温,在氢气气氛下,以5 ℃/min升温至400 ℃还原2 h,即得到催化剂Au-Pd/TiO 2-SiO 2。考察 n (TiO 2)/ n (SiO 2)分别为0、0.016、0.032和0.048时对催化剂性能的影响,因此催化剂标记为Au-Pd/TiO 2-SiO 2-0(简称为a)、Au-Pd/TiO 2-SiO 2-0.016(简称为b)、Au-Pd/TiO 2-SiO 2-0.032(简称为c)、Au-Pd/TiO 2-SiO 2-0.048(简称为d)。
1.3 催化剂表征
采用荷兰帕纳科公司的X' Pert Pro MPD型多晶粉末X射线衍射仪对催化剂的晶体结构进行表征。采用Cu、Kα射线为衍射源,波长为 0.154 nm,电压和电流分别为40 kV和40 mA,扫描角度为10°~75°,扫描速度为2°/min。催化剂的外观形貌采用JSM-7900F扫描电子显微镜进行分析。显微镜分辨率为15 kV(1.0 nm)和1 kV(2.0 nm);加速电压为0.5~30 kV;放大倍数为30×800 000。电感耦合等离子体光发射光谱法(ICP-OES VISTA-MPX Varian系统)用于测量催化剂中准确的金属负载量(Au、Pd和Ti)。
催化剂的比表面积、孔容和孔径分布采用TriStar 3000型多功能吸附仪(美国麦克Micrometrics公司)进行分析。测试前,将样品置于300 ℃、真空环境下脱气4~6 h。以液氮为介质,在77 K下对氮气进行吸附、脱附,记录相对压力为0.01~0.998的吸附等温线。采用Brunauer-Emmett-Teller(BET)法计算样品的比表面积,孔径分布采用Barrett-Joyner-Halenda(BJH)法进行计算,采用相对压力为0.998的数据计算催化剂的孔容。固体紫外漫反射采用耶拿生产的SPECORD plus210紫外光谱仪分析。以硫酸钡为背景和稀释剂,测试范围为200~800 nm,扫描速度为2 nm/min。
采用吸附吡啶的红外光谱仪Nicolet 6700对催化剂的表面酸碱性进行定性分析。红外光谱仪配备的MCT检测器和KBr分光器利用液氮进行冷却。测试的扫描次数为64,分辨率为4 cm -1 。测试步骤:待测样品在300 ℃下真空预处理3 h,然后放在装有吡啶的干燥器中在抽真空的状态下吸附1 h,关泵后继续吸附24 h。最后将吸附了吡啶的样品置于150 ℃真空处理3 h脱除物理吸附的吡啶,空白对照样品也要在300 ℃下真空预处理3 h除去水分。
扫描透射电子显微镜(STEM)-高角度环形暗场(HAADF)图像和X射线能量色散谱(XEDS)在JEOL JEM-2100F上获得,加速电压为200 kV,用于分析双金属纳米颗粒的粒径和元素分布。采用赛默飞世尔科技公司生产的K-Alpha X射线光谱仪分析催化剂表面物种的化学状态。以Al电极为阳极,电子动能为1 486.6 eV。以C 1s结合能(284.5 eV)为内标对谱图进行校准。
1.4 催化剂活性评价
苯甲醇氧化反应在配有聚四氟乙烯内衬的100 mL反应釜(SLM100,北京Easychem科技发展公司)中进行。操作步骤:称取10.8 g苯甲醇加入到反应釜中,并加入50 mg催化剂。安装好后检查气密性,以0.1 MPa的O 2连续吹扫4次后保持釜内O 2压力为0.2 MPa。反应釜升温至110 ℃,氧气压力保持在0.8 MPa,转速为800 r/min下恒温反应2 h。反应结束后,将反应釜置于冷水中冷却,待温度降至低于30 ℃,打开反应釜加入20 mL乙醇溶解所有产物,使用带过滤器的取样器取液体样品进行分析,催化剂过滤回收以备循环反应使用。采用配有氢火焰离子化检测器(FID)的气相色谱(Agilent 6870)和DB-1柱(30×0.32×0.25)对反应产物进行分析,以十二醇做内标物,选用内标法分析苯甲醇氧化产物。
苯甲醇的转化率计算公式为 X t BA = (n 0 BA -n t BA )/n 0 BA 。式中,n 0 BA 为反应器中初始的苯甲醇的物质的量;n t BA 为反应时间t后反应器中苯甲醇的物质的量。
产物的选择性计算公式为S t B =n t B N j/((n 0 BA -n t BA )N BA )。式中,n t B 为反应时间t后某种产物 B 的物質的量;N j为产物 B 的碳原子数;N BA 为反应物苯甲醇的碳原子数,N BA =6。
1.5 理论计算
计算在Materials Studio的Dmol 3模块中完成。采用自旋非限制的广义梯度近似Perdew-Burke-Ernzerhof(PBE)泛函方法。通过Grimme的PBE-D2方法考虑长程色散力。金属离子核用密度泛函理论半核赝势(DSSP)来描述,而对于价电子函数则用双数值加极化(DNP)基组表示。能量、位移和梯度收敛的公差分别设置为1.0×10 -5 Ha、2.0 × 10 -3 Ha/和 5×10 -3 。
A n B m合金的形成能E f 计算公式为E f = [E( A n B m) -nE ( A ) - mE( B )]/(n+m)。式中, E( A n B m) 为 A n B m合金的能量;n和m分别为合金中 A和B金属原子的个数; E( A)为体相单质中单个A金属原子的能量; E( B)体相单质中单个B金属原子的能量。
2 结果分析
2.1 催化剂孔结构
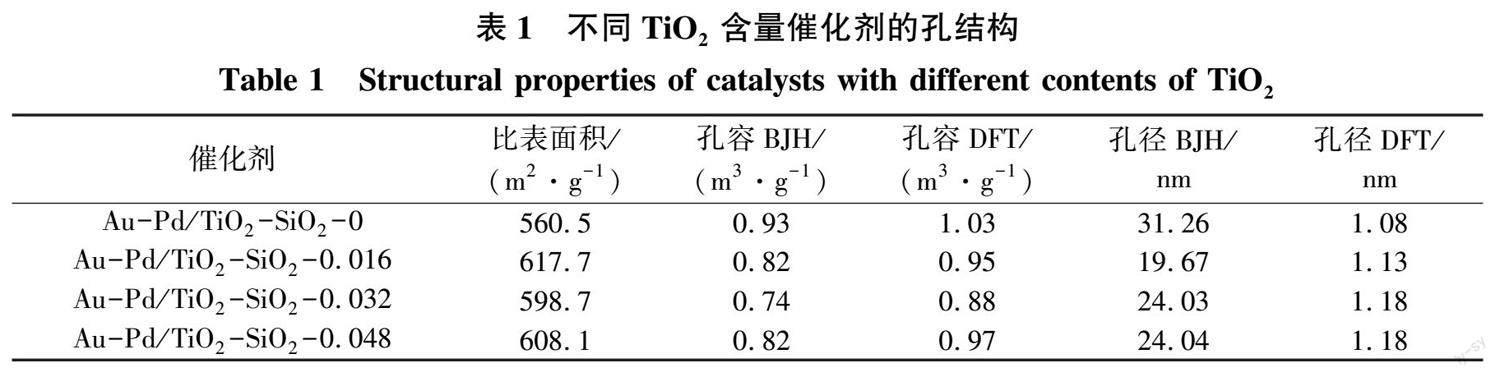
不同TiO 2含量催化剂的N 2吸附-脱附曲线和孔径分布见图1。不同TiO 2含量催化剂的孔结构数据见表1。
由图1看出,不同TiO 2含量催化剂的N 2吸附-脱附曲线为Ⅳ型等温线,滞后回环为H-3型,催化剂孔道为狭缝孔。由孔径分布曲线看出催化剂孔结构为介微复合的结构,TiO 2的引入对催化剂的介微复合的孔结构无明显影响。纯硅负载的催化剂在介孔范围内有较宽的分布,而加入TiO 2的样品在较低的介孔范围内的分布相对集中,随着TiO 2的含量继续增加,孔径分布范围逐渐增大。从表1数据可见TiO 2的引入使得催化剂的比表面积有一定程度的升高,孔容变化不大,孔径分布相对集中。
2.2 催化剂晶体结构分析
不同TiO 2含量催化剂的XRD谱图见图2(a)。可以看出,所合成催化剂上均未观察到Au和Pd的衍射峰(Au的衍射角2 θ 为38.25°、44.46°、64.69°;Pd的衍射角2 θ 为46.6°、68.1°),表明一锅法所制得的Au-Pd/TiO 2-SiO 2催化剂中金属Au和Pd的纳米颗粒分布较为均匀。XRD谱图中也没有明显的TiO 2的衍射峰,只有一个无定型的SiO 2的鼓包峰,且随着 n (TiO 2)/ n (SiO 2)的增加,SiO 2的衍射峰强度有所降低,表明Si与Ti间存在一定的相互作用。图2(b)为不同TiO 2含量催化剂的固体紫外光谱。可以看出,纯Au催化剂在522 nm出现金纳米颗粒的表面等离子体共振峰,而Au-Pd/TiO 2-SiO 2催化剂上这一振动峰消失,表明一步法合成了 TiO 2- SiO 2负载的金钯纳米合金催化剂。
XRD分析表明Au-Pd/TiO 2-SiO 2催化剂上未看到明显的晶体衍射峰,因此采取透射电镜(TEM)对催化剂的晶体结构进行进一步的解析,以催化剂Au-Pd/TiO 2-SiO 2-0.016为例。从图2(c)可以看出,催化剂Au-Pd/TiO 2-SiO 2-0.016上金钯纳米颗粒(深黑色圆点)均匀分散在钛硅载体上,钛硅载体为直径在100~200 nm的簇状结构。进一步放大可以清晰地看到钛硅载体的晶格,表明所合成催化剂的为金钯纳米合金负载在纳米级分散的钛硅分子筛上,而不是无定型的TiO 2-SiO 2。XRD谱图上没有检测到钛硅分子筛的晶相衍射峰主要是由于所合成的为纳米级的钛硅分子筛,颗粒粒径较小且钛硅之间存在一定的相互作用。
2.3 催化剂表面酸性
不同TiO 2含量催化剂的吡啶吸附红外光谱图见图3。酸量和酸强度数据见表2。可以看出,吡啶吸附红外光谱图中1 450 cm -1 处为吡啶在L酸位的吸附特征峰,1 540 cm -1 处为吡啶在B酸位的吸附特征峰,
with different amount of TiO 2 而1 490 cm -1 处为吡啶与L酸和B酸共同作用的吸收峰。从图3看到所有Au-Pd/TiO 2-SiO 2催化剂上,无论是否引入TiO 2,都存在明显的L酸位的吡啶吸附特征峰(1 447、1 577、1 596和 1 614 cm -1 ),且随着TiO 2的引入,总酸量明显增加(表2)。催化剂Au-Pd/TiO 2-SiO 2-0上几乎不存在吡啶在B酸位上的吸附特征峰(1 540 cm -1 ),随着TiO 2含量的增加,催化剂Au-Pd/TiO 2-SiO 2-0.016上存在少量B酸位,催化剂Au-Pd/TiO 2-SiO 2-0.032和Au-Pd/TiO 2-SiO 2-0.048上检测到明显的B酸位的吡啶吸附特征峰,同时1 490 cm -1 处为吡啶与L酸和B酸共同作用的吸收峰也明显增强。说明催化剂Au-Pd/TiO 2-SiO 2-0和Au-Pd/TiO 2-SiO 2-0.016上以L酸位为主,而催化剂Au-Pd/TiO 2-SiO 2-0.032和Au-Pd/TiO 2-SiO 2-0.048上同时存在B酸位和L酸位,且B酸量随着TiO 2含量的增加而增加。吡啶吸附红外光谱分析可以发现,少量TiO 2的引入,催化剂Au-Pd/TiO 2-SiO 2-0.016上酸量的增加主要来自于L酸位的增加(表2),而当TiO 2含量进一步增加时,催化剂Au-Pd/TiO 2-SiO 2-0.032和Au-Pd/TiO 2-SiO 2-0.048上酸量的增加同時来源于B酸位和L酸位的增加。
2.4 贵金属纳米颗粒表界面
贵金属纳米颗粒在钛硅分子筛上的分布通过透射电镜(TEM)进行分析,结果见图4,其中(a)~(c)为催化剂a、b和c的TEM谱图, (d)~(i)为催化剂b的EDS元素分布。可以看出,Au-Pd纳米颗粒均匀地分布在钛硅分子筛上,颗粒分布在2~5 nm。少量TiO 2的引入一定程度上加强了Au-Pd纳米颗粒的分散,但进一步增加TiO 2的加入量,纳米颗粒的粒径变化不明显,说明TiO 2的引入对Au-Pd纳米颗粒的分散度影响不大。从元素分布图上可以看出金钯元素的分布一致,说明形成了很好的金钯合金,且Ti元素均匀分布于整个催化剂载体,说明形成了 钛硅分子筛,而不是TiO 2和SiO 2的混合物,这与 图1给出的TEM分析结果一致。
不同TiO 2含量Au-Pd/TiO 2-SiO 2催化剂上各元素的X射线光电子谱图见图5。催化剂上各元素实测含量与结合能变化见表3。
可以看出:催化剂Au-Pd/TiO 2-SiO 2-0中Au 4f 7/2 的结合能为83.2 eV,表明Au元素以Au δ - 状态存在(Au 0 的结合能为84.0 eV) [16] ,而该催化剂上部分Pd以Pd 2+ 状态存在,表明一步法合成过程中金钯间存在电子转移,钯上的部分电子转移给金,形成了Au-Pd合金结构;引入TiO 2后Au 4f 7/2 的结合能向高的结合能方向移动(83.6 eV),表明引入Ti后金物种(Au δ - )失去电子;随着TiO 2的引入和含量的增加,还原态的Pd 0 的比例明显增加,氧化态的Pd 2+ 比例大大下降, 说明引入Ti后Pd物种得到电子;Ti和Si分别以Ti 4+ 和Si 4+ 的状态存在,随着TiO 2含量增加,Ti 4+ 上的电子结合能向低结合能方向移动(从461.0到460.7 eV),Si物种上几乎没有电子转移。以上结果说明TiO 2的引入使得金钯的合金程度降低,这可能是由于添加过多的TiO 2与Pd表面强烈相互作用减弱了Au和Pd之间的相互作用 [15] 。
2.5 催化性能评价与构效关系
不同TiO 2含量催化剂上苯甲醇部分氧化反应数据见表4。可以看出,未引入TiO 2的催化剂Au-Pd/TiO 2-SiO 2-0上,苯甲醇转化率较高(85.1%),但产物苯甲醛选择性较差(60.9%)。引入少量TiO 2后,催化剂Au-Pd/TiO 2-SiO 2-0.016上苯甲醇转化率略微提高(88.2%),但有用产物苯甲醛的选择性大幅提高(93.3%),苯甲醛产率高达82.3%。随着TiO 2含量进一步增加,催化剂Au-Pd/TiO 2-SiO 2-0.032和Au-Pd/TiO 2-SiO 2-0.048上苯甲醇的转化率和苯甲醛的选择性均呈现降低的趋势。
不同TiO 2含量催化剂上苯甲醇部分氧化反应性能与催化剂结构以及贵金属纳米合金颗粒的表界面性质密切相关。XRD、固体紫外和TEM结果证明通过一步法合成了钛硅分子筛负载的金钯纳米合金催化剂。Wu等 [10,17-18] 认为金钯纳米合金催化剂的活性与合金程度密切相关,而合适的 n (Pd 0 )/ n (Pd 2+ ) 比例直接决定金钯纳米合金表面对O 2分子的活化。Au-Pd/TiO 2-SiO 2-0和Au-Pd/TiO 2-SiO 2-0.016催化剂上苯甲醇转化率较高(大于85%),主要是由Au-Pd合金程度和 n (Pd 0 )/ n (Pd 2+ ) 决定的,Wu等 [10] 研究表明 n (Au)/ n (Pd)为1/3、 n (Pd 0 )/ n (Pd 2+ )约等于1时,金钯合金催化剂的活性最高,催化剂Au-Pd/TiO 2-SiO 2-0.016上最高的苯甲醇转化率与此结论一致。随着TiO 2含量的增加,苯甲醇转化率大幅度降低,结合XPS表征结果分析,这主要是由于添加过多的Ti物质与 n (Au)/ n (Pd) 表面强烈的相互作用使得金钯的合金程度降低,从而使得催化剂上苯甲醇氧化活性降低。合金界面的构筑对催化剂的性能起到非常关键的作用 [19] ,通过理论计算发现Au-Ti合金形成能为 -0.71 eV ,Pd-Ti合金形成能为-0.74 eV,远高于Au-Pd合金形成能(-0.43 eV),证实了Ti的引入会造成Au-Pd合金程度的降低,这与XPS表征结果一致。
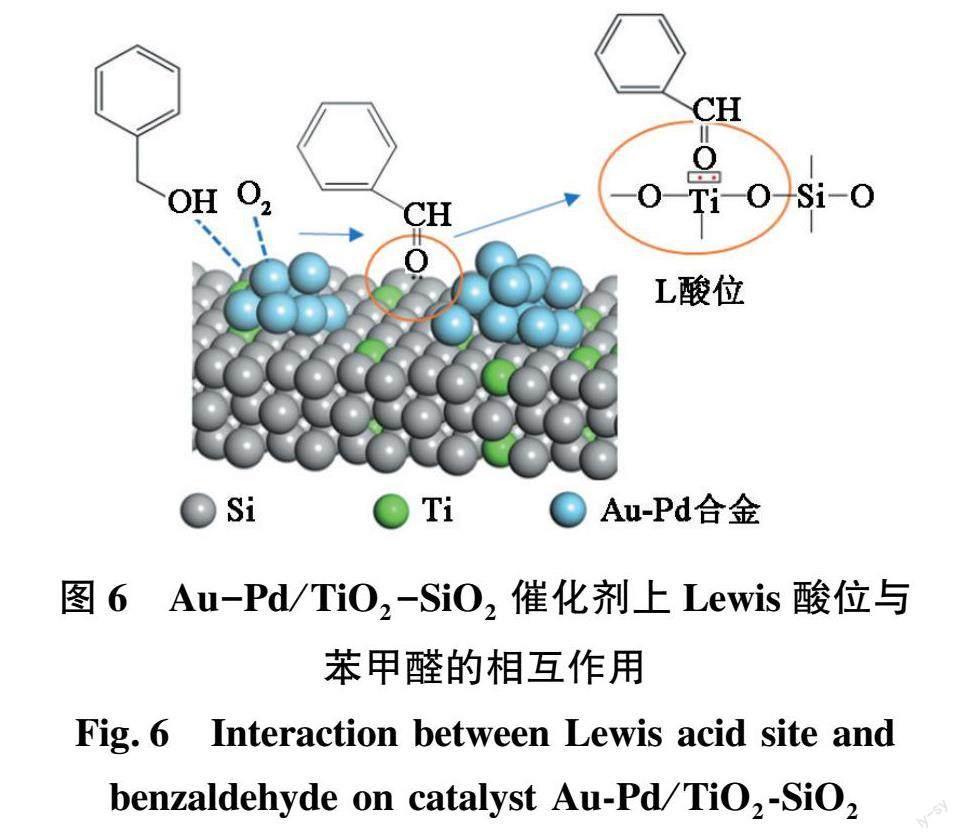
吡啶吸附红外光谱结果表明少量TiO 2的引入,Au-Pd/TiO 2-SiO 2-0.016催化剂上酸量的增加主要来自于L酸位的增加。Liu等 [11-13] 研究表明催化剂表面L酸位对醛有很好的保护作用(图6),可以避免其被深度氧化,因此催化剂Au-Pd/TiO 2-SiO 2-0.016上苯甲醛的选择性高达93.3%。大量TiO 2的加入不仅增加了催化剂表面的L酸位,也增加了B酸位,B酸位不利于产物苯甲醛的保护,因此在催化剂Au-Pd/TiO 2-SiO 2-0.032和Au-Pd/TiO 2-SiO 2-0.048上苯甲醛選择性降低。总的来说少量TiO 2的加入可以通过调变Au-Pd合金上的电子结构改善催化剂活性,通过调变载体的酸碱性提高苯甲醛的选择性。
3 结 论
(1)通过一锅法合成钛硅分子筛负载的金钯纳米合金催化剂。
(2)当 n (TiO 2)/ n (SiO 2)为0.016时,催化剂Au-Pd/TiO 2-SiO 2-0.016上具有最高的苯甲醇转化率(88.2%)和苯甲醛选择性(93.3%)。这主要是因为少量TiO 2的引入改善了贵金属纳米颗粒在载体表面的分散,同时调变了金钯合金表面的电子结构,优化了 n (Pd 0 )/ n (Pd 2+ ),增强了合金表面对O 2的活化能力,提高了反应活性。同时少量TiO 2的引入增加了催化剂Au-Pd/TiO 2-SiO 2-0.016表面L酸位的数量,由于L酸位与C O基间的酸碱相互作用,避免了苯甲醛的进一步被氧化,大大提高了苯甲醛的选择性。而大量TiO 2的引入导致Au-Pd/TiO 2-SiO 2-0.032和Au-Pd/TiO 2-SiO 2-0.048催化剂上金钯合金程度降低,反应活性降低,同时产生了大量吸附强度较高的Bronsted酸位,使得产物选择性大大降低。
(3)Au-Ti和Pd-Ti合金形成能大于Au-Pd合金形成能,證明Ti的引入确实能够削弱Au-Pd间的相互作用,通过调变TiO 2可以有效调变Au-Pd的合金程度和表面电子结构,进而调变催化活性。
参考文献 :
[1] 曹运祥,吴萍萍,马腾腾,等.过渡金属氧化物修饰的金纳米催化剂苯甲醇氧化性能[J].工业催化,2018,26(5):31-35.
CAO Yunxiang, WU Pingping, MA Tengteng, et al. Transition metal oxide promoted gold nanoparticle catalysts for benzyl alcohol oxidation[J]. Industrial Catalysis, 2018,26(5):31-35.
[2] 单风祥.Au-CNT催化剂的制备及其催化苯甲醇氧化反应研究[D].大连:大连理工大学,2021.
DAN Fengxiang. Preparation of Au CNT catalyst and its application in benzyl alcohol oxidation[D]. Dalian: Dalian University of Technology,2021.
[3] ZHU J, WANG P, LU M. Selective oxidation of benzyl alcohol under solvent-free condition with gold nanoparticles encapsulated in metal-organic framework[J]. Applied Catalysis A: General, 2014,477:125-131.
[4] 江勤.苯甲醇氧化脱氢制苯甲醛绿色催化工艺研究[D].杭州:浙江大学,2018.
JIANG Qin. Study on green catalytic process for oxidation of benzyl alcohol to benzaldehyde[D]. Hangzhou: Zhejiang University, 2018.
[5] LIU C, LIN C, CHEN J, et al. SBA-15-supported Pd catalysts: the effect of pretreatment conditions on particle size and its application to benzyl alcohol oxidation[J]. Journal of Catalysis, 2017,350:21-29.
[6] ZHANG X, WANG Z, ZHONG Y, et al. TiO 2 nanorods loaded with AuPt alloy nanoparticles for the photocatalytic oxidation of benzyl alcohol[J]. Journal of Physics and Chemistry of Solids, 2019,126:27-32.
[7] 涂子傲,王伟建.苯甲醇氧化制备苯甲醛负载型催化剂的研究进展[J].安徽化工,2019,45(5):4-7.
TU Ziao, WANG Weijian. Study progress in the preparation of benzaldehyde supported catalysts by oxidation of benzyl alcohol[J]. Anhui Chenical Industry, 2019,45(5):4-7.
[8] VWEMA P, MORI K, KUWAHARA Y, et al. Synthesis of plasmonic gold nanoparticles supported on morphology-controlled TiO 2 for aerobic alcohol oxidation[J]. Catalysis Today, 2020,352:255-261.
[9] HOU W, DEHM N, SCOTT R, Alcohol oxidations in aqueous solutions using Au, Pd and bimetallic AuPd nanoparticle catalysts[J]. Journal of Catalysis, 2008,253(1):22-27.
[10] WU P, CAO Y, ZHAO L, et al. Formation of PdO on Au-Pd bimetallic catalysts and the effect on benzyl alcohol oxidation[J]. Journal of Catalysis, 2019,375:32-43.
[11] LIU H, JIANG T, HAN B, et al. Selective phenol hydrogenation to cyclohexanone over a dual supported Pd-Lewis acid catalyst[J]. Science, 2009,326(5957):1250-1252.
[12] PINEDA A, OJEDA M, ROMERO A, et al. Mechanochemical synthesis of supported cobalt oxide nanoparticles on mesoporous materials as versatile bifunctional catalysts[J]. Microporous and Mesoporous Materials, 2018,272:129-136.
[13] WU P, SONG L, WANG Y, et al. High-performance benzyl alcohol oxidation catalyst: Au-Pd alloy with ZrO 2 as promoter[J]. Applied Surface Science, 2021,537:148059.
[14] 刘欣梅,张新功,耿春香,等.纳米TiO 2的合成与光催化性能[J].中国石油大学学报(自然科学版),2011,35(6):174-178.
LIU Xinmei, ZHANG Xingong, GENG Chunxiang, et al. Synthesis of nano-TiO 2 and its photocatalytic properties[J]. Journal of China University of Petroleum(Edition of Natural Science),2011,35(6):174-178.
[15] LEE D, KIM J, KIM W, et al. Selective hydrogenation of 1,3-butadiene on TiO 2-modified Pd/SiO 2 catalysts[J]. Applied Catalysis A: General, 2003,244(1):83-91.
[16] ZHANG Z, WANG Y, LI X, et al. Synergistic effect on Au-Pd bimetallic catalyst during oxidation of benzyl alcohol to sodium benzoate[J]. Chinese Journal of Catalysis, 2014,35(11):1846-1853.
[17] XIA C, BACK S, RINGE S, et al. Confined local oxygen gas promotes electrochemical water oxidation to hydrogen peroxide[J]. Nature Catalysis, 2020,3(2):1-10.
[18] ZHANG Y, ZHANG J, ZHANG B, et al. Boosting the catalysis of gold by O 2 activation at Au-SiO 2 interface[J]. Nature Communications, 2020,11(1):1-10.
[19] 張颖,兰晓孟,孔垂旸,等.Cu/In 2O 3界面作用增强CO 2催化加氢性能[J].中国石油大学学报(自然科学版),2023,47(2):166-172.
ZHANG Ying, LAN Xiaomeng, KONG Chuiyang, et al. Interfacial interaction of Cu/In 2O 3 to enhance performance of CO 2 catalytic hydrogenation[J]. 2023,47(2):166-172.
(编辑 刘为清)
