高含硫天然气净化装置清洗体系的研制与应用
2024-03-12刘长松杜永慧母建民
刘长松,杜永慧,裴 欣,刘 晶,王 平,母建民
1.中国石化中原油田普光分公司,四川 达州 635002;2.中国石化中原油田分公司石油工程技术研究院,河南 濮阳 457001
由于高含硫天然气净化装置处理的天然气含硫组分较高(H2S 体积分数大于2%),导致不同净化处理单元会因设备腐蚀产生大量的FeS。如,普光天然气净化厂处理装置易于形成和积聚FeS的部位为胺液回收罐、硫冷器、硫磺冷却器、酸性水回收罐及酸性水缓冲罐等[1]。在装置检修期间,空气进入后与FeS 发生强烈的氧化还原反应并放出大量的热,易引发火灾和爆炸事故[2-4]。此外,工艺物料中的H2S、SO2和硫醇等有毒有害物质扩散,会造成严重的人身伤害和环境污染。为此,高含硫天然气净化装置在检修前需采取清洗措施,以清除设备和管道上的FeS和H2S等有害物质,保证净化装置的正常运行。
目前,石油化工领域清除FeS和H2S的常用方法主要有蒸汽吹扫、酸洗、碱洗和多级氧化剂清洗等,但这些方法存在清洗效果有限、清洗废液中含有锰铬等重金属离子、成本较高等问题[5-7]。
针对普光天然气净化厂处理装置及目前清洗体系出现的相关问题,开发高含硫天然气净化装置的清洗体系,该体系由主剂、氧化助剂、螯合助剂、渗透助剂与分散助剂组成,以FeS 转化率、H2S吸收率为指标,考察清洗体系的构成对清洗效果的影响,并在普光天然气净化厂开展了现场试验,以期为该体系的应用提供基础数据。
1 实验
1.1 主要原料
FeS 粉泥(粉碎至48 μm 左右),山东首化化学有限公司;抗坏血酸、1,10-菲啰啉、乙酸钠、NaOH、乙酸、无水乙醇、次氯酸钠、盐酸、氧化剂F、高铁酸钾、四羟甲基硫酸磷、柠檬酸、乙二胺四甲叉膦酸、重铬酸钾、次氯酸钠、双氧水和乙二胺四乙酸二钠等,皆为市售分析纯。
1.2 主要设备及仪器
Mettler TOLEDO 电子天平,梅特勒-托利多仪器(上海)有限公司;GENESYS 10 Series Spectrophotometers 分光光度计,深圳市深赛科学仪器有限公司;DF-101 型集热式恒温加热磁力搅拌器,巩义予华仪器有限责任公司;烘箱,上海精密仪器仪表有限公司;恒温水浴,西安联星试验仪器有限公司;300目筛子,南京中湖科技有限公司。
1.3 实验方法
1.3.1 FeS转化率测定
精确称取5 g 粉碎的FeS 粉末,加入1.25 mL水搅拌成泥状,加入清洗剂100 mL,混合均匀后常温静置反应8 h 后过滤,称取滤渣0.1 g,加入1∶1 的盐酸,加热使粉状物完全溶解,冷却后转移至1 000 mL 的容量瓶中,并加蒸馏水至刻度。分别取2 份盐酸溶解的滤渣试液各5 mL,参照标准《GB/T 3049—2006 铁含量测定的通用方法1,10 菲啰啉分光光度法》测定试液中的总铁与Fe2+含量,按式(1)计算FeS 转化率。每项实验均进行3组平行实验。
式中:Y为FeS 的转化率,%;ρFe为试液中总铁质量浓度,mg/L;ρFe(Ⅱ)为试液中Fe2+质量浓度,mg/L。
1.3.2 H2S吸收率测定
H2S 吸收测定装置如图1 所示[8-9]。实验的具体步骤如下:清洗剂吸收瓶中加入化学清洗剂,碱液吸收瓶中加入质量分数10%的NaOH溶液。将FeS 固体加入启普发生器中,在球形漏斗中缓慢加入1∶1 盐酸,与反应固块接触,产生气体,待无气体逸出后,关闭导气管上的旋塞。采用气体测硫管分别测定H2S 发生装置、清洗剂吸收瓶和碱液吸收瓶中的H2S 浓度,按式(2)计算清洗剂的H2S 吸收率。每项实验均进行3 组平行实验。

1—启普发生器;2—调温电炉;3—缓冲瓶;4—清洗剂吸收瓶;5—碱液吸收瓶图1 H2S吸收测定装置
式中:R为H2S 吸收率,%;ρ0为H2S 发生装置中的H2S 质量浓度,mg/L;ρ1为清洗剂吸收瓶中的H2S质量浓度,mg/L;ρ2为碱液吸收瓶中的H2S 质量浓度,mg/L。
2 结果与讨论
为达到较好的清洗效果,高含硫天然气净化装置清洗体系主要由主剂与氧化、螯合、分散和渗透等助剂组成。主剂的作用是将FeS 氧化分解,将Fe2+转化为Fe3+,同时吸收H2S,且反应后不产生锰铬等重金属离子。助剂的筛选要确保无毒害、污染小,其中,氧化助剂辅助主剂进一步提高FeS去除能力;螯合助剂能将氧化生成的Fe3+螯合生成可溶于水的螯合物[10],以促进FeS 持续地氧化分解;分散助剂的作用是将反应后的产物均匀分散,防止沉降于装置中[11];渗透助剂能够降低表面张力,具有湿润、渗透使清洗体系更易进入污垢内部的作用。
2.1 化学清洗体系主剂的筛选及浓度优化
2.1.1 化学清洗体系主剂的筛选
将20 g/L的氧化剂F、高铁酸钾、重铬酸钾、次氯酸钠和双氧水各100 mL,分别加入5 g FeS粉泥后混合均匀,反应8 h 后过滤烘干,测定FeS 转化率,结果见表1。

表1 不同主剂对FeS转化率的影响
由表1 可知:氧化剂F 的FeS 转化率最高,达到64.81%。因此,确定清洗体系的主剂为氧化剂F。
2.1.2 化学清洗体系主剂的浓度优化
配制不同浓度的氧化剂F 溶液,分别与FeS粉泥混合反应,测定FeS转化率,结果见图2。
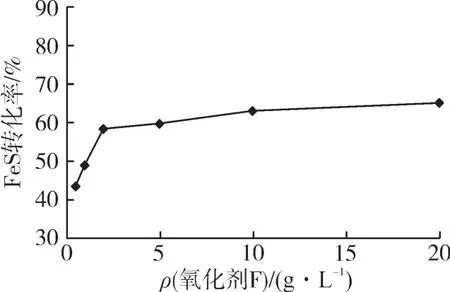
图2 氧化剂F浓度对FeS转化率的影响
由图2 可知:当氧化剂F 浓度增加时,FeS 转化率也随之增大;但当其质量浓度超过2 g/L 时,FeS 转化率上升趋势变缓。综合考虑成本因素,主剂氧化剂F的质量浓度确定为2~5 g/L。
2.2 化学清洗体系助剂的筛选及浓度优化
2.2.1 氧化助剂的筛选及浓度优化
配制5 g/L 的氧化剂F 溶液,分别向其中加入1 g/L 的氧化助剂高铁酸钾、次氯酸钠、氯酸钾和过硫酸钠,观察溶液的配伍性,将配伍性好的溶液分别与FeS 粉泥混合反应,测定FeS 转化率,结果见表2。

表2 不同氧化助剂与主剂的配伍性及其对FeS转化率的影响
由表2 可知:主剂氧化剂F 与次氯酸钠、过硫酸钠的配伍性较好,而且加入过硫酸钠后的FeS转化率较高,为75.23%。因此确定氧化助剂为过硫酸钠。
配制质量浓度为5 g/L 的氧化剂F 溶液,分别加入不同浓度的过硫酸钠,与FeS 粉泥混合反应,测定FeS 转化率,优化氧化助剂的用量,结果见图3。
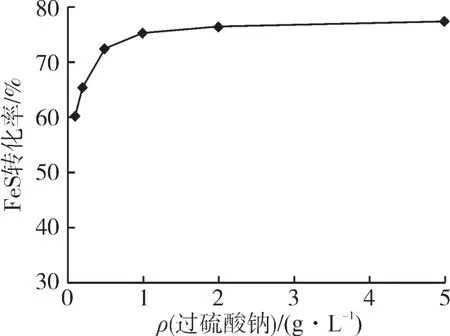
图3 过硫酸钠浓度对FeS转化率的影响
由图3 可知:当过硫酸钠质量浓度大于1 g/L时,FeS 转化率上升趋势变缓。因此确定过硫酸钠质量浓度为1~2 g/L。
2.2.2 螯合助剂的筛选及浓度优化
配制5 g/L 氧化剂F、1 g/L 过硫酸钠混合溶液,分别向其中加入质量浓度为1 g/L 的螯合助剂四羟甲基硫酸磷、乙二胺、乙二胺四乙酸二钠和乙二胺四甲叉膦酸,观察溶液的配伍性,将配伍性好的溶液分别与FeS 粉泥混合反应,测定FeS 转化率,结果见表3。

表3 不同螯合助剂与主剂、氧化助剂的配伍性及其对FeS转化率的影响
由表3 可知:乙二胺四甲叉膦酸与主剂、氧化助剂的配伍性较好,且加入该剂后的FeS 转化率增至86.58%。因此确定螯合助剂为乙二胺四甲叉膦酸。
按上述配方配制溶液,分别加入不同浓度的乙二胺四甲叉膦酸,与FeS 粉泥混合反应,测定FeS转化率,优化螯合剂的用量,结果见图4。

图4 乙二胺四甲叉膦酸浓度对FeS转化率的影响
由图4 可知:当乙二胺四甲叉膦酸的质量浓度大于0.1 g/L 时,FeS 转化率上升趋势变缓。因此,确定乙二胺四甲叉膦酸质量浓度为0.1~0.2 g/L。
2.2.3 分散助剂的筛选及浓度优化
配制5 g/L 氧化剂F、1 g/L 过硫酸钠、0.1 g/L乙二胺四甲叉膦酸混合溶液,分别向其中加入1 g/L 的烷基酚聚氧乙烯醚(OP-10)、聚山梨醇酯80(吐温80)、NaH2PO4、分散助剂D、六偏磷酸钠,观察溶液的配伍性以及加入分散助剂60 min后清洗剂溶液的分散性,结果见表4。

表4 不同分散助剂与主剂、氧化助剂、螯合助剂的配伍性及分散性能评价
由表4 可知:OP-10、NaH2PO4、分散助剂D 与主剂及氧化助剂、螯合助剂的配伍性较好,特别是60 min 后加入分散助剂D 的溶液分散性仍然较好。因此,确定采用分散助剂D 为体系的分散助剂。
按上述配方配制溶液,加入不同浓度的分散助剂D,与FeS 粉泥反应后测定FeS 转化率,优化分散助剂的用量,结果见图5。
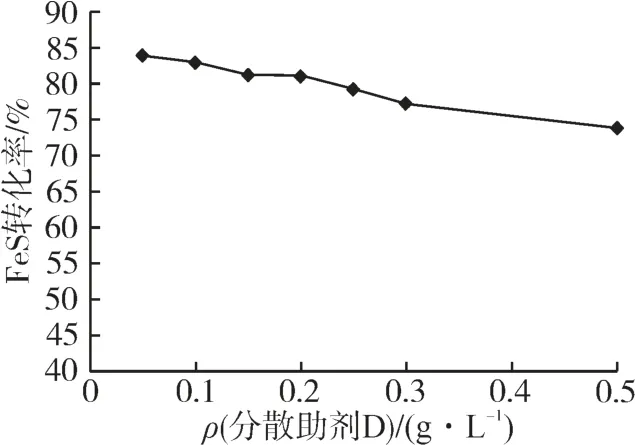
图5 分散助剂D浓度对FeS转化率的影响
由图5 可知:随着分散助剂D 浓度的增加,FeS 转化率随之降低,当分散助剂D 质量浓度为0.15~0.20 g/L 时,FeS 转化率降低趋势较缓,且在此浓度范围分散助剂仍能保持一定的分散性。为此,确定分散助剂D的质量浓度为0.15~0.20 g/L。
2.2.4 渗透助剂的筛选及浓度优化
配制5 g/L 氧化剂F、1 g/L 过硫酸钠、0.1 g/L乙二胺四甲叉膦酸和0.15 g/L 分散助剂混合溶液,分别加入1 g/L 的渗透助剂脂肪醇聚氧乙烯醚(AEO)、K2SO4和Na2SO4,观察溶液的配伍性,将配伍性好的溶液分别与FeS粉泥混合反应,测定FeS转化率,结果见表5。

表5 不同渗透助剂与主剂、氧化助剂、螯合助剂、分散助剂的配伍性及其对FeS转化率的影响
由表5 可知:AEO、Na2SO4与主剂及其他助剂的配伍性较好,加入Na2SO4后的FeS 转化率相对较高,为85.86%,为此确定渗透助剂为Na2SO4。
按上述配方配制溶液,分别向其中加入不同浓度的Na2SO4,与FeS 粉泥反应后测定FeS 转化率,优化渗透助剂的用量,结果见图6。
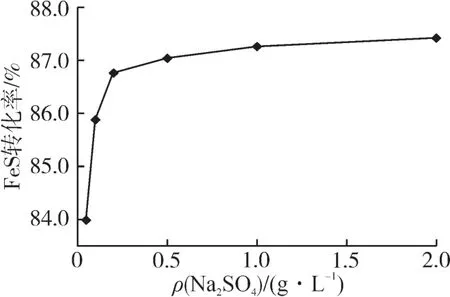
图6 渗透助剂D浓度对FeS转化率的影响
从图6 可知:Na2SO4的加入能够适当增加FeS转化率,当Na2SO4质量浓度大于0.2 g/L时,增加趋势变缓,为此,确定渗透助剂Na2SO4质量浓度为1.0~2.0 g/L。
该清洗体系最终FeS 转化率在85.86%,比现有清洗体系FeS转化率(75%)高10%左右。
2.3 化学清洗体系H2S吸收率评价
在H2S 吸收效果测定装置中加入化学清洗体系及所需药剂,反应停止后分别测定H2S 吸收率,结果见表6。

表6 H2S吸收率评价结果
由表6可知:本研究建立的化学清洗体系H2S吸收率达到95.4%,与现有清洗体系H2S 吸收率(92%)相比,它对H2S吸收效果更好。
3 现场应用
该化学清洗体系于2022 年10 月应用于普光净化厂第五联合装置低压火炬收集罐152-D-708,共注入化学清洗药剂2 t,采用浸泡方式进行清洗,结果见表7。

表7 高含硫天然气净化装置化学清洗体系应用情况
由表7 可知:清洗后开孔检测H2S 为0,温度为20.8 ℃,152-D-708 罐内FeS 的清洗较为彻底,检测清洗后的废液总磷含量为0.24 mg/L(污水排放标准要求≤0.5 mg/L),无锰铬等重金属离子,现场应用取得了较好的效果。与现有清洗剂相比,该化学清洗体系节约成本40%以上。
4 结论
1)清洗体系通过主剂、氧化助剂、渗透助剂与螯合助剂的协同作用,提高了FeS 的转化率,渗透助剂能够辅助主剂与FeS 更充分地反应,分散助剂能够均匀分散反应后的产物,它们的共同作用提高了清洗体系的清洗效果。
2)高含硫天然气净化装置化学清洗体系具有较高的FeS 转化率(85.86%)与良好的H2S 吸收率(95.4%)。
3)现场应用表明,该清洗体系清洗效果良好,废液中总磷含量仅为0.24 mg/L,无锰铬等重金属离子,对环境无毒害、污染小,且成本节约40%以上。
