基于网络药理学探讨清肾颗粒主要药物治疗慢性肾脏病作用机制
2024-03-08孙璇君金华张磊王亿平
孙璇君,金华,张磊,王亿平
安徽中医药大学第一附属医院,安徽 合肥 230031
慢性肾脏病(chronic kidney disease,CKD)是由各种原因造成的肾脏结构和/或功能异常或不明原因肾小球滤过率下降(<60 mL/min·1.73 m2)超过3个月[1]。研究表明,CKD流行性广、发病率高[2-3],其防治工作至关重要。清肾颗粒是安徽中医药大学第一附属医院开发的院内制剂,为治疗CKD常用方,相关临床研究表明,其可达到改善肾功能及并发症的目的[4-6],目前尚未进行药理机制研究。本研究利用网络药理学方法,选取清肾颗粒的君药、臣药及重要使药,即大黄、黄连、白花蛇舌草、丹参,探讨其治疗CKD的作用机制,为其临床应用提供理论基础。
1 资料与方法
1.1 活性成分及靶点获取
利用TCMSP数据库(https://www.tcmsp-e.com/),分别以大黄、黄连、白花蛇舌草、丹参为检索词,以口服生物利用度(OB)≥30%且类药性(DL)≥0.18为条件进行筛选,使用PubChem(https://pubchem.ncbi.nlm.nih.gov/)数据库获得上述成分的SDF结构,并将上述成分导入SwissTargetPrediction数据库,以药物靶点预测值>0作为筛选条件。
1.2 疾病靶点获取
以“chronic renal failure”为关键词,分别检索OMIM 数据库(https://www.omim.org/)、GeneCards数据库(https://previous.genecards.org/)、TTD数据库(https://ngdc.cncb.ac.cn/)获取CKD相关靶点,合并后删除重复值,获取CKD靶点。
1.3 中药成分-疾病靶点获取
将以上4味中药活性成分对应靶点及CKD靶点输入Venny2.1 平台(https://bioinfogp.cnb.csic.es/tools/venny/)取交集,得到4味中药治疗CKD潜在靶点。
1.4 中药-活性成分-靶点-疾病网络构建
将4 味中药活性成分及治疗CKD 潜在靶点导入Cytoscape3.7.2软件,使用Network Analyzer插件进行网络拓扑分析,构建药物-活性成分-靶点-疾病网络。按照degree值大小排序,degree值与重要性呈正相关。
1.5 蛋白相互作用网络构建
将“1.3”项中交集靶点导入STRING 数据库(https://string-db.org/),设置为“Homo sapiens”,交互分数≥0.4,构建交集靶点蛋白相互作用(PPI)网络,并下载.tsv格式文件。
1.6 核心靶点筛选
利用Cystoscape3.7.2 软件的Network Analyzer 插件对PPI网络进行拓扑分析,计算出degree值、中介中心性(BC)、平均最短路径长度(ASPL)和紧密中心性,结果以degree值排序,使用R3.6.1对前30个靶点绘制条形图。将“1.5”项中的.tsv文件导入Cytoscape软件,使用MCODE模块进行基因簇分析,以基因分值大于平均分作为核心靶点筛选标准。
1.7 GO功能与KEGG通路富集分析
利用R3.6.1 调用BiocManager、ClusterPr ofiler 等程序包,以P<0.05、Q<0.05为筛选条件,进行GO功能分析,包括细胞组分(CC)、分子功能(MF)和生物过程(BP)。利用ClusterProfiler、org.Hs.eg.db等软件包进行KEGG通路富集分析,利用pathview包绘制信号通路图,根据P值排序,选取前20位绘图。
2 结果
2.1 药物活性成分及作用靶点收集
通过检索TCMSP数据库,共获取大黄、黄连、白花蛇舌草、丹参活性成分99种,药物靶点873个。将活性成分按degree值排序,排名前10位见表1,包括槲皮素、木犀草素、丹参醇A等活性成分。

表1 白花蛇舌草、大黄、丹参、黄连活性成分
2.2 药物-活性成分-靶点-疾病网络构建
通过检索OMIM、GeneCards、TTD数据库,去重后获得1 010个CKD相关靶点。将CKD相关靶点与药物活性成分对应靶点取交集,得到102个交集靶点,即为大黄、黄连、白花蛇舌草、丹参治疗CKD的潜在靶点。利用Cytoscape3.7.2软件构建药物-活性成分-靶点-疾病网络,见图1。

图1 白花蛇舌草、黄连、丹参、大黄治疗CKD药物-活性成分-靶点-疾病网络
2.3 蛋白相互作用网络构建及核心靶点筛选
将102个交集靶点导入STRING数据库,得到由102个节点、1 250条边构成的PPI网络(见图2)。导入Cytoscape3.7.2软件,利用Network Analyzer工具计算网络中各节点的拓扑属性,核心靶点的基因分值以大于平均分作为筛选标准,并使用R3.6.1对前30个靶点绘图(见图3),由大到小排序,前5位核心靶点依次为VEGFA、EGFR、AKT1、SRC、STAT3。

图2 白花蛇舌草、黄连、丹参、大黄治疗CKD靶点PPI网络
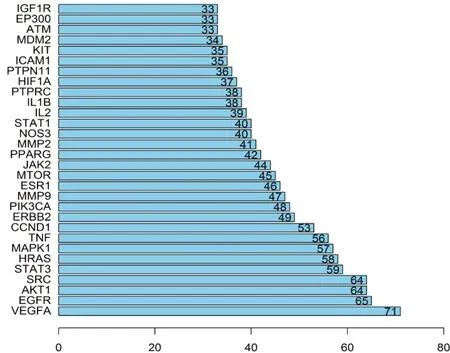
图3 基于拓扑分析的核心靶点筛选(前30位)
2.4 GO功能与KEGG通路富集分析结果
将102 个交集靶点导入R3.6.1,进行GO 功能与KEGG通路富集分析。其中GO富集分析得到2 212个BP条目、36个CC条目、126个MF条目。BP主要涉及肽基酪氨酸磷酸化、肽基酪氨酸修饰、蛋白质自身磷酸化、肌肉细胞增殖等;CC主要涉及薄膜筏、膜微畴、膜区域、质膜筏、细胞顶端部分、顶端质膜、焦点黏附、细胞-基质黏附体连接等;MF主要包括蛋白酪氨酸激酶活性、跨膜受体蛋白酪氨酸激酶活性、跨膜受体蛋白激酶活性、生长因子结合、胰岛素受体底物结合等。根据P值选取各项前20条目绘图,见图4。

图4 白花蛇舌草、黄连、丹参、大黄治疗CKD靶点GO功能富集分析
共得到143条KEGG通路,靶点主要富集于缺氧诱导因子1(HIF-1)信号通路、PI3K-Akt信号通路、Rap1信号通路、MAPK信号通路等。按照P值选取前20条目绘制条形图,见图5。
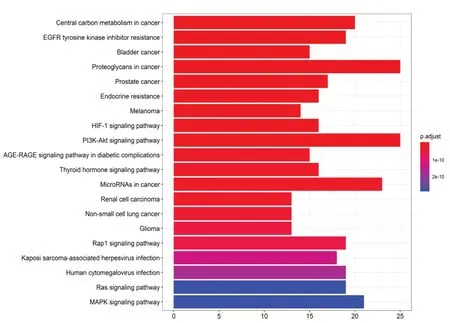
图5 白花蛇舌草、黄连、丹参、大黄治疗CKD靶点KEGG通路富集分析
3 讨论
引起CKD的原因很多,如急/慢性原发性肾小球肾炎、间质性肾炎、肾病综合征,代谢性疾病如高血压病、1型或2型糖尿病、高尿酸血症,结缔组织病如系统性红斑狼疮、抗中性粒细胞抗体血管炎等。西医治疗多为单靶点治疗,鉴于CKD机制的复杂性,需要多靶点、多通路进行治疗。研究表明,中医药防治CKD作用显著[7]。清肾颗粒中大黄味苦性寒,具有泻下清热、解毒逐瘀之功,为君药,黄连、白花蛇舌草及丹参具有清热利湿、化瘀泄浊之功[8]。
治疗CKD除针对原发病治疗之外,中医药防治也至关重要。清肾颗粒可以显著改善患者血肌酐、尿素氮,减轻大小鼠肾脏炎症及纤维化,调节免疫及纠正贫血,并通过不同信号通路如PI3K-Akt、Janus激酶信号通路等实现对肾间质纤维化治疗作用[9-11]。Lourenço等[12]通过对CKD猫模型研究中发现,VEGFR在CKD模型组中表达明显下降,且与CKD生物标志物如血肌酐呈负相关性。Patel等[13]指出,单侧输尿管梗阻模型小鼠中的TGF-β1下游EGFR与肾纤维化呈正相关性,而Kim等[14]指出,AKT基因沉默小鼠的肾纤维化程度明显加重。Li等[15]研究表明,SRC家族激酶对于急性肾损伤(AKI)治疗发挥关键作用。Park等[16]研究表明,STAT3 可能影响AKI 到CKD 的发展,在此过程中,STAT3亚型有不同程度的表达。
GO富集分析结果表明,BP主要涉及肽基酪氨酸磷酸化、肽基酪氨酸修饰、蛋白丝氨酸/苏氨酸激酶活性的正向调节、蛋白质自身磷酸化、肌肉细胞增殖等;MF主要富集于蛋白酪氨酸激酶活性、跨膜受体蛋白酪氨酸激酶活性、跨膜受体蛋白激酶活性、生长因子结合、胰岛素受体底物结合等。CC主要涉及囊泡腔、前缘薄膜、嗜苯胺蓝粒腔等。氨基酸代谢是CKD关键调节机制之一,这与GO富集分析结果一致[17]。
KEGG 结果显示,HIF-1、PI3K-Akt、Rap1、MAPK信号通路参与治疗CKD。Liang等[18]研究表明,活化Rap1能调节TNF-α以控制肾纤维化。Ye等[19]研究发现,TGF-β1/Smad3 和HIF1 信号通路在老龄小鼠AKI中发挥作用。Shi等[20]指出,PI3K信号通路参与AKI过程,而Rana等[21]研究发现,MAPK信号通路参与CKD 小鼠发病。本研究发现,VEGFA、EGFR、AKT1、SRC、STAT3等重要靶点及HIF-1、PI3K-Akt、Rap1、MAPK等重要信号通路参与CKD治疗。
综上所述,本研究通过网络药理学方法探讨中药复方清肾颗粒中白花蛇舌草、黄连、丹参、大黄治疗CKD的潜在活性成分可能是槲皮素、木犀草素、丹参醇A等,核心靶点涉及VEGFA、EGFR、AKT1,可能涉及HIF-1、PI3K-Akt、Rap1、MAPK 等信号通路。本研究为进一步揭示清肾颗粒治疗CKD的作用机制提供了新思路。但限于中药数据库相关信息招募过程中潜在的遗漏,仍需开展相关实验验证,才能更好地阐明中药多成分-多靶点-多途径治疗CKD的生物学特性与作用机制。
