高中化学解题中建模思想的有效运用研究
2024-03-06沈宝华
沈宝华
(福建省宁德市民族中学,福建 宁德 355000)
模型是对实际问题的抽象和简化,每个模型都有自己的适用范围和条件[1].化学是一门抽象的学科,化学问题的复杂性和抽象性使学生往往难以直观地理解和掌握,因此,模型认知在化学学习中的应用是非常重要的.模型认知思维可以帮助学生将抽象的化学概念转化为具体的形象,从而更好地理解和应用化学知识,高中化学中,模型认知是学生必须培养的核心素养[2].
1 建模思想在高中化学中的有效运用
化学模型对于解题具有十分重要的作用,下面选取两个模型,结合理论和实证进行分析.
1.1 “工业生产和流程综合推断”模型运用研究
以工业生产为背景考查知识点,具有信息量多、综合度高的特征,对考生的提取信息能力、分析信息能力以及归纳能力和问题解决能力提出了更高的要求.该类题多以流程图或文字表述的形式呈现,核心的问题是“物质的转化” 与 “物质的分离”,考查的知识点多涉及物质间转化、物质与能量的转化、对物质转化的控制、物质的分离方法以及一些定量问题.对该类题搭建模型,可以帮助学生理顺思路,其具体模型如图1所示.

图1 “工业生产和流程综合推断”模型图
例1高纯六水氯化锶晶体可作有机合成的催化剂.工业上用难溶于水的碳酸锶粉末为原料(含少量碳酸钡、氧化亚铁、二氧化硅等杂质)制备高纯六水氯化锶晶体,其过程如图2所示.

图2 高纯六水氯化锶晶体(SrCl2·6H2O)制备流程图
已知:
Ⅰ.温度为25 ℃时,氢氧化铁的Ksp[Fe(OH)3]=1.0×10-38,氢氧化亚铁的Ksp[Fe(OH)2]=1.0×10-16.
Ⅱ.在温度为61 ℃时,高纯六水氯化锶晶体会逐渐开始失去结晶水.
请回答以下问题:
(1)以SrSO4为主要成分的天青石,在经过多个步骤的反应之后,才能制备得到工业碳酸锶.该过程的第一步是天青石和过量的焦炭反应被还原为硫化锶,反应条件为隔绝空气并微波加热,请写出该反应的化学方程式____.
(2)在图2的制备流程图中,①步骤是工业碳酸锶的粉碎步骤,并且将粉碎之后的工业碳酸锶加水配置为浆液,小明认为该步骤是为了加快反应步骤的进行,理由是____.
(3)在工业碳酸锶的浆液中加入了工业盐酸,并且得到了锶元素的浸出率和温度以及时间的关系,具体信息如图3所示.

图3 浸出温度、时间对锶浸出率的影响
根据图3,可以得出合适的工业生产条件为____.
(4)步骤③中所得的滤渣主要成分,除氢氧化铁之外,还有____(请填写物质的化学式);当温度为 25℃,若要使Fe3+沉淀完全,则需要将溶液的pH调整为____(当某一离子的浓度降至1.0×10-5mol/L时,则可认为该离子已经沉淀完全).
(5)下列以下说法, ____是正确的.
A.步骤⑤在对SrCl2·6H2O晶体进行干燥时,可以采用减压干燥的方法
B.在步骤④中,当进行冷却结晶时,应通入HCl气体
(6)如果需要获得无水氯化锶产品,则必须对高纯六水氯化锶晶体(SrCl2·6H2O)(M=267 g·mol-1)进行脱水处理.脱水过程首先需要在170 ℃温度下进行预脱水处理,此时高纯六水氯化锶晶体的失重达到33.7%,则经过预脱水后,产物的化学式应为____.

小结对于一个完整的无机化工生产,其通常具有的流程如图4所示.在进行该类题型的求解时,要结合模型,对五大步骤进行分析,从大量的信息中梳理出来相关的信息.而后运用已学知识进行求解.
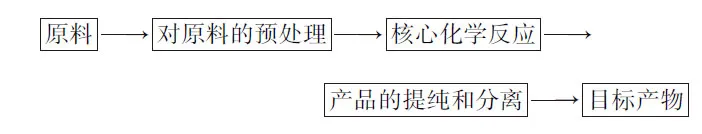
图4 无机化工生产流程图
1.2 “盖斯定律”模型运用研究
运用“盖斯定律”进行相关运算的模型如图5所示.

图5 “盖斯定律”模型图
例2甲烷(CH4)与二氧化碳(CO2)重整是二氧化碳利用的研究热点之一.该重整反应体系主要涉及以下反应:




根据盖斯定律,反应a的ΔH1=____(写出一个代数式即可).
解析根据模型进行分析.目标反应式为a,然后对其他反应式进行变换消元,可以得出a=b+c-e=c-d.根据盖斯定律则有ΔH1=ΔH2+ΔH3-ΔH5=ΔH3-ΔH4.
小结对于该类题型,要结合模型流程进行分析.首先要确定需要研究的反应,确定其中反应物和生成物的状态和化学计量数关系;然后再进行“消元加减”处理.
2 结束语
建模思维对高中学习至关重要,模型的运用可以将做题步骤流程化,降低题目的分析难度.然而,在化学学习的启蒙阶段,学生对于抽象概念的理解能力有限,模型认知思维的培养难度较大.因此,教师需要根据学生的认知水平和学习能力,采用适当的教学方法和策略,激发学生的兴趣和好奇心,培养他们的模型认知思维能力.教师可以通过引导学生观察、实验、探索和讨论,帮助他们建立起化学模型.同时,教师还应该将宏观和微观结合起来,引导学生从宏观现象中推导出微观模型,从而加深对化学知识的理解.
