吡咯氮掺杂还原氧化石墨烯泡沫活化过二硫酸钠去除双酚A
2024-02-27左怡丹龙俊宏和丽金金华蕾夏丽红罗利军戴建辉
左怡丹,龙俊宏,宋 洁,和丽金,金华蕾,夏丽红,石 苗,罗利军*,戴建辉
(1 云南民族大学 化学与环境学院,云南省教育厅环境功能材料重点实验室,云南 昆明 650500;2 云南省红河州开远市住房和城乡建设局,云南 开远 661600)
新污染物是一类具有生物毒性、环境持久性、生物累积性等特征的有毒有害化学物质,主要包括国际公约管控的持久性有机污染物、内分泌干扰物、抗生素和微塑料4大类。它们会在极低的浓度下对生态环境或人体健康造成较大危害,已经成为“十四五”生态环境保护和治理的重点。双酚A(bisphenol A,BPA)是一种典型的环境内分泌干扰物,具有弱的雌激素作用和相对较强的抗雌激素效应,长期暴露在低浓度BPA中会损害生物的生殖健康[1],其也是污水处理厂出水中雌激素效应的主要贡献者之一[2]。然而,BPA是生产聚碳酸酯等的主要原料,其制品的生产和使用会造成大量BPA进入水体。因此,研究开发新技术实现BPA新污染物的末端治理,降低新污染物环境风险,具有重要意义。


还原石墨烯泡沫又称三维还原氧化石墨烯泡沫,是以单层二维蜂窝状晶格结构的还原氧化石墨烯作为基本单元、以无序堆砌方式铰接而成的三维多孔材料。除继承还原氧化石墨烯的优点外,还原氧化石墨烯泡沫还具备抗压能力强、机械性能好、密度小、易回收等优点,可广泛用于防护装备材料、油水分离材料、新型显示材料等,可解决片状还原氧化石墨烯在使用过程中可能释放至环境中带来的环境风险问题。基于此,为了制备孔道相对均匀、孔体积更大的氮掺杂还原氧化石墨烯,本文以吡咯为氮源,采用水热-冷冻干燥法制备易回收的氮掺杂还原氧化石墨烯泡沫(N-RGF),并用于活化过二硫酸盐降解双酚A。
1 材料与方法
1.1 主要试剂与材料
双酚A(BPA,≥99%),西格玛奥德里奇公司;天然石墨粉(≥99%)、乙酸乙酯(色谱纯),赛默飞世尔科技(中国)有限公司;过二硫酸钠(Na2S2O8,分析纯)、无水乙醇(≥99.7%)、甲醇(色谱纯)、乙腈(色谱纯)、吡咯(CP),上海科丰化学试剂有限公司;甲醇(分析纯)、乙醇(分析纯)、苯醌(BQ,分析纯),阿达玛斯有限公司;呋喃甲醇(FFA,≥98%),国药集团化学试剂有限公司;5,5-二甲基-1-吡咯啉-N-氮化物(DMPO)、2,2,6,6-四甲基哌啶(TEMP),罗恩试剂有限公司;乳腺癌MCF-7 细胞系,中国科学院上海生命科学研究院生物化学和细胞生物学研究所;酚红DMEM培养基、澳洲胎牛血清(FBS),赛默飞世尔科技(中国)有限公司;青霉素-链霉素溶液、MTT试剂,碧云天生物技术研究所。
1.2 氮掺杂还原氧化石墨烯泡沫的制备
首先,通过改进的Hummers方法制备氧化石墨[23]。其次,称取0.2 g氧化石墨于100 mL去离子水中,超声得到2 mg/mL氧化石墨烯(GO)溶液。量取一定体积的2 mg/mL GO溶液至烧杯中,缓慢滴加1 mL吡咯(10 s/滴),搅拌至溶液透明均匀。最后,将上述溶液转移至高压高温反应釜中,180 ℃水热反应20 h,冷却至室温,用去离子水冲洗后真空冷冻干燥(-60 ℃,48 h),制得氮掺杂还原氧化石墨烯泡沫(N-RGF)。
1.3 材料表征
利用FEI Nova Nano-SEM 450型扫描电子显微镜对所制材料的形貌进行表征;利用Rigaku TTRⅢ型X射线衍射仪对材料的晶相进行分析;利用NICOLET-IS10型傅里叶变换红外光谱仪对材料表面的官能团进行分析;利用PHI5000 Versaprobe-Ⅱ型光电子能谱仪测定材料表面的元素种类、化学状态以及各元素的含量;利用Micromerritics TriStar Model 3020型N2吸附脱附比表面积分析仪测定材料的比表面积、孔径及孔体积;利用STA449F31型热分析仪对材料的热稳定性进行分析。
1.4 活化过硫酸盐降解BPA实验
N-RGF活化过二硫酸钠(peroxodisulfate,PDS)降解BPA的实验过程[18]如下:加入0.025 g N-RGF于一定体积的10 mg/L BPA溶液中,搅拌120 min达到吸附/解吸平衡。加入适量的PDS进行活化降解BPA,每隔30 min取样1 mL,用0.45 μm的玻璃纤维膜过滤至液相瓶,采用高效液相色谱仪测定BPA含量[24]。所制材料对BPA的吸附去除率、活化PDA降解BPA的去除率(降解去除率)、总去除率和准一级降解速率分别按公式(1)、(2)、(3)和(4)进行计算。
吸附去除率=(C0-Cq)/C0×100%,
(1)
降解去除率=(Cq-Ct)/Cq×100%,
(2)
总去除率=吸附去除率+降解去除率,
(3)
准一级降解速率ln(Ct/Cq)=-κt。
(4)
式中:C0为BPA的初始质量浓度;Cq为吸附平衡时溶液中的BPA质量浓度;Ct为BPA在降解过程中任意某一时刻的质量浓度;κ为拟一级降解速率常数;t为时间,单位为min。
2 结果与讨论
2.1 材料表征与分析
2.1.1 扫描电子显微镜(SEM)分析
利用SEM对N-RGF的形貌和结构进行表征,结果如图1所示。与RGF相似[18],N-RGF也为网状泡沫三维结构,其孔径较小且分布较窄(2~3.5 μm),片层RGO相互堆积情况较少,呈展开状态。分析其原因主要是具有共价结构的聚吡咯很容易与RGO骨架层结合,可以作为溶胀剂和氮源,能够有效防止RGO堆积[25]。此外,从SEM图像可知,制备的N-RGF具有体积更大、弹性更好、密度更小的特点。

图1 N-RGF的SEM图
2.1.2 X射线衍射(XRD)分析
为研究所制备材料的晶相,利用XRD对GO和N-RGF进行表征分析,结果如图2所示。从图可知,GO在2θ为13°处有1个衍射宽峰,表明氧化石墨呈无定型态。当氧化石墨烯(超声剥离氧化石墨产物)和吡咯复合,13°处的衍射峰完全消失,N-RGF在2θ为25.1°处出现宽峰。这归因于高温水热环境恢复了石墨烯表面部分π—π共轭体系,且引入吡咯后N-RGF中的含氧官能团更易失去[26]。该宽衍射峰表明N-RGF的层间距远低于氧化石墨[27],且RGO薄片之间π—π堆叠有助于形成三维网络结构。
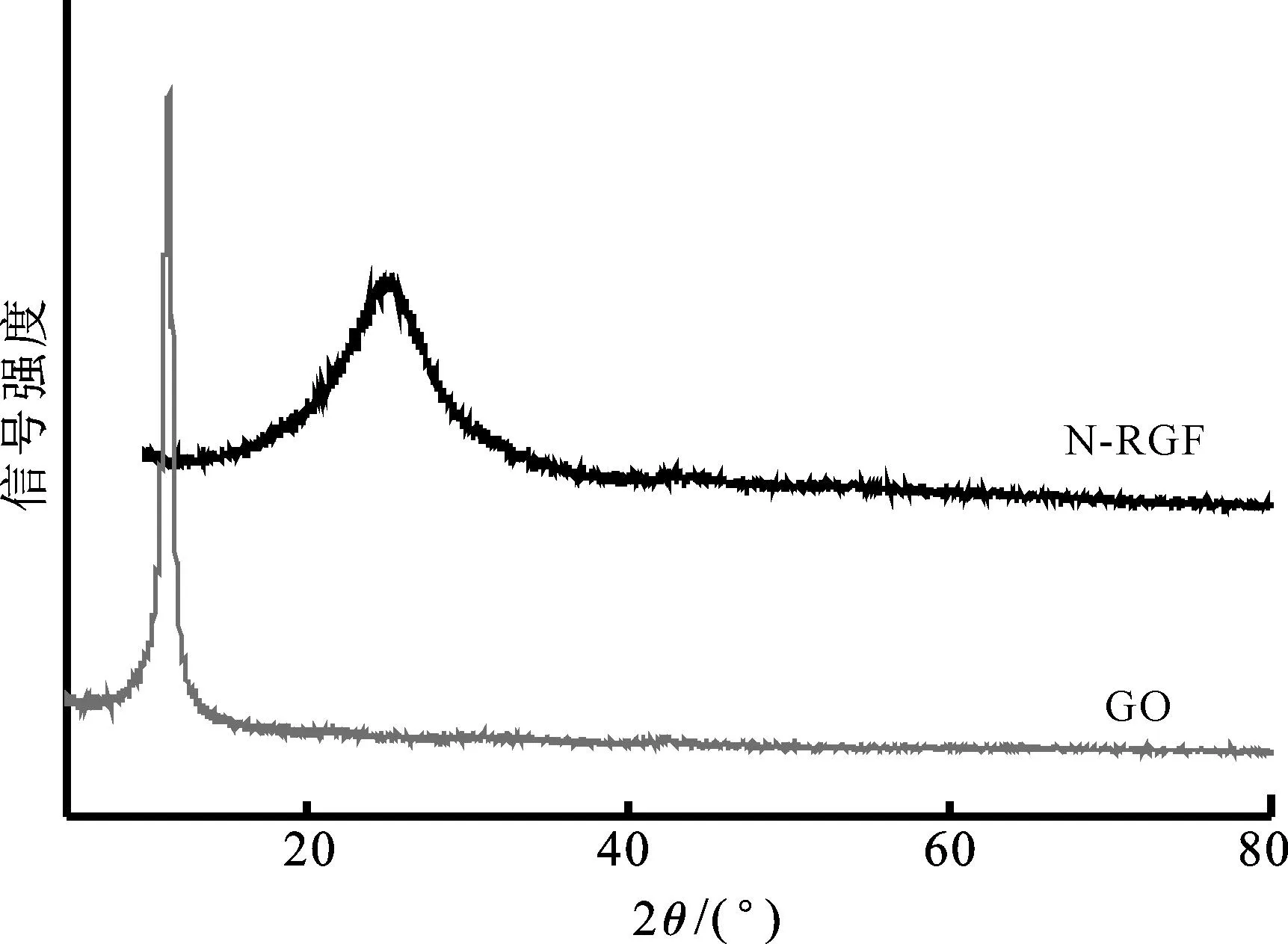
图2 GO和N-RGF的XRD图
2.1.3 傅里叶变换红外光谱(FT-IR)分析
为研究含氧官能团的变化,对GO和N-RGF进行FT-IR分析,结果如图3所示。
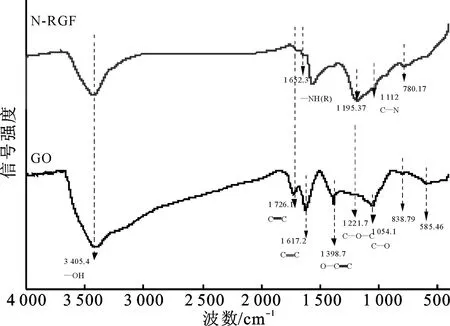
图3 N-RGF和GO的FT-IR谱图
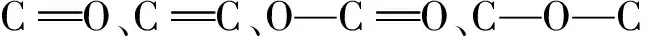
2.1.4 光电子能谱(XPS)分析

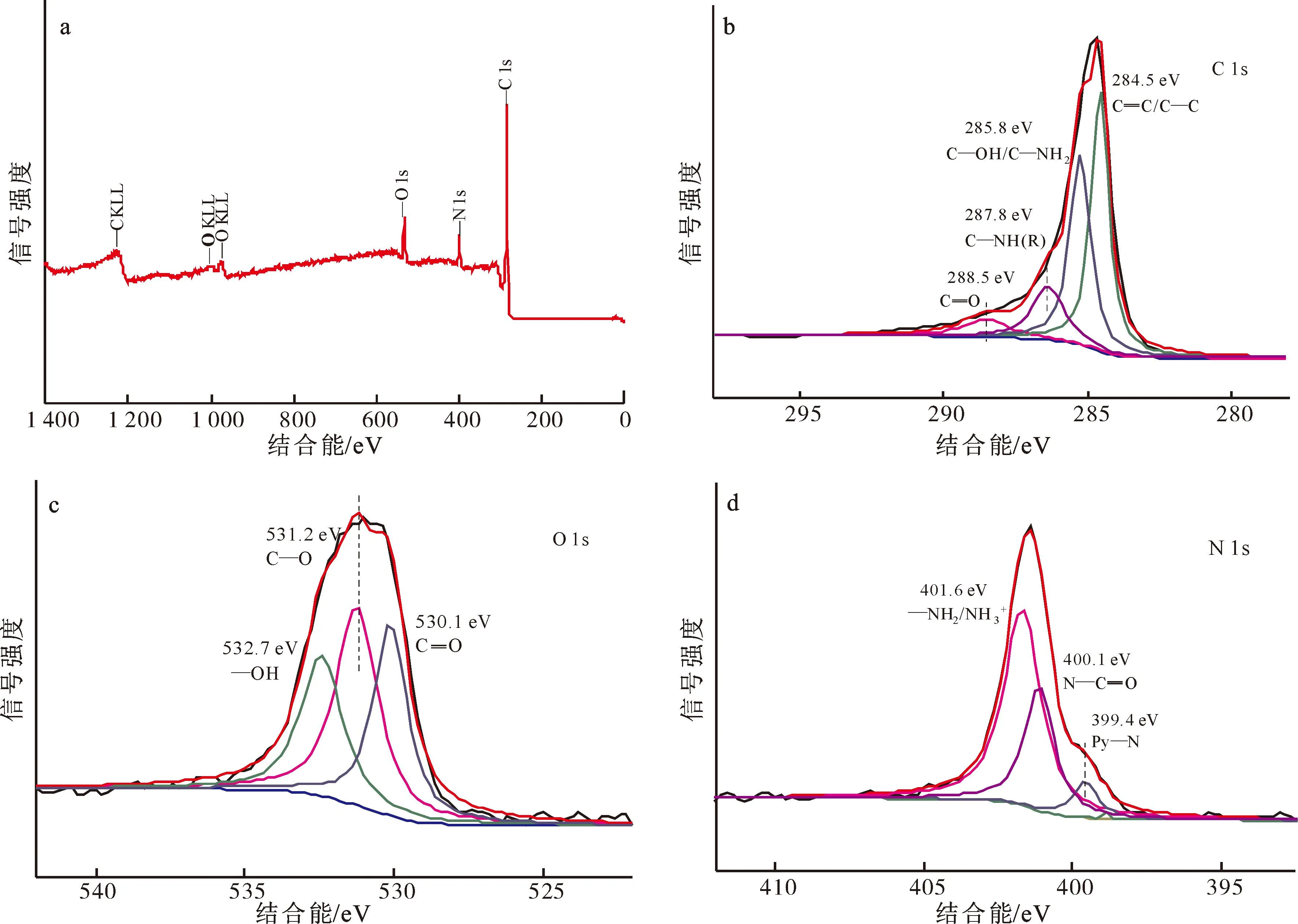
图4 N-RGF的XPS全谱图(a)及C 1s(b)、O 1s(c)、N 1s(d)分峰拟合图
2.1.5 N2吸附脱附比表面积(BET)分析
采用BET对N-RGF的比表面积和孔结构进行分析,结果如图5所示。N-RGF的吸附主要发生在相对压力小于1时,吸附脱附等温线属于Ⅱ型,且具有H3型滞后型,表明N-RGF的孔隙主要是片层结构堆积形成的大型狭缝孔,这与SEM分析结果一致(图1)。N-RGF的比表面积和孔体积分别为90.029 m2/g和0.541 7 cm3/g,大的比表面积和孔体积可提供更多的吸附位点和活化位点,有利于N-RGF活化PDS降解有机污染物。

图5 N-RGF的N2吸附脱附等温线及孔径分布
2.1.6 热重(TG)和微分热重(DTG)分析
利用TG和DTG对N-RGF的官能团结构和热稳定性进行分析,结果如图6所示。当加热温度为100 ℃时,N-RGF没有明显失重现象,表明所制材料表面未吸附大量水分子,表现出一定的疏水性,有助于N-RGF通过疏水相互作用力吸附疏水性BPA。继续升高温度至150~500 ℃,N-RGF的质量持续下降,失重28.40%,说明羧基和碳基等官能团可通过热分解生成H2O、CO和CO2[13]。当温度从100 ℃升高至180 ℃时,N-RGF失重不明显,但当升温至200 ℃时,N-RGF的质量急剧下降,这可能与N-RGF中氮和含氧官能团的分解有关[26]。
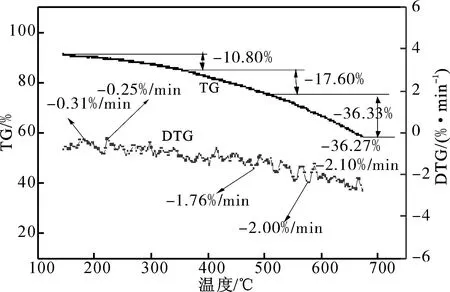
图6 N-RGF热重分析
与本课题组前期以氨水为氮源制备的氮掺杂还原氧化石墨烯泡沫(平均孔径为1~5 μm,孔体积为0.195 8 cm3/g,石墨相氮含量为1.09%)相比[18],本文以吡络为氮源制备的N-RGF孔径更小且分布更加均匀(2~3.5 μm)、孔体积更大(0.541 7 cm3/g)、石墨相氮含量更高(4.3%)、弹性和稳定性更好。基于此,以吡咯为氮源,采用简单水热-冷冻干燥技术制备的石墨烯基泡沫材料更适合用于吸波材料、超级电容器、油水分离材料、力学材料及环境保护领域。
2.2 吸附/活化性能分析
2.2.1 N-RGF制备条件的优化
图7为不同吡咯加入量、水热温度和水热时间对N-RGF活化PDS去除BPA的影响,实验条件为0.5 g/L催化剂、0.1 g/L PDS、BPA初始质量浓度为10 mg/L。图7a为不同吡咯加入量所制备的N-RGF活化PDS去除BPA的时间曲线。当氮掺杂量(通过吡咯加入量折算得到)从2.5%增加至7.5%时,N-RGF对BPA的总去除率从62.55%增加至82.64%;氮掺杂量继续增加至15.0%,总去除率反而降至62.41%,说明适量氮掺杂可有效提高N-RGF活化PDS降解BPA的能力,但吡咯加入过量不仅会使吡咯聚至N-RGF表面,堵塞N-RGF的孔道,减少其活性位点,还会减少N-RGF的含量[32]。图7b为不同水热反应时间制备的N-RGF活化PDS去除BPA的时间曲线。当水热反应时间从12 h增加到20 h时,BPA总去除率从56.83%增加至80.50%,继续增加水热反应时间至28 h,总去除率降至47.55%。图7c为不同水热反应温度制备的N-RGF活化PDS去除BPA的时间曲线。当水热温度从140 ℃增加到180 ℃时,N-RGF对BPA的总去除率从73.40%增加至81.56%,继续升温至220 ℃,总去除率降至63.70%,主要原因可能是高水热温度会造成N-RGF孔结构坍陷,减少活性位点[33]。因此,N-RGF的最佳制备条件为氮掺杂量7.5%,180 ℃水热反应20 h。

图7 不同氮掺杂量(a)、水热反应时间(b)和水热反应温度(c)制备的N-RGF活化PDS去除BPA的性能曲线
2.2.2 N-RGF活化PDS降解BPA条件的优化
为明确N-RGF活化PDS降解BPA的最优条件,测试不同pH值和不同PDS质量浓度对去除BPA的影响,其中BPA初始质量浓度为10 mg/L,结果如图8所示。图8a为不同初始pH值对N-RGF活化PDS去除BPA的影响。当溶液初始pH值从2增加至6时,BPA总去除率从66.30%增加至77.30%,当溶液初始pH值继续增加至10时,BPA总去除率降至63.59%,表明弱酸和中性条件更有利于N-RGF活化PDS去除BPA。弱碱条件下,BPA以二价阴离子的形式(pH值大于9)存在,与带负电的N-RGF之间存在相互排斥作用,减少了对BPA的吸附去除[34]。图8b为不同PDS质量浓度对N-RGF活化PDS去除BPA的影响。当PDS质量浓度从0.05 g/L增加至0.10 g/L时,BPA总去除率从60.42%增加至82.64%,继续增加PDS至0.30 g/L时,BPA总去除率降至67.62%。其主要原因是N-RGF活化PDS主要发生在催化剂表面,是由氮掺杂后邻近带正电的碳原子活性位点决定的[35],随着PDS质量浓度的增加,带正电的碳原子吸附过二硫酸根阴离子的量也会增加,BPA的降解去除率将增加;但当催化剂表面的活性位点已被完全占有,进一步增大PDS的质量浓度不会再增加产生的活性物种。因此,N-RGF活化PDS降解BPA的最优条件为溶液初始pH值为6,PDS质量浓度为0.1 g/L。
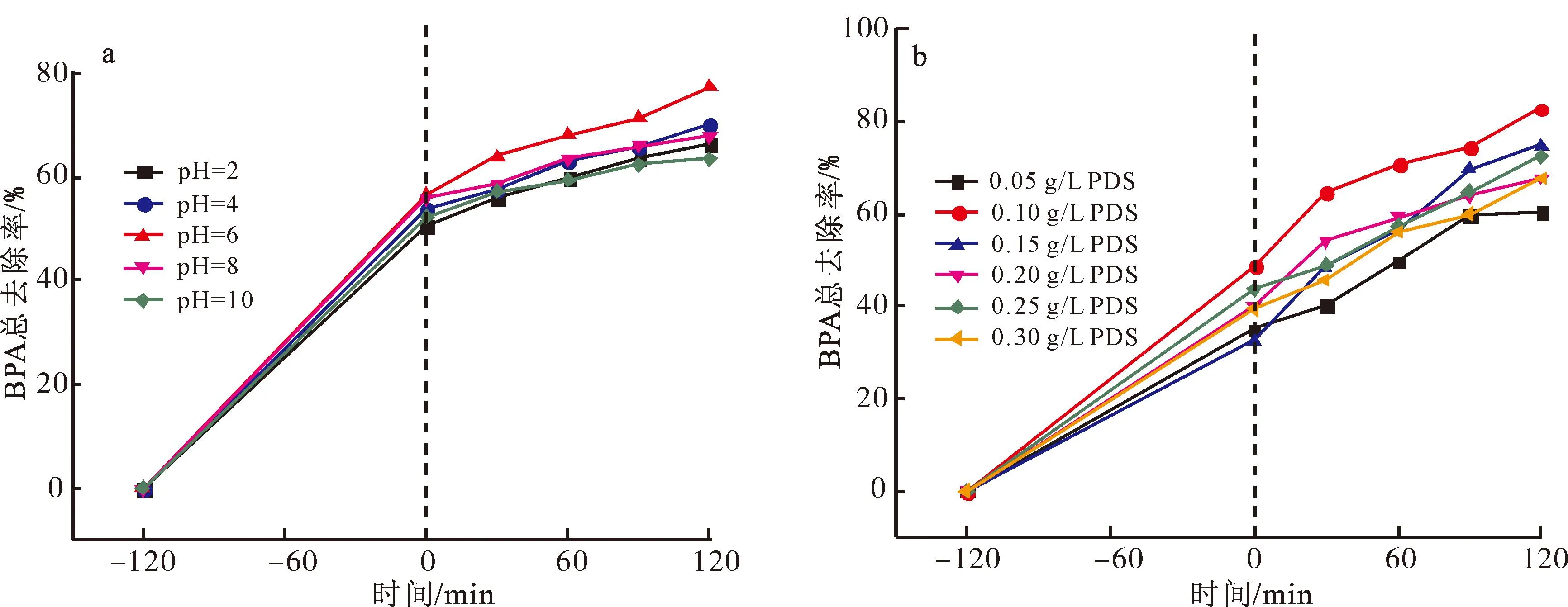
图8 不同pH值(a)和PDS质量浓度(b)对N-RGF活化PDS去除BPA的影响
2.2.3 性能评价
对RGF/PDS、N-RGF/PDS和PDS体系降解BPA的性能进行比较。活化PDS 120 min时,RGF和N-RGF对BPA的吸附去除率分别为48.29%和48.43%,降解去除率分别为8.47%和34.22%,总去除率分别为56.76%和82.64%(图9a)。动力学研究进一步显示(图9b),RGF和N-RGF活化PDS对BPA的拟一级降解动力学常数分别为0.001 42 min-1和0.008 35 min-1,N-RGF的催化活性是RGF的5.88倍。
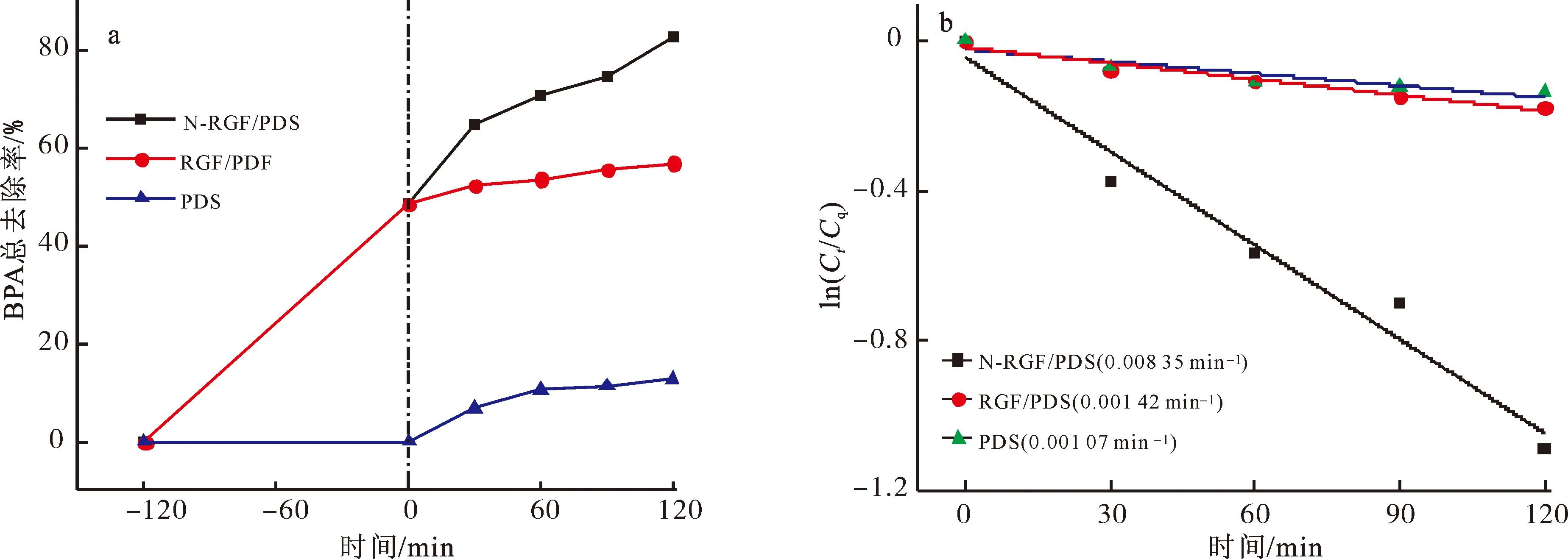
图9 RGF/PDS、N-RGF/PDS和PDS体系降解BPA的性能比较(a)及相应的伪一级动力学拟合曲线(b)

2.3 BPA去除机理研究
2.3.1 活性物种分析
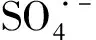

图10 活性物种捕获实验(a)及DMPO(b)和TEMP(c)的EPR图谱

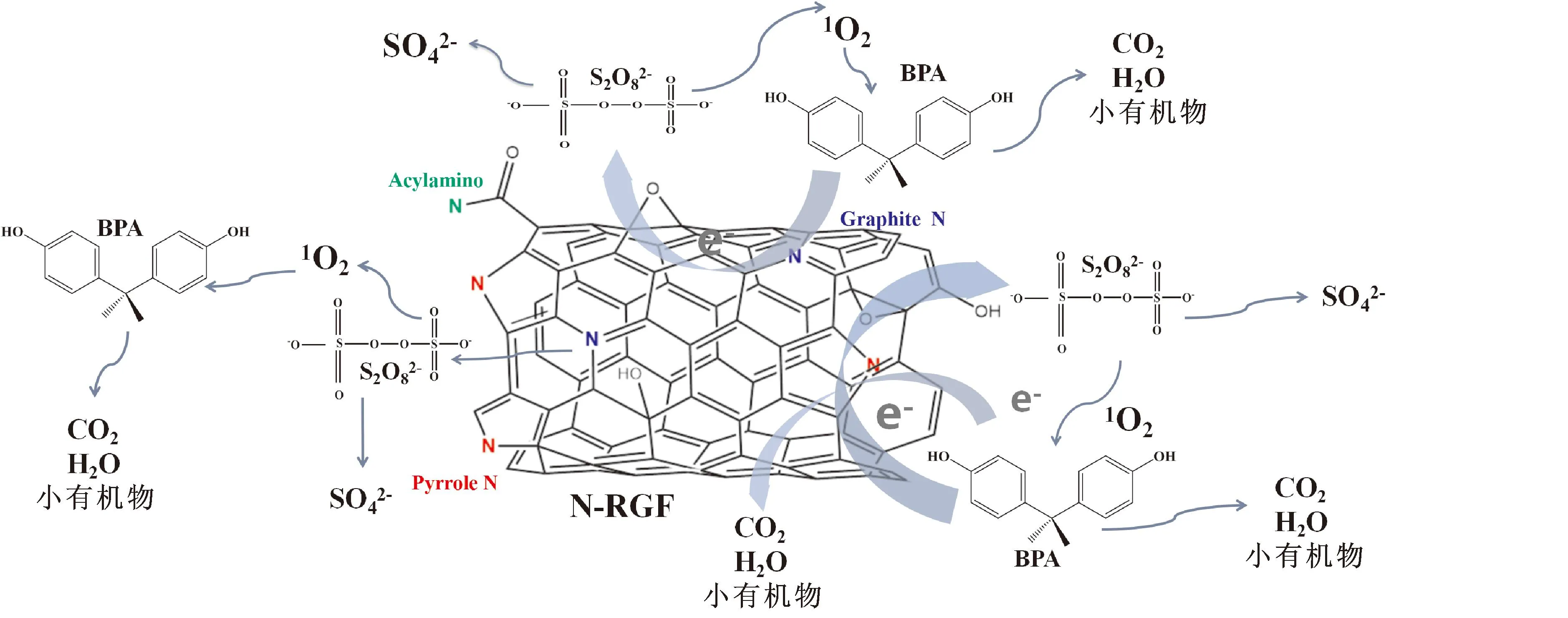
图11 N-RGF活化PDS去除BPA机理图
2.3.2 降解中间体检测及降解途径分析
新污染物降解中间体的检测是高级氧化技术研究的重要内容。本研究利用高效液相-质谱联用仪分析鉴定降解产物,提出了可能的降解途径,结果如图12所示。N-RGF活化PDS降解BPA的可能中间体有10个,因1O2具有低氧化能力(0.98 eV),矿化能力相对较弱[39],降解主要产生羟基化和醌类等中间体,其可能的降解途径如下:1)BPA中的2个富电子苯基在被1O2攻击后,β-裂解异丙基产生苯酚(P1,m/z=94)和4-异丙烯基苯酚(P2,m/z=134),P2进一步通过羟基化生成4-羟基苯乙酮(P3,m/z=136)或被1O2氧化降解为对苯醌(P4,m/z=108),然后苯醌在1O2作用下氧化开环,分解为有机酸、CO2和H2O。2)BPA在异丙基位断裂后,进一步羟基化生成4-(2-羟基丙-2-基)苯酚(P5,m/z=152)。3)BPA在异丙烯桥位裂解生成4-异丙基苯酚 (P6,m/z=136)和2-苯基丙-2-醇(P7,m/z=136),且由于羟基化产物不稳定,经异丙基乙烯桥[40]裂解后,易分解为单环芳烃。
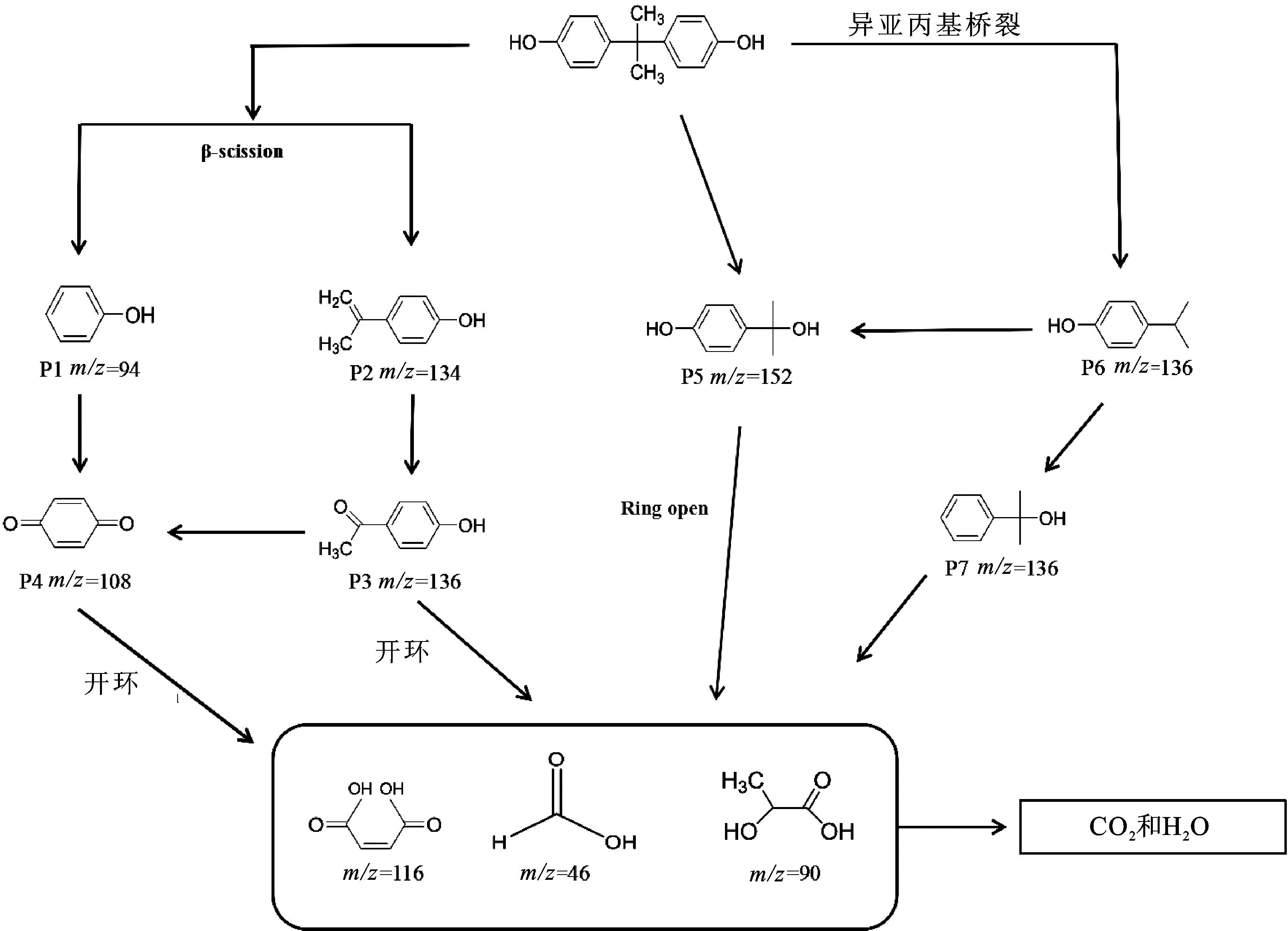
图12 N-RGF活化PDS降解BPA的可能途径
2.4 降解过程雌激素活性评价
进一步研究N-RGF活化PDS降解BPA过程中产生的雌激素活性,评价可能的环境风险。利用MTT比色法检测乳腺癌细胞MCF-7的活力[41],结果如图13所示。与对照组的细胞存活率(100%)相比,10 mg/L BPA溶液处理的MCF-7细胞经24 h增殖后,细胞存活率为112.14%,说明BPA雌激素可以促进MCF-7细胞增殖。然而,利用120 min时的降解液处理MCF-7细胞,经过24 h增殖后,细胞存活率降为86.35%,说明降解液不能促进MCF-7细胞增殖,降解液的雌激素活性基本消除。同理,当用10 mg/L BPA溶液处理MCF-7细胞,经过48 h增殖后,BPA溶液的细胞存活率为108.65%,而利用降解液处理的MCF-7细胞存活率仅为67.25%。由此可知,利用N-RGF活化PDS降解BPA能够有效减少或消除BPA的雌激素活性,且产生的10个可能的中间体没有雌激素活性或活性均小于母体BPA的雌激素活性。雌激素活性消除主要是产生的1O2破坏了BPA苯环上的对羟基,而对羟基在雌激素活性中起着重要作用[42]。
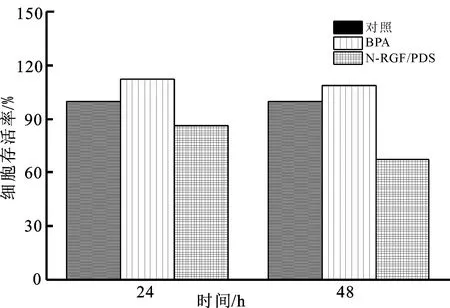
图13 N-RGF活化PDS降解BPA过程中的产物对MCF-7细胞活力的影响
2.5 溶解性有机质及无机阴离子的影响
为探究天然水体中普遍存在的天然有机质和无机阴离子对N-RGF活化PDS降解BPA的影响,将N-RGF分别用于降解含有4 mg/L胡敏素(HA)、富里酸(FA)、Cl-和HCO3-的BPA溶液,结果如图14所示。当体系中有HA和FA时,BPA总去除率均从82.64%增加至99.9%,可能是HA和FA中含有大量的酚羟基和羧基[43],可加速N-RGF表面的电子转移,促进N-RGF活化PDS降解BPA。然而,当体系中有4 mg/L Cl-和HCO3-时,BPA的总去除率分别为49%和83.4%,说明HCO3-不影响N-RGF活化PDS降解BPA,而Cl-对N-RGF活化PDS降解BPA具有明显抑制作用,其主要原因可能是Cl-与PDS的直接反应(化学式(1)、(2))减少了体系中的PDS含量,影响PDS活化产生1O2,进而影响BPA降解[44]。
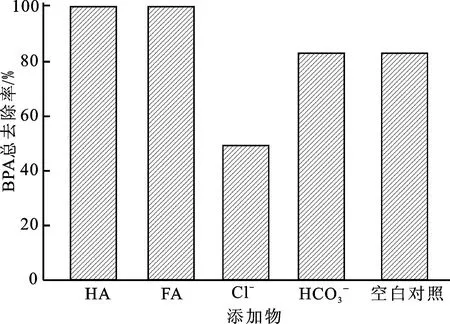
图14 HA、FA、Cl-、HCO3-对 N-RGF活化PDS降解BPA的影响
Cl-+S2O82-+ H+→SO42-+Cl2+ H2O,
(化学式1)
Cl-+ S2O82-→SO42-+HOCl。
(化学式2)
2.6 材料稳定性研究
为探究N-RGF的可重复使用性和稳定性,将N-RGF重复应用于活化PDS去除初始质量浓度10 mg/L BPA的溶液中,实验条件为0.5 g/L催化剂和0.1 g/L PDS,在N-RGF活化PDS降解BPA 120 min后,用镊子取出N-RGF,甲醇、水交替洗涤N-RGF至中性。由图15可知,N-RGF重复使用5次时对BPA的吸附去除率分别为49.38%、46.84%、47.16%、48.42%和42.66%,降解去除率分别为29.74%、27.54%、30.96%、23.72%和32.59%,总去除率分别为79.12%、74.38%、78.12%、72.41%和75.25%。重复使用5次后N-RGF对BPA的总去除率保持在72%,表现出足够的稳定性,且具有易回收能力。这种易回收性将减少RGO使用时释放带来的环境风险,降低使用成本。
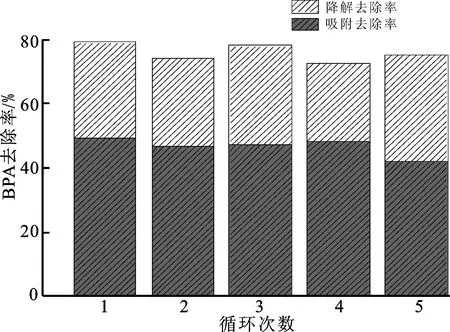
图15 N-RGF活化PDS降解BPA的重复使用实验
3 结论
以吡咯为氮源和溶胀剂,通过水热-冷冻干燥法制备出了易回收的氮掺杂还原氧化石墨烯泡沫(N-RGF),其最佳制备条件是氮掺杂量7.5%、水热温度180 ℃、反应时间20 h。制备的N-RGF呈网状三维多孔结构,孔道分布相对均匀(2~3 μm),且具有孔体积大和石墨相氮含量高的优势。RGF和N-RGF活化PDS降解BPA的总去除率分别为56.76%和82.64%,N-RGF活化PDS降解BPA的动力学常数是RGF的5.88倍,且N-RGF表现出更好的稳定性。N-RGF活化PDS降解BPA的主要活性物种是单线态氧,属非自由基活化,可消除水中溶解性有机质HA和FA的抑制问题。N-RGF活化PDS降解BPA的可能中间体有10个,且无明显的雌激素活性。
