丽江山荆子链状化学成分研究
2024-02-27刘怡君郎利娟白惠荣肖朝江
刘怡君,杨 丽,郎利娟,白惠荣,姜 北,肖朝江*
(1.云南省滇西抗病原植物资源筛选研究重点实验室,云南 大理 671000;2.大理大学药物研究所,云南 大理 671000;3.大理大学药学院,云南 大理 671000;4.毕节医学高等专科学校,贵州 毕节 551700)
丽江山荆子Malus rockiiRehd.系蔷薇科Rosaceae 苹果属Malus植物,属乔木,别名喜马拉雅山荆子,主要分布于我国云南、四川、西藏等地,生长于海拔2 400~3 800 m 的山谷杂木林中〔1〕。丽江山荆子果实可治疗肝病、腹泻、眼疾、月经不调等〔2〕。课题组前期研究发现根皮苷为丽江山荆子的主成分,其具有较好的体内外降脂活性,以及中等的体内抗疟和镇痛活性〔3〕;课题组还从丽江山荆子中分离得到2 个二苯并呋喃类化合物,二者在体外均具有显著的降脂活性〔4〕。
为进一步了解丽江山荆子的化学成分,本实验对丽江山荆子干燥枝叶95%乙醇提取物进行化学成分研究,从中分离鉴定了7 个链状化学成分,分别为反式植醇(1)、植物烯醛(2)、棕榈酸植酯(3)、1-十六烷酸甘油单酯(4)、9,12,13-三羟基-(10E,15Z)-十八碳二烯酸甲酯(5)、α-亚麻酸(6)、十八醇(7),所有化合物均为首次从丽江山荆子中分离得到,其中化合物1~6 为首次从苹果属植物中分离得到。化合物1~7的结构式见图1。
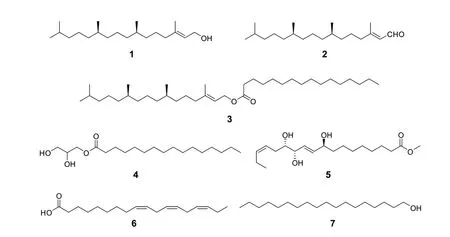
图1 化合物1~7的结构式
1 仪器与材料
AvanceⅢ-400 型核磁共振波谱仪(德国Bruker公司);AL204 型万分之一电子天平(梅特勒-托利多仪器上海有限公司);薄层色谱硅胶板GF254、柱层析硅胶(青岛海洋化工有限公司);MCI gel CHP20∕P120(75~150 μm)、MCI gel CHP20P(37~75 μm)(日本三菱公司);Sephadex LH-20 葡聚糖凝胶(瑞典Amersham Bioscience 公司);工业纯石油醚、氯仿、乙酸乙酯、丙酮、甲醇,经重蒸后使用。
本实验所用植物样品于2018年6月采自云南省大理苍山,经大理大学药学院生药教研室张德全教授鉴定为丽江山荆子,植物标本(编号:20180611-2)存放于大理大学云南省滇西抗病原植物资源筛选研究重点实验室。
2 提取与分离
丽江山荆子干燥枝叶13.0 kg,粉碎后经95%乙醇冷浸提取4次,每次24 h,合并冷浸液,减压浓缩得总浸膏2.1 kg。总浸膏经硅胶柱色谱,氯仿-丙酮梯度洗脱(1:0→0:1),得8 个主要组分(Fr.A~Fr.H)。Fr.A(65.0 g)经反复硅胶柱色谱(石油醚-乙酸乙酯50:1→10:1,石油醚-丙酮100:1→10:1)和Sephadex LH-20凝胶柱色谱(氯仿-甲醇1:1)洗脱得到化合物1(208.0 mg)和化合物7(800.0 mg)。Fr.B(62.5 g)经反复硅胶柱色谱(石油醚-乙酸乙酯100:1→10:1,石油醚-丙酮1∶0→0∶1,纯氯仿)和Sephadex LH-20 凝胶柱色谱(氯仿-甲醇1∶1)洗脱得到化合物2(10.3 mg)、化合物3(11.8 mg)和化合物6(224.0 mg)。Fr.C(28.0 g)经反复硅胶柱色谱(氯仿-乙酸乙酯5:1,氯仿-丙酮100∶1)洗脱得到化合物4(65.0 mg)。Fr.E(40.0 g)经反复硅胶柱色谱(石油醚-丙酮10:1,氯仿-丙酮50:1→40:1)、Sephadex LH-20凝胶柱色谱(氯仿-甲醇1:1)和MCI柱色谱(70%甲醇)洗脱得到化合物5(10.5 mg)。
3 结构鉴定
化合物1:无色油状物。1H-NMR(400 MHz,CDCl3)δ:5.40(1H,t,J=7.0 Hz,H-2),4.14(2H,d,J=7.0 Hz,H-1),1.98(2H,t,J=7.4 Hz,H-4),1.66(3H,brs,H-20),0.87(6H,d,J=6.4 Hz,H-16,17),0.85(3H,d,J=6.1 Hz,H-18),0.84(3H,d,J=6.6 Hz,H-19)。以上波谱数据与文献〔5〕报道基本一致,故鉴定该化合物为反式植醇。
化合物2:黄色油状物。1H-NMR(400 MHz,CDCl3)δ:9.99(1H,d,J=8.2 Hz,H-1),5.88(1H,d,J=8.2 Hz,H-2),2.16(3H,s,H-20),0.86(6H,d,J=6.4 Hz,H-16,17),0.85(3H,d,J=6.6 Hz,H-18),0.84(3H,d,J=6.6 Hz,H-19);13C-NMR(100 MHz,CDCl3)δ:191.5(d,C-1),127.3(d,C-2),164.6(s,C-3),41.0(t,C-4),24.8(t,C-5),36.5(t,C-6),32.7(d,C-7),37.4(t,C-8),24.5(t,C-9),37.3(t,C-10),32.8(d,C-11),37.3(t,C-12),24.7(t,C-13),39.4(t,C-14),28.0(d,C-15),22.7(q,C-16),22.8(q,C-17),19.8(q,C-18),19.6(q,C-19),17.6(q,C-20)。以上波谱数据与文献〔6〕报道基本一致,故鉴定该化合物为植物烯醛。
化合物3:白色固体。1H-NMR(400 MHz,CDCl3)δ:5.33(1H,t,J=7.1 Hz,H-2),4.58(2H,d,J=7.1 Hz,H-1),2.29(2H,t,J=7.6 Hz,H-2'),2.00(2H,t,J=6.7 Hz,H-4),1.69(3H,brs,H-20),0.81~0.87(15H,overlap,H-16,17,18,19,16');13CNMR(100 MHz,CDCl3)δ:61.3(t,C-1),118.2(d,C-2),142.7(s,C-3),39.9(t,C-4),25.1(t,C-5),36.7(t,C-6),32.9(d,C-7),37.5(t,C-8),24.5(t,C-9),37.3(t,C-10),32.7(d,C-11),37.4(t,C-12),24.9(t,C-13),39.4(t,C-14),28.0(d,C-15),22.7(q,C-16),22.8(q,C-17),19.8(q,C-18),19.8(q,C-19),16.4(q,C-20),174.0(s,C-1'),34.5(t,C-2'),24.9(t,C-3'),29.2~29.8(t,C-4'~13'),32.0(t,C-14'),22.8(t,C-15'),14.2(q,C-16')。以上波谱数据与文献〔7〕报道基本一致,故鉴定该化合物为棕榈酸植酯。
化合物4:白色粉末。1H-NMR(400 MHz,CDCl3)δ:4.18(1H,dd,J=11.6,4.8 Hz,H-1a),4.13(1H,dd,J=11.6,6.1 Hz,H-1b),3.92(1H,m,H-2),3.68(1H,dd,J=11.5,3.8 Hz,H-3a),3.58(1H,dd,J=11.5,5.9 Hz,H-3b),2.34(2H,t,J=7.6 Hz,H-2'),1.61(2H,m,H-3'),1.24(24H,brs,H-4'~15'),0.87(3H,t,J=6.8 Hz,H-16');13C-NMR(100 MHz,CDCl3)δ:65.1(t,C-1),70.3(d,C-2),63.3(t,C-3),174.5(s,C-1'),34.2(t,C-2'),24.9(t,C-3'),29.2~29.7(t,C-4'~13'),32.0(t,C-14'),22.7(t,C-15'),14.2(q,C-16')。以上波谱数据与文献〔8〕报道基本一致,故鉴定该化合物为1-十六烷酸甘油单酯。
化合物5:白色固体。1H-NMR(400 MHz,CD3COCD3)δ:5.61(2H,overlap,H-10,11),5.32(2H,overlap,H-15,16),3.93(1H,brs,H-9),3.80(2H,overlap,H-12,-OH),3.64(1H,s,-OH),3.57(1H,s,-OH),3.48(3H,s,-OCH3),3.30(1H,brs,H-13),2.20(1H,m,H-14a),2.17(2H,t,J=7.5 Hz,H-2),1.98(1H,m,H-14b),1.93(2H,m,H-17),1.46(2H,m,H-3),1.34(2H,m,H-8),1.19(8H,brs,H-4~7),0.81(3H,t,J=7.5 Hz,H-18);13C-NMR(100 MHz,CD3COCD3)δ:174.1(s,C-1),34.2(t,C-2),25.6(t,C-3),29.7(t,C-4),30.0(t,C-5),30.2(t,C-6),26.1(t,C-7),38.3(t,C-8),72.0(d,C-9),136.5(d,C-10),130.4(d,C-11),75.3(d,C-12),75.3(d,C-13),31.3(t,C-14),126.6(d,C-15),133.3(d,C-16),21.2(t,C-17),14.5(q,C-18),51.4(q,-OCH3)。以上波谱数据与文献〔9〕报道基本一致,故鉴定该化合物为9,12,13-三羟基-(10E,15Z)-十八碳二烯酸甲酯。
化合物6:无色油状固体。1H-NMR(400 MHz,CDCl3)δ:5.35(6H,m,H-9,10,12,13,15,16),2.80(4H,m,H-11,14),2.34(2H,t,J=7.5 Hz,H-2),2.06(4H,m,H-8,17),1.63(2H,m,H-3),1.25~1.32(8H,brs,H-4~7),0.97(3H,t,J=7.5 Hz,H-18)。以上波谱数据与文献〔10〕报道基本一致,故鉴定该化合物为α-亚麻酸。
化合物7:白色粉末。1H-NMR(400 MHz,CDCl3)δ:3.64(2H,t,J=6.7 Hz,H-1),1.56(2H,qui,J=6.7 Hz,H-2),1.25(30H,brs,H-3~17),0.87(3H,t,J=6.8 Hz,H-18)。以上波谱数据与文献〔11〕报道基本一致,故鉴定该化合物为十八醇。
4 讨论
本实验首次从丽江山荆子干燥枝叶95%乙醇提取物中分离鉴定了7 个链状化合物,包括2 个链状二萜类化合物(1 和2)、4 个脂肪酸类化合物(4~7),以及1 个链状二萜和长链脂肪酸的加合物(3),所有化合物均为首次从丽江山荆子中分离得到,其中化合物1~6为首次从苹果属植物中分离得到。根据文献报道,反式植醇具有抗菌活性,高度抑制MTB C171Q 受体结核分枝杆菌KasA,体外活性接近异烟肼〔12〕;α-亚麻酸具有抗过敏、抗炎、改善肥胖引起的胰岛素抵抗等药理活性〔13-14〕。由此推断,丽江山荆子的民间用药有一定合理性,其潜在药用价值亟待开发。
