超声评估椎动脉走行变异
2024-02-26刘一铭丁舒健文艳玲
张 峰,刘一铭,陈 瑶,丁舒健,文艳玲
(中山大学附属第六医院超声科,广东 广州 510655)
椎动脉(vertebral artery, VA)起源于左、右侧锁骨下动脉,于颅内汇合成为基底动脉,是脑干及颅内后循环的供血动脉。解剖学上,VA分为V1段(颈段,自锁骨下动脉分支至进入C6横突孔)、V2段(横突孔内段,经C6横突孔至C2横突孔)、V3段(枕段,入C2横突孔后经C1横突孔走行于C1动脉沟内,穿硬膜入颅前)及V4段(颅内段,经枕骨大孔,在脑桥及延髓交界处合成基底动脉)[1]。VA解剖变异较多,临床将其未经C6横突孔上行定义为VA走行变异(VA course variation, VA-CV);既往相关研究[2-7]多关注VA-CV解剖结构、临床症状和转颈后变化。本研究观察超声评估VA-CV解剖结构及相关血流动力学变化的价值。
1 资料与方法
1.1 研究对象 回顾性分析2019年10月—2022年11月中山大学附属第六医院经超声诊断的41例VA-CV患者(VA-CV组),男22例、女19例,年龄35~84岁、平均(55.2±13.8)岁;其中8例为双侧VA-CV、33例为单侧VA-CV(左侧11例、右侧22例)。纳入标准:①年龄>18岁;②图像质量良好,清晰显示双侧VA和锁骨下动脉起源及走行。排除标准:①冠心病、卒中、风湿结缔组织病史;②颈动脉重度狭窄(狭窄率70%~90%)及闭塞;③颅内及颅外段VA、基底动脉和锁骨下动脉狭窄率>50%。同期纳入41例非VA-CV患者(对照组),男21例、女20例,年龄26~79岁、平均(54.8±11.5)岁。本研究经医院伦理委员会批准(2023ZSLYEC-237),检查前所有患者均知情同意。
1.2 仪器与方法 采用Philips Epiq7超声诊断仪、L11-3线阵探头(3.0~11.0 MHz)及C5-1凸阵探头(1.0~5.0 MHz)。由分别具有5、20年工作经验的超声科医师各1名,参照《中国脑卒中血管超声检查指导规范》[8]扫查颈部,检测VA有无变异(VA经C6横突孔上行为走行正常,反之为变异),以及变异侧别、V1段起源位置、锁骨下动脉近段(proximal subclavian artery, PSCA)长度[VA起始点与锁骨下动脉分支水平(左侧锁骨下动脉为至主动脉弓,右侧锁骨下动脉为至无名动脉)的距离[8],见图1、2]、VA进入横突孔位置及V2段管径。将VA-V1段起源于锁骨下动脉且PSCA≥14 mm(对照组右侧PSCA中位数的50%)定义为起源正常,将起源于锁骨下动脉且PSCA<14 mm定义为低位起点,将未起源于锁骨下动脉定义为起源异常[4]。于CDFI模式下测量VA收缩期峰值血流速度(peak systolic velocity, PSV)及舒张末期血流速度(end-diastolic velocity, EDV)。上述测值均以2名医师所测平均值作为最终结果。
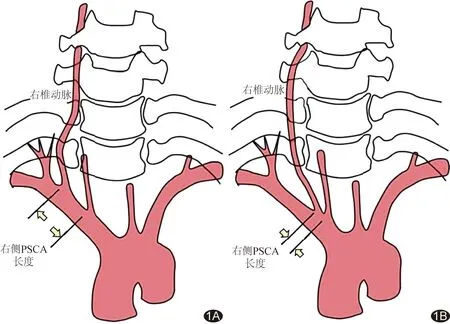
图1 测量右侧PSCA长度示意图 A.对照组; B.VA-CV组
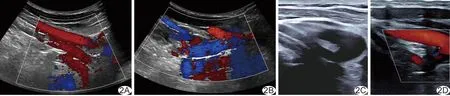
图2 超声测量PSCA长度 A、B.于CDFI模式下测量对照组左侧(A)及右侧(B)PSCA长度; C.二维超声测量VA-CV组右侧PSCA长度; D.于CDFI模式下测量VA-CV组右侧PSCA长度 (*为测量游标,分别置于VA起始点及锁骨下动脉分支水平)
2 结果
2.1 一般资料 2组患者性别、年龄差异均无统计学意义(χ2=0.049,P=0.825;t=-0.147,P=0.883)。
2.2 VA-CV解剖结构 于VA-CV组共检出49支变异VA,包括左侧19支、右侧30支;17支VA起源异常,其中左侧16支起源于主动脉弓、右侧1支起源于右侧甲状颈干。VA-CV组内左侧VA起源异常多于右侧、右侧VA低位起源多于左侧(P均<0.001),见表1。49支变异VA中,33支(左侧13支、右侧20支)自C5-6横突孔进入椎间隙,11支(左侧3支、右侧8支)自C4-5横突孔进入椎间隙,5支(左侧3支、右侧2支)自C3-4横突孔进入椎间隙。
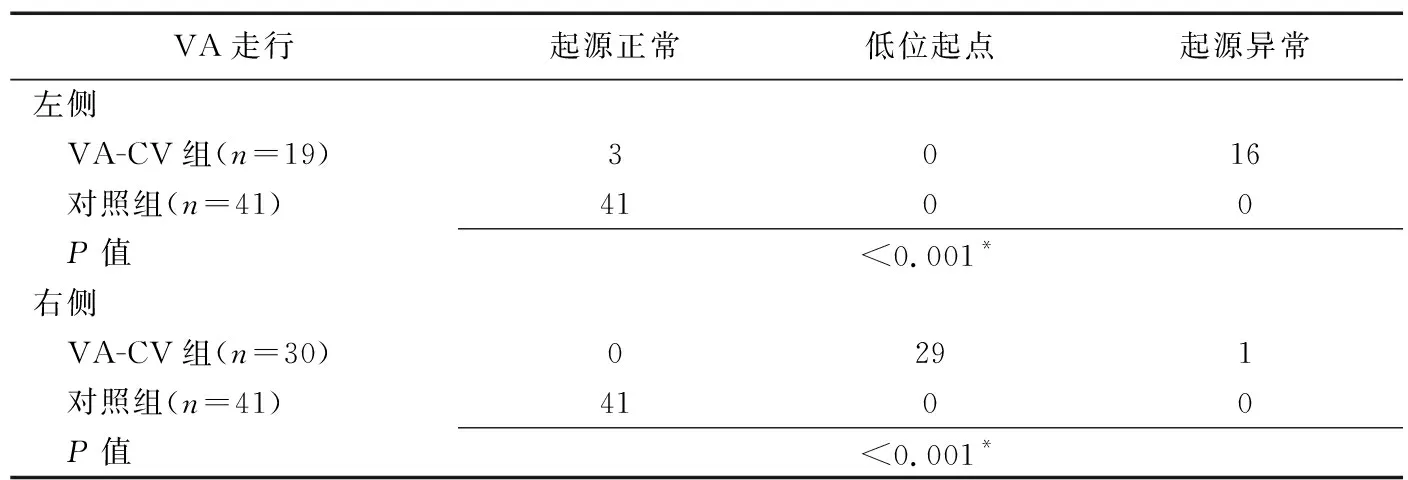
表1 组间VA起源比较(支)
2.3 PSCA长度 因VA起源异常时无法计算PSCA长度,统计分析PSCA时予以剔除。观察者间测量PSCA长度的一致性良好,ICC=0.987[95%CI(0.975,0.993)]。对照组左、右侧PSCA长度分别为(35.91±5.09)mm、(28.66±4.98)mm。VA-CV组剔除左侧17支起源异常VA后仅余3支左侧变异VA,未能进行统计分析;右侧29支变异VA的PSCA长度为(5.44±3.65)mm,小于对照组[(28.66±4.98)mm](t=-22.357,P<0.001)。VA-CV组内,右侧VA-CA患者中,VA自C5-6、C4-5及C3-4横突孔进入椎间隙者PSCA长度分别为(6.79±3.48)mm(n=19)、(3.48±2.40)mm(n=8)及0.5 mm(n=2),自C5-6横突孔进入者PSCA长度大于自C4-5、C3-4进入者(P=0.048、0.032)。
2.4 VA超声指标 VA-CV组内,左侧VA-CV患者V2段管径小于且EDV低于对照组(P均<0.05),右侧VA-CV患者V2段管径、PSV及EDV与对照组差异均无统计学意义(P均>0.05),见表2。
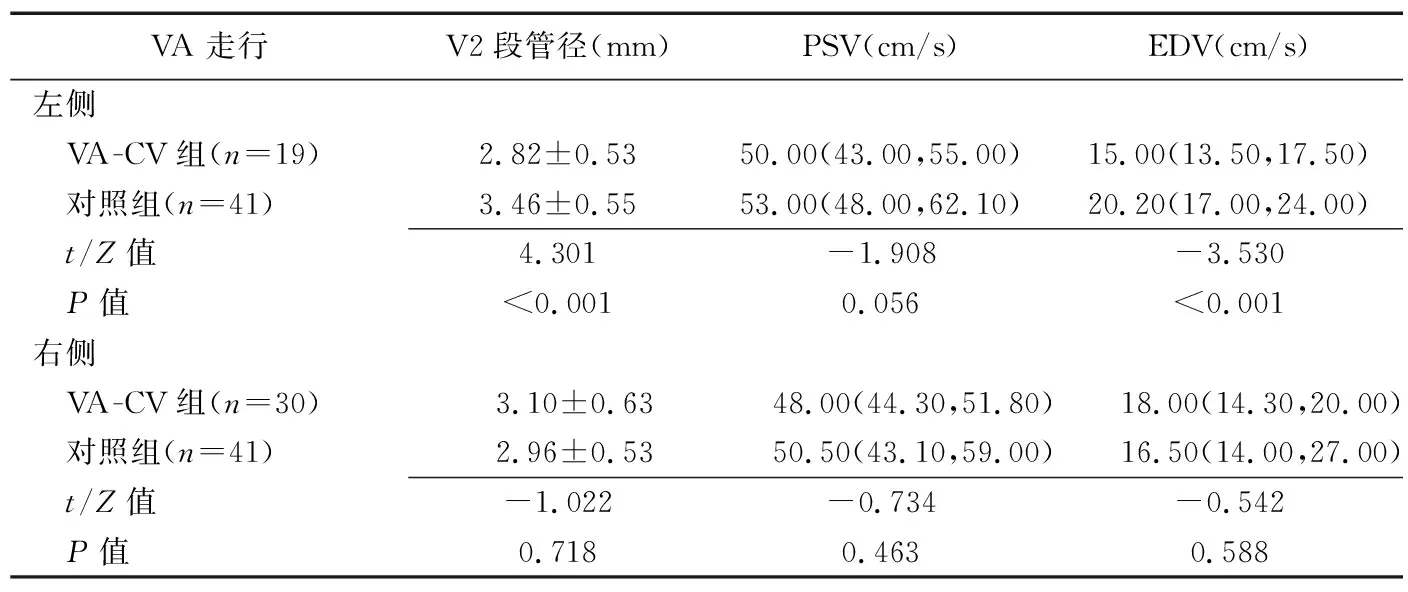
表2 组间VA超声指标比较
3 讨论
人类胚胎发育过程中,共7对节间动脉与主动脉背侧相连,逐渐从椎间隙进入横突孔而完成由下而上的融合,其中第6节间动脉最后形成VA近段(V1段);期间每支节间动脉均可能出现发育不全,导致不同部位走行变异或起源变异[5]。本研究中,右侧VA-CV多于左侧,与张蕾等[2-3]所见基本相符;且VA-CV与VA起源相关:左侧VA-CV多合并VA起源异常,右侧VA-CV的VA多为低位起点。张蕾等[2]报告23例右侧VA-CV患者的PSCA长度为(0.39±0.49)cm。YI等[9]回顾性分析223例VA-CV患者446支VA的CT血管造影资料,发现异常起源VA走行变异率达50%。本研究检出的49支变异VA中,17支存在起源异常(17/49,34.69%)。
VA与锁骨下动脉远端夹角可影响介入操作选择经VA入路、曝光时间、对比剂用量、技术失败率及并发症发生率等[10]。VA起始段是后循环病变中最常发生狭窄的部位。锁骨下动脉近端、尤其VA起始部存在低速涡旋流动,这种血流状态不仅可对血管壁造成横向冲击力而损伤血管内膜,也为血液中的脂类等大分子物质和血细胞在该区域附壁堆积形成粥样斑块提供了条件[11]。此外,VA与锁骨下动脉远端的夹角还与VA起始位置有关:VA起始位置越低,其与锁骨下动脉所构成的角度越小。本研究右侧VA-CV患者PSCA小于对照组,且VA横突孔入孔位置越高,其PSCA越短,可能由于多合并VA低位起点,使其与锁骨下动脉远端的夹角变小。本课题组前期研究[12]结果证实走行变异为VA起始段狭窄的保护因素。临床行颈动脉压迫试验时,可能因VA低位起点而压迫到VA,进而影响颅内段血流并导致误判。本研究还发现左侧VA-CV多合并VA异常起源于主动脉弓,此时锁骨下动脉近段狭窄可不影响VA血流。上述研究结果提示,超声检出VA-CV时,应注意分别分析锁骨下动脉血流及VA频谱变化。
VA发育不良可能与血管生长方式、遗传、血流动力学有关,目前对此尚未完全明确;“血流剪切力理论”提出VA发育不良可能与左侧VA起源于主动脉弓一级分支(如左锁骨下动脉)或发育过程中受到更高的血流剪应力有关;“优势半球理论”认为多数人为右利手、左侧大脑为优势半球,左侧大脑半球需要更多血流以满足功能需求,导致左侧VA管径常大于右侧[13]。本研究发现左侧VA-CV患者VA管径较为细小,提示VA-CV与管径发育不良有关。关于血流动力学改变,本研究VA-CV组中,右侧VA-CV患者PSV、EDV与对照组差异均无统计学意义,左侧VA-CV患者EDV低于对照组而PSV与对照组差异无统计学意义,提示VA-CV可能不影响VA-V2段PSV,而EDV降低则与其管径较小有关。
本研究的主要局限性:①为单中心回顾性分析,可能存在选择性偏倚;②基于二维声像图测量血管长度可能存在误差,且未与数字减影血管造影或CT血管造影等进行对照;③未涉及高血压、高血脂、糖尿病及吸烟史等因素的影响。
综上所述,超声可客观评价VA走行变异、起源异常及血流动力学变化。右侧VA-CV较左侧常见,且多呈低位起点;入横突孔位置越高,则PSCA长度越短;左侧VA-CV常合并管径变窄、起源异常及EDV降低。
利益冲突:全体作者声明无利益冲突。
作者贡献:张峰研究实施、撰写文章;刘一铭统计分析;陈瑶研究实施;丁舒健图像处理;文艳玲指导、修改文章。
