维生素A醋酸酯的合成方法综述
2024-02-21王子强尹实邓家诚
王子强,尹实,邓家诚
(杭州下沙生物科技有限公司,浙江 杭州 310000)
1913年,美国Margaret Davis 等4 位科学家发现鱼肝油可以治愈干眼病,并从鱼肝油中提纯出一种黄色黏稠液体;1920年,英国科学家将其正式命名为维生素A,国际上正式将维生素A 看作营养上的必需因素,缺乏后会导致夜盲症[1]。但早在1000 多年前,中国唐代医学家孙思邈(公元581~682年)在《千金方》中就记载了用动物肝脏可治疗夜盲症,其实这就是维生素A 的作用描述,也是最早的关于维生素A 的实用记录之一。
维生素A 通过促进视觉细胞内感光细胞形成,具有维持视觉功能;维生素A 可以调控基因表达,减弱上皮细胞向鳞片状分化,从而增加上皮生长因子受体的数量,因此具有维持上皮结构完整和健全的功能;维生素A 也具有类固醇激素的作用,可促进糖蛋白合成,从而具有促进骨骼生长发育、抗氧化衰老、促进细胞分化、调节红细胞生成等功能[2-3]。维生素A 遇酸、空气、氧化性物质以及高温、紫外线容易被破坏,因此市场上大部分维生素A 为较稳定的维生素A醋酸酯[4]。
维生素A醋酸酯(vitamin A acetate)别名视黄酯,是一种脂溶性维生素,呈透明状,显亮黄到淡红色的油状物,可溶于水和醇、醚、烃、卤代烃等大多数有机溶剂。维生素A醋酸酯具有5 个共轭双键,理论上有32 个几何异构体,但由于立体位阻效应,自然界仅有全反式体9-顺式体,13-顺式体,9,13-双顺式体和有位阻的11-顺式体; 而且全反式的生物活性最高,如图1所示,分子式:C22H32O2,分子量:328.5,化学名称为全反-3,7-二甲基-9-(2,6,6-三甲基-1-环己烯基)-2,4,6,8-壬四烯-1-乙酯,是维生素A 的天然形式[5-6]。

图1 维生素A醋酸酯结构式
本文详细介绍维生素A醋酸酯的7 条合成路线,包括以格氏反应为特征的Hoffmann-La Roche 路线、M.Rosenberger 路线、乙炔基锂路线,以Witting 反应为特征的BASF 路线、Witting-Horner 路线、氯化亚膦酸酯路线,以Julia-Lythgoe烯基化反应为特征的Rhone-Poulenc 路线。将这7条合成路线的优缺点进行归纳,并提出相应的改进方向,以期对未来合成研究提供参考。
1 维生素A醋酸酯的化学合成工艺
1.1 Hoffmann-La Roche 合成路线
Isler 等[7-8]开发了一种维生素A醋酸酯合成方法,如Scheme 1所示。β-紫罗兰酮与氯乙酸甲酯,在甲醇钠存在的条件下,经过Darzens 缩合得到C14醛,之后与C6烯炔醇经过格氏缩合得到碳骨架,再经过氢化、乙酰化、脱水反应得到维生素A醋酸酯,该路线总收率59%左右。

Scheme 1
该路线于1948年首次实现了工业化,以格氏反应为特征,也是世界各地采用最多的维生素A醋酸酯合成方法。优点是技术成熟,中间体立体构型较为清晰,未使用特殊原料,对设备要求较低;缺点是中间体六碳醇的合成难以消除反式中间体,以及通过Darzens 缩合制备十四醛中间体时,β-紫罗兰酮难以反应完全,其与十四醛沸点相差很小,难以通过精馏分离,会被带入下一工序,影响缩合物质量。Roche 路线步骤较长,工艺路线在骨架合成之后仍然需要经过4 步反应才能合成最终产品。又因为大多数中间体官能团较为活泼,工艺控制要求比较严格,因此使得其收率难以保证。中间体C6烯炔醇的合成以丙酮为原料,通过Aldol 缩合、脱水得到丁烯酮,丁烯酮再与乙炔锂反应后经硫酸转换得到;由于C6烯炔醇生产过程中的丁烯酮精制容易引起聚合,炔化过程要用到危险的乙炔作为原料,以及C6烯炔醇的蒸馏过程容易引起爆炸,存在严重的安全隐患。
1.2 M.Rosenberger 路线
1980年,Rosenberger 等[9]开发了开发了一条新的合成十四醛路线,见Scheme 2。使用硫鎓(CH3)3S+X-与β-紫罗兰酮反应得到环氧中间体,以溴化镁为催化剂,乙醚为溶剂,将其水解为烯醇式结构,经烯醇互变反应得到十四醛,提高了十四醛的质量与收率,两步收率可达80%左右。

Scheme 2
采用硫鎓(CH3)3S+X-与β-紫罗兰酮反应得到环氧中间体,避免使用氯乙酸甲酯这个气味较大的有毒试剂,对环境污染较小。该路线(CH3)3S+X-的X-对反应收率的影响较大,(CH3)3S+X-在NaH 催化下有较好的反应收率;但相应的(CH3)3S+X-制备需要相对高压设备,对生产要求相对严格,而且该路线仅改进了Roche 路线的前两步反应,整体收率并未有较大改变,同样具有Roche 路线的缺点。
1.3 乙炔基锂合成路线
郑兆祥等[10]开发了一种维生素A醋酸酯制备方法,见Scheme 3。4-羟基-2-丁酮经乙炔基锂加成、氨基锂取代得锂氧基保护的C6中间体,再经过与C14醛加成、选择性氢化、酰化、溴代、脱溴等步骤得到维生素A醋酸酯。其中乙炔基锂加成反应温度为-15 ℃~-10 ℃,溶剂为四氢呋喃、甲苯、乙醚、异丙醚中的一种或多种;C6中间体与C14醛加成酸化单步重量收率在97%左右; 原料4-羟基-2-丁酮的利用率可以达到60%~65%。
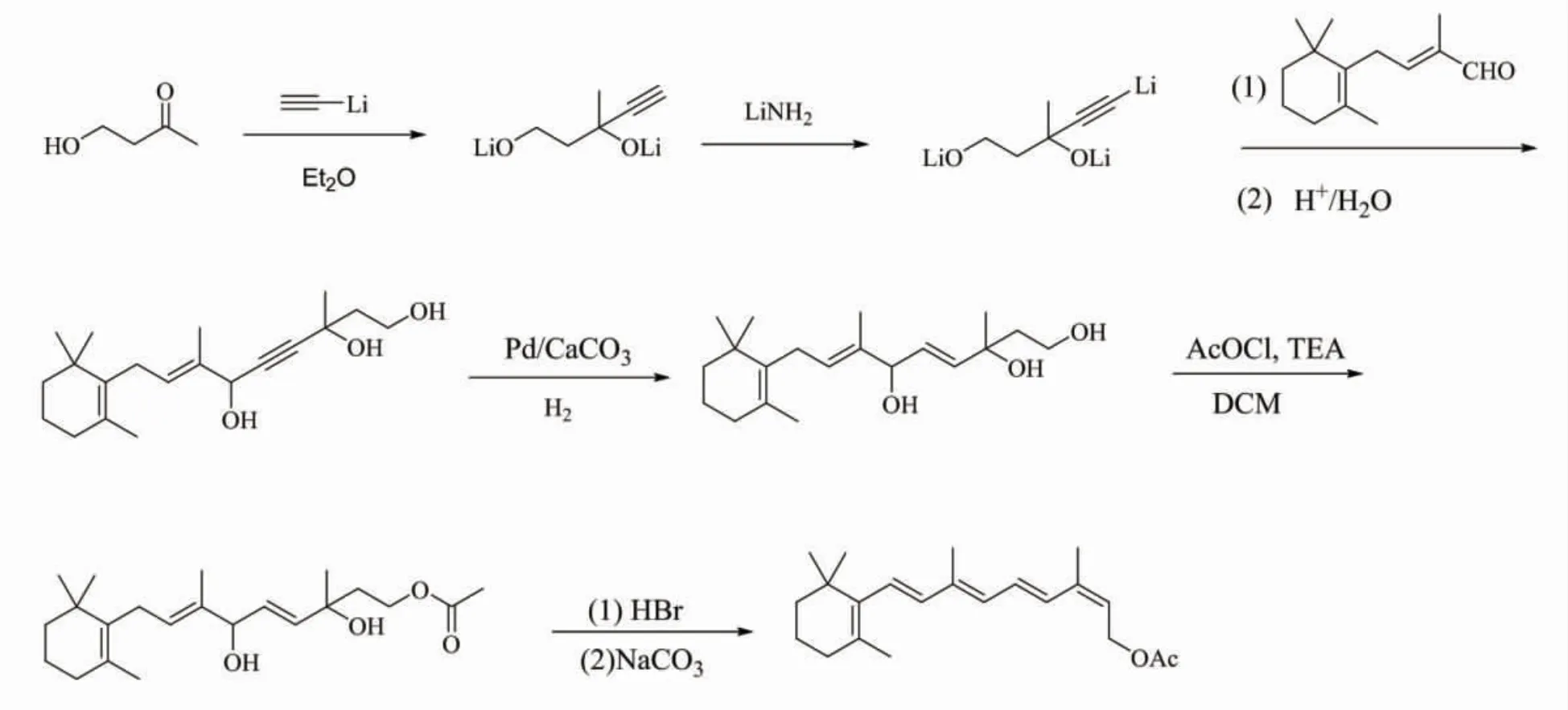
Scheme 3
乙炔基锂合成路线是对Roche 路线的改进,由4-羟基2-丁酮与乙炔基锂反应制备C6中间体的方法避免了C6烯炔醇这个剧毒中间体的生成,提高了工艺安全性;使用锂试剂,由于目前市场上锂价格较高,该方法不适用大规模工业化生产。该路线避开了Roche 合成路线中制备剧毒中间体顺式六碳醇甲基乙烯酮,且不用经过C6烯炔醇提纯过程,提高了工艺路线安全性和原料利用率。
1.4 BASF 合成路线
迄今为止,各种合成路线中能与Hoffmann-La Roche 合成路线竞争的主要是BASF 公司开发的C15+C5路线。这条路线是BASF 公司Pommer等[11-12]于20世纪50年代开发的,以Wittig 反应为特征后经不断完善,于1971年投产,其反应路线如Scheme 4所示。β-紫罗兰酮与乙炔进行加成反应得到乙炔-β-紫罗兰酮,选择性加氢后得乙烯-β-紫罗兰酮,然后与三苯基膦·HX 复合物或者分别与三苯基膦和HX 反应得到C15膦卤代盐,C15膦卤代盐与C5醛酯在碱性环境下经Wittig 反应得到维生素A醋酸酯,最后一步所用的碱为甲醇钠、氢氧化钾、环氧乙烷等,反应溶剂为甲醇、乙醇、N,N-二甲基甲酰胺、四氢呋喃等;之后经过光学异构化反应,得到全反式维生素A醋酸酯。该路线反应较为经典,每一步收率均较高,整体收率在64%左右。
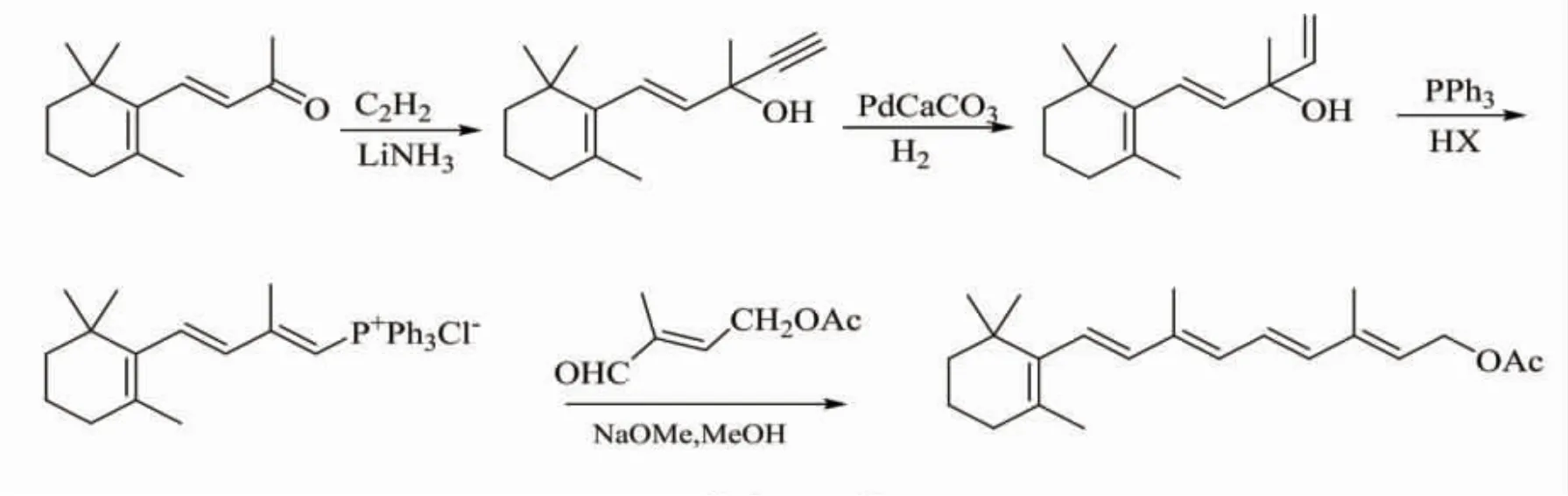
Scheme 4
BASF 合成路线工艺路线短、收率高,直接采用经典的Wittig 缩合反应且其碳骨架经过一步合成后便得到目标产物。但是其中乙炔化、Wittig 反应需要无水和低温等对工艺要求较高,反应生成的三苯基氧膦需要使用剧毒的光气进行回收,异构化过程中需要加入有致癌性的光敏剂,且制备过程中的中间体不稳定,一般企业较难实现工业化生产。
1.5 Wittig-Horner 合成路线
Tanak[13]等采用C14醛与亚甲基双膦酸四乙基酯在氢化钠作用下反应得到3-甲基-5-(2,6,6-三甲基-1-环己烯-1-基)-1,4-戊二烯膦酸二乙基酯,C15膦酸二乙酯在叔丁醇钾作用下与C5醛酯反应得到维生素A醋酸酯,通常以二甲基亚砜(DMSO)为溶剂,整体反应收率可达90%左右,见Scheme 5 。
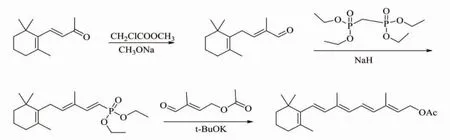
Scheme 5
Wittig-Horner 路线的优点是其极高的立体选择性和工艺路线短,其收率也较高,整体收率在90%左右;但此路线需要进行原料C14醛的制备等繁琐工艺,而且采用DMSO 作溶剂在回收和使用时也存在环保等问题。此合成方法路线立体选择性高,同时避免使用了三苯基膦和剧毒的光气,工业化难度相对较低,是目前研究改进的热门方向。
1.6 氯化亚膦酸酯合成路线
Babler[14]报道了C15磷酸酯的制备方法,见Scheme 6。β-紫罗兰酮经过炔化反应得到C15炔醇,之后和氯化亚膦酸酯反应,再进行选择性加氢反应得到C15膦酸酯,C15膦酸酯再与C5醛酯进行缩合反应得到维生素A醋酸酯,该路线整体收率在83%左右。

Scheme 6
氯化亚膦酸酯合成路线是对BASF 路线与Wittig-Horner 路线的改进路线,选择性较好,具有潜在工业化前景。该路线避免了使用三苯基膦和剧毒的光气,但氯化亚磷酸酯合成成本较高,且部分工艺需要无水、低温等条件,对设备要求较高。
1.7 Rhone-Poulenc 合成路线
Rhone-Poulenc 公司的Chaykovsky[15]以Julia-Lythgoe 烯基化反应为特征,如Scheme 7所示。β-紫罗兰酮经过炔化和催化半氢化反应得到C15醇,之后和氢溴酸反应发生重排得到溴代产物。溴代产物和苯亚磺酸钠反应得到C15砜,C15砜与氯代C5酯在有机锌化合物催化下发生Julia-Lythgoe 烯基化反应得到维生素A醋酸酯。
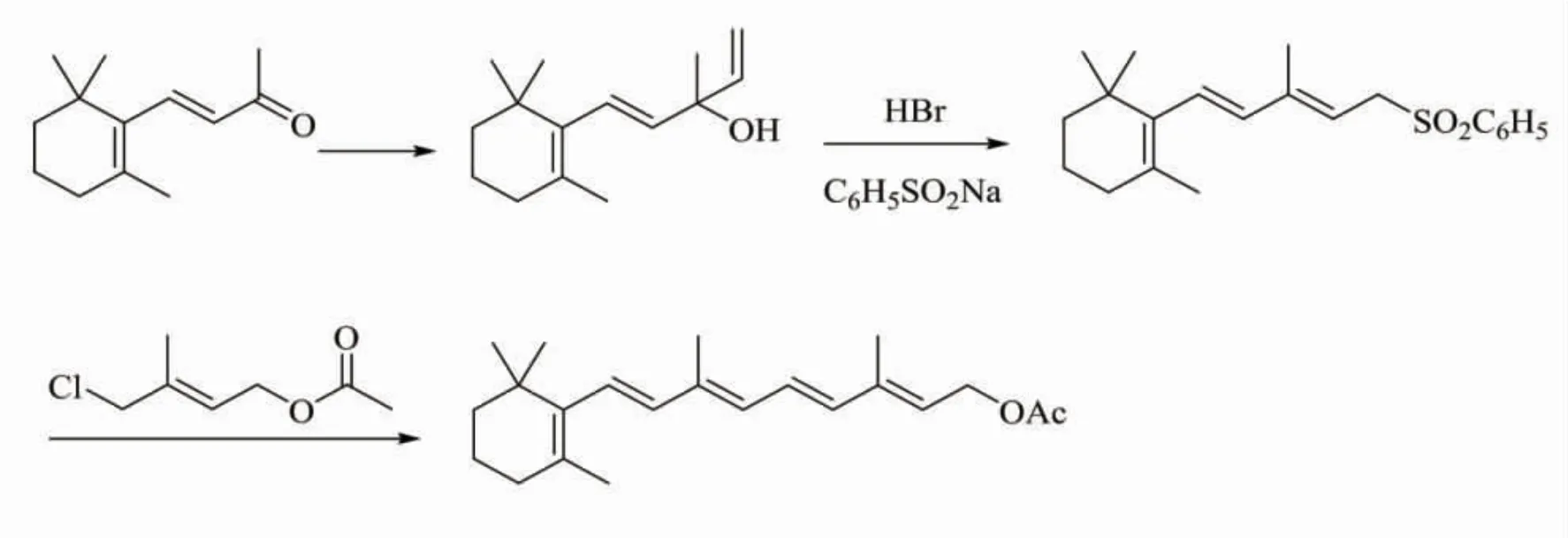
Scheme 7
Rhone-Poulenc 路线在缩合中使用强碱,导致空间异构体发生变化,目前未有良好方法分离其异构体,且采用砜脱除形成双键,反应收率较低。此合成方法采用Julia-Lythgoe 烯基化反应,但是会从砜转变为相应的9-顺异构体。9-顺体是顺式体中最稳定的异构体,但目前还没有资料显示能够对该种顺式体有好的异构化方法。因此,该路线有明显的劣势,未能得到广泛应用。
2 总结与建议
维生素A醋酸酯广泛用于非处方药、营养补充剂、饲料添加剂以及食品加工业。7 条维生素A醋酸酯合成路线中,Roche 合成路线和BASF 合成路线是已经工业化的两条路线,但是实际生产中还存在着收率不高、三废较多等问题。
(1)Roche 合成路线中,C6烯炔醇合成步骤较多,采用Mannich 反应合成丁烯酮,然后再与乙炔氯化镁反应合成C6烯炔醇,可获得高收率和高纯度产品,但是该方法采用了干盐酸气体,要实现工业化生产必须解决加压下设备腐蚀问题。
(2)BASF 合成路线工业化难点在于Wittig 反应的副产物三苯基氧膦的回收处理,目前主要是通过与光气反应制备二氯三苯基膦,再与赤磷反应,还原三苯基膦进行回收。因光气剧毒且不稳定,对工厂设备以及管理要求较高。
(3)氯化亚膦酸酯合成路线是具有较高工业化前景的路线,既无复杂的C14醛合成,也无需经过C6烯炔醇的合成,是Wittig-Horner 路线的改进,未来可从改进氯化亚磷酸酯合成工艺方面进行研究。
