水热法制备半水硫酸钙晶须的工艺研究
2024-02-20刘田田孟雪璐陈利国周长城李明波徐海涛
刘田田,孟雪璐,陈利国,周长城,李明波,徐海涛,
(1. 南京工业大学 环境科学与工程学院,南京 211816;2. 南京杰科丰环保技术装备研究院有限公司,南京 211100)
石灰石-石膏法烟气脱硫工艺应用范围广、技术成熟,全球实际应用率约90%[1]。然而,该工艺在脱硫过程中会产生大量的副产物—脱硫石膏。脱硫石膏是一种优质的石膏资源,可用于水泥、农业、建材等领域[2],其主要成分为二水硫酸钙(CaSO4·2H2O),纯度较高。使用脱硫石膏制备的硫酸钙晶须具有韧性好、电绝缘性好、强度高、耐高温、抗腐蚀、易进行表面处理等优点,在聚氨酯、塑料、陶瓷和水泥等领域前景广阔[3]。
硫酸钙晶须是硫酸钙的纤维状单晶体。根据结晶水数量的不同,可分为二水、半水和无水硫酸钙晶须3种,其中无水和半水硫酸钙晶须强度较高,使用价值较高[4]。目前硫酸钙晶须的制备方法主要有水热法和常压酸化法。常压酸化法因其对设备要求较高、污染较大、产物性能欠佳等缺陷,目前尚处于实验室研究阶段。水热法通过改变水热反应条件来控制晶体的生长,可以制备出不同形貌和尺寸的晶须,与常压酸化法相比,具有原料转化率高、产品纯度高、分散性好等优点。
本工作以二水硫酸钙(CaSO4·2H2O)(模拟脱硫石膏)为原料、硫酸为矿化剂,采用水热合成法制备半水硫酸钙晶须,考察了CaSO4·2H2O用量、硫酸钾加入量、硫酸浓度、反应温度、反应时间和添加剂等因素对硫酸钙晶须形貌的影响,并进行了表征,分析了硫酸钙晶须的生长机理,以期为硫酸钙晶须的工业化生产作参考。
1 实验部分
1.1 试剂和仪器
CaSO4·2H2O、硫酸、硫酸钾、氯化钙(CaCl2)、氯化锌(ZnCl2)、氯化镁(MgCl2)、氯化铜(CuCl2)、柠檬酸(CA)、十二烷基苯磺酸(SDBS):分析纯。
85-2型磁力搅拌器:金坛医疗仪器厂;TGXF-C型高压反应釜:上海岐耀仪器设备有限公司;DHG-9140A型恒温干燥箱:上海一恒科学仪器有限公司;GM-0.5A型真空抽滤装置:天津津腾实验设备有限公司;D2 PHASER 型 X-射线衍射仪(XRD):德国布鲁克公司;GeminiSEM 300型场发射扫描电子显微镜:德国卡尔蔡司公司。
1.2 硫酸钙晶须的制备
将一定量的CaSO4·2H2O与适量去离子水混合制成浆液,加入一定量的硫酸钾和硫酸,在转速240 r/min的条件下搅拌30 min;移入高压反应釜,在一定温度下进行水热反应,反应过程中开启搅拌;反应结束后,将物料冷却至室温,抽滤,在80℃下烘干,得到硫酸钙晶须。
1.3 样品表征
采用XRD表征硫酸钙晶须的物相结构;采用SEM表征硫酸钙晶须的微观形貌。
2 结果与讨论
2.1 硫酸钾加入量对硫酸钙晶须形貌的影响
在制备晶体材料时,常添加无机试剂用于调节浆液的组成及特性。研究表明,硫酸钾对硫酸钙晶须的直径和长径比具有显著影响[5]。为了提高硫酸钙晶须的品质,在CaSO4·2H2O用量(浆液中CaSO4·2H2O的质量分数)5%、反应温度140 ℃、反应时间120 min的条件下,考察硫酸钾加入量(硫酸钾与CaSO4·2H2O的质量比)对硫酸钙晶须形貌的影响,结果见图1。由图1可见:硫酸钾加入量对硫酸钙晶须的形貌和长径比影响显著;当硫酸钾加入量为1%时,硫酸钙晶须的长径比较大,但表面较粗糙(图1a);当硫酸钾加入量为 3%时,硫酸钙晶须的表面光滑度有所提升(图1b);进一步提高硫酸钾的加入量,硫酸钙晶须的形貌逐渐变差,长径比减小(图1c和图1d)。
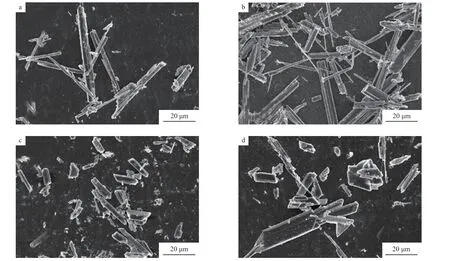
图1 不同硫酸钾加入量下制得的硫酸钙晶须的SEM照片
图2为不同硫酸钾加入量下制得的硫酸钙晶须的XRD谱图。由图2可见:当硫酸钾加入量为1%时,谱图中以无水硫酸钙(CaSO4)的特征峰为主;当硫酸钾加入量增至3%时,出现了半水硫酸钙(CaSO4·0.5H2O)的特征峰;随着硫酸钾加入量的进一步增大,CaSO4和CaSO4·0.5 H2O的特征峰逐渐减弱直至消失,全部转化为CaSO4·2H2O的特征峰。可见,适宜的硫酸钾加入量为3%。

图2 不同硫酸钾加入量下制得的硫酸钙晶须的XRD谱图
2.2 硫酸浓度对硫酸钙晶须形貌的影响
釆用水热法制备晶体材料时,常加入易溶于水的酸或碱作为矿化剂,以促进原料溶解和结晶的顺利进行[6]。研究表明,向浆液中加入硫酸可以提高硫酸钙的溶解度[7],从而有利于晶须生长。在CaSO4·2H2O用量5%、硫酸钾加入量为3%、反应温度140 ℃、反应时间120 min的条件下,考察硫酸浓度对硫酸钙晶须形貌的影响,结果见图3。由图3可见:硫酸浓度对硫酸钙晶须的形貌影响较大;当硫酸浓度为0.1 mol/L时,硫酸钙晶须形貌良好,长径比较大;随着硫酸浓度的增加,硫酸钙晶须的直径和长径比变化不大,但出现了大量不规则块状结晶。有研究认为,硫酸浓度主要影响Ca2+和SO42-的结合速率,或者是晶格的生长速率,Ca2+的吸附常数大于SO42-,其在晶体中的体积也比SO42-大得多,增加浆液中的SO42-有利于增强Ca2+和SO42-在晶核表面的结合速率,促进晶体生长[8];但当硫酸浓度过高时,体系中分子间相互作用加强,反而会抑制Ca2+与SO42-的结合,使晶核形成和晶体生长受阻,降低了晶须产率[9]。

图3 不同硫酸浓度下制得的硫酸钙晶须的SEM照片
2.3 反应时间对硫酸钙晶须形貌的影响
硫酸钙晶须的生长是一个缓慢而复杂的过程,反应时间是影响晶须长径比的重要因素[10]。在CaSO4·2H2O用量5%、硫酸钾加入量3%、硫酸浓度0.1 mol/L、反应温度140 ℃的条件下,考察反应时间对硫酸钙晶须形貌的影响,结果见图5。
图4为不同硫酸浓度下制得的硫酸钙晶须的XRD谱图。由图4可见:当硫酸浓度为0.1 mol/L时,硫酸钙晶须的谱图中以CaSO4和CaSO4·0.5H2O的特征峰为主;随着硫酸浓度的增加,CaSO4·0.5H2O特征峰逐渐减弱;当硫酸浓度增加至0.3 mol/L时,CaSO4·0.5H2O特征峰逐渐消失,同时伴有大量的CaSO4·2H2O特征峰出现。综上,选择适宜的硫酸浓度为0.1 mol/L。
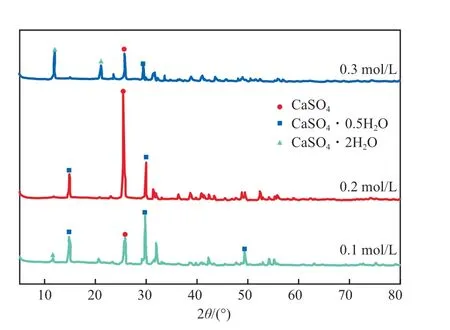
图4 不同硫酸浓度下制得的硫酸钙晶须的XRD谱图
由图5可见:随着反应时间的延长,硫酸钙晶须的形貌变化明显,长径比呈现出先增大后减小的趋势;当反应时间为60 min时,由于结晶时间较短,仅有少量晶须产生,同时伴有颗粒状结晶生成,晶须表面粗糙,横截面不均匀,粗细不一,长度为10~50 μm(图5a);当反应时间为120 min和240 min时,生成的硫酸钙晶须形貌良好,表面光滑度较高,长度为10~70 μm,长径比显著增大(图5b和图5c);当反应时间为360 min时,晶须表面光滑度进一步提升,横截面更均匀,但晶须直径变大,且分布不均匀。

图5 不同反应时间下制得的硫酸钙晶须的SEM照片
图6为不同反应时间下制得的硫酸钙晶须的XRD谱图。由图6可见:反应时间为60 min时,几乎没有硫酸钙晶须生成;延长反应时间至120 min后,谱图中逐渐出现了CaSO4和CaSO4·0.5H2O的特征峰;当反应时间进一步延长至240 min时,CaSO4和CaSO4·0.5H2O的特征峰开始减弱,CaSO4·2H2O的特征峰增强;当反应时间为360 min时,CaSO4·0.5H2O的特征峰消失,以CaSO4·2H2O的特征峰为主。综上,适宜的反应时间为120~240 min。
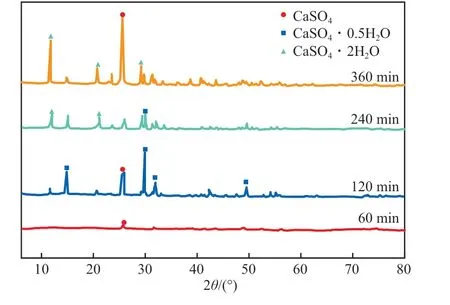
图6 不同反应时间下制得的硫酸钙晶须的XRD谱图
2.4 反应温度对硫酸钙晶须形貌的影响
反应温度是影响硫酸钙晶须生长的重要因素,其影响机理十分复杂,涉及到成核、过饱和度和晶体生长速率等多个因素[11]。在水热法制备硫酸钙晶须的过程中,浆液中的硫酸钙必须处于过饱和状态。研究表明,当反应温度低于110 ℃时,难以生成CaSO4·0.5H2O晶须;当反应温度达到200 ℃时,水热产物会转变为纺锤状硫酸钙颗粒[12]。
在CaSO4·2H2O用量5%、硫酸钾加入量3%、硫酸浓度0.1 mol/L、反应时间120 min的条件下,考察反应温度对硫酸钙晶须形貌的影响,结果见图7。由图7可见:当反应温度为120 ℃时,硫酸钙晶须形貌不均匀,部分晶须呈块状(图7a);当反应温度为140 ℃时,有大量晶须生成,且晶须细长均匀,形态规整,表面较为光滑(图7b),这是因为随着反应温度的升高,晶体成核速率加快,晶须的长径比也逐渐增大[13];继续升高反应温度至160 ℃时,晶须直径的生长速率加快,导致晶须长径比降低,同时出现了较多短柱形晶体,形貌变差(图7c)。

图7 不同反应温度下制得的硫酸钙晶须的SEM照片
图8为不同反应温度下制得的硫酸钙晶须的XRD谱图。由图8可见:当反应温度为120 ℃时,谱图中主要为CaSO4的特征峰;当反应温度升高至140 ℃时,开始出现CaSO4·0.5H2O的特征峰,并逐渐占主导地位;继续升高温度至160 ℃时,开始出现CaSO4·2H2O的特征峰。综上,选择适宜的反应温度为140 ℃。
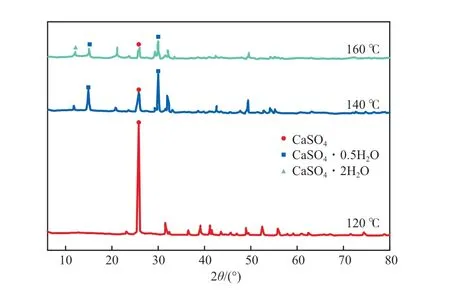
图8 不同反应温度下制得的硫酸钙晶须的XRD谱图
2.5 CaSO4·2H2O用量对硫酸钙晶须形貌的影响
CaSO4·2H2O用量是影响硫酸钙晶须形貌的另一重要因素。当反应器中CaSO4·2H2O含量过低时,可用于硫酸钙晶须生长的原料数量有限,如果晶须生长所需的大量Ca2+和SO42-在反应过程中不能及时得到补充,就会降低体系的过饱和度,影响晶须生长;当CaSO4·2H2O含量过高时,又会使体系长期处于过饱和状态,晶核的形成与生长始终同时进行,导致后期形成的晶核因生长时间较短而较为细小,同时,也会导致部分原料在反应过程中难以通过结晶消耗殆尽。
在硫酸钾加入量3%、硫酸浓度0.1 mol/L、反应温度为140 ℃、反应时间120 min的条件下,考察CaSO4·2H2O用量对硫酸钙晶须形貌的影响,结果见图9。

图9 不同CaSO4·2H2O用量下制得的硫酸钙晶须的SEM照片
由图9可见:CaSO4·2H2O用量对硫酸钙晶须的形貌影响显著;当CaSO4·2H2O用量为5%时,硫酸钙晶须形貌良好,长径比较大,均匀性较好,表面略显粗糙(图9a);当CaSO4·2H2O用量为7%时,硫酸钙晶须形貌变差,出现大量块状晶体,均匀性变差(图9b);当CaSO4·2H2O用量为9%时,硫酸钙晶须长度变短,伴随大量块状晶体生成(图9c);当CaSO4·2H2O用量为11%时,生成大量短柱状晶须,表面凹凸不平,同时伴有大量块状晶体(图9d)。
图10为不同CaSO4·2H2O用量下制得的硫酸钙晶须的XRD谱图。由图10可见:当CaSO4·2H2O用量为5%时,谱图中以CaSO4·0.5H2O的特征峰为主,伴随少量CaSO4的特征峰;随着CaSO4·2H2O用量的增加,开始出现CaSO4·2H2O的特征峰,因此,适宜的CaSO4·2H2O用量为5%。

图10 不同CaSO4·2H2O用量下制得的硫酸钙晶须的XRD谱图
2.6 不同添加剂对硫酸钙晶须形貌的影响
添加剂可以改善硫酸钙晶须的结晶速率和形貌,常用的添加剂包括表面活性剂、羧酸、聚合物、磷酸盐以及金属阳离子等。在CaSO4·2H2O用量5%、硫酸钾加入量3%、硫酸浓度0.1 mol/L、反应温度140 ℃、反应时间120 min的条件下,分别添加3%(添加剂与CaSO4·2H2O的质量比)的CA、SDBS、MgCl2、CaCl2、CuCl2和ZnCl2,考察添加剂对硫酸钙晶须形貌的影响,结果见图11。

图11 不同添加剂下制得的硫酸钙晶须的SEM照片
由图11a可见:CA能显著改变硫酸钙晶须的生长特性;添加CA后,硫酸钙晶须的形貌变差,长径比较小,部分呈块状,这是因为CA能与硫酸钙晶核表面的Ca2+通过络合作用形成新的界面,降低了Ca2+在晶须各个晶面上的吸附速率,从而降低了晶须的生长速率[14]。添加SDBS后,硫酸钙晶须的生长明显受到抑制,产物呈颗粒状(图11b)。添加CaCl2后,所得到的硫酸钙晶须长度为30~80 μm,形貌最优(图11d),ZnCl2次之(图11f),MgCl2再次(图11c),CuCl2最差(图11e)。
图12为不同添加剂下制得的硫酸钙晶须的XRD谱图。由图12可见:CA、SDBS和MgCl2作添加剂时,主要的特征峰均为CaSO4;以CuCl2作添加剂时,除CaSO4· 0.5H2O的特征峰外,还出现了CaSO4·2H2O的特征峰;以CaCl2和ZnCl2为添加剂时,主要特征峰为CaSO4·0.5H2O,伴随少量CaSO4的特征峰。可见,以CaCl2和ZnCl2为添加剂时,所制得的硫酸钙晶须品质最优。
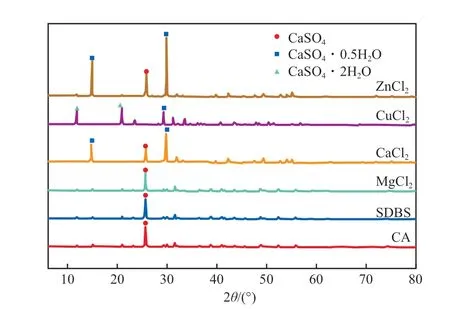
图12 不同添加剂下制得的硫酸钙晶须的XRD谱图
3 结论
a)以CaSO4·2H2O为原料、硫酸为矿化剂,采用水热合成法制备半水硫酸钙晶须,考察了CaSO4·2H2O用量、硫酸钾加入量、硫酸浓度、反应温度、反应时间和添加剂等因素对硫酸钙晶须形貌的影响。实验结果表明,制备硫酸钙晶须的最佳工艺条件为:CaSO4·2H2O用量 5%、硫酸钾加入量3%、硫酸浓度0.1 mol/L、反应温度140 ℃、反应时间120 min。
b)不同添加剂对硫酸钙晶须的生长影响显著。添加CaCl2和ZnCl2可以有效改善硫酸钙晶须的形貌,其中以CaCl2的效果最好,晶须长度为30~80 μm;添加CA、SDBS后,硫酸钙晶须的形貌明显变差。
