聚酰胺微塑料对十二烷基苯磺酸钠的吸附
2024-02-20陈金垒章雨晨陈雅婷黄华斌
陈金垒,章雨晨,陈雅婷,黄华斌
(厦门华厦学院 环境与公共健康学院,福建 厦门 361024)
2004年,THOMPSON等[1]首次提出微塑料的概念,并将其定义为尺寸小于5 mm的塑料碎片和颗粒。微塑料具有较强的疏水性及非晶态结构,广泛存在于河流、湖泊和海洋等环境中[2]。微塑料比表面积大、吸附污染物的能力强[3],进入水体后极易对水生生物造成危害,进而威胁人类健康[4]。因此,研究水体中微塑料对有机污染物的吸附行为具有十分重要的意义。
十二烷基苯磺酸钠(SDBS)是一种常见的阴离子表面活性剂(LAS),可在水体中长期存在,对水生生态系统具有较大的环境风险[5]。研究表明,水体中的SDBS会促进微塑料对有机污染物的吸附,从而产生更复杂的环境效应[6]。XIA等[7]考察了聚氯乙烯(PVC)微塑料对SDBS的吸附特征,结果表明:PVC微塑料对SDBS的等温吸附特征可以用Langmuir模型描述;PVC微塑料对SDBS的饱和吸附量(qsat)可达1 043 μg/g。但PVC微塑料对SDBS的吸附机理尚未深入探讨。
聚酰胺(PA)塑料中含有酰胺基团,可与环境污染物发生氢键作用、n-π电子供受体(EDA)作用,从而表现出更高的吸附性能[8]。SONG等[9]研究发现PA 微塑料对腐殖酸(HA)的吸附量可达0.399 mg/g,为聚丙烯(PP)微塑料的1.1倍。但关于PA微塑料对SDBS吸附性能的研究,目前还鲜见报道。
本工作考察了PA微塑料对SDBS的吸附性能,分析了pH和共存离子等因素对SDBS吸附量的影响,探讨了PA微塑料对SDBS的吸附机理,为深入理解水体中微塑料和表面活性剂之间的相互作用提供依据。
1 材料与方法
1.1 试剂与材料
NaCl、KCl、Na2SO4、NaCO3、CaCl2、HCl、NaOH、SDBS:分析纯。
PA微塑料:购自上海麦克林生化科技有限公司,平均粒径(140.7±1.8)μm,比表面积0.880 2 m2/g。
1.2 吸附实验
1.2.1 吸附动力学实验
将50 mL质量浓度为30 mg/L和60 mg/L的SDBS溶液分别移入100 mL的锥形瓶中,各加入0.1 g PA微塑料;将锥形瓶置于气浴恒温振荡器中,在温度25 ℃、转速180 r/min的条件下反应72 h。间隔一定时间取样1 mL,水样经0.45 μm滤膜过滤后,采用紫外分光光度计(UV-1800PC-DS2型,上海美谱达仪器有限公司)测定波长为242 nm处的吸光度,计算溶液中SDBS的质量浓度和吸附量。
1.2.2 等温吸附实验
将50 mL一定质量浓度(20~80 mg/L)的SDBS溶液移入100 mL的锥形瓶中,加入0.1 g PA微塑料,在转速180 r/min的条件下,考察不同温度(25℃和35 ℃)下PA微塑料对SDBS的吸附特征。
1.2.3 影响因素实验
将50 mL质量浓度为60 mg/L的SDBS溶液移入100 mL的锥形瓶中,加入0.1 g PA微塑料,在温度25 ℃、转速180 r/min的条件下,考察初始pH(2~11)对SDBS吸附特征的影响。
调节SDBS溶液pH至8,考察Na+、K+、Ca2+、SO42-和CO32-在不同浓度(1 mmol/L和10 mmol/L)条件下,对PA微塑料吸附SDBS的影响。
所有实验均设置三组平行样。
1.3 PA微塑料的表征
采用场发射扫描电子显微镜(Apreo 2型,美国赛默飞世尔科技公司)观察PA微塑料的表面形貌;采用傅里叶变换红外光谱仪(Nicolet iS5型,美国赛默飞世尔科技公司)分析PA微塑料的表面官能团;采用X射线光电子能谱仪(ESCALAB 250Xi型,美国赛默飞世尔科技公司)分析PA微塑料表面元素及其化学形态。
2 结果与讨论
2.1 吸附动力学
分别采用准一级动力学模型、准二级动力学模型和颗粒内扩散模型拟合PA微塑料对SDBS的吸附动力学过程,结果见表1和表2。由表1可见:准二级动力学模型拟合的R2(0.949~0.983)比准一级动力学模型拟合的R2(0.856~0.926)更高,表明准二级动力学模型能够更好地描述PA微塑料对SDBS的吸附动力学过程,这与PA微塑料对其他有机物的吸附动力学结果一致[10]。

表1 准一级、二级动力学模型的拟合结果
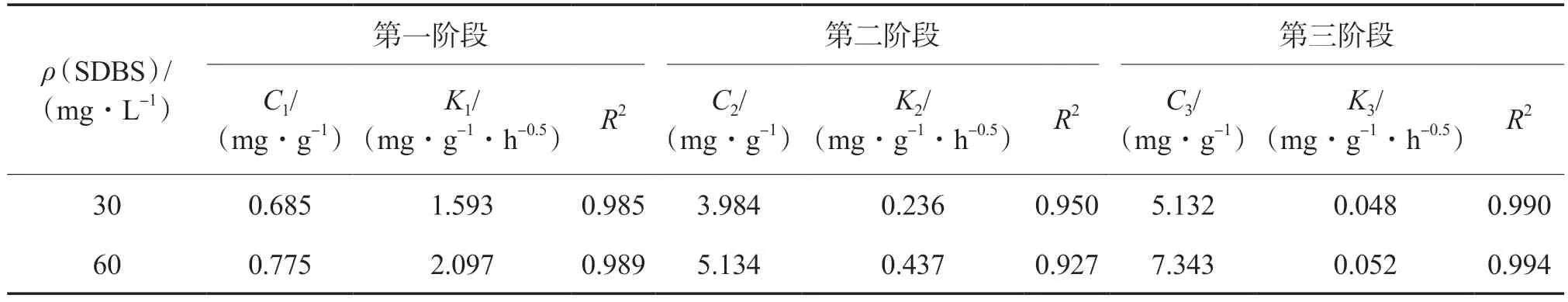
表2 颗粒内扩散模型的拟合结果
颗粒内扩散模型将吸附过程分为3个阶段:第一阶段是外扩散或传质过程,SDBS分子迅速从溶液迁移到PA微塑料表面;第二阶段为内扩散或孔隙扩散过程,SDBS分子逐渐进入PA微塑料表面的褶皱孔隙;第三阶段为SDBS在PA微塑料上的吸附平衡过程,通常需要较长时间才能达到。由表2可见:颗粒内扩散模型各阶段拟合的R2均较高,但模型常数C值均不为零,表明内扩散过程不是PA微塑料吸附SDBS的唯一限速步骤,PA微塑料对SDBS的吸附速率还受外扩散和表面吸附的影响[11]。
2.2 等温吸附
吸附等温线可用于评价有机污染物在微塑料上的qe与其在水溶液中的平衡质量浓度(ρe)之间的关系[12]。此外,环境温度的变化也会影响微塑料对有机污染物的吸附能力[13]。分别采用Langmuir和Freundlich等温吸附模型拟合不同温度下PA 微塑料对SDBS的吸附过程,结果见表3。由表3可见:25 ℃和35 ℃条件下,Langmuir模型的R2分别为0.993和0.988,均高于Freundlich模型(0.945和0.952),表明Langmuir模型能更好地描述PA微塑料对SDBS的吸附等温过程,这与LIU等[14]采用PA微塑料吸附苯甲酸、磺胺甲基嘧啶的研究结果一致;当温度由25 ℃上升至35 ℃时,PA微塑料对SDBS的qsat由10.896 mg/g增加至12.370 mg/g,表明升高温度有利于PA微塑料对SDBS的吸附,这与WAGSTAFF等[10]采用PA微塑料吸附水中药物污染物的研究结果一致。与PVC微塑料相比[7],PA微塑料对SDBS的吸附能力更强,因此,应关注PA微塑料作为水中SDBS载体时所带来的环境风险。
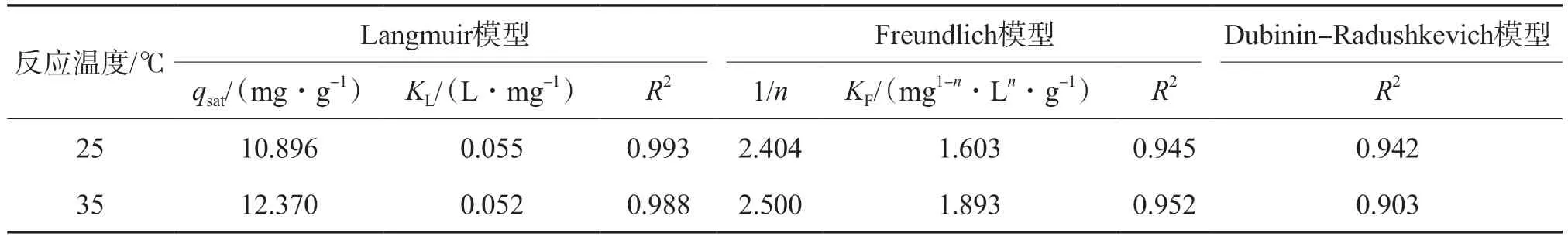
表3 PA微塑料对SDBS等温吸附模型的拟合结果
此外,表3还显示了Dubinin-Radushkevich模型对不同温度下PA微塑料吸附SDBS的拟合结果,可以看出:不同温度下,Dubinin-Radushkevich模型的R2均大于0.9,表明PA微塑料对SDBS的吸附过程可能涉及微孔填充机制[14]。
2.3 影响因素
2.3.1 初始pH
溶液pH不仅影响有机物的形态分布,而且会改变微塑料的表面电荷性质,从而影响微塑料对有机物的吸附能力[15]。不同初始pH条件下,PA微塑料对SDBS的吸附特征见图1。由图1可见: PA微塑料对SDBS的吸附量随pH的增加而逐渐降低;酸性条件下,PA微塑料对SDBS的吸附性能更好。这是因为PA微塑料的零电荷点(pHzpc)为5.3[9],在酸性条件下(pH<5),PA微塑料的表面带正电荷,SDBS带负电荷,静电引力作用有利于SDBS在PA微塑料表面的富集;当pH>pHzpc时,由于酰胺官能团的去质子化作用,PA微塑料表面带负电荷,随着pH的逐渐增大,PA微塑料与SDBS之间的静电斥力增强,吸附作用受到抑制,当初始pH增加至11时,PA微塑料对SDBS的吸附量最低,为4.530 mg/g。
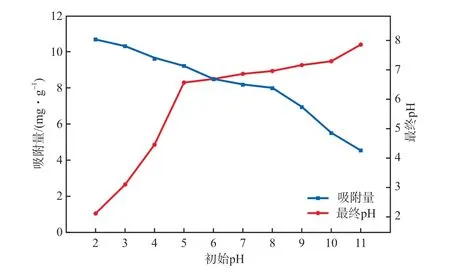
图1 初始pH对PA微塑料吸附SDBS的影响
2.3.2 共存离子
水环境中其他离子的存在,可能会影响污染物在吸附剂表面的富集[16]。研究表明,微塑料对有机污染物的吸附特性受盐度等环境因素的影响[17]。不同浓度下,Na+、Ca2+、K+、SO42-、CO32-对PA微塑料吸附SDBS的影响见图2。由图2可见:Na+、K+、SO42-对PA微塑料吸附SDBS的影响较为一致;当Na+、K+、SO42-的浓度为1 mmol/L时,对SDBS的吸附呈现轻微的抑制作用,当Na+、K+、SO42-的浓度为10 mmol/L时,对SDBS的吸附有明显的促进作用。研究表明,阳离子可以取代微塑料表面官能团中的氢原子,抑制氢键的形成,减弱微塑料对有机物的吸附能力[11],随着浓度的增加,阳离子与带负电荷的微塑料结合,扰乱了其表面的电荷平衡,压缩双电层的厚度,从而减弱微塑料与有机物之间的静电斥力[14],吸附能力增强。研究表明,溶液中SO42-的存在会降低有机物的溶解度,从而促进有机物在固相中的分布[11],因此,当SO42-浓度增加至10 mmol/L时,PA微塑料对SDBS的吸附能力增强。当Ca2+浓度为1 mmol/L时,PA微塑料对SDBS的吸附量显著提高,继续增加Ca2+浓度至10 mmol/L时,高浓度的Ca2+会破坏PA微塑料的双电层结构,促进微塑料颗粒聚集,从而减少PA微塑料表面的吸附位点,导致其对SDBS的吸附量显著降低。当向SDBS溶液中加入CO32-后,PA微塑料对SDBS的吸附能力受到明显的抑制,这可能是由于CO32-的加入使体系呈碱性环境,加剧PA微塑料与SDBS之间静电斥力作用[11],从而导致其吸附量的降低。
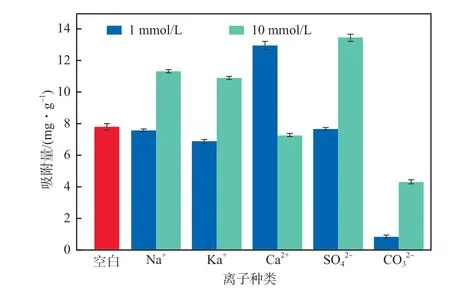
图2 不同浓度共存离子对PA微塑料吸附SDBS的影响
2.4 PA微塑料的表征结果
2.4.1 SEM
PA微塑料吸附SDBS前后的SEM照片见图3。由图3可见:吸附前,PA微塑料表面呈不规则褶皱状,含有较大的孔隙和裂缝;吸附SDBS后,PA微塑料表面较为光滑,孔隙和裂缝量明显变少,这表明PA微塑料对SDBS的吸附过程中存在孔隙填充机制,这与MEJÍAS等[18]的研究结果一致。
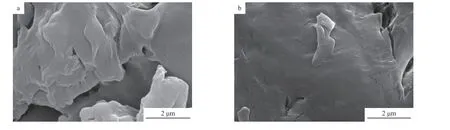
图3 吸附SDBS前(a)后(b)PA微塑料的SEM照片
2.4.2 FTIR
PA微塑料吸附SDBS前后的FTIR谱图见图4。其中,PA-SDBS-20表示初始SDBS质量浓度为20 mg/L时吸附平衡后的PA微塑料,以此类推。由图4可见:吸附前,PA微塑料在波数1 634 cm-1、1 538 cm-1、1 261 cm-1、684 cm-1和575 cm-1附近的吸收峰分别归属于酰胺基团的N—C=O(酰胺Ⅰ带)、C—N—H(酰胺Ⅱ带)、C—N(酰胺Ⅲ带)、N—H(酰胺Ⅴ带)和C=O(酰胺Ⅵ带)的特征峰[8,19],2 931 cm-1和2 860 cm-1附近的吸收峰与C—H的伸缩振动有关[20],1 460 cm-1附近的吸收峰归属于C—H的弯曲振动[9],3 293 cm-1附近的吸收峰归属于N—H的伸缩振动[19];吸附SDBS后,酰胺基团的特征峰强度随着SDBS浓度的增加而增大,这可能是由于PA微塑料中酰胺基团的供质子官能团与SDBS的氧原子之间形成了氢键[8],TONG等[21]认为氢键作用在PA微塑料吸附有机物的过程具有重要作用。
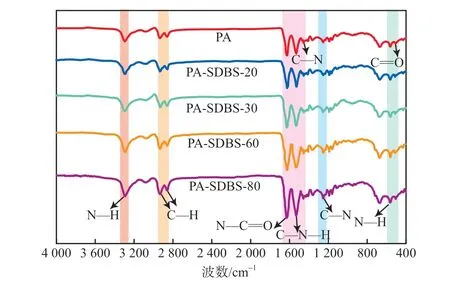
图4 吸附SDBS前后PA微塑料的FTIR谱图
为了进一步探究PA微塑料对SDBS吸附过程中各官能团的变化顺序,采用二维红外相关光谱(2D-FTIR-COS)技术解析PA和PA-SDBS的FTIR谱图,得到PA微塑料吸附溶液中SDBS的同步和异步相关谱图,见图5。图中红色代表正相关,蓝色代表负相关。由图5a及图5b可见:沿对角线在波数575,684,1 261,1 460,1 538,1 634,2 931,3 293 cm-1处出现了8个主要自动峰,可分别归属于酰胺Ⅵ带、酰胺Ⅴ带、酰胺Ⅲ带、C—H(弯曲振动)、酰胺Ⅱ带、酰胺Ⅰ带、C—H(伸缩振动)和N—H(伸缩振动);同步谱图中,所有自动峰均出现正信号(显示为红色),表明各自动峰在吸附过程中是同步变化的。异步相关谱图可以提供吸附过程中微塑料各官能团的变化顺序[22]。由图5c和图5d可见:交叉峰在吸附过程中存在明显差异,特别是一些含氮官能团,如C—N—H、N—C=O及N—H等。
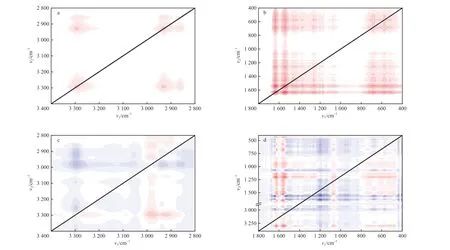
图5 PA微塑料吸附SDBS的2D-FTIR-COS谱图
表4为PA微塑料吸附SDBS的2D-FTIR-COS同步和异步谱图中各个交叉峰的分配结果和符号(括号中为异步结果)。异步谱图中:(v1,3 239)处的交叉峰信号均为正信号,说明3 293 cm-1处的峰均滞后于其他峰出现;(v1,1 538)处的交叉峰信号均为负信号,表明1 538 cm-1处的峰将先于其他峰出现。由此推断PA微塑料吸附SDBS的官能团反应顺序为:C—N—H(酰胺Ⅱ带)>C=O(酰胺Ⅵ带)>N—C=O(酰胺Ⅰ带)>C—H(伸缩振动)>N—H(酰胺Ⅴ带)>C—H(弯曲振动)>C—N(酰胺Ⅲ带)>N—H(伸缩振动)。
2.4.3 XPS
吸附SDBS前后PA微塑料的C 1s、N 1s及O 1s的XPS谱图见图6。由图6a可见:吸附前,PA微塑料的C 1s谱图中,在284.8,285.9,287.6 eV处有3个特征峰,分别对应C—C/C—H、C—N及N—C=O[8],与FTIR的分析结果基本一致。有研究表明,烷基和芳香环之间可形成弱氢键,提高微塑料与含苯环化合物之间的吸附能力[23]。本研究中上述官能团在吸附SDBS后变化较小,表明PA微塑料对SDBS的吸附机制可能包括PA中含碳官能团与SDBS中苯环的相互作用。
由图6b可见:吸附前,PA微塑料的N 1s谱图中存在N—H(399.4 eV)和O=C—N(401.4 eV)[8,24];吸附SDBS后,PA中O=C—N的位置偏移至401.7 eV处,且含量明显减少,表明酰胺基团参与了吸附反应。由图6c可见:吸附前,PA微塑料的O 1s谱图中,N—C=O和C=O分别位于531.0 eV和532.2 eV处[14,25];吸附SDBS后,C=O基团对应的结合能增加了0.3 eV,表明吸附SDBS后,PA微塑料的平均氧电荷增加[20],C=O中O原子的电子密度降低,表明羰基倾向于失电子,与SDBS的芳香环发生n-πEDA作用。可见,PA中的酰胺基团可通过n-πEDA作用或氢键作用对SDBS进行吸附。
2.5 吸附机制
综上,PA微塑料对SDBS的吸附过程可能涉及以下机制(见图7):1)PA中的羰基和SDBS中的苯环发生n-πEDA作用;2)PA中的氨基与SDBS中的磺酸基发生氢键作用;3)当pH<pHzpc时,SDBS与表面带正电荷的PA微塑料发生静电吸引作用;4)SDBS通过孔隙填充作用吸附在PA上。
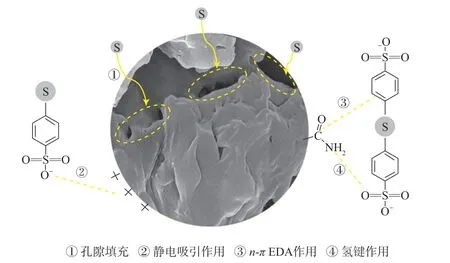
图7 PA微塑料对SDBS的主要吸附机理示意
3 结论
a)PA微塑料对SDBS的吸附过程符合准二级动力学模型和Langmuir等温吸附模型;随着初始pH的增加,PA微塑料对SDBS的吸附量逐渐降低;当Na+、K+、SO42-的浓度为1 mmol/L时,PA微塑料对SDBS的吸附呈现轻微的抑制作用,当Na+、K+、SO42-的浓度为10 mmol/L时,PA微塑料对SDBS的吸附有明显的促进作用;当Ca2+浓度为1 mmol/L时,SDBS吸附量显著提高,继续增加Ca2+浓度至10 mmol/L时,SDBS吸附量显著降低;CO32-对PA微塑料吸附SDBS的过程具有明显的抑制作用。
b)PA吸附SDBS的官能团反应顺序为C—N—H(酰胺Ⅱ带)>C=O(酰胺Ⅵ带)>N—C=O(酰胺Ⅰ带)>C—H(伸缩振动)>N—H(酰胺Ⅴ带)>C—H(弯曲振动)>C—N(酰胺Ⅲ带)>N—H(伸缩振动)。
c)PA微塑料对SDBS的吸附机理包括PA中的羰基和SDBS中的苯环发生的n-πEDA作用、PA中的氨基与SDBS中的磺酸基发生的氢键作用、静电作用和孔隙填充等。
