表面氟化g-C3N4光催化降解罗丹明B的性能研究
2024-02-04刘小刚陈梦雨李艳艳兰玉典
刘小刚,张 欣,陈梦雨,李艳艳,兰玉典
(信阳师范大学 化学化工学院, 河南 信阳 464000)
0 引言
大量燃烧高能量密度的化石燃料造成了严重的温室气体排放[1],从而导致全球变暖,并威胁到地球上生命的生存。因此,寻求先进可持续的技术解决这一困境至关重要。受植物自然光合作用过程的启发,科学界试图将太阳能转化为化学能。FUJISHIMA[2]等在1972年首次将TiO2用作光催化剂用于水裂解,这一开创性工作激发了科学家开发各类高效稳定的光催化剂。近年来,开发的金属氧化物半导体光催化剂(如CdS[3]、SnO2[4]和WO3[5]等),大多存在光生电子-空穴复合速率高和光催化活性低的局限性。开发光生载流子分离效率高、光催化性能优异、可重复性好、成本低的可见光响应型光催化剂至关重要。
石墨相氮化碳(g-C3N4,缩写为CN)制备方法简单、化学性质稳定、可见光吸收性能优异,在诸多半导体光催化剂中脱颖而出[6],但其导电性差,且光生电子-空穴复合率较高,限制了其广泛使用。因此,调节CN的表面化学性质、促进光生电荷的分离对于提高其光催化性能具有重要科学意义。在CN基体中引入非金属杂原子,可促进其网状结构中π-共轭电子的离域,从而显著调节表面性质、光吸收性能和载流子传输效率。目前常用的非金属掺杂方法一般有水热法、溶剂热法、热聚法等,虽然可以提升CN的光催化性能,但制备方法耗能高、条件苛刻,且不利于目标产物的分离和纯化,亟待开发一种简单的非金属改性方法。
氟离子具有极强的电负性(3.98)和较小的离子半径(0.131 nm),是金属氧化物理想的n型掺杂剂,形成的金属-氟键比其他金属-离子键弱,极易电离,从而对催化剂的表面微观结构、电负性、活性位点产生明显影响。本研究利用氟离子独特的理化性质,实现对CN的表面氟化,对改性之后CN的光吸收性能、光生电子和空穴的分离和传输效率、光催化降解有机污染物(RhB)性能进行研究,为表面阴离子修饰半导体光催化剂提供实验参考。
1 实验部分
1.1 材料与试剂
三聚氰胺,RhB,北京百灵威科技有限公司;氢氟酸(HF),分析纯,上海沃凯生物技术有限公司。
1.2 样品的制备
1.2.1 块状CN的合成
通过热聚合法制备块状CN。称取一定质量的三聚氰胺放入带盖坩埚中,把坩埚放入马弗炉以3 °/min的升温速率升温到550 ℃,并保持4 h。样品冷却至室温后,研磨便可得到原始块状CN。
1.2.2 表面氟化CN材料的制备
分别取0.1、0.2、0.4、0.6 mL HF加去离子水至50 mL备用。分别称取0.3 g CN分散到上述氢氟酸溶液中,然后在室温下搅拌24 h。离心、洗涤、60 ℃干燥得到产物,根据加入HF的体积命名为CN-xF(x=0.1、0.2、0.4、0.6)。
1.3 测试与表征
XRD分析采用日本理学MiniFlex600型X-射线粉末衍射仪,以Cu/Kα为放射源,扫描角度2θ=10°—70°,扫速10 °/min;SEM分析采用日立S 4800型冷场发射扫描电子显微镜来表征样品的形貌特征XPS分析采用Al Kα辐射为激发光源的K-ALPHA 0.5 EV型X射线光电子能谱仪来表征样品的表面化学成分;UV-Vis DRS采用UH4150型紫外-可见漫反射光谱仪表征样品的光吸收能力;FT-IR分析采用NICOLET iS50型红外光谱仪来表征样品的结构信息;吸光度测试采用721 G型可见分光光度计进行测试;电化学分析采用CHI660E型电化学工作站进行测试。
1.4 光催化降解RhB
称量0.05 g光催化剂,分散到100 mL(10 mg/L)的RhB溶液中,转移至石英管,超声均匀。光反应前,在黑暗中吸脱附1 h,使光催化剂与RhB吸附-解吸达到平衡,然后用300 W氙灯光照5 h。在光催化反应过程中,每隔1 h取一次样,每次取4 mL溶液,离心并用紫外分光光度计在554 nm波长下测量上清液的吸光度,最后计算RhB的去除率。
1.5 光电化学测试
采用电化学工作站进行光电化学测试,电极制备过程如下:取5 mg光催化剂分散到200 μL去离子水中,滴加1滴杜邦膜溶液,超声5 min,然后涂到(1 cm×3 cm)FTO导电玻璃上,烘干、冷却至室温。采用三电极系统进行光电化学测试,所制备的电极为工作电极、铂电极为对电极、Ag/AgCl电极为参比电极,0.2 mol/L的Na2SO4溶液为电解液。在偏压为0 V下进行光电流-时间(i-t)测试,测试时间为400 s,每20 s挡光或开光一次。在0.01~10 000 Hz范围下测试电化学阻抗(EIS)。
2 结果与讨论
2.1 样品的表征与分析
2.1.1 XRD分析
图1为 样品的XRD谱图。
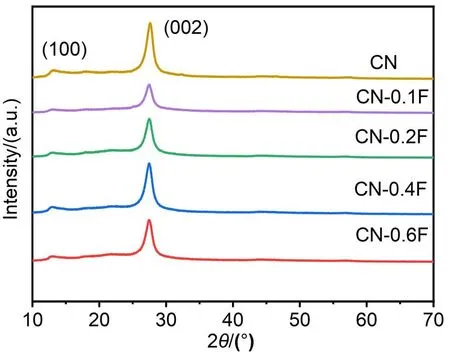
图1 CN和CN-xF的XRD谱图
从图1可以看出,经过HF处理的CN与原始CN都存在两种明显的衍射峰,表明加入少量体积的HF没有使CN材料的晶体结构遭到破坏,并且所制备的样品符合石墨相氮化碳的晶体结构特征。衍射峰2θ≈13°和衍射峰2θ≈27°分别对应于CN的(100)晶面与(002)晶面,其中(100)晶面属于三嗪环的面内周期排布,(002)晶面则反映共轭芳香碳氮杂环的层间堆积[7]。经过表面氟化后的材料衍射峰强度略有降低,说明加入HF对CN的晶粒尺寸和结晶度有一定影响,这可能是F-独特的化学性质所导致。观察发现(002)晶面的峰向低角度略微移动,说明共轭芳香碳氮杂环的层间间距略有扩大,这可能与引入电负性较大的F有关[8]。
2.1.2 SEM分析
如图2(a,b)所示原始CN呈现出不规则块体形貌且表面较光滑,加入HF之后样品尺寸略微变小且较大的块体被分裂成小块体,由图2(b,d)所示光滑的表面被剥离并出现更多的孔结构,还观察到在块体周围有少量剥离的碎块。随着HF体积增大,CN尺寸变小和碎块化更明显。由此可见,经过HF处理,成功地把块状CN的尺寸变小,并且促进CN块状结构的剥离和分散。较小的尺寸可以增大光催化剂与RhB的接触面积,而且较多的孔结构可以增加光催化剂的比表面积和反应活性位点。

图2 CN(a, c)和CN-0.2F(b, d)的SEM图
2.1.3 XPS分析
如图3a所示,相比于CN,在XPS全谱中CN-0.2F出现一个微小的F 1s峰,表明氟离子已经成功嫁接到CN表面。由图3b所示,CN样品在284.8 eV和288.1 eV出现双重特征峰,分别对应污染碳的C—C键和CN骨架中三嗪环结构的N=C—N键。后者在氟处理之后的CN-0.2F样品中向高结合能方向移动,表明氟化会显著改变CN的表面电子结构。在N 1s的XPS精细谱中(图3c),CN出现结合能为398.6、400.2、401.2、404.1 eV 4个特征峰,分别对应于C—N=C、N—(C)3、C—N—H和N—O键[9]。对CN-0.2F而言,其C—N=C键向高结合能方向移动,进一步表明氟离子修饰会调节CN的电子结构。由于氟离子极强的电负性和电离度,氟离子引入到CN时会改变CN骨架中的电子分布和结构,吸引与之相邻的C原子上的电子,C原子被诱导和极化,促进π-共轭电子的离域,产生新的反应活性位点。另外,氟离子较小的离子半径和刻蚀特性,可能对CN的表面结构进行重组,从而调节光生电荷的分离效率。由图3d的F 1s精细谱可知,CN-0.2F在689.6 eV处出现较宽的特征峰,对应C—F[10],表明F离子以C—F键的形式掺入到CN的骨架中。借助XPS半定量分析方法确定了所制备CN和CN-0.2F样品中元素的相对含量,如表1所示。CN的C/N原子比为0.80,而CN-0.2F的C/N原子比提高至0.89,原因可能是氟离子的引入诱导CN产生一定的缺陷位点,这有助于促进光生电荷的分离和传输,从而提升光催化性能。

表1 CN和CN-0.2F的XPS元素半定量分析 (单位: At.%)
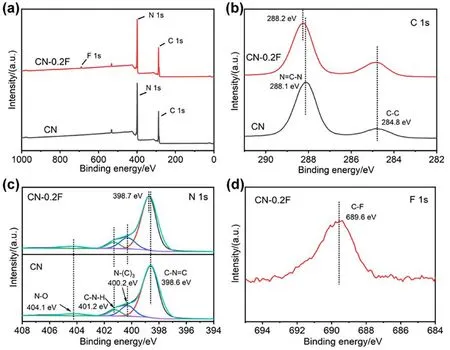
图3 CN和CN-0.2F的XPS谱图 (a)全谱图、(b)C 1s、(c)N 1s、(d)F 1s
2.1.4 FT-IR与UV-Vis DRS分析
采用FT-IR表征样品的化学结构。如图4a所示,在809 cm-1处的吸收峰可归因于三嗪单元弯曲振动,1247~1641 cm-1范围内的吸收峰归因于C-N杂环的伸缩振动,3000~3600 cm-1的宽带吸收峰归因于催化剂表面吸附的H2O和未缩合氨基基团的N-H伸缩振动[11]。由此可见,加入HF后并未改变CN样品的基本结构,这是因为加入HF的量较少,观察不到与F相关的化学结构。图4b为样品的UV-Vis DRS图谱,CN样品的吸收带边约为467 nm,而CN-xF样品的可见光吸收有轻微减弱,吸收带边略微蓝移,原因可能是HF的刻蚀使CN的颗粒尺寸降低,引起了“量子限制效应”。值得注意的是,根据Tauc图(图4b插图)可知,CN-xF样品保持了CN材料的本征带隙2.79 eV。
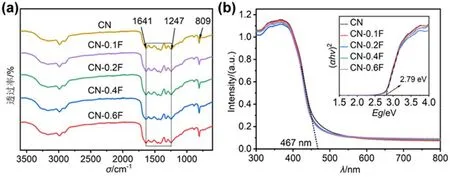
图4 CN和CN-xF的FT-IR图谱(a) 和UV-Vis DRS图(b) (插图为相应的Tauc图)
2.2 光催化降解RhB性能研究
图5a为所制备样品的光催化降解RhB性能图。CN光照5 h后的降解率仅为29.8%,而表面氟化之后的CN-xF其降解率明显提升,并且随着HF量的增加降解率呈现先上升后下降的趋势,当加入HF的体积增加至0.2 mL时所得到的CN-0.2F降解率达到最大(47.9%),是原始CN样品的1.6倍。适宜量的表面氟离子可以提高光生载流子的分离效率,过多的表面氟离子会形成新的光生电荷的复合中心,不利于光催化性能的提升[12]。通过拟合可得准一级反应速率常数k,如图5b所示。CN、CN-0.1F、CN-0.2F、CN-0.4F和CN-0.6F的k值分别为8.95×10-4、9.98×10-4、1.68×10-3、1.64×10-3、1.35×10-3min-1。

图5 CN和CN-xF随时间降解RhB图(a)和准一级反应动力学曲线(b)
2.3 电化学实验分析
所制备样品在紫外光照射下的i-t图如图6a所示。CN-0.2F与CN相比具有更大的光电流,原始CN的光电流密度较低为(-0.19 μA/cm2),但其有较好的稳定性,相比之下CN-0.2F光电流密度较高为(-0.38 μA/cm2),但降低了瞬态光电流的稳定性。说明表面氟离子修饰可以促进CN样品的光生电子和空穴的分离效率,使CN-0.2F表现出提升的光电流。为了进一步研究样品的界面电荷传输性能,测试了其电化学交流阻抗谱,如图6b所示。CN-0.2F比CN的圆弧半径更小,通过模拟等效电路图(图6b插图)获得CN与CN-0.2F的Rct(电极和电解质界面电阻) 值分别为101 000 Ω和62 759 Ω,表明表面氟化可以提升CN的界面电荷传输和迁移能力,有利于提高其光催化性能。
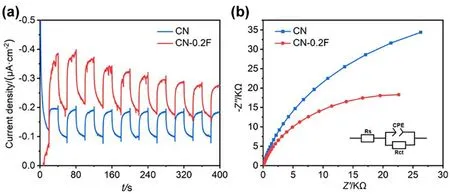
图6 CN和CN-0.2F的i-t 图(a)和电化学交流阻抗图(b)
2.4 光催化机理研究
基于以上表征分析,CN-xF可能的光催化降解RhB反应机理如图7所示。
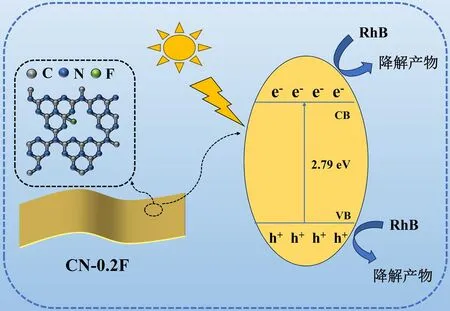
图7 所提出的光催化降解RhB机理示意图
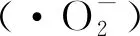
3 结论
采用一步简单HF浸渍法制备了表面氟化的CN-xF。氟离子表面改性可以显著改变CN表面电子结构,有利于促进光生电子-空穴的分离效率和传输性能,提高CN的光催化降解RhB性能。在优化的实验条件下,CN-0.2F在5 h后对RhB的降解率可达47.9%,是CN降解率的1.6倍。本研究中表面氟化处理方法简单易行,对于表面阴离子修饰其他光催化材料具有较好的借鉴意义。
