具有三光子性质的碘代咔唑基三吡啶锰(Ⅱ)配合物的合成及光动力学活性
2024-01-25李雅琴刘玲玲蔡昌婷
张 琼,李雅琴,刘玲玲,蔡昌婷,乔 瑞,宣 俊*
(1.安徽大学化学化工学院,功能无机材料化学安徽省重点实验室,安徽 合肥 230601;2.阜阳师范大学 化学与材料工程学院,安徽 阜阳 236037)
配合物非线性光学材料在上世纪八十年代以后迅速发展,成为科研人员关注的热点课题[1]。由于金属原子本身具有不同的d 或f 电子数、不同的氧化数和配位数,配体结构也具有多样性,这使得形成的非线性光学材料具有独特的光电性能。因此相对于单纯的无机或者有机非线性光学材料有着更多的优势[2]。除此之外,配合物的吸收谱带较多,分子内部存在着光子从配体到中心金属离子的跃迁以及从中心金属离子到配体的跃迁,这使得配合物的基态偶极化和极化率较大,基态与激发态之间的能级差则相对较小。这一特点可以提高配合物非线性光学材料光电响应的速度,通过将配体设计成具有一定结构特征的新型配体,使这一类型的材料得到进一步的发展[3-5]。
光敏剂是指在光化学反应中,通过将光能转移到一些对可见光不敏感的反应物上来提高感光性能的物质[6]。性质优良的光敏剂通常具有以下特点:1)纯度较高的单一化合物;2)稳定性良好;3)荧光一般处在近红外区;4)三重态量子产率比较高;5)分子的暗毒性小,光毒性大;6)具有较好的靶向性,并且容易被人体组织吸收[7-11]。本文引入卤素离子来修饰配体,目的在于增加配合物分子的光敏活性,让配合物更好的应用于光动力学治疗中。
锰是第四周期的过渡金属,是生物体必须的微量元素之一,它的最外层电子结构是d5,5 个单电子分别占据五个3d 轨道,处于半充满的状态[12]。近年来,锰(Ⅱ)配合物由于其优越的光电性能引起了科研人员的广泛关注,对比铱(Ⅲ)、铂(Ⅱ)、金(Ⅰ)等贵金属配合物,锰(Ⅱ)配合物表现出类似的长寿命磷光发射和高发光量子效率,并且具有成本低,毒性小的优点,在光电功能材料领域逐渐占据一席之地[13-17]。
本文围绕一种咔唑基三吡啶锰(Ⅱ)配合物MB3 进行了一系列探讨。具体的设计思路如下:1)咔唑基三吡啶作为一种三齿配体,可以与Mn螯合形成稳定的配位化合物,使得形成的配合物表现出较好的非线性光学性质[18-19]。2)引入碘原子,可以改善分子间体系的交叉过程,使得配合物的ROS 产率得到提高[20]。3)金属中心的引入可以促进配合物的非线性光学性质[21]。
1 实验部分
1.1 试剂与仪器
试剂:2-乙酰基吡啶、乙醇、氢氧化钾、中间体A3、氨水、饱和MnCl2溶液等。所有溶剂均为分析纯,并且已按照标准方法进行了纯化和干燥。
仪器:核磁共振谱仪(JNM-ECZ400S,TMS 为内标);傅立叶红外显微系统(Vertex80+Hyperion 2000,KBr 压片);液相色谱质谱联用仪(LTQ Orbitrap XL);紫外分外光度计(U-3900 Spectrophotometer);荧光分光光度计(F-7000 FL Spectrophotometer);超高分辨率激光共聚焦显微镜(TCS SP8 STED 3X);全自动协调飞秒激光器Coherent Astrella+TOPAS Prime (1 100-2 600 nm,1 kHz,120 fs)。
1.2 配体B3 及配合物MB3 的合成路线

图1 配体B3 及配合物MB3 的合成路线
配体B3 的合成:称取2-乙酰基吡啶(2.6 g,0.022 mol)加入500 mL 的圆底烧瓶中,用适量的乙醇溶液溶解,称取氢氧化钾(1.2 g,0.023 mol),用少量的水溶解后加入上述圆底烧瓶,常温搅拌30 min。称取A3(4.4 g,0.01 mol),用乙醇溶液溶解后加入体系,搅拌15 min,用恒压滴液漏斗将40 mL 左右的氨水逐滴滴入体系中,80 ℃回流4 h,停止加热,旋干溶剂,用乙醇分散后即可析出棕黄色固体。1H NMR (400 MHz,d6-CD3COCD3) δ 8.92 (s,2H),8.79 (dd,J=1.9,0.5 Hz,1H),8.75(dd,J=1.8,0.9 Hz,1H),8.74 (t,J=1.0 Hz,1H),8.73-8.72 (m,1H),8.04 (dd,J=8.6,1.9 Hz,1H),8.01-7.95 (m,2H),7.73 (ddd,J=9.0,8.6,1.1 Hz,2H),7.67-7.59 (m,1H),7.57 (s,1H),7.47-7.41(m,3H),4.30 (d,J=7.6 Hz,2H),1.45-1.18 (m,15H).13C NMR (100 MHz,d6-CDCCl3) δ 156.67,155.95,150.88,149.24,141.79,140.09,136.94,129.70,128.70,125.93,124.78,123.84,123.51,122.45,121.49,119.57,118.82,112.13,110.74,109.67,39.45,31.11,28.87,28.60,24.45,23.09,14.10,11.12.IR (KBr,cm-1): 2952,2630,1647,1397,1010,834,705.ESI-MS m/z: calcd for: M:636.17,found:637.18[M+H+].
配合物MB3 的合成:称取配体B3(63.7 mg,0.10 mmol)于无水乙腈中,加热使其溶解,将上述配体溶液逐滴滴加到溶于无水乙腈的饱和MnCl2溶液中,常温搅拌20 min 后收集黄色固体。Mp:357-359℃。IR (KBr,cm-1): 3427,2936,2364,1600,1473,1100,864,800,717,673.MALDITOF-MS m/z:calcd for:M:761.05,found:761.27.
2 光物理性质
2.1 紫外-可见吸收光谱与单光子荧光光谱
选取DMSO 作为溶剂,测定MB3 的单光子吸收和发射光谱,探究配合物MB3 吸收能量后的电子跃迁行为以及激发态回落时的发光现象。测定结果如下:
如图2(a)所示,配合物MB3 在280~300 nm处表现出较高的吸收,此峰归属于配合物分子内部的π-π*跃迁;在300~350 nm 处表现出相对较弱的吸收,此峰归属于配体分子内电荷转移(ICT);在380 nm 附近的吸收是配合物的中心金属离子Mn(Ⅱ)到配体的电荷转移(1MLCT)。如图2(b)所示,MB3 在440 nm 左右表现出较强的荧光。
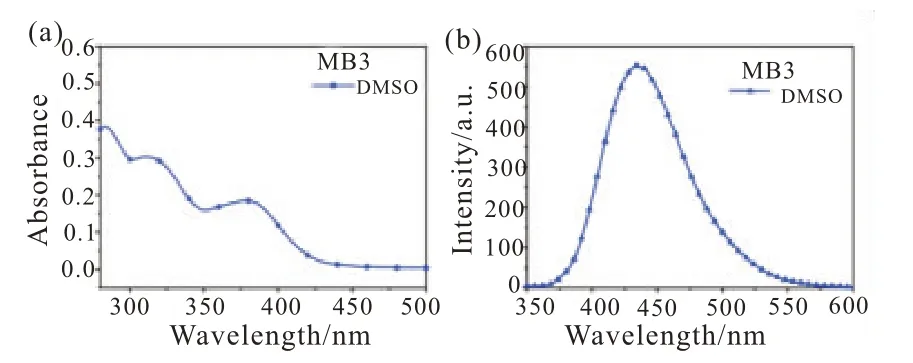
图2 (a)MB3 的紫外-可见吸收光谱(b)MB3 的单光子荧光光谱(测试浓度:10-5mol/L)
2.2 三光子荧光光谱
实验采用荧光对比法在1 150~1 550 nm 的飞秒激光激发下测试了配合物的三光子荧光光谱,进一步研究配合物MB3 的非线性光学性质。以罗丹明6 G 作为标准样品进行对比,计算公式如下:
下标“s”和“r”分别代表样品和参比(参比溶液是溶于乙醇的10-3mol/L 的罗丹明6 G)。f 为光纤光谱仪采集到的荧光信号的整体荧光收集效率强度。Q,n,c 分别为荧光的量子产率,溶剂的折射率,溶液的浓度。测试结果如下:
由图3(a)可知,配合物MB3 在1 150-15 50 nm 的激发下具有明显的三光子荧光信号。随着激发波长增加,配合物的荧光先增强后又减弱。在激发波长为1 450 nm 时,配合物的三光子荧光强度达到峰值。将配合物MB3 的三光子发射位置与单光子发射位置对比后,发射位置出现了接近100 nm 的红移。根据上述公式计算得到MB3在1450 nm 激发下,其的三光子吸收截面达到2.2×10-79cm6s2photon-2,表明配合物MB3 具有较强的三光子吸收性质。

图3 (a)MB3 的三光子激发荧光光谱;(b)三光子吸收截面(a/b,测试浓度10-3mol/L)
3 生物应用探索
3.1 活性氧检测与细胞毒性测试
考虑到碘原子引起的重原子效应,研究了配合物MB3 的活性氧(ROS)生成能力。2,7-二氯二氢荧光素二乙酸(H2DCF-DA)是商用指示剂,本身是不带有荧光的,但经过氢氧化钠活化半个小时后会水解产生HDCF,HDCF 与ROS 反应生成DCF,发出荧光。如图4(a)和(b)所示,光照条件下,指示剂在520 nm 左右发出强烈的绿色荧光,随着时间推移荧光强度逐渐变大,表明配合物MB3 能够生成ROS,并且生成ROS 的速度较快。继续探索了生成活性氧的种类,使用Bruker NanoX 波段光谱仪,在298 K 条件下对配合物MB3 进行了ESR 测定。如图4(c)所示,光照条件下,MB3 在空气饱和的水溶液中记录了特征信号,没有光照则未能检测到特征信号。光照后在3 600 G 和3 460 G 之间观察到相对强度为1:1:1的特征单线态氧三元组信号,表明光照条件下,配合物MB3 产生的ROS 的种类为1O2。

图4 (a)在525 nm PBS 光照射下,MB3 存在下的H2DCFDA 的荧光强度(b)525 nm PBS 光照射下,MB3 产生的ROS(c)光照前后,TEMP 捕获MB3 的ESR 信号(c=1.0×10-3 mol/L)(d)配合物在HeLa 细胞中的毒性测试
上述测试结果表明,MB3 有作为光敏剂的潜力,进一步进行了相关细胞毒性实验。如图4(d)所示,黑暗条件下,不同浓度的MB3 与HeLa 细胞孵育培养24 h 后细胞的存活率仍然保持在80%以上,表明配合物MB3 暗毒性较低;光照条件下,细胞的存活率则有着明显的下降趋势,细胞存活率随着MB3 浓度增大而逐渐减小。由此可知,配合物MB3 具有较低的暗毒性和较高的光毒性,具有良好的光动力学应用前景。
3.2 细胞内的ROS 检测
利用商用ROS 荧光探针2,7-二氯-氢荧光素(DCFH-DA)观察ROS 的产生。DCFH-DA 进入细胞后,被细胞内存在的酯酶水解,生成对ROS敏感的探针DCFH,DCFH 与ROS 快速反应生成荧光化合物2,7-二氯荧光素(DCF)。因此,可以通过DCF 的荧光强度来评估细胞内活性氧的水平。DAPI 是一种可以穿过细胞膜,与DNA 紧密结合的荧光染料,在358 nm 激光下,复合物DAPI-DNA 发出蓝色荧光,可以用于标记细胞核。如图5 所示,将MB3 和DCFH-DA 孵育HeLa 细胞30 分钟,光照条件下,随着时间的推移,观察到明显的荧光增强现象,表明细胞内具有有效的ROS生成,生物测试结果与化学测试结果相一致。
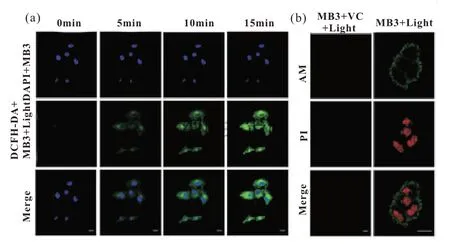
图5 (a)以DCFH-DA 为指示剂进行共聚焦显影在HeLa细胞内检测ROS 的产生;(b)AM/PI(5 μm)处理MB3(10 μm)体外PDT 疗效观察不同处理后的HeLa 细胞。
以钙黄素(AM)和碘化丙啶(PI)为指标,直观评价MB3 作为光敏剂时对癌细胞的杀伤效果,以证实PDT 的高效率。当出现钙黄素的绿色荧光时,说明细胞状态良好;但当出现碘化丙啶的红色荧光时,说明细胞已经死亡。如图5(b)所示,MB3 孵育HeLa 细胞30 分钟后进行AM/PI 染色。Vc 能够抑制ROS 产生过程,光照后加入Vc组出现绿色荧光,说明细胞未死亡;而PDT 组出现红色荧光,说明癌细胞已死亡。综上所述,MB3诱导细胞死亡的机制结果表明,MB3 产生的ROS破坏癌细胞使得细胞死亡。
4 结论
本文设计合成了一种碘原子修饰的咔唑三吡啶锰配合物MB3,配合物具有良好的非线性光学性质,最大三光子吸收截面可达到2.2×10-79cm6s2photon-2。ROS 生成和细胞成像表明MB3 在细胞内和细胞外均具有优异的单线态氧生成能力,其细胞毒性测试显示MB3 具有较高的光毒性和较低的暗毒性,光照条件下能够在细胞内产生活性氧诱导癌细胞死亡,具有应用于光动力学治疗的潜力。
