ICP-MS法检测种植中药材中的无机溴化物含量
2024-01-24武晓剑马艳宁辛振强
武晓剑,姜 悦,马艳宁,辛振强,殷 红,钱 勇,*
(1.上海诗丹德标准技术服务有限公司,上海 201314;2.国家中药现代化工程技术研究中心中药标准分中心,上海 201314;3.宁波立华制药有限公司,浙江 宁波 315174)
溴甲烷、二溴乙烷、1,2-二溴-3-氯丙烷等有机溴化物常作为杀虫剂、杀菌剂、土壤和谷物熏蒸剂用于植物保护,其使用后在环境中的残留物分解产生的含溴无机物被统称为无机溴化物[1-2]。虽然土壤中的无机溴污染也可能来自于灌溉用水,但大量研究表明,经熏蒸剂熏蒸过的土壤中种植的农作物无机溴化物含量远高于未经熏蒸土壤中的农作物[3],因此可以认为农作物中高浓度的无机溴化物主要由熏蒸剂带来的[1,4]。我国近几年才开始禁用溴甲烷等熏蒸剂,但其残留的无机溴化物却可长时间存在于土壤中,半衰期达1.5~2年[5]。毒理学研究表明,动物体内的无机溴化物会影响甲状腺激素的合成[6],摄入溴化物的动物出现明显的发育迟缓,体重、脑重、脑组织中蛋白质含量永久性缺损等现象[4]。考虑到无机溴化合物的毒性,很多国家将其列入了农药清单,并对最大使用量进行了限制规定。美国联邦法规第40篇180节123段“溴甲烷熏蒸产生的无机溴残留,残留物的允许限值”[7]、欧盟农药数据库[8]、日本农业化学品肯定列表[9]中,均明确了各种食品中的无机溴化物的限量要求。《美国药典2021 通则<561>植物源类产品》[10]中规定,植物源类药品中无机溴化物不得超过125 mg/kg。我国暂时没有中药材中无机溴化物的限量要求,也没有相应的检测方法。因此,建立一种简便、准确、灵敏的检测中药材中无机溴化物的方法是迫切而有重要实践意义的。
美国和日本学者曾开发过针对食品中无机溴化物的检测方法,如环氧醇类衍生后的气相色谱(电子捕获器)法、非抑制性离子色谱法、X-射线衍射光谱仪[5,11-12],这些方法均需对样品进行衍生化等预处理,操作过程复杂且设备费用高,所以国外一些政府实验室依然会采用低成本的溴酚红分光光度法测试水和蘑菇产品中的无机溴化物[3],但该方法需要先对样品进行灰化,将溴离子氧化为溴,与苯酚反应后再用光谱法进行检测。国内对于食品中无机溴污染物尚无完善的检测研究[13],现仅有利用离子色谱法对出口食品的商检行业标准所涉及无机溴化物的检测[13-14]。
本方法利用无机溴化物,如溴离子、溴酸根离子等溶于水的性质,先用水提取中药样品中溴元素的各种价态化合物,然后用电感耦合等离子体质谱仪(ICP-MS)进行检测,采用更加准确的内标法定量。ICP-MS 相对于气相色谱、离子色谱、光谱等方法[5,11-14]具有速度快、灵敏度高、可大批量检测等优点,且检出限均低于上述方法或行业标准[15]。本研究建立了方便、灵敏、高通量的无机溴化物检测方法,该方法可应用于中药材产品市场筛查、风险评估等,大大填补了药品安全控制领域的空白。同时,该方法还可用于中药及其制品的海外注册、出口检测等,方法的低检出限更能满足美国和欧洲市场对于中药材中无机溴化物的检测要求,有效地提高了产品质量控制手段,为消除贸易壁垒提供重要的技术支持。
1 材料与方法
1.1 材料与设备
1.1.1 材料与试剂
溴(Br)标准溶液(质量浓度为1 000µg/mL),艾吉析科技(上海)有限公司;锗(Ge)单元素标准溶液(质量浓度为1 000µg/mL),国家有色金属及电子材料分析测试中心;蒸馏水,广州屈臣氏食品饮料有限公司;硝酸(分析纯),上海泰坦科技股份有限公司;氨水(分析纯),上海泰坦科技股份有限公司;白芍饮片,宁波立华制药有限公司;白芍药材、赤芍饮片、甘草饮片、黄芪饮片、人参饮片、苍术药材、白术饮片、川贝母饮片、黄芩饮片、半夏药材、柴胡药材,均购于亳州中药材交易市场。
1.1.2 仪器与设备
ICPMS 2030 型电感耦合等离子体质谱仪,日本岛津公司;SB25-12DTD 型超声仪,宁波新芝生物科技股份有限公司;L550型离心机,湖南长沙湘仪仪器有限公司。
1.2 方法
1.2.1 样品处理
1.2.1.1 样品中无机溴化物提取方式的筛选
以白芍饮片作为代表性中药进行样品处理方法的筛选。尝试采用其他金属元素测试常用的加酸后微波消解方式,即将饮片于60 ℃干燥2 h后粉碎,过3号筛后精密称取粉末0.5 g,精确加入质量浓度为100µg/L的溴标准溶液0.5 mL,置于微波消解罐中,加硝酸5 mL,密闭进行消解。消解完全后,将消解液转入50 mL量瓶中,加入锗元素标准溶液(1µg/mL)200µL,用水稀释至刻度,摇匀后用ICP-MS 进行检测,考察常用微波消解方式是否适合中药中无机溴的测定。
1.2.1.2 样品中无机溴化物提取溶剂的筛选
将白芍饮片粉碎后,精密称取0.5 g,置于50 mL容量瓶中,精确加入质量浓度为100µg/L的溴标准溶液0.1 mL;分别采用pH 为9.0 的氨水溶液(碱溶液)、体积分数为10%的硝酸溶液(酸溶液)及蒸馏水作为溶剂超声提取(功率500 W,频率40 kHz,下同)30 min,放冷至室温后定容至刻度,摇匀,以4 000 r/min 离心5 min,收集上清液,采用ICP-MS进行检测,考察样品在酸、碱、蒸馏水不同体系中无机溴化物含量以进行提取溶剂的筛选。每种提取溶剂下平行制备6 份加标样品。
1.2.1.3 样品中无机溴化物提取时间的筛选
白芍饮片粉碎后,精密称0.5 g置于50 mL量瓶中,精确加入质量浓度为100µg/L的溴标准溶液0.1 mL,蒸馏水定容至刻度,采用超声方式对中药样品中的无机溴化物进行提取,考察超声提取时间分别为30、45、60 min时样品中无机溴含量。每种超声提取时间条件下平行制备6份加标样品。
1.2.2 标准曲线的建立
用蒸馏水稀释溴标准溶液(1 000µg/mL),配制10µg/mL溴标准贮备液。精密量取一定量的标准贮备溶液,分别用蒸馏水稀释配制成0、0.01、0.02、0.05、0.10、0.20µg/mL 的溴标准溶液。用蒸馏水将锗单元素标准溶液稀释并定容,配制成1µg/mL的锗内标溶液。用ICP-MS对溴标准溶液分别进行测定,以溴元素质量浓度为横坐标,以内标(Ge)校正过的溴元素信号强度为纵坐标,绘制标准曲线。
1.2.3 样品中无机溴化物的测定
1.2.3.1 样品前处理方法
取中药适量,粉碎后过3 号筛,精密称取粉末样品0.5 g,置于50 mL 容量瓶中。加蒸馏水30 mL 左右,超声提取30 min,冷却至室温后用蒸馏水定容至刻度,摇匀,以4 000 r/min 离心5 min,收集上清液作为待测样品溶液。
1.2.3.2 ICP-MS参数
高频功率1.20 kW;采样深度5.0 mm;等离子体气流量8 L/min;辅助气流量1.10 L/min;载气流量0.70 L/min;池气体流量6.0 mL/min;池电压-21 V;能量过滤器7.0 V;轮廓积分时间mid。
1.2.4 数据处理
采用Labsolutions ICPMS 软件对数据进行采集和分析,内标法测定无机溴化物含量。
2 结果与分析
2.1 ICP-MS检测条件的确定
由于氩的第一电离能为1 520 kJ/mol,溴的第一电离能为1 140 kJ/mol[16],所以在氩形成的等离子体中,溴元素可以进行电离,然后用质谱进行捕获和分析。因此,可以采用以氩气为载气的ICP-MS 检测样品中以不同价态存在的溴元素。
溴元素的同位素中含有质量数为35的质子和质量数为30~63 的中子,因此溴的同位素从65Br 到98Br均有存在,但大部分半衰期都很短,从纳秒到小时不等[16],除了79Br和81Br两个同位素,其他均无法在自然界中长期、稳定的存在。79Br 和81Br 的丰度分别为50.69%和49.31%[16],在以氩气为碰撞气体的条件下,81Br 由于受到40Ar40Ar1H 的干扰,其本底比79Br 高4~5倍,因此选择79Br作为质谱测量的质量数[13]。
2.2 样品处理方法的确定
2.2.1 样品中无机溴化物提取方式的确定
采用其他金属元素常用的加酸微波消解方式进行提取,平行制备6 份加标样品,使用ICP-MS 检测,内标法计算无机溴的含量、加标回收率及相对标准偏差,结果如表1所示。由表1可以看出,6份平行样品无机溴含量的检测结果差异较大。常用的加酸后微波消解法检测溴元素的回收率和精密度不好的原因,推测可能是由于加入的酸在微波的高温下可以将Br-氧化成溴单质,而溴在消解过程中由于压力增大而挥发,产生随机缺失。因此决定不采用微波处理,仅使用酸、碱、水作为溶剂超声提取中药中的无机溴化物。

表1 样品中无机溴含量检测结果(采用加酸微波消解方式处理)Table 1 Detection results of inorganic bromide content in samples(treated by acid solution combined with microwave digestion)
2.2.2 样品中无机溴化物提取溶剂的确定
由表2 可见,酸、碱溶液提取的平行样品间检测结果差异较大,这可能是因为溴化物在酸、碱环境中都可发生反应,溴单质、溴化氢、溴酸根等的动态变化以及溴化氢和溴的挥发等都会使检测结果产生较大波动,从而使检测的精密度下降;而水可以相对较稳定地从药材基质里提取溴离子和溴酸根离子等无机溴化物。因此,选择蒸馏水作为中药样品中无机溴化物的提取溶剂。
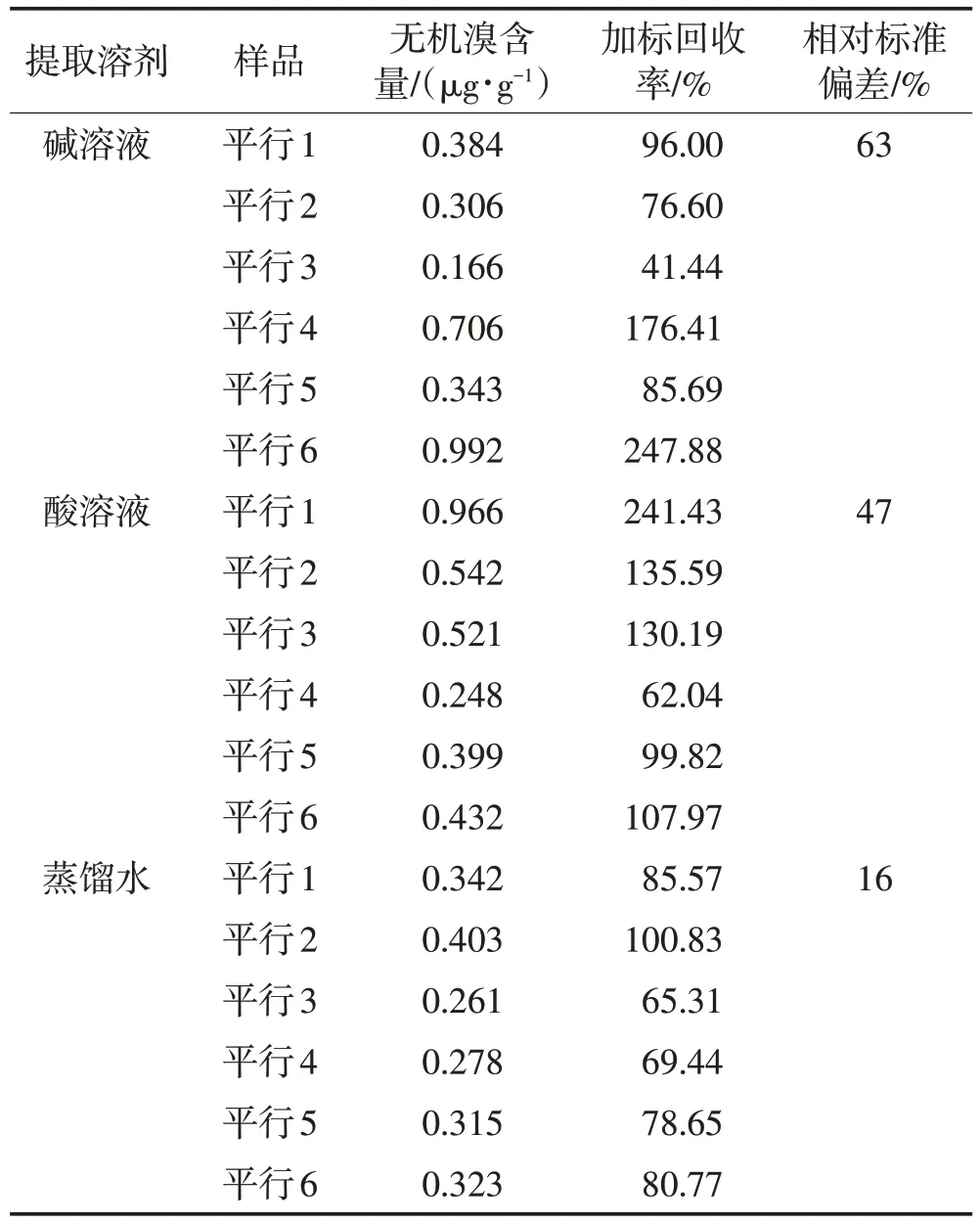
表2 样品中无机溴含量的检测结果(采用不同溶剂提取)Table 2 Detection results of inorganic bromide content in samples(extracted by different solvents)
2.2.3 样品中无机溴化物超声提取时间的确定
由表3 可知,随着提取时间的延长,无机溴含量略有下降。采用t检验分析法对不同超声时间下提取效果进行显著性分斩,结果见表4。由表4可知,超声30 min 与45、60 min 相比,结果均呈现显著性差异(P<0.05),分析原因可能为超声时间的延长使超声仪中的水升温,导致溴化物含量降低。因此,确定超声提取时间的30 min。

表3 样品中无机溴含量的检测结果(不同超声提取时间)Table 3 Detection results of inorganic bromide content in samples(different ultrasonic extraction time)
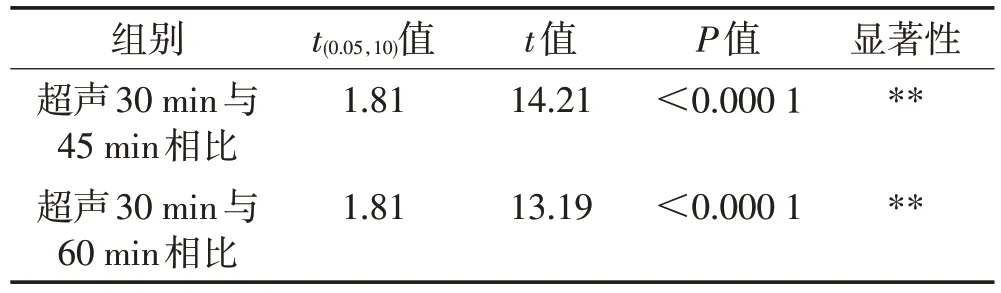
表4 不同超声提取时间差异显著性分析Table 4 Significance analysis of the difference between different ultrasonic extraction time
2.3 线性和范围
按照“1.2.3.2”的ICP-MS 检测方法,对溴标准溶液进行回归分析以确定该方法中元素的线性。以溴元素质量浓度为横坐标,以内标(Ge)校正过的溴元素信号强度为纵坐标,绘制标准曲线,结果见图1。

图1 溴元素标准曲线Fig.1 Calibration curve of bromide
溴元素标准曲线方程为y=44.826x+0.256 1,决定系数为0.999 7,说明该方法在溴元素质量浓度为0~0.20µg/mL范围内具有良好的线性。
2.4 准确度和精密度
按照优化的方法对6份平行加标样品进行测定,用溴元素加标回收率来评价方法的准确度;用回收率的相对标准偏差评价方法精密度的重复性,用ICH Q14 分析方法开发建议的F检验来评价方法中间精密度,结果见表5。

表5 回收率和精密度结果Table 5 Results of recoveries and precision
从表5可以看出,两次之间重复试验的加标回收率均在109.9%~121.3%,说明该方法回收率较好,准确度较高;单次试验相对标准偏差为1.8%,方法的重复性较好。两次重复试验相对标准偏差为2.7%,统计两次重复试验的F值为1.02,远小于临界值F(0.05,5)=5.05,说明两次重复试验无显著性差异,方法的重现性好,精密度较高。
2.5 检出限和定量限
根据《中华人民共和国药典》[17]中电感耦合等离子体质谱法检出限和定量限的评价方法,测定不少于7 份的空白样品溶液,分别以连续测定空白样品溶液响应值的3 倍标准偏差(3SD)、10 倍标准偏差(10SD)所对应的待测元素浓度作为检测限、定量限。用ICP-MS 对空白溶液分别检测10 次,再分别用3 倍和10 倍的响应值换算得出:无机溴化物的检出限为1µg/g,定量限为2µg/g。检出限和定量限低于《美国药典2021 通则<561>植物源类产品》[10]对于植物源类药品中无机溴化物的要求,且均低于美国、欧盟、日本对于食品中无机溴化物的限值[7-9]。
2.6 中药无机溴化物含量ICP-MS检测法的运用示例
采用水超声提取基质中的无机溴,然后用ICPMS对溴元素进行检测,采用内标法定量方法,分别检测了白芍、赤芍、甘草、黄芪、人参、苍术、白术、川贝母、黄芩、半夏、柴胡等中药,均未检出无机溴化物,以上药物加标回收率为103.2%~120.4%,表明用ICP-MS测试水提取药材中的无机溴化物具有较好的准确度和重复性。
3 结论
本试验建立了中药无机溴化物含量的ICP-MS检测方法。方法采用蒸馏水为溶剂,超声提取中药样品中无机溴化物,并用ICP-MS进行检测。经试验表明,该方法线性良好、准确度高、精密度好、灵敏度高,可用于中药基质中痕量无机溴化物的检测,且由于其分析时间短,成本较低,提高了试验效率。该方法也可应用于中药中无机溴的高通量检测工作。
