感兴趣区范围对MRI影像组学模型预测ICC分化程度的影响*
2024-01-23马喜娟钱贤灵钱宝鑫师毅冰
王 晴 马喜娟 钱贤灵 杨 春 钱宝鑫 师毅冰,,*
1.蚌埠医学院研究生院 (安徽 蚌埠 233000)
2.徐州市中心医院影像科 (江苏 徐州221009)
3.复旦大学附属中医院放射科(海 200032)
4.北京慧影医疗科技股份有限公司(北京 100192)
肝内胆管细胞癌(intrahepatic cholangiocarcinoma,ICC)起源于肝内二级胆管,是第二大常见的肝脏原发恶性肿瘤,近年来其发病率逐年上升,约占肝内原发性恶性肿瘤的10%- 15%[1]。ICC有三种大体病理类型:管周浸润型、腔内生长型及肿块型。肿块型肝内胆管细胞癌(intrahepatic mass-forming cholangiocarcinoma,IMCC)是最常见的类型[2],预后最差,总生存期[2-3]较短。
分化程度是指肿瘤细胞和正常细胞之间的相似程度[4],肿瘤细胞分化程度越高,恶性程度越低;而相反,肿瘤细胞分化程度低,则常为高度恶性。研究表明患者的生存率与肿瘤分化程度密切相关[5]。ICC的分化程度关系到患者预后[6-8]及治疗方式的选择,低分化ICC具有高复发风险,需要应加强随访或联合放化疗综合治疗进而改善患者的预后[7]。而对于高分化ICC患者,有效的手术切除可明显改善病人长期生存率[9]。因此,若能早期非侵入性地准确评估肿瘤分化程度,有助于患者制定个体化治疗方案,对于改善预后具有重要意义。
术前主要通过活检样本评估病变组织的生物学特征。然而,活检获得的组织样本较小,而肿瘤的异质性会导致基于活检样本的生物学特征评价不能代表整个肿瘤[6]。而影像组学的优点就在于,它可以获得肿瘤的宏观成像特征,对肿瘤的生物学特性进行全面和无创的重复评估[10],定量并客观地描述肿瘤的异质性[11],达到对肿瘤分类和预测的目的。因此,影像组学被广泛认为是迈向肿瘤个体化治疗发展的关键一步。
近年来有研究表明,瘤周微环境在肿瘤的进展和侵袭性中起着关键作用[12]。通过提取并分析瘤周影像组学特征,可以捕捉到肿瘤微环境的异质性和复杂性,从而更好地评估其生物行为,并为患者提供早期干预的可能性[13]。本研究将在原始肿瘤内感兴趣区(region of interest of tumor,ROItumor)的基础上,分别选取扩大三个尺度:8mm、10mm、12mm,探讨瘤内结合瘤周区域ROI的MRI影像组学特征对预测肿块型ICC分化程度的效能。
1 资料与方法
1.1 研究资料本回顾性研究经徐州市中心医院及上海复旦大学附属中山医院医学伦理委员会批准,免除受试者知情同意。回顾性收集2016年1月至2022年6月经手术病理证实并在术前行MRI检查的ICC患者191例。参考以往ICC影像组学研究中的分组比例,按照7:3随机分组法[14-15],将所有患者分为训练组(n=133)和验证组(n=58)。
入组标准:接受根治性切除术,术后病理证实为单发的ICC患者;病理信息完整;既往无相关肝脏手术治疗史;术前30 天内行MRI检查;单个癌灶;MRI检查所有图像质量达到诊断标准。排除标准:既往肝脏肿瘤治疗史;手术与MRI间隔超过30天;MRI图像质量差,包括有呼吸运动伪影效应的病变;两个或两个以上癌灶。
1.2 临床病理及影像特征通过电子病历系统获取患者的临床特征,包括性别、年龄、甲胎蛋白、糖类抗原19-9及癌胚抗原。
ICC标本采样采用 “7 点”基线取样方案[16],病理分化程度由每家医院的两名独立病理学家采用Edmondson-Steiner分级系统共同进行评估[17],并分为非低分化组(Ⅰ、Ⅱ级)和低分化组(Ⅲ、Ⅳ级)。如在评估过程中有任何分歧,将通过讨论达成共识。
所有MR图像均由两位腹部放射科医生使用双盲法独立分析并记录肿瘤大小、肿瘤形态(类圆形,分叶状及不规则)及有无肝包膜回缩。当两位放射科医生意见不同时,最后由一名高年资影像医生进行复核。
1.3 MRI检查方法收集入组的所有ICC患者均在术前完成了MRI平扫及增强检查。以GE 3.0T Discovery 750 MRI Systems为例,扫描序列包括:(1)横断面T2WI加权脂肪抑制成像:TR 4500ms,TE 88ms,层厚6-6.5mm,层间距1-2mm,矩阵320×224- 448×448;(2)横断面扩散加权成像(DWI):TR5454ms,TE49ms,层厚6-8mm,层间距1-2mm,矩阵130×96,b=0,800 s/mm2;(3)横断面T1梯度回波序列T1WI平扫及增强扫描:TR 3.54ms,TE 1.67ms,层厚4.8-5 mm,层间距0 mm。增强扫描通过注射20μmol/kg钆喷酸葡胺(Gd-DTPA),分别在20~30s、60~70s、180s时获取动脉期(T1WI-AP)、门静脉期(T1WI-PVP)、延迟期(T1WI-DP)图像。
1.4 影像组学分析本研究的影像组学分析流程见图1,主要包括:ROI勾画,特征提取,特征筛选,模型构建与评估。
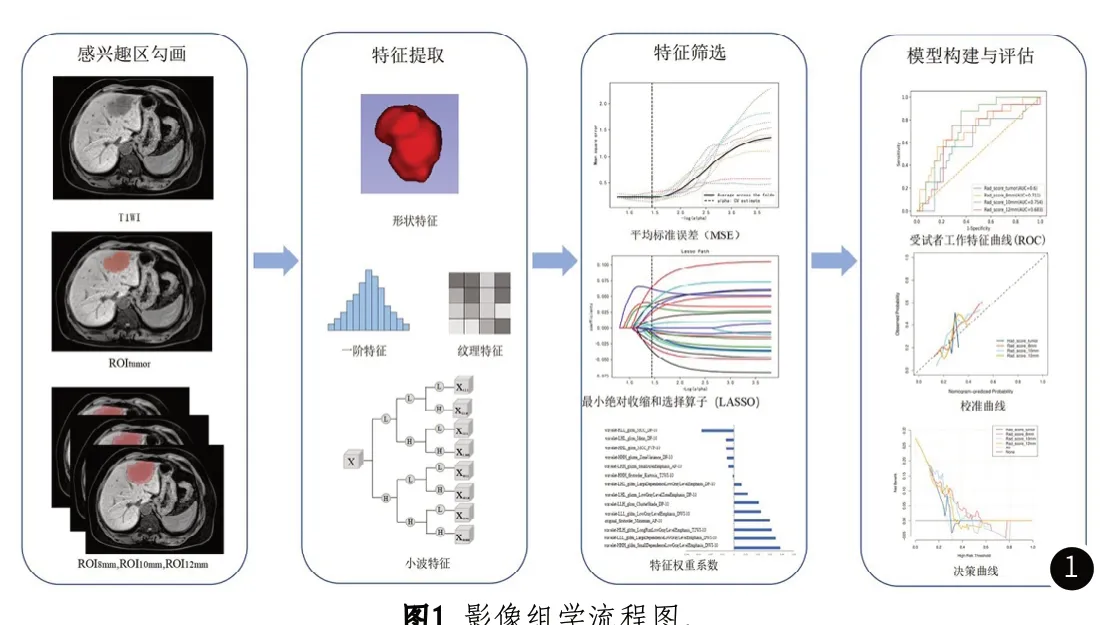
图1 影像组学流程图。
1.4.1 感兴趣区勾画 为了减少图像之间的异质性,所有的图像都重新采样到相同的体素大小(1×1×1mm3)并采用N4偏场校正对MRI图像进行预处理。本研究参照将瘤内和瘤周区域进行整体分割的方法勾画ROI[18-20]。对于每例纳入患者的MRI图像,由两名具有五年以上腹部影像经验的放射科医师使用开源软件3D Slicer 4.13.0版软件采用双盲法进行勾画,勾画时均知道患者患有ICC,但不了解病理结果和临床表现。两位医师在T2WI、DWI、T1WI、T1WI-AP、T1WI-PVP、T1WI-DP六个序列图像上沿着肿瘤边界手动逐层勾画病灶,得到的三维ROI标记为ROItumor,随后使用软件的“margin”模块自肿瘤边界向外分别扩张8、10、12mm,在手动去除扩张后肝实质外区域后,得到包含了瘤内与瘤周8、10、12mm的整体区域,分别标记为ROI8mm、ROI10mm、ROI12mm。如果两名放射科医师在勾画ROI时出现争议,则通过讨论达成一致意见。
1.4.2 特征提取 使用3D Slicer软件的Radiomics模块,分别从6个序列的ROI中提取影像组学特征。在特征筛选之前,使用z-score对影像组学特征进行标准化处理,提高数据的可比性,以确保结果的可重复性。
1.4.3 特征筛选 采用单变量选择法(SelectKBest)分析特征与分类结果的关系,选择P<0.05的特征。随后通过十折交叉验证的最小绝对收缩和选择算子(least absolute shrinkage and selection operator,LASSO)算法,筛选出具有非零系数的影像组学特征,根据各特征系数对所选特征进行加权得到相应ROI范围的影像组学评分(rad-score)。
1.4.4 模型构建与评估 利用逻辑回归(logistic regression,LR)机器学习算法对各个ROI范围的Rad-score建立ROItumor,ROI8mm,ROI10mm,ROI12mm模型,用于预测ICC的病理分化程度,并通过验证组进行验证。绘制各个模型的受试者工作特征(receiver operating characteristic,ROC)曲线,通过比较曲线下面积(area under the curve,AUC)、敏感度、特异度、准确度来评价各模型预测ICC分化程度的效能,采用Hosmer-Lemeshow检验评估模型的拟合优度并绘制校准曲线,决策曲线分析(decision curve analysis,DCA)评估模型的临床效用。
1.5 统计分析本研究采用使用R 4.2.3版软件和Python3.6.8版软件进行统计分析。计数资料使用卡方检验χ2或Fisher精确检验,以频数(%)表示。计量资料采用独立样本t检验或者Mann-Whitney U检验。采用Kolmogorov Smirnov检验对计量资料进行正态性检验,符合正态分布的计量资料进行独立样本t检验,用(±s)表示;不符合正态分布的则进行 Mann-Whitney U检验,用中位数(上、下四分位数)表示。DeLong检验用于比较不同ROC曲线之间的AUC差异。双侧P值小于0.05被认为具有统计学意义。
2 结 果
2.1 临床影像学特征表1总结了训练组和验证组患者临床影像学特征的比较。191例患者中男137例,女54例,年龄60.65±11.15岁,年龄范围:29~86岁,低分化125例,非低分化66例。训练组低分化83例,验证组低分化42例。训练组与验证组患者的病理分化程度差异无统计学意义(P>0.05)。典型病例见图2。
2.2 影像组学特征提取及选择针对每例患者,在每个ROI范围的各个序列分别提取851个影像组学特征。这些特征的主要类型包括:形状特征(14个)、一阶特征(18个)、纹理特征(75个)及经过小波变换的小波特征(744个)。即每个ROI范围在六个序列通过特征融合总共提取5106个特征。经过SelectKBest 在ROItumor、ROI8mm、ROI10mm、ROI12mm分别筛选出665,558,568,549个特征。最后经过LASSO回归后,在ROItumor、ROI8mm、ROI10mm、ROI12mm分别筛选出26,22,14,18个与ICC分化程度相关的影像组学特征。
2.3 模型构建与评估通过LR分别构建ROItumor、ROI8mm、ROI10mm、ROI12mm模型,在训练组中,4种影像组学模型的 AUC分别为0.891,0.839,0.767,0.807,验证组分别为0.600,0.711,0.754,0.683(图3,表2)。ROItumor、ROI8mm、ROI12mm模型在训练组表现出色(AUC为0.891~0.807),但在验证组中无法取得稳定的表现(AUC为0.6~0.711),模型泛化能力欠佳,均存在过拟合的现象。ROI10mm模型在在所有模型中最为稳定(训练组AUC=0.767;验证组AUC=0.754),其验证组AUC表现最好,依次优于ROI8mm,ROI12mm,ROItumor模型(P=0.458,0.281,0.052)。
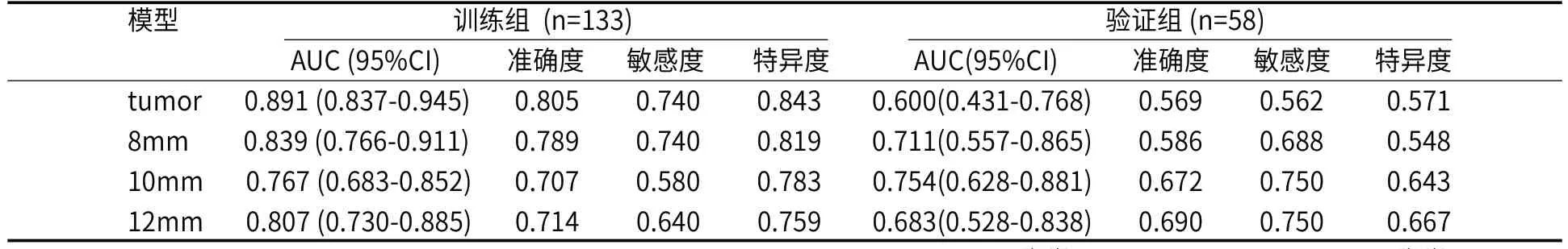
表2 不同ROI的影像组学模型的性能

图3A-图3B 四种ROI模型受试者工作特征(ROC)曲线。图3A为训练组;图3B为验证组。 AUC为曲线下面积。
分别绘制四个ROI范围的模型在验证组的校准曲线(图4A)。经过Hosmer-Lemeshow检验,所有模型P>0.05,表明它们均具有良好的校准度,即预测的风险概率与实际发生的风险相一致。决策曲线(图4B)显示四组模型明显高于全活检时的临床净收益,说明四组模型均有价值。四组模型阈值范围为0.12~0.58,净收益最高为0.2。当阈值为0.24时,临床净收益从高到底依次ROI10mm、ROI8mm、ROI12mm、ROItumor这与AUC的结果一致。经综合分析ROI10mm模型泛化能力最好,预测效能最优。
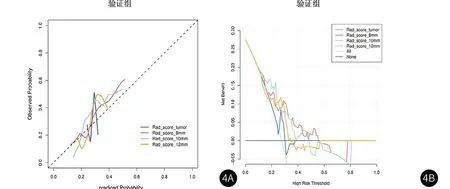
图4A-图4B 校准曲线与决策曲线。图4A 四种ROI模型的校准曲线(验证组);图4B 四种VOI模型的决策曲线(验证组)。
3 讨 论
ICC的分化程度在患者诊疗方案的选择及预后预测中起到重要作用。本研究采用4个不同ROI范围分别MRI影像组学模型预测肿块型ICC的病理分化程度。结果显示四个模型均具有预测价值,而ROI范围的选择对模型效能有一定影响,ROI10mm模型最为稳定,预测效能最优,更具备在临床应用中的潜力,有益于辅助临床制订个体化诊疗决策。
3.1 影像组学模型在预测肿瘤分化程度的结果与意义影像组学作为一种非侵入性的新兴技术,其在不同的肿瘤领域应用广泛[13,21]。此前已有很多研究着眼于肝细胞癌,利用影像组学技术有效地预测了肝细胞癌(HCC)的病理分级[22-26],展现了影像组学在肝脏肿瘤领域应用的巨大潜力[27]。但ICC与HCC之间存在许多差异[28],如肿瘤的生长模式、病理组织学和预后等。
Peng等人[4]发现超声影像组学模型能够有效预测ICC的分化程度,但其在验证组中为AUC=0.712,低于本研究,这可能是因为(1)MRI有着更高的空间分辨率和丰富的组织对比度,影像质量更高,更能清晰地显示ICC的细节信息。这样的优势可以帮助提取更准确的特征,从而提高模型的预测性能。(2)本研究将多序列MRI影像进行融合,以展示肿瘤的不同特征,能够提供更多关于肿瘤分化程度的信息。Fiz[29]等人也建立了基于瘤内和瘤周的PET-CT影像组学模型,用于有效预测分化程度,其研究结果AUC优于本研究,原因可能如下:(1)ROI分割方式不同;(2)提取到的特征不同;(3)建模和特征筛选方法不同。但是PET获得的代谢图像的干扰因素较多[30],它显示的肿瘤代谢边界与实际肿瘤边界总是存在差别使一些纹理特征不够稳定[31]。并且高昂的检查费用和较低的空间分辨率也限制了PET/CT检查的临床应用[32],这些都对PET-CT影像组学模型的实际运用带来挑战[33]。
目前尚无基于CT或MRI的影像组学研究用于预测ICC分化程度,我们所构建的多模态融合的MRI影像组学模型,经过进一步验证和优化,可能为预测ICC患者的分化程度提供一种无创定量工具选择。
3.2 影像组学特征与分化程度的关系与意义在四种ROI范围下进行筛选去冗余后得到的MRI影像组学特征中,属于一阶特征的峰度(kurtosis)和属于纹理特征的长行程低灰度强调(LongRunLowGrayLevelEmphasis)出现频率最高,表明它们在预测ICC的分化程度中发挥更重要的作用。峰度值越高可能越意味着肿瘤组织在影像上具有尖锐的灰度值分布。而长行程低灰度强调反映了灰度尺度上的肿瘤异质性。值得注意的是,这两个特征也是Fiz[29]等人最终筛选到的与ICC分化程度相关的组学特征,再次证明了这些特征对ICC分化程度评估的重要性,它们可能与ICC组织的异质性和恶性程度密切相关。值得注意的是,四种ROI筛选后的大部分特征均属于经过小波变换的小波特征,这一结果与Peng等人基于超声影像组学预测ICC分化程度[4],Zhang等利用CT增强影像组学预测ICC淋巴结转移[14]以及Zhou等用MRI影像组学预测ICC微血管浸润[34]使用小波特征构建的模型一致。这表明小波特征可能与ICC的生物活性密切相关,是预测ICC表型富有价值的成像生物标志物。
3.3 瘤周影像组学的研究意义瘤周区域是现代肿瘤学中主要的研究对象[12]。最近越来越多的学者开始意识到只提取肿瘤原发灶的影像特征而忽略瘤周影像组学特征的研究存在缺陷和不足,将瘤周影像组学特征纳入到影像组学研究中[35-37],以更全面地了解肿瘤的特征。
ICC作为一种鲜有包膜高度侵袭性的肿瘤,它呈现着早期浸润和广泛转移的特点[38],在外科学上,切缘宽度取决于肿瘤侵袭性,是ICC患者术后复发和生存期的独立预后因素[39],对R0切除者,保留0.5cm到1cm切缘宽度可提高长期生存[40]。而在影像学上,瘤周影像组学特征更是被发现是有效预测ICC预后的独立危险因素[29],这些都一定程度证明ICC的瘤周区域蕴含着肿瘤异质性的丰富信息,需要进一步深入研究。目前对ICC影像组学研究仅选取单一的瘤周范围,无法确定多大尺度的瘤周区域可以更好的代表肿瘤微环境信息。因此本研究自肿瘤边界向外径向扩张了8-12mm,一共确定4个不同的ROI范围。结果显示,ROI范围的选择会影响组学模型的预测能力,结合瘤周10mm与瘤内区域可能会提高模型的预测效能,使得模型更加稳定。
我们的研究中,tumor,8mm,12mm范围的模型泛化能力不佳,出现了明显的过拟合现象,它们无法较好识别验证组中的新数据,这也是目前大多数影像组学模型都存在的问题[41-42]。泛化性是评价机器学习模型优劣的重要指标,而模型性能则主要通过验证集得到验证。将肿瘤边界外10mm的瘤周范围纳入研究范围的ROI10mm模型在验证组具有最佳的预测效能,其在未见过的数据上的表现更稳定,它的泛化能力比其他模型都更好,从而更具备在临床应用中的潜力。并且瘤周10mm范围这一结果与先前ICC和HCC的影像组学研究中[18,20,35,43]的有效瘤周范围一致。当然,这也需要在未来通过一个大样本量的外部验证集来最终确定模型的效能。总的来说,瘤周范围的选择在影像组学分析中起到关键作用。为了提高预测模型的效果,我们建议对瘤周范围进行系统分析和比较,以选择合适的尺度优化预测模型,以更好地辅助临床决策。
3.4 局限性与展望本研究存在以下局限性:(1)为回顾性研究,结果有待大样本的外部验证进一步证实;(2)患者的MRI图像来自不同的机器,可能会引入一定的选择偏倚,但我们通过图像预处理的方法减小误差;(3)本研究仅选择了一种ROI勾画方式,未来可以通过比较不同的分割方式来优化预测模型。
4 结 论
本研究基于4个不同范围的ROI提取筛选了影像组学特征,并通过训练集进行学习、调试构建了预测模型,在测试集进行验证。结果表明ROI范围对MRI影像组学模型预测ICC的分化程度有一定影响,瘤灶本身加入合适的瘤周范围可以帮助构建更加稳定的模型,协助临床决策。
