中国慢性胃炎诊治指南(2022年,上海)*
2024-01-15中华医学会消化病学分会中华医学会消化病学分会消化系统肿瘤协作组
中华医学会消化病学分会 中华医学会消化病学分会消化系统肿瘤协作组
胃炎指各种病因引起的胃黏膜炎症,显微镜下表现为组织学炎症。慢性胃炎(chronic gastritis)是由多种病因引起的胃黏膜慢性炎症,是主要由幽门螺杆菌(Helicobacter pylori, Hp)感染所引起的临床常见病。按照慢性胃炎分类的悉尼系统[1],可将慢性胃炎分为慢性非萎缩性胃炎(chronic non-atrophic gastritis)和慢性萎缩性胃炎(chronic atrophic gastritis)。虽然慢性胃炎并非急重症或疑难病,但因其系多种胃病或其他器官疾病的基础疾病,影响人们的生活质量和生命健康,故而为广大医务工作者和病患所重视。
自2017 年《中国慢性胃炎共识意见(2017 年,上海)》[2]制定以来,国际上先后出台了《欧洲胃癌前状态和癌前病变管理指南:2019年更新》[3]、《筛查与根除幽门螺杆菌预防胃癌:台北全球共识》[4]、《美国胃肠病学会胃黏膜肠化生管理临床实践指南》[5]、《美国胃肠病学会萎缩性胃炎诊断与管理专家意见》[6]等一系列相关共识和指南。美国《Sleisenger and Fordtran 胃肠病和肝病(第11 版)》[7]“胃炎和胃病”章节也作了部分更新;我国《第六次全国幽门螺杆菌感染处理共识报告(非根除治疗部分)》[8]亦顺利颁布。此外,慢性胃炎与胃癌的相关进展、根除Hp 对萎缩性胃炎癌变的预防作用、内镜和病理诊断手段包括人工智能技术等均取得长足进步,表明更新慢性胃炎共识意见势在必行。为此,由中华医学会消化病学分会主办、上海交通大学医学院附属仁济医院消化学科暨上海市消化疾病研究所承办的《中国慢性胃炎诊治指南(2022 年,上海)》研讨会议(以下简称研讨会)于2022年12月24日在上海召开。
一、指南形成方法
本指南涉及慢性胃炎的流行病学特征、病因和分类、临床表现、内镜诊断和随访的意义与人工智能的应用、组织学病理检查、实验室检查、治疗原则和策略、慢性萎缩性胃炎的转归及其影响因素和癌变预防、国内外有关萎缩性胃炎的争议问题共九大类临床问题,包含53项推荐意见,由中华医学会消化病学分会的16名专家组成撰写小组,按照循证医学研究对象、干预措施、对照、结局(participant,intervention,comparison,and outcome;PICO)原则撰写草案,并在研讨会前对指南草案进行反复讨论和修改。研讨会期间,来自全国的99名消化病学专家认真听取撰写小组专家针对每项推荐意见的汇报,在充分讨论后采用改良Delphi 法以无记名投票形式通过或放弃该项推荐意见。推荐意见的证据质量等级和推荐强度分级标准参照美国内科医师协会临床指南委员会标准(表1、表2)[9]。针对每项推荐意见,投票意见为完全同意和(或)基本同意者>80%视为通过,反之则全体成员再次讨论;如第2次投票仍未达到前述通过所需要求,则当场修改后进行第3 次投票,确定接受或放弃该项推荐意见。

表1 美国内科医师协会临床指南委员会制定的证据质量等级标准

表2 美国内科医师协会临床指南委员会制定的推荐强度分级标准
二、临床问题和推荐意见
1.临床问题1:慢性胃炎的流行病学特征
推荐意见1-1:慢性胃炎是我国人群最常见的消化系统疾病;我国慢性萎缩性胃炎患病率较高。
证据质量:高;推荐强度:强推荐
慢性胃炎是我国人群最常见的消化系统疾病,目前我国基于内镜诊断的慢性胃炎患病率接近90%[10]。Hp 感染是慢性胃炎发生的主要病因,相关meta 分析显示全球约44.3%的人口感染Hp[11],而慢性活动性胃炎患者的Hp 感染率高达99.4%,即所谓的Hp 相关性胃炎[12]。我国Hp 感染率为40.6%~55.8%[13-14],因此,慢性胃炎的患病率较高。
美国胃肠病学会估计美国人群慢性萎缩性胃炎患病率约为15%[6]。我国缺乏慢性萎缩性胃炎的流行病学数据,国内一项大规模横断面调查显示,在8 892 例经内镜诊断为慢性胃炎的患者中,慢性萎缩性胃炎和慢性非萎缩性胃炎的构成比分别为17.7%和82.3%,且内镜诊断为慢性萎缩性胃炎的比例低于组织学诊断(25.8%)[15]。有研究[16]显示,如以组织学诊断为“金标准”,胃镜诊断慢性萎缩性胃炎的准确性仅为50.3%。因大部分慢性萎缩性胃炎患者无明显消化道症状或未行胃镜检查,慢性萎缩性胃炎的实际患病率可能更高,估算我国整体人群的慢性萎缩性胃炎患病率>20%。
慢性胃炎亦可根据病因分为Hp 胃炎和非Hp胃炎,Hp 胃炎京都全球共识将Hp 胃炎定义为感染性疾病[17]。随着对Hp感染重视程度的提升和Hp筛查、根除的推广,我国Hp感染率正以每年0.9%的趋势缓慢下降[13],慢性萎缩性胃炎的患病率亦有望下降。
推荐意见1-2:慢性胃炎的患病率一般随年龄增长而上升。
证据质量:高;推荐强度:强推荐
英国胃肠病学会的胃腺癌高危患者诊断和管理指南指出,慢性萎缩性胃炎的发生风险与年龄呈正相关,且男性略高于女性[18]。美国一项研究[19]对6年间接受胃镜检查的48万余例受试者进行分析,结果显示慢性活动性胃炎的患病率约由10~19 岁的5%升至30~39岁的12%,慢性萎缩性胃炎的患病率约由60~69 岁的0.8%%升至70~79 岁的1.2%,此后继续随年龄增长而增高。慢性萎缩性胃炎发病的年龄依赖特征与Hp感染关系密切。
我国最新家庭Hp 感染控制和管理共识报告指出,Hp 感染主要发生于儿童和青年时期,且感染率随年龄增长而升高[20]。一项针对我国甘肃省武威市2 163名居民的横断面研究[21]表明,<39岁人群的Hp感染率随年龄增长不断升高,于30~39岁达到峰值。随着Hp 持续感染时间的累积和炎症反应对胃黏膜损伤的加剧,慢性萎缩性胃炎的发生风险不断增高。与此同时,慢性萎缩性胃炎的发病率亦会随我国人口老龄化进程加深而呈上升趋势[10]。
推荐意见1-3:慢性萎缩性胃炎的患病率与胃癌发病率呈正相关。
证据质量:高;推荐强度:强推荐
慢性萎缩性胃炎与胃癌的发生关系密切,属于胃癌前疾病,国外文献多统称为广义的癌前病变[18]。慢性萎缩性胃炎是慢性胃炎按照Correa模式向胃癌进展的重要阶段,是Hp 感染、环境和遗传因素共同作用的结果,与胃癌发病率呈正相关。在不同国家或地区人群中,慢性萎缩性胃炎的患病率存在差异,可能与Hp 感染率不同有关。我国胃黏膜癌前状态和癌前病变的处理策略专家共识指出,累及全胃的伴或不伴肠化生的重度慢性萎缩性胃炎具有较高的胃癌发生风险[22]。
2.临床问题2:慢性胃炎的病因和分类
推荐意见2-1:幽门螺杆菌感染是慢性胃炎最主要的病因。
证据质量:高;推荐强度:强推荐
70%~90%的慢性胃炎患者胃黏膜有Hp 感染,感染一般难以自发清除,从而导致慢性感染[23]。Hp 感染引起慢性胃炎发病的因果关系符合科赫(Koch)法则[24];Hp 胃炎是一种感染性疾病[17]。Hp感染引起胃炎的机制与细菌毒力因子直接或通过免疫反应间接损伤胃黏膜、诱发炎症反应有关[25]。Hp 感染者几乎均发生慢性活动性胃炎[12],部分Hp感染者在慢性胃炎的基础上发生胃黏膜萎缩和(或)肠化生[17,25]。
推荐意见2-2:胆汁反流、长期服用非甾体抗炎药和(或)阿司匹林等药物、酒精摄入是慢性胃炎相对常见的病因。
证据质量:中等;推荐强度:强推荐
胆汁、非甾体抗炎药(nonsteroidal anti-inflammatory drug, NSAID)和(或)阿司匹林等药物、酒精可通过不同机制损伤胃黏膜,这些因素长期损伤胃黏膜所致的疾病炎症反应相对较轻,本应属于胃病(gastropathy)范畴[26],但通常仍将其作为胃炎。这些因素是Hp阴性慢性胃炎相对常见的病因[27]。
推荐意见2-3:自身免疫因素在自身免疫性胃炎发病中起主要作用,该类型胃炎在我国较少见。
证据质量:高;推荐强度:强推荐
机体免疫功能异常导致自身抗体如抗壁细胞抗体和抗内因子抗体产生,抗壁细胞抗体可引起胃体黏膜炎症、萎缩,抗内因子抗体可导致维生素B12吸收不良。自身免疫性胃炎(autoimmune gastritis,AIG)主要表现为胃体萎缩性胃炎,伴有血和(或)胃液抗壁细胞抗体和(或)抗内因子抗体阳性,严重者因维生素B12缺乏而有恶性贫血表现[28]。AIG 的发病与遗传因素相关,研究发现一些遗传易感基因,如人类白细胞抗原(human leucocyte antigen,HLA)-DRB1*03 和HLA-DRB1*04 与AIG 相关,Hp 感染可能是部分AIG的始发因素[28-29]。
AIG 在北欧和北美国家报道较多,而我国少有报道[30-31]。美国人群中AIG 患病率为0.5%~2.0%,而伴有维生素B12缺乏的恶性贫血型AIG 患病率为0.15%~1.00%[6]。AIG 的发生具有性别倾向性,女性患者比例高于男性。AIG可与自身免疫性甲状腺炎等自身免疫病并存。
推荐意见2-4:慢性胃炎的分类尚未统一,一般基于其病因、内镜所见、胃黏膜病理变化、胃炎分布范围等相关指标进行分类。
证据质量:中等;推荐强度:强推荐
目前一般基于悉尼系统(病因、胃黏膜萎缩、胃炎分布范围等)进行慢性胃炎分类[27]。世界卫生组织(WHO)国际疾病分类第11 版(ICD-11)胃炎分类见表3。

表3 世界卫生组织国际疾病分类第11版胃炎分类
推荐意见2-5A:基于病理所见可将慢性胃炎分为慢性萎缩性胃炎和慢性非萎缩性胃炎两大类。
证据质量:高;推荐强度:强推荐
推荐意见2-5B:基于胃炎分布范围可将慢性胃炎分为胃窦为主胃炎、胃体为主胃炎和全胃炎三大类。
证据质量:中等;推荐强度:强推荐
按照悉尼系统分类方法,慢性胃炎分为慢性萎缩性胃炎和慢性非萎缩性胃炎两大类[27];胃黏膜萎缩可分为单纯性萎缩和化生性萎缩,胃黏膜腺体有肠化生者属于化生性萎缩[32]。胃体为主胃炎尤其是伴有胃黏膜萎缩者,多数胃酸分泌减少,发生胃癌的风险增加;胃窦为主胃炎多数胃酸分泌增多,发生十二指肠溃疡的风险增加[17]。该种胃炎分类方法有助于预测其并发症发生风险。
推荐意见2-6:其他特殊类型胃炎包括巨大肥厚性胃炎、嗜酸细胞性胃炎、淋巴细胞性胃炎、肉芽肿性胃炎、感染性胃炎、放射性胃炎和化学性胃炎。
证据质量:低;推荐强度:条件推荐
除Hp 感染外,同属螺杆菌属的海尔曼螺杆菌感染也是感染性胃炎的病因之一(<1%);其他感染性胃炎可见于各种病原体感染,包括结核分枝杆菌、梅毒螺旋体、念珠菌、寄生虫等,但均少见[33]。巨大肥厚性胃炎、嗜酸细胞性胃炎、淋巴细胞性胃炎、肉芽肿性胃炎、放射性胃炎、化学性胃炎等相对少见。随着我国克罗恩病发病率的上升,肉芽肿性胃炎的诊断率可能会有所提升。巨大肥厚性胃炎和嗜酸细胞性胃炎的报道相对较多。巨大肥厚性胃炎病因不明,病例报道提示巨细胞病毒和Hp 感染可能与之相关[34]。嗜酸细胞性胃炎与食物过敏原介导的慢性炎症反应相关[35]。淋巴细胞性胃炎与Hp感染[36]、乳糜泻[37]等相关。放射性胃炎可由急、慢性放射性损伤所致[38]。肉芽肿性胃炎可分为感染性和非感染性,前者见于各种病原体感染,后者与异物、克罗恩病、嗜酸性肉芽肿、过敏性肉芽肿等相关。
推荐意见2-7:部分其他自身免疫病可引起或伴随慢性胃炎,患者常合并上腹部非特异性消化不良症状。
证据质量:中等;推荐强度:强推荐
风湿性疾病如系统性红斑狼疮、系统性硬化病、皮肌炎、干燥综合征、类风湿关节炎等均可引起慢性胃炎,其临床表现为非特异性,如腹痛、恶心、呕吐、厌食、吞咽困难等[39]。克罗恩病可累及从口腔至肛门的任何部位,约7%的克罗恩病患者有胃部受累,多见于年轻患者[40]。自身免疫性胰腺炎也可引起胃炎,其病理特征为胃黏膜固有层弥漫性淋巴浆细胞浸润和IgG4/IgG 比值升高(特别是在胃黏膜固有层下部),血清IgG4水平也可能升高[41]。
推荐意见2-8:心力衰竭、慢性肾功能衰竭、门静脉高压症、糖尿病等也可引起慢性胃炎。
证据质量:中等;推荐强度:条件推荐
慢性肾功能不全定期血液透析的患者可发生慢性胃炎,患病率约为50%,表现为胃节律失常和胃排空延迟。心力衰竭、门静脉高压症、糖尿病、甲状腺疾病等也可导致慢性胃炎,一般为慢性非萎缩性胃炎[42-44]。荨麻疹患者在疾病发作期常出现胃炎症状,可能与血清组胺升高有关[45]。
3.临床问题3:慢性胃炎的临床表现
推荐意见3-1:慢性胃炎无特异性临床表现,部分患者可无任何症状,有症状者主要表现为持续或反复发作的上腹痛、腹胀、饱胀感等,与消化不良症状谱相似。
证据质量:高;推荐强度:强推荐
我国一项多中心研究[15]纳入8 892 例慢性胃炎患者,分析显示13.1%的患者无任何症状,有症状者按发生率高低依次表现为上腹痛(52.9%)、腹胀(48.7%)、餐后饱胀(14.3%)和早饱感(12.7%),近1/3的患者同时存在2 个及以上上述症状,与功能性消化不良症状谱相似。中华医学会消化病学分会胃肠动力学组对来自全国25 家医院、经胃镜检查诊断为慢性胃炎的745 例门诊患者的问卷调查显示,根据症状发生率高低,常见症状依次为饱胀感(73.4%)、上腹不适(63.1%)、上腹痛(61.3%)和嗳气(52.2%),除上腹痛外,其余症状均在餐后出现或加重[46]。日本一项纳入9 125 例慢性胃炎患者的临床研究[47]中,40%的患者有至少1 个消化不良症状,慢性胃炎患者的临床表现和精神心理状态与功能性消化不良患者比较,差异均无统计学意义(P均>0.05)。Carabotti 等[48]的研究发现,胃窦局灶性胃炎患者的消化不良症状与全胃炎患者比较,差异无统计学意义(P>0.05)。Huang 等[49]分析了2 923 例无症状体检者的内镜检查结果,发现99.59%的个体有内镜下异常表现,绝大多数为慢性胃炎(95.11%)。
中青年慢性活动性胃炎以Hp胃炎为主[15];老年慢性胃炎的病因除Hp 感染外,还包括服用NSAID、合并胆汁反流以及其他理化因素,有症状者较中青年多[50]。一项纳入262 例功能性消化不良患者的回顾性研究[51]显示,胆汁反流性胃炎患者上腹痛症状更明显。在NSAID 服用者中,高达40%会出现上腹部不适、隐痛、恶心呕吐、上腹饱胀、嗳气、食欲减退等上消化道症状,严重并发症如上消化道出血、溃疡穿孔发生风险增加3~5倍[52]。
推荐意见3-2:慢性胃炎患者伴有消化不良症状可能与心理应激、睡眠障碍、焦虑抑郁情绪等有关,需重视慢性胃炎与消化心身疾病共病情况。
证据质量:中等;推荐强度:条件推荐
随着医学模式向生物-心理-社会医学模式的转变,部分慢性胃炎患者因合并心理应激、睡眠障碍、焦虑抑郁情绪或非特异性躯体化症状,被认为属于消化心身疾病范畴[53]。杨其法等[54]社区居民慢性胃炎危险因素的病例对照研究中,多因素Logistic回归分析发现,在慢性胃炎的主要危险因素中,睡眠障碍排第4 位(OR=1.384)。德国一项研究[55]分析了4 181名18~79岁社区居民的健康体检资料,结果显示慢性胃炎与非慢性胃炎居民合并焦虑障碍的比例分别为27.0%和15.3%。除焦虑外,慢性胃炎症状的严重程度与心理应激也呈正相关,其影响因素主要包括压力、不良饮食习惯和生活方式等[56]。我国一项纳入300 例慢性胃炎患者的研究[57]发现,精神心理因素与慢性胃炎的黏膜病变严重程度相关,焦虑、抑郁、负性事件、精神压力和某些人格特征与慢性萎缩性胃炎和肠化生之间可能存在双向因果关系。
荐意见3-3:自身免疫性胃炎常无特异性症状,随病情进展可相继出现缺铁性贫血、恶性贫血、维生素B12缺乏相关周围神经病变等,并发1型胃神经内分泌肿瘤、胃腺癌,伴发其他自身免疫病(如1 型糖尿病、自身免疫性甲状腺炎)的风险增加。
证据质量:高;推荐强度:强推荐
AIG 患者在发生胃体萎缩前无典型临床表现,进展至胃体萎缩后,老年患者常见维生素B12缺乏相关神经系统症状,而年轻患者多因消化系统症状就诊[58]。随着胃黏膜萎缩的进行性加重,AIG 患者会逐渐出现铁、维生素B12、叶酸等必需微量营养素吸收障碍,临床上主要引起缺铁性贫血(iron deficiency anemia, IDA)、恶性贫血、周围神经病变等[28]。一项多中心横断面研究[59]报道,654例AIG 患者的男女比为1:2.3,48.3%(316 例)的患者存在贫血,其中恶性贫血占41.8%(132/316),IDA 占35.4%(112/316),IDA 更常见于女性和年轻患者,恶性贫血则在男性和老年患者中更常见。一项纳入593例慢性胃炎患者的研究[60]发现,维生素B12缺乏引起的神经系统症状可能出现于血液系统症状之前,可引发脊髓亚急性联合变性,主要表现为四肢远端或双下肢对称性麻木、行走不稳等。1 型胃神经内分泌肿瘤的发生与AIG 密切相关,系由AIG 致壁细胞减少、低胃酸水平刺激胃泌素大量分泌所致。AIG 患者常合并其他自身免疫病,与自身免疫性甲状腺炎和1 型糖尿病具有强相关性,发病率较健康人群增高3~5倍。研究表明,约24%~35%的自身免疫性甲状腺炎患者和约5%~10%的1 型糖尿病患者患有AIG[61-62]。
推荐意见3-4:前述特殊类型胃炎的临床表现各异。
证据质量:低;推荐强度:条件推荐
淋巴细胞性胃炎缺乏特异性临床表现,常见消化不良、上腹痛、烧心、呕吐、体质量减轻等症状;与Hp感染密切相关,部分患者可合并乳糜泻[63-64]。
轻型肉芽肿性胃炎无任何症状,病变范围较大时,可因胃溃疡或胃排空障碍而出现上腹痛、腹胀、恶心、呕吐、消化道出血和贫血[65];部分病例可发生幽门梗阻[66]。
嗜酸细胞性胃炎临床表现与累及部位和范围相关,嗜酸性粒细胞以黏膜、黏膜下浸润为主时多见腹痛、恶心、呕吐,以浸润肌层为主时可出现幽门梗阻[67]。
巨大肥厚性胃炎表现为渐进性、隐匿性的腹痛、恶心、呕吐症状,常伴有因严重蛋白质丢失导致的外周水肿[68]。
4.临床问题4:慢性胃炎内镜诊断、随访的意义与人工智能的应用
推荐意见4-1:慢性胃炎的内镜诊断主要依据普通白光内镜或特殊成像方法所见的黏膜炎症变化,需与病理检查结果结合作出最终判断。
证据质量:高;推荐强度:强推荐
慢性胃炎的基础病变多为炎症反应(充血渗出)或萎缩,据此将慢性胃炎分为慢性非萎缩性胃炎和慢性萎缩性胃炎[69],有利于与病理诊断统一。慢性非萎缩性胃炎内镜下可见黏膜红斑、出血点或斑块,黏膜粗糙伴或不伴水肿、充血渗出等基本表现。慢性萎缩性胃炎的诊断包括内镜诊断和病理诊断。内镜下可见黏膜红白相间,以白为主,皱襞变平甚至消失,部分黏膜血管显露;可伴有黏膜颗粒或结节状等表现[69]。肠化生在内镜下表现为黏膜欠光滑或灰色斑,白光内镜检查对肠化生的诊断与病理检查结果符合率较低[70]。
慢性胃炎可同时存在糜烂、出血或胆汁反流等征象,这些征象在内镜检查中可获得可靠证据。糜烂分为平坦型和隆起型两种类型,平坦型表现为胃黏膜片状糜烂灶,病灶大小从针尖样至长径数厘米不等;隆起型又称疣状糜烂,可见单个或多个疣状、膨大皱襞状或丘疹样隆起,病灶长径为5~10 mm,顶端可见黏膜缺损或脐样凹陷,中央有糜烂[71]。疣状胃炎包括成熟和未成熟两种类型,其中未成熟型隆起较低,病变可自行消失;成熟型隆起高峻,中央凹陷小而深,病变持续存在。疣状胃炎的病因和发病机制目前尚未完全阐明,一般认为疣状胃炎有癌变倾向,出现异型增生的比例较高[72]。疣状糜烂胃黏膜的胃小凹形态主要为稀疏粗大状的线状、斑块状和绒毛状[73],单发的疣状糜烂须与早期胃癌鉴别。糜烂的发生可能与Hp 感染、服用引起胃黏膜损伤的药物等有关[72],因此在诊断时应加以描述,如慢性非萎缩性胃炎或慢性萎缩性胃炎伴糜烂[17]。
染色内镜系将染料喷洒于需观察的胃黏膜表面,或处理光谱信息,以强化病变组织与周围正常组织的对比度,从而提高内镜诊断与病理检查的符合率。一项比较白光内镜与电子染色内镜诊断肠化生效能的多中心、前瞻性研究[74]显示,白光内镜诊断肠化生的特异性为98%,敏感性仅为53%,而电子染色内镜诊断肠化生的特异性为97%,敏感性提高至87%。慢性胃炎的内镜诊断须与病理检查结果结合作出最终判断。
关于普通白光内镜下未发现明显异常改变或病变者,是否可描述为“胃镜下正常胃黏膜像”,值得进一步研究。
推荐意见4-2:推荐内镜下初步评估胃炎的幽门螺杆菌感染状态。
证据质量:中等;推荐强度:强推荐
未感染Hp 的胃黏膜平滑而有光泽,胃体部大弯的皱襞细长、笔直,有时可见胃底腺息肉。胃角、胃体部小弯处观察到黏膜上皮下规律排列的集合小静脉(regular arrangement of collecting venule,RAC)是无Hp 感染的重要特征,胃角、胃体部小弯RAC 阳性作为排除Hp 感染标准的敏感性和阴性预测值均较高[75]。Hp 感染内镜下通常表现为弥漫性发红、黏膜肿胀和黏液白浊。除此之外,内镜下还可出现黏膜萎缩、皱襞异常、黄色瘤、增生性息肉等表现。
推荐意见4-3:内镜下应评估萎缩、肠化生的范围,电子染色放大内镜和显微内镜对慢性胃炎的诊断和鉴别诊断有一定价值。
证据质量:高;推荐强度:强推荐
于内镜下判断胃黏膜萎缩的范围,有助于评价胃癌发生风险。在内镜观察中,可根据木村-竹本分型(其临床意义和科学性参见本指南“三、待解决的临床问题”)判断胃黏膜萎缩范围,萎缩界限从胃窦开始向小弯侧发展,不超过贲门者为闭合型(close type,C 型),超过贲门向大弯侧发展为开放型(open type,O 型)。闭合型和开放型又分别分为3个亚型。C-1,萎缩界限局限于胃窦部;C-2,萎缩界限超过胃角;C-3,萎缩界限超过胃角且接近贲门。O-1,萎缩界限刚超过贲门;O-2,萎缩界限已遍及整个胃底;O-3,萎缩界限延伸至胃体。萎缩边界的变化可反映萎缩的范围和程度,C-1→C-2→C-3→O-1→O-2→O-3 为连续的变化过程,萎缩严重程度逐级递增[76]。胃黏膜萎缩范围越广,胃癌发生风险越高,内镜下开放型胃黏膜萎缩患者的胃癌风险为闭合型患者的7.27 倍[77]。一项纳入9 378 例研究对象的胃癌内镜筛查研究[78]同样显示,内镜下木村-竹本分型能对筛查人群进行风险分层,且对人群随访具有指导意义。
应用染色内镜联合放大内镜可进一步观察黏膜表面的微细形态变化[79]。显微内镜(包括激光共聚焦显微内镜和细胞内镜)光学活检技术对胃黏膜的观察可达到细胞水平,能实时辨别胃小凹、上皮细胞、杯状细胞等微细结构变化,对慢性胃炎的诊断和组织学变化的分级(Hp感染、萎缩和肠化生)具有一定参考价值。光学活检可选择性地对可疑部位进行靶向活检,有助于提高活检取材的准确性,减少活检取材标本数[80]。显微内镜与电子染色内镜相结合可进一步提高病变检出效能[81]。
推荐意见4-4:组织学病理活检对慢性胃炎的诊断至关重要,应根据病变情况和需要进行活检。临床诊断时建议至少在胃窦(胃角)和胃体分别活检;可疑病灶处另取活检组织。有条件时,活检可在电子染色放大内镜和显微内镜引导下进行。
证据质量:中等;推荐强度:强推荐
建议有条件的单位或在进行临床研究时,根据新悉尼系统的要求取5 块活检标本[27],即在胃窦和胃体各取2 块,在胃角取1 块(图1)。胃窦2 块组织取自距幽门2~3 cm 处的小弯(A1)和大弯(A2),胃体2块组织取自距胃角近侧4 cm 处的小弯(B1)和距贲门8 cm 处的胃体大弯中部(B2)。临床诊断时可取2~3 块活检标本,分别取自胃窦(A1)、胃角和(或)胃体(B1)部位。病理标本应分瓶放置。
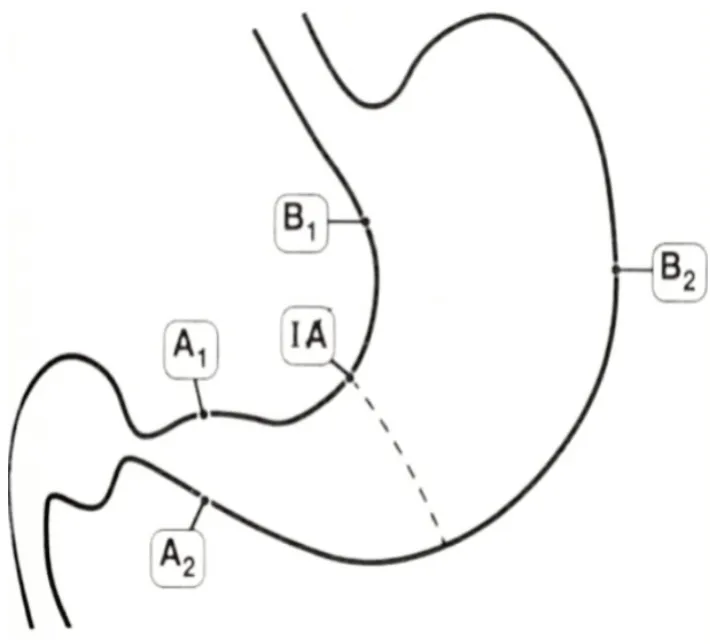
图1 新悉尼系统5点取材示意图
推荐意见4-5:应规范慢性胃炎的内镜检查报告,描述内容应包括幽门螺杆菌感染状态、萎缩和肠化生的范围、疑似病变的部位和特征,以及胃镜活检的部位和标本数。
证据质量:低;推荐强度:强推荐
应规范慢性胃炎的内镜检查报告,描述内容除胃黏膜病变部位和特征外,建议包括Hp 感染状态、萎缩和肠化生的范围、疑似病变部位和特征,以及胃镜活检的部位和活检取材标本数等。慢性胃炎的完整诊断应包括分类、伴随征象、萎缩范围分级等。例如,慢性非萎缩性胃炎伴疣状糜烂,慢性萎缩性胃炎(C-3,伴平坦糜烂)。
推荐意见4-6:经内镜和病理诊断为局限于胃窦的轻度萎缩性胃炎不一定需要定期进行内镜随访;累及胃体的萎缩性胃炎,每1~3年进行1次内镜检查;如伴随其他胃癌危险因素,则需更密切地进行内镜随访。
证据质量:低或中等;推荐强度:强推荐
萎缩和肠化生的程度和范围对于预测胃癌有一定意义;对于局限于胃窦的轻度或中度慢性萎缩性胃炎,伴或不伴轻度肠化生,可酌情进行内镜随访。如患者同时存在胃癌家族史、呈现不完全型肠化生、萎缩和肠化生范围广泛以及持续的Hp 感染等胃癌危险因素,建议至少每3 年进行1 次内镜随访并靶向活检[3,18]。
已有多项临床研究证实了病理学萎缩程度以及胃炎评价系统OLGA(operative link for gastritis assessment)和肠化生评价系统OLGIM(operative link for gastric intestinal metaplasia assessment)对胃癌的预测价值。重度萎缩性胃炎患者同时存在胃癌家族史时,约每年进行1次内镜随访获益更大[3,18]。
此外,对于病理结果为异型增生(概念详述见下文“临床问题5”),而普通白光内镜检查未发现明确病变的患者,推荐立即进行高清内镜[放大内镜和(或)染色内镜]检查,并对可疑病变进行活检。参照欧洲共识并根据我国国情,活检结果为高级别上皮内瘤变(high-grade intraepithelial neoplasia,HGIN)或高级别异型增生时,应立即复查高清内镜,证实诊断后考虑内镜下处理甚至外科手术;活检结果为低级别上皮内瘤变(low-grade intraepithelial neoplasia,LGIN)或低级别异型增生时,于6 个月~1 年内复查高清内镜[3,18]。美国学者则认为,即使是中重度萎缩性胃炎,也只需间隔3 年进行1 次内镜监测[6],这一观点不排除与美国胃镜检查费用较高且胃癌发病率较低有关。
与胃癌相关性较强的危险因素为Hp 感染和胃癌家族史;血清学证实的恶性贫血亦为胃癌危险因素;此外,来自胃癌高发地区、胃次全切除术后≥15年、年龄≥45 岁、男性、高盐摄入史和吸烟史也是胃癌不容忽视的危险因素[18]。有研究提示巨大肥厚性胃炎可能与胃癌相关[82],因此需定期行内镜随访,对于不能排除癌变的患者,可行外科手术治疗。淋巴细胞性胃炎可伴有淋巴瘤,随着病程的进展,部分患者可能发展为恶性淋巴瘤,应定期行内镜随访[83]。
为便于监测、随访病灶,有条件时可考虑行有目标的光学活检或胃黏膜定标活检(mucosa target biopsy,MTB)[84],以提高活检阳性率和监测随访的准确性。萎缩病灶本身呈灶状分布,原定标部位的变化不等同于未定标部位的变化。因此,不能拘泥于与前次活检部位的一致性而忽视对新发病灶的活检。目前认为萎缩和肠化生的范围是判断其严重程度的重要指标,而这是MTB结果所无法显示的。
推荐意见4-7:建议自身免疫性胃炎患者至少每3年进行1次内镜随访。
证据质量:低;推荐强度:条件推荐
AIG 的远期并发症为胃癌和胃神经内分泌肿瘤[85-86]。有研究[87]显示8.2%的AIG 患者胃黏膜萎缩状态分期属于高危胃炎分期(OLGA Ⅲ~Ⅳ期)。一项meta 分析显示,恶性贫血患者的胃癌发生率为0.27%/人年[88],高于普通人群。另一项长达20 年的随访研究[89]发现,恶性贫血患者的胃癌发生风险为普通人群的2.9 倍,1 型胃神经内分泌肿瘤的发生风险则为普通人群的13倍。
此外,多项研究发现恶性贫血患者不仅胃肿瘤发病率增高,小肠腺癌、食管鳞状细胞癌、胆管癌和血液系统恶性肿瘤的发病率也增高[90-91],故有必要对AIG 进行密切随访。结合欧洲指南和我国国情,推荐AIG 患者至少每3 年进行1 次内镜随访[3],并应完善抗壁细胞抗体和抗内因子抗体检测,同时评估贫血程度和维生素B12、铁缺乏情况。对于合并1 型胃神经内分泌肿瘤的患者,建议内镜下切除,并每1~2 年进行1 次内镜随访[6]。对于病灶长径≥10 mm和(或)组织学分级>2 级的1 型胃神经内分泌肿瘤,最新欧洲胃肠内镜学会指南建议行内镜下切除后随访监测,即使是治愈性切除的患者,也应每1~2年随访1次[92]。
推荐意见4-8:人工智能具有综合胃黏膜图像信息、辅助识别幽门螺杆菌胃炎的价值,其真正的临床应用潜力需更多临床研究验证。
证据质量:低;推荐强度:条件推荐
Hp胃炎准确的内镜诊断需要足够的技能培训,耗时、耗力且存在一定主观性。近年来,基于深度学习的人工智能在多个医学领域发挥愈加重要的作用,尤其是在医学成像方面。
Shichijo 等[93]于2017 年发表的研究回顾性收集30 000余张胃镜图片,建立识别Hp胃炎的卷积神经网络(convolutional neural network, CNN),用于识别Hp 阳性或阴性胃炎(首次CNN)和Hp 感染部位(2次CNN)并评估其效能。首次CNN 的敏感性、特异性、准确性和诊断时间分别为81.9%、83.4%、83.1%和198 s;2 次CNN 的敏感性、特异性、准确性和诊断时间分别为88.9%、87.4%、87.7%和194 s;而23 名内镜医师的相应数据分别为79.0%、83.2%、82.4%和(230±65) min。即与内镜医师相比,基于CNN 的内镜图像诊断Hp 胃炎具有更高的准确性和更短的诊断时间。后期研究证实,与白光成像相比,基于图像增强内镜,如蓝激光成像、联动成像技术的人工智能模型对Hp感染具有更高的诊断水平[94],尤其是在识别无Hp 感染、现症Hp 感染和Hp 根除后胃炎方面,基于联动成像技术的人工智能模型具有与有经验的内镜医师相似的识别能力[95]。使用源自多部位的多张内镜图像可显著提高CNN 模型识别Hp胃炎的能力,每例患者(8.3±3.3)张胃镜图像,诊断敏感性为91.6%(95%CI:88.0%~94.4%),特异性为98.6%(95%CI: 95.0%~99.8%),准确性为93.8%(95%CI: 91.2%~95.8%)[96]。2020 年发表的一项评价人工智能识别Hp 胃炎的系统综述和meta 分析显示,人工智能模型利用内镜图像预测Hp 胃炎的合并敏感性、特异性、ROC 曲线下面积(area under the curve, AUC)和诊断OR值分别为87%、86%、0.92 和40(95%CI: 15~112)[97],提示了人工智能算法用于Hp胃炎内镜诊断的良好性能。人工智能识别Hp胃炎在临床实践中具有可行性,可作为避免操作者依赖和活检依赖的有效措施。
推荐意见4-9:人工智能具有辅助识别慢性萎缩性胃炎、肠化生、异型增生的潜在价值。
证据质量:低;推荐强度:条件推荐
慢性萎缩性胃炎、肠化生、异型增生有进展至肠型胃癌的风险。传统白光内镜诊断胃萎缩和肠化生的可靠性不足,而新兴内镜技术如色素内镜、放大内镜、激光共聚焦显微内镜的应用,往往受到技术可行性和成本的阻碍。人工智能通过深度学习可发现更多抽象和有用的图像特性,有助于提高诊断的准确性、一致性和诊断速度。
2020年,Guimarães等[98]首次报道利用真实世界内镜图像,开发训练针对慢性萎缩性胃炎的深度学习系统,该系统的总体准确性高于内镜专家(93%对80%,P=0.030)。研究提出,针对胃癌前病变,深度学习能克服传统白光内镜检查较高的观察者间变异性。Zhang 等[99]回顾性收集慢性萎缩性胃炎和慢性非萎缩性胃炎的内镜图像,构建萎缩性胃炎识别和分级(轻、中、重度)CNN 模型,该模型诊断萎缩性胃炎的准确性、敏感性和特异性分别为94.2%、94.5%和94.0%,均高于内镜专家;轻、中、重度萎缩性胃炎的检出率分别为93%、95%和99%,呈现逐级升高的趋势。Lin 等[100]2021 年发表的研究回顾性收集我国不同地区14 家医院的白光内镜图像和相应胃活检组织,评估CNN 模型同时识别萎缩性胃炎和肠化生的准确性,结果显示该模型识别胃黏膜萎缩的AUC、敏感性、特异性、准确性分别为0.98、96.2%、96.4%和96.4%;识别肠化生的AUC、敏感性、特异性、准确性分别为0.99、97.9%、97.5%和97.6%,表明白光内镜图像CNN 模型用于识别萎缩性胃炎和肠化生也有很高的诊断准确性。因此,人工智能对于确定萎缩性胃炎的存在及其严重程度分级和发展过程具有巨大的潜在价值。
5. 临床问题5:慢性胃炎的组织学病理检查需要注意的问题
推荐意见5-1:活检标本应足够大,取材深度应达到黏膜肌层(图2)。不同部位的标本需分开装瓶。内镜医师应向病理医师提供取材部位、内镜所见、内镜诊断、简要病史等临床资料。
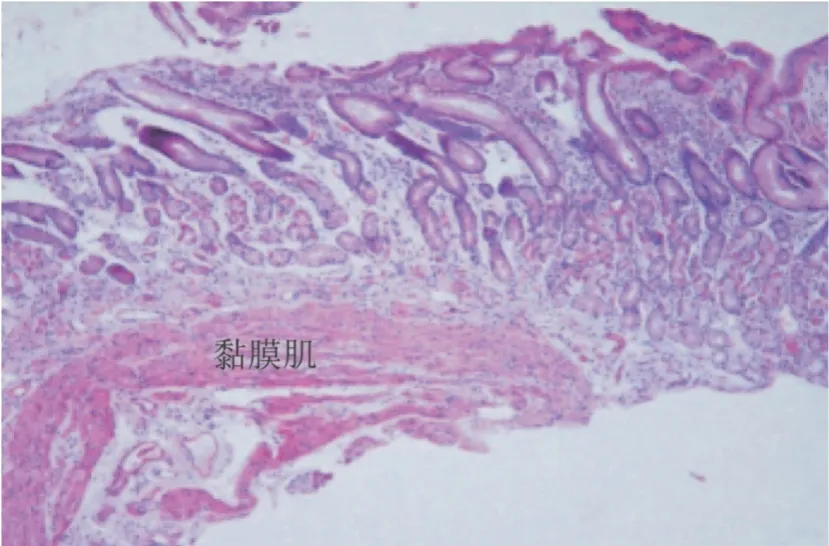
图2 取材深达黏膜肌层的胃黏膜(HE染色,×100)
证据质量:高;推荐强度:强推荐
标本取材过浅(少)而未达黏膜肌层,则失去了判断有无萎缩和(或)萎缩严重程度的依据。组织学病理活检时应核实取材部位,且送检标本需按取材部位分开装瓶。此外,临床和实验室检查资料也非常重要,如嗜酸细胞性胃炎的诊断须结合临床。严重Hp 胃炎的胃体黏膜亦可有明显炎症反应或萎缩。内镜医师应向病理医师提供取材部位、内镜所见、内镜诊断、简要病史等临床资料,加强临床医师与病理医师的联系有助于获取更多反馈信息,如有无胆汁反流、用药史等[2,69]。
推荐意见5-2:慢性胃炎有5 种组织学变化,即幽门螺杆菌、慢性炎症、活动性、萎缩和肠化生,分别分为无(0)、轻度(+)、中度(++)和重度(+++)四级。分级标准采用我国慢性胃炎的病理诊断标准(附录)和新悉尼系统的直观模拟评分法(图3)。
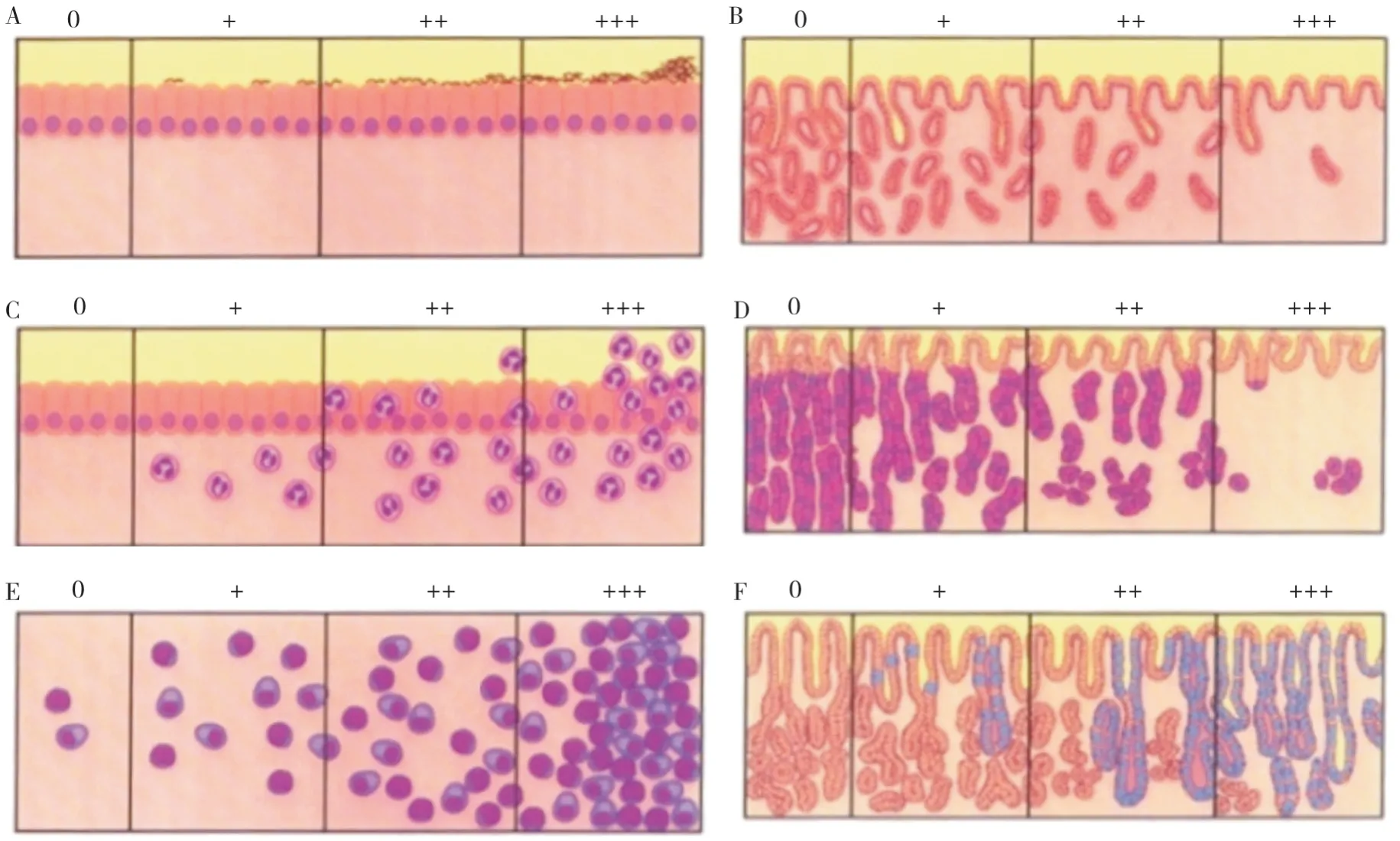
图3 新悉尼系统直观模拟评分法示意图
证据质量:高;推荐强度:强推荐
为提高国际间对慢性胃炎交流的一致性,新悉尼系统提出了直观模拟评分法[27]。我国慢性胃炎的病理诊断标准采用文字描述[2],内容具体且易操作,与新悉尼系统类似。将我国文字描述的病理诊断标准与新悉尼系统的直观模拟评分图结合,可提高我国慢性胃炎病理诊断与国际诊断标准的一致性。对伴有活动性弥漫性炎症而HE 染色切片未发现Hp者,应通过特殊染色仔细寻找Hp,推荐采用较简便的Giemsa 染色,也可按各病理室惯用的染色方法,有条件的机构可行免疫组化染色。胃肠黏膜是人体免疫系统的主要组成部分,存在生理性免疫细胞,主要为淋巴细胞、组织细胞、树突细胞、浆细胞,这些细胞形态在HE 染色下难以与慢性炎症细胞区分。建议病理医师结合内镜检查结果,在内镜检查无明显异常的情况下,如标本在高倍视野下平均每腺管有1个单个核细胞浸润,可不将其认定为“病理性”胃黏膜[1-2,69],而视作基本正常胃黏膜(图4)。
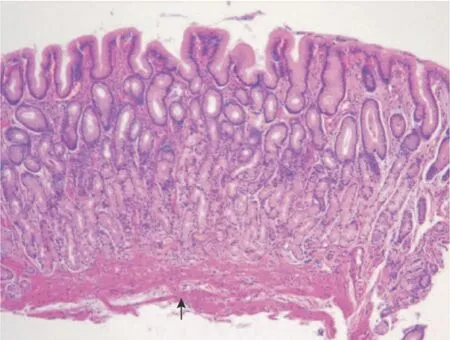
图4 基本正常胃黏膜(HE染色,×100)
此外,需注意观察非Hp 感染患者胃黏膜活检标本中胃黏膜深层和黏膜下层小血管内是否存在微血栓或机化血栓。黏膜浅层灶性出血和表面上皮脱落的组织学表现考虑为细小动脉血栓机化后再通所致,表面上皮不完整加上胃酸的作用,可能是患者出现上腹部不适症状的原因[101]。
推荐意见5-3:慢性胃炎的病理诊断应包括部位分布特征和组织学变化程度,有病因可循者应报告病因。胃窦与胃体炎症反应程度相差2级及以上时,加上“为主”修饰词,如“慢性(活动性)胃炎,胃窦为主”。病理检查应报告每块活检标本的组织学变化,推荐使用表格式慢性胃炎病理报告。
证据质量:中等;推荐强度:强推荐
病理诊断应报告每块活检标本的组织学变化,可向临床医师反馈更详细的信息,有利于减少随机活检误差造成的结论偏倚[69]。表格式慢性胃炎病理报告(图5)信息简明、全面,便于进行临床治疗前后比较。
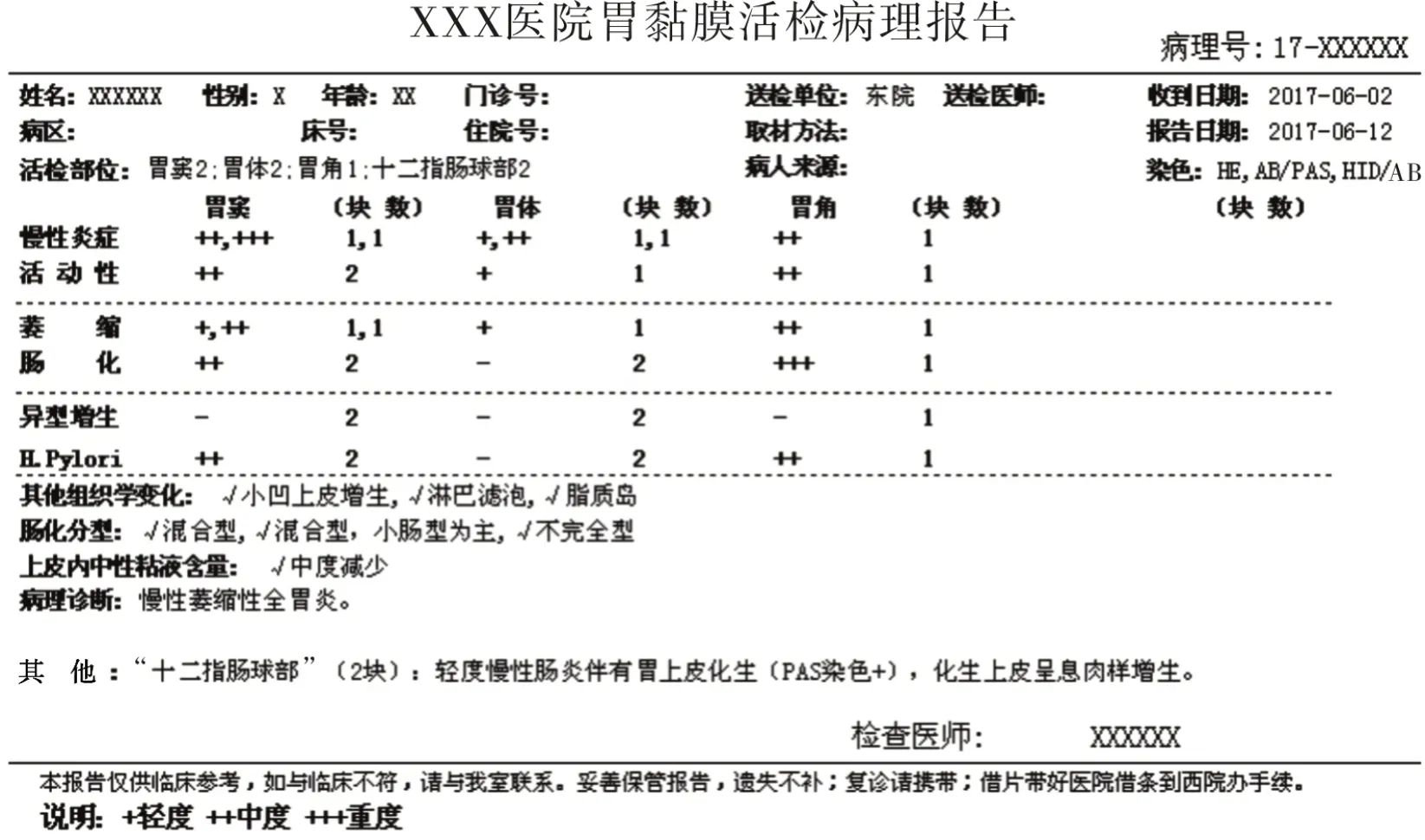
图5 表格式慢性胃炎病理报告
推荐意见5-4:慢性胃炎病理活检显示固有腺体减少,即可诊断为萎缩性胃炎,不必考虑活检标本的萎缩块数和程度。临床医师可根据病理结果并结合内镜表现,最后作出萎缩范围和程度的判断。
证据质量:中等;推荐强度:强推荐
早期胃黏膜萎缩呈灶性分布。即使活检标本数少,只要活检病理显示固有腺体减少,即可诊断为萎缩性胃炎。需要注意的是,任何引起黏膜损伤的病理过程均可能造成腺体数量减少,如取自糜烂或溃疡边缘的活检组织见腺体减少,不诊断为萎缩性胃炎;局限于胃小凹区域的肠化生不诊断为萎缩;黏膜层出现淋巴滤泡不诊断为萎缩,应观察其周围区域腺体情况判断是否为萎缩。此外,活检组织取材位置过浅(未达黏膜肌层)、组织包埋方向不当等因素均会影响萎缩情况的判断,不宜作出萎缩的病理诊断。
推荐意见5-5:肠化生范围和亚型对预测胃癌发生风险均有一定价值。
证据质量:中等;推荐强度:强推荐
研究强调应重视肠化生范围,范围越广,胃癌发生风险越高。通过AB-PAS 染色、HID-AB 染色等黏液染色区分肠化生分型对胃癌预测亦有积极意义,不完全型和(或)大肠型肠化生与胃癌发生的关系更为密切[102-104]。但从病理检查的实际情况来看,慢性胃炎的肠化生以混合型居多,不完全型和(或)大肠型肠化生的检出与活检标本数量密切相关,即存在取样误差问题。
推荐意见5-6:异型增生(上皮内瘤变)是最重要的胃癌前病变。有异型增生(上皮内瘤变)者,应注明程度,建议使用二级分类法,如低级别和高级别异型增生(或低级别和高级别上皮内瘤变)。
证据质量:高;推荐强度:强推荐
异型增生和上皮内瘤变大致为同义词,均属于胃癌前病变。上皮内瘤变是WHO 国际癌症研究机构推荐使用的术语[105]。不论是国际还是国内,关于术语的应用和译法意见尚不统一,建议病理医师同时使用异型增生和上皮内瘤变这2个术语[106]。关于上述概念,不同分类体系的情况总结于表4[107]。

表4 与胃癌发生相关的组织学表型分类标准
为合理界定胃肠道上皮瘤变(gastrointestinal epithelial neoplasia, GEN)的分类和分级,国际上先后召开了帕多瓦和维也纳国际共识会议,修订后的GEN 分类(维也纳分类)更贴近患者的临床处理,有利于患者的诊治,亦为WHO采纳[105,107]。
活检诊断受标本取材位置过浅或抽样误差所局限。最终诊断应以能显示GEN 完全侵及的范围或最严重级别的内镜或外科手术切除标本的检查结果为依据。
需要特别说明的是,胃癌的癌前情况包括癌前疾病(癌前状态)和癌前病变,前者包括慢性萎缩性胃炎伴或不伴肠化生,后者主要指异型增生或上皮内瘤变。WHO明确称胃黏膜异型增生(上皮内瘤变)为胃癌前病变,在叙述萎缩和肠化生时则仅认为是胃癌前情况(precursors of gastric neoplasms)[107]。尽管国外学者常将萎缩、肠化生和异型增生归为癌前病变[7,17],但国内的内科学教材和临床医师均认为胃癌前病变特指异型增生[108-109]。
推荐意见5-7:应重视贲门炎的诊断,必要时增加贲门部黏膜活检。
证据质量:中等;推荐强度:条件推荐
贲门炎是一种未受重视的慢性胃炎类型,与胃食管反流病、Barrett 食管等存在一定联系[110-111],今后需加强研究。如怀疑反流性食管炎合并贲门炎,宜增加贲门部黏膜活检。
推荐意见5-8:内镜下胃体腺区域活检对自身免疫性胃炎的早期诊断至关重要。
证据质量:中等;推荐强度:强推荐
AIG的主要病理变化发生于胃体腺黏膜的腺体分布区域,因此,内镜活检除在胃窦部钳取组织外,还须同时在胃体腺黏膜区域钳取组织。组织取材应足够深,推荐在胃体中部或胃底等明确的胃体腺黏膜区域钳取组织。
AIG 的组织病理学改变可分为早期、活动期和进展期三个阶段[61]。AIG 胃体腺黏膜的主要组织学特点如下。①炎症特点:胃体部黏膜炎症明显重于胃窦部黏膜,主要表现为淋巴细胞、浆细胞为主的慢性炎症细胞浸润的黏膜全层炎,且黏膜深层腺体区域炎症重于黏膜浅层。腺上皮内淋巴细胞浸润是相对明确的特征性表现[112]。②腺体萎缩和化生性改变:固有的胃体腺形态不典型或缺失,常出现假幽门腺化生,可伴有肠化生、胰腺腺泡化生。③神经内分泌细胞增生或神经内分泌肿瘤形成:腺上皮内出现不同程度的神经内分泌细胞增生(单纯性、线性、微结节样、腺瘤样、异型增生),直至神经内分泌肿瘤发生[113],必要时建议加做相关免疫组化染色证实。④胃内隆起病变或息肉:组织学形态多样,包括胃泌酸黏膜假性息肉、胃底腺息肉、胃增生性息肉(部分病例可伴有癌变)、幽门腺腺瘤、肠型腺瘤、神经内分泌肿瘤等[114-115]。胃窦部黏膜无炎症或炎症轻微,一般不伴有腺体萎缩,可见G 细胞增生,建议行免疫组化染色证实。如伴有Hp 现症或既往感染,胃窦部黏膜可出现萎缩和(或)肠化生[114]。此外,部分AIG 患者合并Hp 感染,此时胃体腺黏膜全层炎症均较严重,而胃窦部黏膜炎症以黏膜浅层最为严重。随着胃体腺黏膜腺体的消失,炎症明显减轻甚至近乎消退。值得注意的是,AIG 患者胃酸分泌较少,有时胃内其他细菌滋生,根除Hp后尿素呼气试验仍阳性可能是由其他细菌所致(Hp感染检测假阳性),此时应参考病理切片判断Hp 存在与否[116]。
推荐意见5-9:特殊类型胃炎的确诊需结合病因、临床表现,并依赖内镜和病理检查联合诊断。
证据质量:低;推荐强度:条件推荐
由于缺乏特异的临床表现,确诊特殊类型胃炎需结合病因、临床表现,并依赖内镜和病理检查联合诊断。巨大肥厚性胃炎内镜下表现为胃黏膜皱襞巨大扭曲,病理检查显示胃小凹上皮增生、腺体弯曲和囊性扩张、平滑肌增生、泌酸腺黏膜萎缩、壁细胞和主细胞明显减少[117]。嗜酸细胞性胃炎内镜下表现为黏膜红斑、糜烂、充血等,病理检查显示嗜酸性粒细胞浸润(>30个/HPF)和(或)外周血嗜酸性粒细胞增多;需排除消化道外疾病或寄生虫病的证据[118]。淋巴细胞性胃炎常累及胃体和胃窦,表现为伴或不伴黏膜隆起的糜烂、阿弗他溃疡等;病理检查黏膜固有层可见淋巴细胞和浆细胞浸润,每100个胃上皮细胞中上皮内淋巴细胞≥25个[119]。肉芽肿性胃炎在显微镜下表现为可累及胃体或胃窦全层的肉芽肿改变[65]。感染性胃炎因病原体不同,内镜和病理表现各异,部分内镜下可表现为结节、肿块、溃疡等,黏膜表面被覆脓性分泌物,少数显微镜下可见病原体微生物[120]。放射性胃炎在接受放射治疗后初期表现为弥漫性黏膜充血、水肿伴片状渗血,后续胃黏膜损伤逐渐加重,出现内皮增殖、血管炎、闭塞性动脉内膜炎等黏膜下血管性病变,毛细血管扩张、纤维化,甚至导致黏膜缺血、溃疡[121]。化学性胃炎病理检查显示胃小凹上皮增生、平滑肌纤维增生和炎症细胞稀少[122]。
6.临床问题6:慢性胃炎的实验室检查
推荐意见6-1:临床就诊的慢性胃炎患者,如幽门螺杆菌感染情况未知,均建议行幽门螺杆菌检测。
证据质量:高;推荐强度:强推荐
基于病因可将慢性胃炎分为Hp 胃炎和非Hp胃炎两大类,70%~90%的慢性胃炎为Hp 胃炎[17]。Hp胃炎一般无特异性临床表现,内镜检查观察胃黏膜未发现黏膜可见病变者不能排除Hp 胃炎。因此,对于慢性胃炎患者,进行Hp 检测有助于明确病因和进一步治疗[123]。
推荐意见6-2:幽门螺杆菌根除治疗后所有患者均应常规复查,评估根除治疗效果;最佳非侵入性评估方法为13C或14C-尿素呼气试验;评估应在治疗完成后至少4周进行。
证据质量:高;推荐强度:强推荐
推荐所有患者在根除治疗后行Hp 复查,多数患者根除治疗后无需复查胃镜,可采用非侵入性方法检测Hp,尿素呼气试验是复查的最佳选择,粪便抗原试验可作为备选[123]。应在根除治疗结束后至少4周进行复查,此期间服用抗菌药物、铋剂和某些具有抗菌作用的中药或质子泵抑制剂(proton pump inhibitor, PPI)会影响检测结果[124]。对于胃癌高风险人群,建议根除Hp治疗后定期随访检测Hp。
推荐意见6-3:自身免疫性胃炎应检测血清抗壁细胞抗体、抗内因子抗体和血清胃泌素以明确诊断,同时应检测甲状腺功能和相关抗体以除外相关合并疾病。
证据质量:高;推荐强度:强推荐
随着临床医师对胃神经内分泌肿瘤认识的提高,AIG 的诊断率不断提高。对于内镜下发现胃体黏膜萎缩,特别是伴有贫血的患者,需检测血清抗壁细胞抗体、抗内因子抗体以明确诊断[28]。由于AIG 导致叶酸、维生素B12吸收不良,并常合并自身免疫性甲状腺炎等自身免疫病,同时检测血红蛋白、血清铁、维生素B12、甲状腺功能和相关抗体有助于指导后续治疗。AIG 常合并其他疾病,1 型胃神经内分泌肿瘤常发生于AIG 基础之上,故应同时检测血清胃泌素(如总胃泌素或胃泌素-34)。有研究[125]表明AIG患者胃泌素-17(gastrin-17,G-17)呈升高趋势。另有研究[126]显示AIG 患者的血清嗜铬粒蛋白A 与胃泌素呈正相关,血清嗜铬粒蛋白A 与抗壁细胞抗体和抗内因子抗体联合检测可提高对AIG的预测效能。
7.临床问题7:慢性胃炎的治疗原则和策略
推荐意见7-1:慢性胃炎的治疗应尽可能针对病因,遵循个体化原则。治疗目的是祛除病因、缓解症状、改善胃黏膜炎症反应和预防并发症。
证据质量:中等;推荐强度:强推荐
慢性胃炎的治疗目的是祛除病因、缓解症状和改善胃黏膜组织学。慢性胃炎消化不良症状的处理与功能性消化不良相同。无症状、Hp阴性的慢性非萎缩性胃炎无需特殊治疗;但对于慢性萎缩性胃炎,特别是严重慢性萎缩性胃炎或伴有异型增生的患者应注意预防恶变。严重萎缩性胃炎可能与某些维生素(如维生素B12)和微量营养素(如铁、钙、镁、锌)等吸收障碍有关,可适当补充[127]。
巨大肥厚性胃炎缺乏有效治疗手段,目前的治疗经验主要是基于病例报道,包括抗菌药物[128]、糖皮质激素[129]、抑酸药物[130]等。也有报道提示长效生长抑素类药物可能对巨大肥厚性胃炎有效[131],并需纠正低蛋白血症、贫血等。对于嗜酸细胞性胃炎,需要寻找可能的过敏因素、去除过敏原,部分患者需糖皮质激素治疗[132]。感染性胃炎需应用恰当的抗菌药物治疗。
推荐意见7-2:饮食和生活方式的个体化调整是治疗慢性胃炎的合理建议。
证据质量:低;推荐强度:强推荐
虽然尚无明确证据显示某些饮食摄入与慢性胃炎症状的发生之间存在因果关系,亦缺乏饮食干预疗效的大型临床研究,但饮食习惯和生活方式的调整是慢性胃炎治疗的一部分。目前临床医师常建议患者尽量避免长期大量服用引起胃黏膜损伤的药物(如NSAID)和改善饮食、生活习惯(如避免过多饮用咖啡、大量饮酒和长期大量吸烟)[133]。慢性胃炎患者如主诉某种食物会使症状加重或好转,或饮食频率、进餐量会影响其症状,临床医师可建议其改变食物种类、饮食频率和进餐量[134]。
推荐意见7-3:伴胆汁反流的慢性胃炎可应用具有胆酸结合作用的胃黏膜保护剂,以及促胃肠动力药和(或)抑酸药物。
证据质量:中等;推荐强度:强推荐
胆汁反流是慢性胃炎的病因之一。幽门括约肌功能不全导致胆汁反流入胃,削弱或破坏胃黏膜屏障功能,胃黏膜在消化液的作用下产生炎症反应、糜烂、出血、上皮化生等病变。铝碳酸镁制剂可增强胃黏膜屏障并结合胆酸,从而减轻或消除胆汁反流所致的胃黏膜损伤[135]。促胃肠动力药如伊托必利、西尼必利、莫沙必利、多潘立酮等可防止或减少胆汁反流。一项小型对照研究[136]显示,PPI 在缓解胆汁反流性胃炎的消化不良症状和改善内镜和组织学表现方面有一定作用。必要时可酌情短期应用熊去氧胆酸制剂[137]。
推荐意见7-4:应重视非甾体抗炎药和(或)阿司匹林等药物对胃黏膜的损伤作用,对服用此类药物的患者应进行综合评估,以判断是否需停药,并加强抑酸和(或)胃黏膜保护治疗。
证据质量:高;推荐强度:强推荐
引起胃黏膜损伤的临床常用药物主要有抗血小板药物、NSAID 和(或)阿司匹林等。如出现药物相关胃黏膜损伤,首先应根据患者使用药物的治疗目的评估是否可停用该药物;对于必须长期服用上述药物者,应筛查Hp 并进行根除治疗,根据病情或症状严重程度选用PPI、H2受体拮抗剂(H2receptor antagonist,H2RA)或胃黏膜保护剂[138]。
多项病例对照研究和随机对照试验显示,PPI是预防和治疗NSAID 相关上消化道损伤的首选药物,效果优于H2RA 和胃黏膜保护剂[139-140]。然而有随机对照研究显示,PPI 可能增加NSAID 诱导的小肠损伤风险[141-142],必要时需注重全胃肠道黏膜保护。
对于服用缓释剂型NSAID 者,其胃肠道暴露于药物的时间进一步延长,这部分患者即使每日服用1 次PPI,在24 h 内仍有残余酸分泌,从而存在胃肠道损伤风险[143]。理论上,新型抑酸药钾离子竞争性酸阻滞剂(potassium-competitive acid blocker,PCAB)的持久抑酸作用有望更好地预防胃黏膜损伤[144]。2项随机、双盲、非劣效性研究继以单盲扩展研究分别观察了P-CAB 在长期服用低剂量阿司匹林和非阿司匹林NSAID 者中的疗效,发现其对预防NSAID 相关消化性溃疡复发有效且患者耐受性良好[145-146]。
推荐意见7-5:慢性胃炎患者可根据症状选择单独或联合应用以下药物。
①有胃黏膜糜烂和(或)以上腹痛、上腹部烧灼感等症状为主者,可根据病情或症状严重程度选用胃黏膜保护剂、抗酸剂、H2受体拮抗剂、质子泵抑制剂。
证据质量:高;推荐强度:强推荐
②以上腹饱胀、恶心、与进食相关的腹胀、纳差等为主要症状者,可考虑使用促胃肠动力药和(或)消化酶制剂。
证据质量:低;推荐强度:强推荐
③伴有明显精神心理因素的慢性胃炎患者可使用神经递质调节药物。
证据质量:高;推荐强度:强推荐
胃酸和(或)胃蛋白酶在胃黏膜糜烂(尤其是平坦糜烂)、上腹痛或上腹部烧灼感等症状的发生中起重要作用,抗酸或抑酸治疗对愈合糜烂和消除上述症状有效[147]。胃黏膜保护剂如吉法酯[148]、替普瑞酮[149]、铝碳酸镁制剂、瑞巴派特[150-151]、硫糖铝、聚普瑞锌等可改善胃黏膜屏障,促进胃黏膜糜烂愈合,但对症状改善的作用尚有争议。抗酸剂起效迅速但作用持续时间相对短暂,包括奥美拉唑[152]、艾司奥美拉唑[153]、雷贝拉唑[154]、兰索拉唑[155]、泮托拉唑、艾普拉唑[156]等在内的PPI 抑酸作用强而持久,可根据病情或症状严重程度选用。2022 年2 月25 日国家药品监督管理局对PPI类药品说明书的内容进行了统一修订,修订要求包括警惕长期抑酸治疗可能诱发的骨折、低镁血症、艰难梭菌相关性腹泻,以及药物间相互作用。PPI主要在肝脏经细胞色素P450(cytochrome P450,CYP)2C19、CYP3A4代谢,可能与其他药物发生相互作用,其中奥美拉唑的上述不良反应发生率最高;泮托拉唑和艾普拉唑与CYP2C19亲和力低[157],雷贝拉唑主要经非酶途径代谢,三者受CYP2C19 基因多态性影响较小。在慢性胃炎的治疗中,建议PPI的应用遵循个体化原则,对于长期服用PPI者应掌握适应证、有效性和患者依从性,全面评估风险与获益[158]。在一项多中心、前瞻性、单臂开放标签研究[159]中,10 311 例临床诊断为慢性胃炎且有症状的患者接受H2RA 法莫替丁20 mg/d 治疗4周,结果显示法莫替丁可明显缓解上腹痛、上腹饱胀和烧心症状。
上腹饱胀或恶心、呕吐的发生可能与胃排空迟缓有关,胃动力异常是慢性胃炎不可忽视的因素之一。一项系统综述和meta 分析表明,促胃肠动力药能显著减轻消化不良症状(RR=0.81,95%CI:0.74~0.89)[160]。该类药物包括多巴胺D2 受体拮抗剂(如甲氧氯普胺)、外周性多巴胺D2 受体拮抗剂(如多潘立酮)、选择性5-羟色胺4 受体激动剂(如莫沙必利)[161]、5-羟色胺4受体激动剂和多巴胺受体拮抗剂(如西尼必利)[162],以及有多巴胺D2 受体拮抗和乙酰胆碱酯酶抑制双重作用的伊托必利。一项随机、双盲、安慰剂对照研究[163]显示伊托必利可显著改善消化不良症状。2016 年功能性胃肠病罗马Ⅳ标准指出,伊托必利可有效缓解腹胀、早饱等症状且不良反应发生率低[164]。
此外,可针对与进食相关的中上腹饱胀、纳差等消化不良症状应用消化酶制剂,推荐患者于餐中服用,效果优于餐前和餐后服用,目的在于在进食的同时提供充足的消化酶,以帮助营养物质的消化,缓解相应症状。消化酶制剂种类较多,我国常用的消化酶制剂包括米曲菌胰酶片、复方阿嗪米特肠溶片、胰酶肠溶胶囊、复方消化酶胶囊等。
流行病学调查发现,精神心理因素与消化不良症状相关,尤其是焦虑症和抑郁症。抗抑郁或抗焦虑药物可作为伴有明显精神心理因素者,以及常规治疗无效或疗效较差者的补救治疗,包括三环类抗抑郁药、选择性5-羟色胺再摄取抑制剂、5-羟色胺-去甲肾上腺素再摄取抑制剂、5-羟色胺3 受体拮抗剂,以及小剂量多巴胺D2 受体拮抗剂氟哌噻吨与三环类抗抑郁药美利曲辛的复合制剂等[165-166]。必要时可由相应专科医师评估并协助诊治。
推荐意见7-6:中国传统医药可用于慢性胃炎的治疗。
证据质量:低;推荐强度:条件推荐
多种中药可缓解慢性胃炎的消化不良症状,甚至可能有助于改善胃黏膜病理状况,如摩罗丹[167]、羔羊胃提取物维B12胶囊[168]、胃复春等可用于萎缩性胃炎的治疗;荜铃胃痛颗粒[169]、甘海胃康胶囊[170]、养胃颗粒[171]对上腹痛、上腹饱胀均有一定缓解作用,可针对不同症状选择相应中药治疗。但中药的治疗效果目前尚缺乏国际公认的多中心、安慰剂对照、大样本、长期随访临床研究证据。
推荐意见7-7:证实幽门螺杆菌阳性的慢性胃炎,无论有无症状和并发症,均应进行幽门螺杆菌根除治疗,除非有抗衡因素存在。
证据质量:高;推荐强度:强推荐
几乎所有Hp 感染者(包括健康体检证实的无症状感染者)都存在不同程度的慢性活动性胃炎。根除Hp 后胃黏膜活动性炎症可消退,慢性炎症反应也有不同程度的减轻,其获益远大于可能的负面影响。因此,不论有无症状和(或)并发症,Hp 胃炎均属感染性疾病,均应进行Hp 根除治疗,除非有抗衡因素存在。抗衡因素包括患者伴存的某些疾病、社区高再感染率、卫生资源优先度安排等[17]。
此外,Hp感染诱发的炎症反应与胃黏膜萎缩和(或)肠化生的发生、发展密切相关[172]。根除Hp 可延缓或阻滞胃黏膜萎缩和(或)肠化生的发生、发展,并可使部分患者的胃黏膜萎缩甚至肠化生得到逆转,从而降低胃癌发生风险[173-174]。
推荐意见7-8:幽门螺杆菌胃炎的治疗采用我国2022 幽门螺杆菌感染治疗指南推荐的铋剂四联方案和高剂量双联方案。
证据质量:高;推荐强度:强推荐
我国2022 Hp 感染治疗指南[175]推荐的Hp 根除方案为铋剂四联方案:PPI+铋剂+2种抗菌药物。这一方案目前在临床上广泛应用,并受到国际权威共识推荐[176]。推荐经验性铋剂四联方案的疗程为14 d,除非当地研究证实10 d 疗程有效(根除率>90%)。
常用的根除Hp 抗菌药物中,甲硝唑、克拉霉素、左氧氟沙星耐药率较高,阿莫西林、呋喃唑酮、四环素耐药率相对较低。根除方案中抗菌药物组合的选择应参考当地人群的Hp 耐药率和个人抗菌药物应用史。
抑酸剂在Hp 根除方案中起重要作用,选择作用稳定、疗效高、受CYP2C19 基因多态性影响较小的PPI,可提高Hp 根除率[176]。新一代抑制胃酸药物P-CAB 具有更强效、更持久的抑酸作用,且不受宿主药物代谢基因多态性影响,有助于进一步提高Hp根除率[177]。
此外,近年有研究表明高剂量双联方案与铋剂四联方案疗效相当,且不良反应少,可作为经验性一线治疗方案[178]。
8. 临床问题8:慢性萎缩性胃炎的转归及其影响因素和癌变预防
推荐意见8-1:慢性胃炎特别是慢性萎缩性胃炎的进展和演变受遗传因素、幽门螺杆菌感染情况以及饮食状况、生活习惯、年龄等因素影响;伴有异型增生者的胃癌发生风险有不同程度的增加。另外,可用“胃龄”反映胃黏膜细胞的衰老状况。
证据质量:高;推荐强度:强推荐
反复或持续Hp 感染、不良饮食习惯等均为胃黏膜萎缩和肠化生加重的潜在因素[179]。饮食和生活方式是影响慢性胃炎特别是慢性萎缩性胃炎进展和演变的重要因素。水土中含有过多硝酸盐、微量元素比例失调、吸烟、长期饮酒、新鲜蔬菜和水果摄入不足、必需营养素缺乏、经常食用霉变、腌制、熏烤、油炸等快餐食物、过多摄入食盐,以及有胃癌家族史,均可增加慢性萎缩性胃炎的发生风险或加重慢性萎缩性胃炎甚至增加癌变风险[180-181]。2018年美国癌症研究所和世界癌症研究基金会更新了《饮食、营养、体育锻炼与胃癌》全球报告,指出增加胃癌发生风险的因素包括肥胖、饮酒、高盐饮食、过多食用加工肉类、烤肉、烤鱼,以及低水果摄入等,而多食用柑橘类水果可降低胃癌发生风险[182]。一项全基因组关联研究的meta 分析和前瞻性队列研究[183]结果显示,坚持良好的生活方式(不吸烟、不饮酒、少吃腌制食品、经常食用新鲜水果和蔬菜),即使患者具有高胃癌遗传风险,胃癌发生风险亦可降低47%。
慢性萎缩性胃炎常合并肠化生,少数出现异型增生,经历长期演变,其中少数病例可发展为胃癌[17,184-185]。大部分低级别异型增生可逆转,较少发展为胃癌[186-187]。国外研究显示高级别异型增生患者在4~48 个月的随访期内癌变率为60%~85%,诊断后5年内年癌变率为6%[188-189];而低级别异型增生患者随访12 个月以上的癌变率为33%[190]。我国情况是否与之相符,尚有待探讨。
多数慢性萎缩性胃炎患者病情较稳定,特别是不伴有Hp 持续感染者。某些患者随着年龄增长,会因衰老而出现萎缩等组织病理学改变[191]。必须认识到无论在任何年龄段,持续Hp 感染均有可能导致慢性萎缩性胃炎[192]。
同年龄个体的胃黏膜衰老程度不尽相同,即可能有不同的胃龄,可依据胃黏膜细胞端粒长度测定和计算胃龄[191]。胃龄与实际年龄差异较大者,可能更需要密切随访。
推荐意见8-2:OLGA 和OLGIM 分期能反映慢性胃炎患者的胃黏膜萎缩、肠化生程度和范围,能用于胃癌风险分层,是制订个体化胃镜监测计划的可靠依据。
证据质量:高;推荐强度:强推荐
2005 年国际萎缩研究小组提出了胃黏膜炎症反应、萎缩程度及其范围的分级、分期标准,即慢性胃炎的萎缩分级、分期标准OLGA 分期(表5)[193],基于胃炎新悉尼系统对炎症和萎缩程度的半定量评分方法,采用胃炎分期代表胃黏膜萎缩范围和程度,将慢性胃炎的组织病理学与癌变风险联系起来,可为临床医师预测病变进展和制订疾病管理措施提供更为直观的信息。Rugge 等[194]对93 例慢性胃炎患者的长期(>12 年)随访研究发现,绝大部分OLGA 0~Ⅱ期患者胃炎分期维持不变,癌变均发生于OLGA Ⅲ、Ⅳ期患者中。该团队的另一项研究[195]纳入7 436 例慢性胃炎患者,入组时接受胃镜检查,平均随访6.3 年,分析显示入组时OLGA 0、Ⅰ、Ⅱ、Ⅲ、Ⅳ期患者的肿瘤性病变(LGIN、HGIN 和胃癌)发生率分别为0.03/1 000 人年、0.34/1 000 人年、1.48/1 000 人年、19.1/1 000 人年和41.2/1 000 人年,多因素分析显示OLGA分期是肿瘤性病变发生的唯一预测因素(OLGA Ⅲ期,HR=712.4; OLGA Ⅳ期,HR=1 450.7),表明OLGA分期与胃肿瘤发生风险显著相关。同一团队以1 755 例因消化不良症状接受胃镜检查者为研究对象的前瞻性队列研究[196]中,中位随访时间为55 个月,上皮肿瘤(LGIN、HGIN 和胃癌)患病率为0.4%,均发生于初始胃镜检查OLGA Ⅲ、Ⅳ期患者中,OLGA 0、Ⅰ、Ⅱ期患者上皮肿瘤发生率为0(95%CI: 0~0.4),OLGA Ⅲ、Ⅳ期患者分别为36.5/1 000 人年(95%CI:13.7/1 000 人年~97.4/1 000人年)和63.1/1 000 人年(95%CI: 20.3/1 000 人年~195.6/1 000人年),进一步证实了OLGA 分期对胃上皮肿瘤具有风险分层作用。国内研究[197]也证实高OLGA分期患者更易检出早期胃癌,OLGA分期能有效地根据胃癌风险程度对胃炎患者进行风险分层。
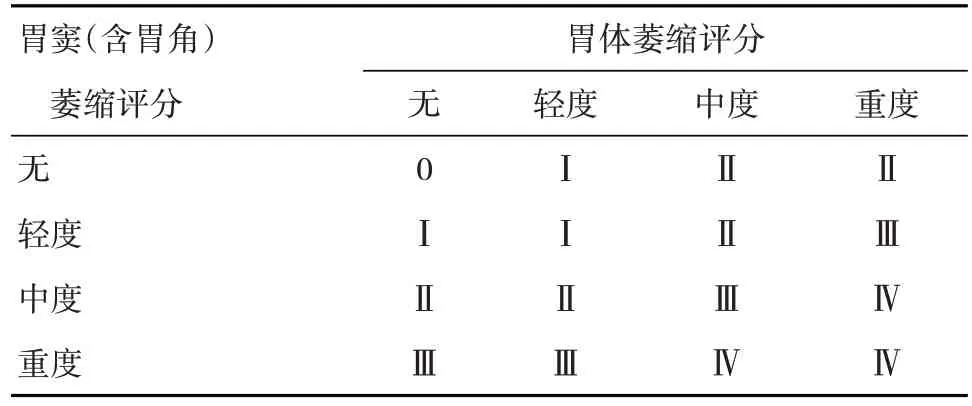
表5 慢性胃炎萎缩分级、分期标准(OLGA分期)
由于萎缩判断的观察者间一致性相对较低,又提出了慢性胃炎的肠化生分级、分期标准OLGIM 分期(表6)[198]。与OLGA 分期相比,OLGIM 分期有着较高的观察者间一致性,但可能遗漏一些潜在的胃癌高危个体[199]。研究[200]显示,在行OLGA 和OLGIM分期的病例中,约0.2% OLGIM 分期较OLGA 分期下调;在按OLGA 分期界定为高危的病例中,<1/10的病例被OLGIM 分期界定为低危,因此,OLGIM 分期为低危不可等同于胃癌发生风险低危。新加坡一项前瞻性、多中心研究[201]显示,OLGIM Ⅲ、Ⅳ期患者有着更高的早期胃肿瘤发生风险(调整HR=20.7,95%CI:5.04~85.6),50%以上由OLGIM Ⅲ、Ⅳ期进展为早期胃肿瘤的患者系于确诊OLGIM Ⅲ、Ⅳ期2年内发生;OLGIM Ⅱ期患者也有一定早期胃肿瘤发生风险(调整HR=7.34, 95%CI: 1.60~33.7),由此建议胃癌风险分层为高危(OLGIM Ⅲ、Ⅳ期)和中危(OLGIM Ⅱ期)的患者胃镜监测间期分别定为2 年和5 年。一项纳入6 项病例对照研究和2 项队列研究、共2 700 例受检者的meta 分析显示,OLGA/OLGIM分期越高(Ⅲ、Ⅳ期),胃癌发生风险越大[202]。

表6 慢性胃炎肠化生分级、分期标准(OLGIM分期)
因此,OLGA 和OLGIM 分期系统可反映萎缩性胃炎的严重程度和癌变风险,能识别胃癌高危患者(OLGA/OLGIM Ⅲ、Ⅳ期),有助于胃癌的早期诊断和预防,是制订个体化胃镜监测策略的可靠指标。在临床实践中,推荐联合使用OLGA 和OLGIM 分期,从而更精确地预测胃癌发生风险。
推荐意见8-3:血清胃蛋白酶原Ⅰ、Ⅱ和胃泌素-17的检测有助于判断胃黏膜萎缩和萎缩部位,是筛查萎缩性胃炎的非侵入性方法。
证据质量:中等;推荐强度:强推荐
胃蛋白酶原(pepsinogen, PG)水平能反映黏膜分泌功能状态,是判断胃黏膜广泛萎缩的标志物,可作为萎缩性胃炎筛查的非侵入性方法[17,176]。胃黏膜萎缩时,PGⅠ、PGⅡ水平下降,PGⅠ下降更为显著,因此PGⅠ/PGⅡ比值(PGⅠ/PGⅡratio,PGR)随之降低。PG测定有助于判断萎缩范围,胃体萎缩者PGⅠ和PGR 降低,血清G-17 水平升高;胃窦萎缩者血清G-17 水平降低,PGⅠ和PGR 在正常参考值范围内;全胃萎缩者血清G-17、PGⅠ和PGR 均降低。一项纳入31项研究(包括2 265例萎缩性胃炎患者)的meta 分析评价了血清PG 对萎缩性胃炎的诊断效能,结果显示敏感性和特异性分别为69%(95%CI:55%~80%)和88%(95%CI: 77%~94%),证明血清PG 检测可作为萎缩性胃炎非侵入性诊断手段;PGⅠ与PGR 联合筛查的敏感性高于两者单独使用(79%对46%和69%),特异性高于单独使用PGR(89%对84%),但略低于单独使用PGⅠ(89%对93%)[203]。另一项评价血清PG 检测对慢性萎缩性胃炎预测效能的meta 分析共纳入14 项研究,以PGⅠ≤70 μg/L且PGR≤3为最佳临界值,诊断慢性萎缩性胃炎的敏感性、特异性、诊断OR值和AUC 分别为59%、89%、12 和0.81;如单独以PGR≤3 为最佳临界值,则相应数据分别为50%、94%、15 和0.85[204]。上述meta 分析结果提示了血清PG 检测筛查萎缩性胃炎的潜能,具有特异性高、非侵入性的优点。但是纳入分析的文献存在异质性,结果受患者种族和文献质量影响。虽然多数研究采用PGⅠ≤70 μg/L且PGR≤3作为筛查萎缩性胃炎的临界值,但因检测试剂和方法不同,临界值也存在差异,在应用PG 筛查萎缩性胃炎前应先对试验进行验证。国内推荐在胃癌高发区采用PGⅠ≤70 μg/L 且PGR≤7 的筛查标准[205]。
关于血清G-17 诊断慢性萎缩性胃炎的meta 分析显示,其敏感性、特异性分别为48%(95%CI:45%~51%)和79%(95%CI: 77%~81%),提示单独应用G-17诊断或筛查萎缩性胃炎并不合适,进一步的分析显示其对亚洲人群的诊断准确性低于非亚洲人群[206]。一项纳入行胃镜检查者的前瞻性研究[207]显示,G-17、PGⅠ和PGR 对自身免疫性萎缩性胃炎的诊断价值(AUC 分别为0.83、0.95 和0.97)优于Hp 相关性萎缩性胃炎(AUC 分别为0.62、0.75和0.67)。
推荐意见8-4:血清胃蛋白酶原Ⅰ、Ⅱ、胃蛋白酶原Ⅰ/Ⅱ比值联合抗幽门螺杆菌抗体检测有助于胃癌风险分层和筛查。
证据质量:高;推荐强度:强推荐
多项研究证实血清PG 检测有助于胃癌高危人群的风险分层,PG检测诊断为萎缩者,以及PG检测虽诊断为萎缩阴性但PGR 较低者,均有较高的胃癌发生风险,应进一步行胃镜检查[208-209]。根据血清PG 联合血清抗Hp 抗体检测结果可将人群分为A(PG 在正常参考值范围内、抗Hp 抗体阴性)、B(PG在正常参考值范围内、抗Hp 抗体阳性)、C(PG 降低、抗Hp 抗体阳性)、D(PG 降低、抗Hp 抗体阴性)四组,各组胃癌发生率不同,这是一个有价值的胃癌风险预测指标,可据此进行胃癌风险分层(ABCD法)[210]。此外,还可联合PG、G-17 与抗Hp 抗体对胃癌风险加以分层,辨识出高危个体进行胃镜检查[211]。国内一项多中心、横断面研究[212]建立了包括年龄、性别、PGR、G-17、抗Hp 抗体等七项指标的胃癌评分系统并对其进行验证,结果显示该模型具有较高的胃癌风险分层价值(AUC=0.76),可用于我国胃癌高危人群的胃癌风险筛查。一项大样本血清学筛查研究[213]比较了上述几种胃癌风险模型在我国胃癌高危人群中的筛查效能,结果显示各个模型均可对胃癌风险进行有效分层,其中胃癌评分系统风险分层效果最佳,低危、中危、高危组胃癌检出率分别为0.53%、1.30%和5.01%。
PGR 与OLGA 分期呈负相关,PGR 越低,OLGA分期越高[194,214],采用PGR≤3 可区分OLGA 低危(0、Ⅰ期)与高危(Ⅲ、Ⅳ期)患者,敏感性和特异性分别为77%和85%,阳性预测值为45%,阴性预测值高达96%[194]。需注意Hp 感染对检测结果的影响,Hp感染可致PGⅠ、PGⅡ水平升高,PGⅡ水平升高更为显著,由此导致PGR 下降。Hp 根除后则表现为PGⅠ、PGⅡ水平下降,PGR上升。
推荐意见8-5:根除幽门螺杆菌可减缓炎症反应向萎缩、肠化生甚至异型增生发展的进程并降低胃癌发生率,但最佳干预时间为胃癌前变化(萎缩、肠化生和异型增生)发生前。
证据质量:高;推荐强度:强推荐
较多研究发现,Hp感染有促进慢性萎缩性胃炎发展为胃癌的作用[215]。根除Hp 可明显减缓癌前病变的进展,并可能降低胃癌发生风险[216-220]。Hp 根除治疗对胃癌的预防作用可持续至根除后22年,且可降低胃癌病死率[221]。Hp 根除对内镜下切除胃癌病灶后的异时性胃癌同样具有预防作用[222]。Hp 胃炎京都全球共识意见倡导根除Hp预防胃癌[17]。
一项根除Hp 后随访15 年的研究[223]显示,Hp 根除治疗组(1 130例)和安慰剂组(1 128例)胃癌发生率分别为3.0%和4.7%。Hp 根除后的随访时间越长,越能显示出根除治疗的胃癌预防效果,即使根除Hp 时病变已进入肠化生或异型增生阶段,仍有较好的癌变预防作用[222]。有研究[224]评估了根除Hp在有胃癌家族史者中的胃癌预防效果,研究纳入1 676 例一级亲属有胃癌史的Hp 感染者,随机接受Hp 根除治疗或安慰剂治疗,结果证明根除Hp 可降低胃癌发生风险。
一项大规模长期人群Hp 筛查和根除研究[225]显示,筛查和根除策略实施14年后,当地Hp流行率由64.2%降至15.0%,再感染率<1%/人年;萎缩性胃炎和肠化生及其严重程度亦随时间推移而减少和降低;根除Hp 化学预防降低胃癌发病率的有效性为53%(95%CI:30%~69%,P<0.001)。
根除Hp 对于轻度慢性萎缩性胃炎癌变有较好的预防作用,并有益于癌前病变组织学好转[226]。Hp根除后,胃黏膜组织环氧合酶-2(cyclooxygenase-2,COX-2)表达和Ki-67 增殖指数均显著下降,前列腺素E2表达亦下调[227]。相关系统综述和meta 分析显示,与欧美国家相比,中国等东亚国家通过根除Hp预防胃癌更符合卫生经济学标准[228]。
推荐意见8-6:某些维生素等可能有助于延缓萎缩性胃炎的进程,从而降低胃癌风险。
证据质量:中等;推荐强度:条件推荐
某些维生素[218,221,229]、微量元素硒[230]、大蒜素可能降低胃癌发病率和发生风险。对于部分低叶酸者,适量(≥1 mg/d)补充叶酸可改善慢性萎缩性胃炎的组织病理学状态而减少胃癌发生[231-232]。一项病例对照研究[233]提示低维生素B12水平可增加非贲门部胃腺癌发生风险。
9. 临床问题9:国内外有关萎缩性胃炎的争议问题
推荐意见9-1:胃黏膜肠化生可在一定程度上被逆转。
证据质量:中等;推荐强度:条件推荐
已有多项研究通过长期随访发现肠化生可在一定程度上被逆转[174,234-236]。研究显示肠化生逆转的总体组织学改善累积风险在随访1、3、5年时波动于19.4%~29.7%之间[237]。肠化生可能存在自发性逆转。一项随访队列研究[238]纳入1 422 名自愿接受活检随访的哥伦比亚胃癌高风险地区居民,随访时间长达3~16年(平均5.1年),年龄≤40岁和>40岁人群的肠化生自发性逆转率分别为5.4/100 人年和3.7/100人年。根除Hp也可能逆转肠化生。2018年发表的一项随访时间长达10 年的前瞻性研究[174]发现,Hp 根除患者胃窦和胃体肠化生逆转率分别为33.9%和44.4%。2021 年发表的一项针对西班牙裔胃癌前病变患者的随访队列研究[234]中,患者随机接受Hp根除或安慰剂治疗,随访时间长达20年,分析显示肠化生逆转率为20%,与萎缩性胃炎的逆转率相近。一些药物干预也显示出对肠化生的逆转作用,如塞来昔布、维生素、摩罗丹等[167,239-241]。
推荐意见9-2:有胃癌前疾病并因心脑血管疾病等基础疾病需长期服用阿司匹林的患者,每日服用低剂量阿司匹林可能有助于降低胃癌发生风险。
证据质量:低;推荐强度:条件推荐
近年来,多项meta 分析结果提示了阿司匹林对胃癌的预防作用[242-243]。然而,绝大多数研究未纳入胃癌前病变患者。2021 年一项评估阿司匹林对常见癌症风险作用的系统综述和meta 分析共纳入11项关于阿司匹林与胃癌发生风险的研究(10 项队列研究,14 933 例胃癌,样本量2 378 794;1 项随机对照试验,46 例胃癌,样本量6 076),对队列研究的meta 分析显示规律服用阿司匹林者胃癌发生风险总体降低33%(RR=0.67, 95%CI: 0.52~0.87,P=0.003),这些研究的异质性很高,但未发现明显偏倚[244]。进一步的亚组分析显示,长期(≥5年)服用阿司匹林可降低胃癌发生风险(3 项研究,RR=0.60,95%CI:0.38~0.94,P=0.027),但每日服用阿司匹林与胃癌发生风险无相关性(2 项研究,RR=0.79,95%CI: 0.53~1.18,P=0.251)。随机对照试验的meta 分析结果显示服用阿司匹林与胃癌发生风险无明显相关性(RR=1.01, 95%CI: 0.54~1.86,P=0.990)。剂量-效应分析显示阿司匹林服用剂量与胃癌发生风险之间无明显关联(R2<0.001,P=0.948)。
然而,阿司匹林可能会导致严重不良反应。一项关于常规剂量阿司匹林一级预防心血管事件的研究[245]显示,尽管治疗相关不良事件的总体发生率较低,但阿司匹林治疗组仍显著高于安慰剂组(16.75%对13.54%,P<0.000 1);最常报告的治疗相关不良事件(发生率≥1.0%)为消化不良(3.60%对3.14%)、鼻出血(1.85%对0.89%)、胃食管反流病(1.12%对0.96%)和上腹痛(1.08%对0.92%),药物相关胃肠出血少见,且更常见于阿司匹林治疗组(0.24%对0.03%,P<0.001)。
综合考虑阿司匹林对胃癌的预防效应和药物相关不良反应,不推荐阿司匹林常规用于胃癌预防。但低剂量阿司匹林具有更好的安全性和更广泛的获益,在降低心血管疾病死亡风险的同时,也降低了多种肿瘤的发生风险[244]。因此,可考虑推荐合并某些可能从阿司匹林治疗中获益的基础疾病的患者使用低剂量阿司匹林预防胃癌。
推荐意见9-3:尽管环氧合酶-2 抑制剂可能降低胃癌或癌前病变的进展风险,但不推荐其用于胃癌或癌前病变的预防。
证据质量:低;推荐强度:条件推荐
近年来一些meta 分析显示,使用COX-2 抑制剂的患者罹患胃癌或癌前病变的风险降低,但针对相关问题的研究较少,且绝大多数研究证据质量不高[243,246]。2012 年发表的一项随机、双盲、安慰剂对照试验纳入1 024 例Hp 阳性胃癌前病变患者接受Hp 根除或安慰剂治疗,其中919 例患者后续再接受塞来昔布或安慰剂治疗,结果显示Hp 根除治疗组(59.3%对41.2%,OR=2.19, 95%CI: 1.32~3.64)和塞来昔布治疗组(52.8%对41.2%,OR=1.72, 95%CI:1.07~2.76)患者病变改善率均显著高于安慰剂组,但未观察到根除Hp 继以塞来昔布对进展期癌前病变的治疗优势[241]。2013年发表的一项前瞻性、非随机对照研究[239]发现,根除Hp 后肠化生仍持续存在的患者使用塞来昔布治疗1 年,肠化生改善率高于未使用塞来昔布治疗者(44.3%对14.3%,P<0.001)。相关meta 分析共纳入5 项关于COX-2 抑制剂与胃癌发生风险的研究(3 项病例对照研究,1 项队列研究,1 项随机对照试验),结果显示COX-2 抑制剂可降低胃癌发生风险(RR=0.45, 95%CI: 0.29~0.70);剂量-效应分析显示,COX-2 抑制剂剂量为200 mg/d时降低胃癌发生风险效果显著(RR=0.50, 95%CI:0.30~0.84)[243]。
COX-2 抑制剂可能引起心血管(高血压、心力衰竭等)、消化道(腹痛、消化不良、烧心等)、肾脏等器官系统不良事件[247-248]。一项评估COX-2 抑制剂治疗骨关节炎安全性的系统综述和meta 分析显示,与安慰剂相比,COX-2 抑制剂的药物相关不良事件发生风险显著增加(RR=1.26, 95%CI: 1.09~1.46),其中上消化道并发症(消化不良、胃炎、烧心)风险增加19%(RR=1.19, 95%CI: 1.03~1.38),尤其是腹痛风险增加达40%(RR=1.40, 95%CI: 1.08~1.80);高血压风险总体增加45%(RR=1.45, 95%CI: 1.01~2.10),然而剔除罗非昔布后分析显示COX-2抑制剂不再增加高血压发生风险(RR=1.21,95%CI:0.80~1.83);心力衰竭和水肿风险总体增加近70%(RR=1.68,95%CI:1.22~2.31),剔除罗非昔布后结果不变(RR=1.67,95%CI:1.21~2.29)[247]。
基于上述研究结果,同时考虑COX-2 抑制剂可能引起的不良反应,不推荐常规应用COX-2 抑制剂预防胃癌或胃癌前病变。
三、待解决的临床问题
1. 关于萎缩性胃炎的实验室检查和癌变风险分析:①胃癌相关抗原MG7水平可能有助于慢性萎缩性胃炎的癌变风险分层。G-17 联合PG(详见前述“推荐意见8-3”)、抗Hp 抗体判断胃窦黏膜萎缩已有报道[249]。MG7 抗体在慢性萎缩性胃炎、肠化生、异型增生和胃癌组织中的表达逐渐升高,血液中也可检测到MG7抗体,有望作为提示慢性萎缩性胃炎癌变的血清学标志物[250]。②胃饥饿素(ghrelin)作为一种生长激素释放肽,也与胃黏膜萎缩有一定相关性。研究[251]显示Hp 感染相关胃黏膜慢性炎症和萎缩改变可能影响胃饥饿素的生物合成,导致其循环水平降低。另一项研究[252]证实,无论有无Hp感染,血浆酰化胃饥饿素水平均随胃黏膜萎缩范围的扩大而下降。根除Hp 48 周后,血浆胃饥饿素水平与内镜下胃黏膜萎缩程度仍有良好的相关性[253]。有研究[254]观察到抗壁细胞抗体阳性AIG 患者的血浆胃饥饿素水平低于抗壁细胞抗体阴性的AIG 患者。③粪便链球菌丰度与萎缩性胃炎的严重程度和进展过程密切相关,是有潜力的反映萎缩性胃炎进展的生物学标志物。对日本Hp 感染相关萎缩性胃炎患者肠道菌群的研究[255]发现,重度萎缩性胃炎患者粪便菌群中链球菌显著富集。国内一项研究[256]发现粪便咽峡炎链球菌和星座链球菌丰度在非萎缩性胃炎、萎缩性胃炎、萎缩性胃炎伴肠化生、伴异型增生和胃癌患者中依次递增,为慢性萎缩性胃炎的非血清学检测提供了思路。此外,对口腔菌群的研究[257]证实,消化链球菌、链球菌、细小单胞菌、普雷沃菌、罗氏菌、颗粒链球菌与胃黏膜萎缩和肠化生的发生和持续存在密切相关。
2.是否所有萎缩性胃炎均应行活检,内镜下分期能否替代病理分期用于预测胃癌风险:内镜下木村-竹本分型与OLGIM 分期预测胃癌的效能相似,某些情况下内镜下分期可代替病理分期。一项来自日本的多中心(10 个机构)、观察性、前瞻性研究[258]应用多种内镜和病理评分系统对115例胃癌患者和265 例非胃癌患者进行胃癌风险分层,比较不同评分系统与胃癌风险之间相关性的强度。多因素分析显示,OLGIM Ⅲ、Ⅳ期(OR=2.8,95%CI:1.5~5.3,P=0.002)和木村-竹本分型开放型(OR=2.5,95%CI: 1.4~4.5,P=0. 003)与胃癌风险之间存在强相关性,OLGA Ⅲ、Ⅳ期与胃癌风险则无相关性(OR=0.6,95%CI:0.3~1.1,P=0.091)。
因上述研究纳入病例数较少,且为观察性研究,其结果尚待验证。综合考虑,本指南推荐,在某些情况下,如患者存在活检禁忌证、胃镜下无可见病灶、无胃癌家族史或无报警症状,可采用内镜下木村-竹本分型代替OLGA、OLGIM 分期进行胃癌风险分层。
附录:慢性胃炎的病理诊断标准
一、活检取材
活检取材标本数和部位由内镜医师根据需要决定,一般为2~5 块。如取5 块,则胃窦2 块组织取自距幽门2~3 cm 处的小弯和大弯,胃体2 块组织取自距胃角近侧4 cm 处的小弯和距贲门8 cm 处的胃体大弯中部,胃角取1块。
标本应足够大,取材深度须达到黏膜肌层,对可能或肯定存在的病灶要单独取标本。不同部位的标本须分开装瓶,并向病理科提供取材部位、内镜所见和简要病史。
二、组织学分级标准
5种组织学变化(Hp、活动性、慢性炎症反应、萎缩和肠化生)分为无(0)、轻度(+)、中度(++)和重度(+++)四级。分级方法采用下述标准,与新悉尼系统的直观模拟评分法并用,病理检查需报告每块活检标本的组织学变化。
1.Hp:观察胃黏膜黏液层、表面上皮、小凹上皮和腺管上皮表面的Hp 分布情况。无:特殊染色未见Hp。轻度:偶见或小于标本全长1/3 有少数Hp。中度:Hp 分布范围超过标本全长的1/3 而未达2/3或连续性、薄而稀疏地存在于上皮表面。重度:Hp成堆存在,基本分布于标本全长。肠化生黏膜表面通常无Hp定植,宜在非肠化生处寻找。
对炎症反应明显而HE 染色未发现Hp 的标本,应通过特殊染色仔细寻找,推荐使用较简便的Giemsa 染色,也可使用各病理室惯用的染色方法,有条件的单位可行免疫组化染色。
2.活动性:慢性炎症反应背景上有中性粒细胞浸润。轻度:黏膜固有层有少数中性粒细胞浸润。中度:中性粒细胞较多存在于黏膜层,可见于表面上皮细胞、小凹上皮细胞或腺管上皮内。重度:中性粒细胞较密集,或除中度所见外,还可见小凹脓肿。
3.慢性炎症反应:根据黏膜层慢性炎症细胞的密集程度和浸润深度分级,以前者为主。正常:单个核细胞数<5个/HPF,如数量略超过正常而内镜下无明显异常,病理可诊断为基本正常。轻度:慢性炎症细胞较少并局限于黏膜浅层,分布范围<黏膜层的1/3。中度:慢性炎症细胞较密集,分布范围<黏膜层的2/3。重度:慢性炎症细胞密集,占据黏膜全层。计算密集程度时应避开淋巴滤泡及其周围的小淋巴细胞区。
4. 萎缩:萎缩指胃固有腺体减少,分为2 种类型。①化生性萎缩:胃固有腺体被肠化生或假幽门腺化生腺体替代。②非化生性萎缩:胃固有腺体被纤维或纤维肌性组织替代,或炎症细胞浸润引起固有腺体数量减少。
萎缩程度以胃固有腺体每减少1/3 为一等级计算。轻度:固有腺体减少数<原有腺体的1/3。中度:固有腺体减少数为原有腺体的1/3~2/3。重度:固有腺体减少数>原有腺体的2/3,仅残留少数腺体,甚至完全消失。局限于胃小凹区域的肠化生不属于萎缩。黏膜层出现淋巴滤泡不属于萎缩,应根据周围区域的腺体情况判断。任何引起黏膜损伤的病理过程均可造成腺体数量减少,如溃疡边缘取材,不一定就是萎缩性胃炎。
取材过浅未达黏膜肌层的标本,可参考黏膜层腺体大小、密度和间质反应情况推断是否存在萎缩,同时加注取材过浅的注释,提醒临床仅供参考。
5.肠化生:肠化生区占腺体和表面上皮总面积<1/3 为轻度肠化生,1/3~2/3 为中度肠化生,>2/3 为重度肠化生。AB-PAS 染色对不明显肠化生的诊断很有帮助。以AB-PAS 染色和HID-AB 染色区分肠化生亚型预测胃癌发生风险的价值仍有争议。
6.其他组织学特征:出现不需要分级的组织学变化时需注明。这类组织学特征分为非特异性和特异性两类,前者包括淋巴滤泡、小凹上皮增生、胰腺化生、假幽门腺化生等;后者包括肉芽肿、集簇性嗜酸性粒细胞浸润、明显上皮内淋巴细胞浸润、特异性病原体等。假幽门腺化生是泌酸腺萎缩的相关表现,诊断时需核实取材部位,如胃角部活检见黏液分泌腺不能诊断为假幽门腺化生,只有出现肠化生才是诊断萎缩的标志。
有异型增生(上皮内瘤变)时应注明,分为低级别和高级别异型增生(或LGIN和HGIN)。
三、慢性胃炎的分类和病理诊断
慢性胃炎分为慢性非萎缩性胃炎和慢性萎缩性胃炎两类;按照病变部位分为胃窦为主胃炎、胃体为主胃炎和全胃炎。有少部分为特殊类型胃炎,如化学性胃炎、淋巴细胞性胃炎、肉芽肿性胃炎、嗜酸细胞性胃炎、胶原性胃炎、放射性胃炎、感染性(细菌、病毒、霉菌、寄生虫)胃炎和巨大肥厚性胃炎。
诊断应包括部位分布特征和组织学变化程度,有病因可循的要报告病因。胃窦和胃体炎症程度相差2级或以上时,加上“为主”修饰词,如“慢性(活动性)胃炎,胃窦为主”。
萎缩性胃炎的诊断标准:慢性胃炎活检病理显示固有层腺体萎缩即可诊断萎缩性胃炎,不必考虑活检标本的萎缩块数和程度。临床医师可根据病理结果结合内镜所见,作出萎缩范围和程度的最终判断。
利益冲突:专家组所有成员声明不存在利益冲突
执笔撰写者(按撰写内容排序):房静远(上海交通大学医学院附属仁济医院消化内科),杜奕奇[海军军医大学第一附属医院(上海长海医院)消化内科],刘文忠(上海交通大学医学院附属仁济医院消化内科),肖英莲(中山大学附属第一医院消化内科),陈卫昌(苏州大学附属第一医院消化内科),任建林(厦门大学附属中山医院消化内科),李延青(山东大学齐鲁医院消化内科),李鹏(首都医科大学附属北京友谊医院消化内科),刘苓(四川大学华西医院消化内科),陈晓宇(上海交通大学医学院附属仁济医院消化内科病理室),金珠(北京大学第三医院消化内科病理室),李景南(中国医学科学院北京协和医学院北京协和医院消化内科),陈萦晅(上海交通大学医学院附属仁济医院消化内科),吕农华(南昌大学第一附属医院消化内科),吕宾(浙江中医药大学附属第一医院消化内科),时永全(空军军医大学第一附属医院消化内科)
参与讨论和定稿者(按姓氏汉语拼音排序):白飞虎(海南医学院第二附属医院消化内科),白文元(河北医科大学第二医院消化内科),陈东风[陆军特色医学中心(重庆大坪医院)消化内科],陈红梅(西藏大学医学院),陈旻湖(中山大学附属第一医院消化内科),陈平(内蒙古医科大学第一附属医院消化内科),陈其奎(中山大学孙逸仙纪念医院消化内科),陈卫昌(苏州大学附属第一医院消化内科),陈晓宇(上海交通大学医学院附属仁济医院消化内科病理室),陈烨(南方医科大学深圳医院消化内科),陈萦晅(上海交通大学医学院附属仁济医院消化内科),陈正义(海口市人民医院消化内科),崔云(上海交通大学医学院附属仁济医院消化内科病理室),丁士刚(北京大学第三医院消化内科),董卫国(武汉大学人民医院消化内科),杜奕奇[海军军医大学第一附属医院(上海长海医院)消化内科],范建高(上海交通大学医学院附属新华医院消化内科),房殿春[陆军军医大学第一附属医院(重庆西南医院)消化内科],房静远(上海交通大学医学院附属仁济医院消化内科),高峰(新疆维吾尔自治区人民医院消化内科),高琴琰(上海交通大学医学院附属仁济医院消化内科),郜恒骏(上海芯超生物科技有限公司),郭晓钟(解放军北部战区总医院消化内科),韩英(解放军总医院第七医学中心消化内科),郝建宇(首都医科大学附属北京朝阳医院消化内科),侯晓华(华中科技大学同济医学院附属协和医院消化内科),姜海行(广西医科大学第一附属医院消化内科),金珠(北京大学第三医院消化内科病理室),蓝宇(北京积水潭医院消化内科),李景南(中国医学科学院北京协和医学院北京协和医院消化内科),李良平(四川省医学科学院四川省人民医院消化内科),李鹏(首都医科大学附属北京友谊医院消化内科),李锐(苏州大学附属第一医院消化内科),李岩(中国医科大学附属盛京医院消化内科),李延青(山东大学齐鲁医院消化内科),林志辉(福建省立医院消化内科),蔺蓉(华中科技大学同济医学院附属协和医院消化内科),刘杰(复旦大学附属华山医院消化内科),刘苓(四川大学华西医院消化内科),刘思德(南方医科大学南方医院消化内科),刘文忠(上海交通大学医学院附属仁济医院消化内科),刘玉兰(北京大学人民医院消化内科),刘占举(同济大学附属第十人民医院消化内科),陆伦根(上海交通大学医学院附属第一人民医院消化内科),陆伟(天津医科大学肿瘤医院消化内科),吕宾(浙江中医药大学附属第一医院消化内科),吕农华(南昌大学第一附属医院消化内科),孟祥军(上海交通大学医学院附属第九人民医院消化内科),缪应雷(昆明医科大学第一附属医院消化内科),聂玉强(广州市第一人民医院消化内科),钱家鸣(中国医学科学院北京协和医学院北京协和医院消化内科),任建林(厦门大学附属中山医院消化内科),沈锡中(复旦大学附属中山医院消化内科),盛剑秋(解放军总医院第七医学中心消化内科),时永全(空军军医大学第一附属医院消化内科),孙刚(解放军总医院第一医学中心消化内科),唐承薇(四川大学华西医院消化内科),田德安(华中科技大学同济医学院附属同济医院消化内科),田字彬(青岛大学附属医院消化内科),庹必光(遵义医科大学附属医院消化内科),万荣(上海交通大学医学院附属第一人民医院消化内科),汪芳裕(解放军东部战区总医院消化内科),王邦茂(天津医科大学总医院消化内科),王斌[陆军特色医学中心(重庆大坪医院)消化内科],王承党(福建医科大学附属第一医院消化内科),王吉耀(复旦大学附属中山医院消化内科),王江滨(吉林大学中日联谊医院消化内科),王俊平(山西省人民医院消化内科),王良静(浙江大学医学院附属第二医院消化内科),王蔚虹(北京大学第一医院消化内科),王晓艳(中南大学湘雅三医院消化内科),王小众(福建医科大学附属协和医院消化内科),王学红(青海大学附属医院消化内科),吴开春(空军军医大学第一附属医院消化内科),吴小平(中南大学湘雅二医院消化内科),肖英莲(中山大学附属第一医院消化内科),谢渭芬[海军军医大学第二附属医院(上海长征医院)消化内科],许洪伟(山东省立医院消化内科),许乐(北京医院消化内科),杨长青(同济大学附属同济医院消化内科),杨仕明(陆军军医大学第二附属医院消化内科),杨幼林(哈尔滨医科大学附属第一医院消化内科),杨云生(解放军总医院第一医学中心消化内科),游苏宁(中华医学会),袁耀宗(上海交通大学医学院附属瑞金医院消化内科),曾维政(解放军西部战区总医院消化内科),张炳勇(河南省人民医院消化内科),张国新(南京医科大学第一附属医院消化内科),张军(西安交通大学医学院第二附属医院消化内科),张开光(安徽省立医院消化内科),张澍田(首都医科大学附属北京友谊医院消化内科),张晓岚(河北医科大学第二医院消化内科),张志广(天津医科大学第二医院消化内科),郑鹏远(郑州大学第五附属医院消化内科),郑勇(石河子大学医学院第一附属医院消化内科),周丽雅(北京大学第三医院消化内科),周群(《中华消化杂志》编辑部),周永健(广州市第一人民医院消化内科),周永宁(兰州大学第一医院消化内科),祝荫(南昌大学第一附属医院消化内科),邹多武(上海交通大学医学院附属瑞金医院消化内科),邹晓平(南京大学医学院附属鼓楼医院消化内科),左秀丽(山东大学齐鲁医院消化内科)
学术秘书:高琴琰、熊华、陈慧敏、邹天慧、周澄蓓(上海交通大学医学院附属仁济医院消化内科)
