原子吸收分光光度仪测定蔬菜维生素C 含量的研究
2024-01-12包蔚朱晓芸徐桦何锴余海芬
包蔚 朱晓芸 徐桦 何锴 余海芬
(上海市嘉定区农业技术推广服务中心,上海 201800)
维生素C 又叫抗坏血酸,广泛存在于植物组织中,尤其是在新鲜的水果、蔬菜中含量较多。同时,维生素C 是一种水溶性维生素,是人体需要量最大的一种维生素[1]。目前,国家标准中关于维生素C含量的测定方法有2,6-二氯靛酚滴定法(以下简称滴定法)和2,4-二硝基苯肼比色法[2],但是2,4-二硝基苯肼比色法操作复杂,且萃取液二甲苯为有机溶剂,具有较强的毒性,不利于操作人员的健康,故不推荐使用该方法。滴定法是根据维生素C 的氧化还原性质,通过样品溶液由蓝色转变为粉红色来辨别其滴定终点的到达,从而计算样品中还原型抗坏血酸的含量[2]。由于多数水果、蔬菜样品的提取液中含有一定的色素,导致采用滴定法滴定时,其终点不易辨认,影响了该方法的准确性。然而,原子吸收法(以下简称原吸法)是利用维生素C 在酸性介质中可将Cu2+定量地还原为Cu+,而Cu+与SCN-反应后可生成CuSCN 沉淀,沉淀经高速离心机有效分离出来后,可用原子吸收分光光度计测定含铜量,这样即可推知样品中维生素C 的含量[3]。在此背景下,笔者以滴定法为对照,以黄瓜、卷心菜、青椒、青菜4 种蔬菜为实验材料,从实验步骤、实验结果、精密度、准确度4个维度,验证了原吸法测定蔬菜中维生素C 含量的可行性。现将相关结果报道如下。
1 材料与方法
1.1 供试材料
选取新鲜、色泽正常、无腐烂变质的黄瓜、卷心菜、青菜、青椒4种蔬菜,每种蔬菜取不同可食部位若干混合作为蔬菜样品。
1.2 试剂与仪器
1.2.1 滴定法
样品提取液用质量浓度为2% 的草酸溶液。另外,称取100 mg 维生素C 标准样品,溶于草酸提取液中并稀释至100 mL,配制成质量浓度为1 mg/mL的维生素C 标准溶液,现配现用。
滴定液的配制方法:称取碳酸氢钠52 mg 溶解在200 mL 热蒸馏水中,然后称取2,6-二氯靛酚溶液50 mg 溶解在上述碳酸氢钠溶液中,冷却后定容至250 mL,过滤至棕色瓶内,放在冰箱中保存。每次使用前,用标准抗坏血酸标定其滴定度。
1.2.2 原吸法
称取草酸20 g,加冰醋酸80 mL,溶解后转移到1 000 mL 容量瓶中,用蒸馏水定容后摇匀,作为样品提取液备用。
准确称取维生素C 标准样品0.1 g,置于100 mL 棕色容量瓶中,用提取液稀释至刻度线,即得到质量浓度为1 mg/mL 的维生素C 标准溶液。然后分别吸取5.0、10.0、20.0、30.0、40.0、50.0 mL标准溶液置于100 mL 容量瓶中,再分别定容至刻度线,即得到质量浓度为50、100、200、300、400、500 μg/mL 的维生素C 标准溶液。
称取硫氰酸铵2 g,溶解后转移到100 mL 容量瓶中定容,即得到质量浓度为2% 的硫氰酸铵溶液。量取1 mol/L 盐酸50 mL、1 mol/L 醋酸钠溶液50 mL,混合后移入250 mL 容量瓶中定容,即得到盐酸-醋酸钠缓冲液(pH 为1.99)。
实验用的其他试剂和仪器:饱和氯化钾溶液、饱和硫酸铜溶液、AAnalyst 800 型原子吸收分光光度仪、5 000 r/min 组织粉碎机等。
1.3 实验方法
1.3.1 滴定法
称取新鲜的蔬菜样品10 g 放入研钵中,碾碎后加5 mL 样品提取液,然后将样品移入l00 mL 容量瓶,并稀释至刻度后摇匀过滤。然后,吸取10 mL滤液放入蒸发皿中,用已标定过的2,6-二氯靛酚溶液滴定,直至溶液呈粉红色30 s 不褪色为止。同时,做空白实验。
1.3.2 原吸法
称取新鲜的蔬菜样品5 g,用组织粉碎机碎成糊状,加入少许样品提取液浸泡后过滤,将滤液转移至250 mL 容量瓶中,用样品提取液定容至刻度线。然后,分别吸取维生素C 标准溶液1 mL 和样品提取液1 mL 于离心管中,再各加入饱和硫酸铜溶液1 mL、2% 硫氰酸铵溶液1 mL、缓冲液0.5 mL和饱和KCl 溶液0.5 mL,充分混合,稍后离心分离,去除上层清液,并用少量水洗涤沉淀2~3 次,加入硝酸0.5 mL 溶解后,转移至100 mL 的容量瓶中加水定容至刻度线,摇匀。用原子吸收分光光度计测定其含铜量,根据所得的维生素C 含量的标准曲线即可得到样品的测定结果。
1.3.3 精密度与准确度分析
实验通过5次平行测定,计算相对标准偏差,来衡量实验的精密度。同时,采用加标回收的方式,通过回收率的比较,来判定实验的准确度。
2 结果与分析
2.1 实验步骤比较
笔者在应用滴定法测定含有色素较多的茄子时发现,茄子样品中含有花青素,滤液显现出大红色,较滴定后的标准溶液颜色深,无法判断滴定终点。由此说明,不宜用滴定法测定含有可溶性色素的蔬菜。
笔者在应用原吸法测定时,在样品提取液中加入饱和硫酸铜溶液和2%硫氰酸铵溶液后,待反应液变成绿色浑浊液体,离心,经沉淀后多次洗涤,再用浓硝酸溶解,最后上机测定。由此说明,原吸法需要反复离心、洗涤、沉淀,步骤较滴定法多。
2.2 实验结果比较
由图1可知,两种方法的测定结果相差不大,且原吸法测得4 种蔬菜样品的维生素C 含量均高于滴定法,其中,结果差异最大的为青椒,两种方法每100 g 样品相差5.84 mg;其次为青菜,两种方法每100 g 样品相差3.82 mg;第3 为黄瓜,两种方法每100 g 样品相差2.22 mg;差异最小的是卷心菜,两种方法每100 g 样品相差1.48 mg。分析其原因,可能是青椒、青菜、黄瓜含有较多的叶绿素,色素含量较多,干扰了滴定结果的判断,导致这3种蔬菜样品的维生素C 含量差异比卷心菜大。
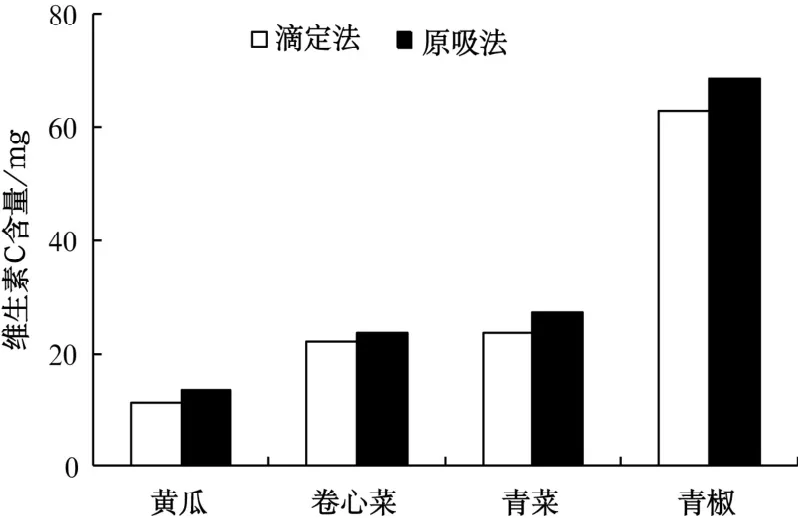
图1 两种检测方法测定维生素C 含量结果比较
2.3 实验精密度比较
采用两种方法测定4种蔬菜样品,其5次平行测定值的相对标准偏差结果见表1。由表1可知,滴定法的相对标准偏差为1.59%~4.67%,原吸法的相对标准偏差为0.89%~2.53%;精密度的要求都在标准要求的范围内,且原吸法的精密度比滴定法高。分析其原因,可能是滴定法的终点判断要满足保持出现粉红色30 s 内不褪色这一条件,主观因素较强,而原吸法的测定结果由仪器读取,人为误差较小,且原吸法测定铜离子比较稳定。

表1 两种检测方法精密度实验结果比较
2.4 实验准确度比较
由表2可知,原吸法的回收率为93.06%~105.29%,滴定法的回收率为97.38%~105.68%,回收率均在80%~120%的范围内。从回收率的数值看,滴定法的准确度要优于原吸法,分析其原因,原吸法需经过多次离心和洗涤,其测定步骤较滴定法多,这对结果的准确性造成了一定影响。由表2还可知,在测定叶绿素含量较高的黄瓜、青菜、青椒等蔬菜时,滴定法的准确度不如原吸法。

表2 两种检测方法加标回收率实验结果比较
3 结论与讨论
采用原吸法测定蔬菜中的维生素C 含量,其准确度和精确度均符合标准,故采用该方法测定蔬菜中维生素C含量具有一定的可行性。与滴定法相比,原吸法测定蔬菜中维生素C 含量的操作步骤较多,但是,在测定色素较多的蔬菜时,原吸法的准确性高于滴定法。因此,原吸法可作为测定蔬菜维生素C 含量的一种补充方法。
