N-乙酰-D-氨基葡萄糖抑制氧化应激和促进巨噬细胞M2 极化减轻大鼠急性胰腺炎
2024-01-12许祖知张靓黄鑫余磊陈鹏飞谢学文陈治非方开晗费书珂
许祖知,张靓,黄鑫,余磊,陈鹏飞,谢学文,陈治非,方开晗,费书珂*
(1. 南华大学衡阳医学院附属第二医院肝胆胰脾外科,湖南衡阳 421000;2. 南华大学衡阳医学院附属第二医院风湿免疫科,湖南衡阳 421000)
急性胰腺炎(acute pancreatitis,AP)是临床中常见的消化系统疾病之一,因多种因素导致胰蛋白酶激活,同时引起病理性细胞通路和细胞器功能障碍,最终导致胰腺腺泡细胞死亡,引发局部乃至全身的炎症反应[1-3]。 严重的炎症和激活的炎症细胞会产生高水平的活性氧(reactive oxygen species,ROS),耗尽内源性抗氧化剂,导致机体氧化和抗氧化失衡,引起氧化应激,从而破坏腺泡细胞并加剧多器官功能障碍[4-5]。 丙二醛(malondialdehyde,MDA)即是常见的脂质过氧化产物之一,其含量反映的是机体脂质过氧化程度。 超氧化物歧化酶(superoxide dismutase,SOD)作为机体内最重要的自由基清除剂维持机体代谢平衡,其含量可反映机体抗氧化的程度[6]。 过氧化物酶体增生物激活受体-γ( peroxisome proliferator activated receptor-γ,PPAR-γ)是一种核受体,最初被确定为脂肪生成的关键核转录因子,而后研究证明其在炎症、癌症和细胞分化中发挥重要的调节作用。 此外,PPAR-γ也被认为是调节巨噬细胞分化和细胞极化的关键抗炎调节剂[7]。 在AP 早期,胰腺组织浸润的巨噬细胞通常为M1 型巨噬细胞,可持续产生高水平的促炎细胞因子、活性氮和活性氧等中间体参与引发和维持炎症,进一步扩大炎症范围,而在AP 晚期,激活的M2 型巨噬细胞则缓解炎症并限制炎症范围[8]。 因此,将巨噬细胞极化从促炎M1 型调整为抗炎M2 型是AP 的有效治疗选择[9]。 氨基葡萄糖(glucosamine,GlcN)是一种天然的氨基单糖,为人体关节软骨基质中合成蛋白聚糖所必需的物质,N-乙酰-D-氨基葡萄糖(N-acetyl-D-glucosamine,GlcNAc)是9 种主要糖核苷酸之一,其在细胞质中合成,并主要以尿苷二磷酸(uridine 5’-diphosphate,UDP)结合的形式被激活[10],是GlcN 类药物的常用临床形式之一,目前广泛应用于临床上骨关节炎的治疗,对于关节软骨起到保护作用[11]。 GlcNAc 除了对关节的保护作用外,同时还在其他多种炎症疾病具有缓解作用。 GlcN 还可以通过抑制ROS 相关的炎症信号来减轻香烟烟雾引起的肺部炎症[12]。GlcN 可抑制炎症细胞中髓过氧化物酶的激活,以及NF-κB、COX-2 和iNOS 的激活,从而抑制结肠粘膜的炎症,证实了在炎症性肠病中的抗炎作用[13]。Chiu 等[14]在实验中发现GlcN 通过抑制NLRP3 炎症小体及NF-κB 的激活减轻细胞的毒性与炎症反应。 然而,对于GlcN 在正常组织和炎症组织中氧化应激的影响,似乎也存在相反的观点。 Moore 等[15]研究表明,GlcN 增强了正常饮食小鼠的胰岛素抵抗,但改善了高脂饮食小鼠的肥胖和胰岛素抵抗。同时,GlcN 促进视网膜Müler 细胞的内质网应激,并导致胰岛素抵抗作用,这表明GlcN 可能加剧糖尿病诱导的高血糖。 这与之前大多研究对于GlcN 抑制氧化应激这一结论相悖。 因此,有必要针对GlcN在不同器官组织疾病中作用机制进行进一步研究。关于GlcNAc 在胰腺相关疾病中的研究较少。 Kim等[16]研究表明,由GlcNAc 和葡萄糖醛酸糖组成的透明质酸(hyaluronic acid,HA),可以作为一种营养剂来促进胰腺导管腺癌的代谢。 然而,目前尚未有GlcNAc 在胰腺炎之间的直接研究。 本研究通过L-精氨酸诱导的AP 大鼠模型,探讨GlcNAc 对胰腺组织形态、炎症因子、氧化应激水平、M1、M2 型巨噬细胞标志物的影响,为AP 的治疗提供新的切入点。
1 材料与方法
1.1 材料
1.1.1 实验动物
7 周龄SPF 级雄性SD 大鼠20 只,体重200 ~250 g,购自斯贝福生物技术有限公司【SCXK(京)2019-0010】。 所有大鼠饲养于南华大学SPF 级动物实验中心【SYXK(湘)2022-0008】,饲养期间自由饮水、饮食,饲喂普通饲料由南华大学实验动物中心提供。 饲养环境:遵守日照/黑暗环境各12 h,在湿度40%~60%,温度20 ~ 26℃下饲养。 本实验所有操作已通过南华大学伦理审查会审批(USC2022 10DS18)。
1.1.2 主要试剂与仪器
N-乙酰-D-氨基葡萄糖(上海源叶生物科技有限公司,货号:S11029),IL-1β、IL-6、TNF-α 试剂盒(武汉华美生物工程有限公司,货号分别为:CSBE08055r、CSB-E04640r、CSB-E11987r),HO-1 抗体和β-actin 抗体(proteintech、货号:27282-1-AP、66009-1-Ig)、NRF2 抗体和PPAR-γ 抗体(Abcam,货号:ab62352、16643-1-AP),CD206 抗体(PTG、货号:18704-1-AP、26903-1-AP),CD86 抗体(PTG、货号:26903-1-AP 或13395-1-AP),F4/80(Santa,货号:sc-377009)。 电泳槽和转膜系统(北京六一,中国),光学显微镜(Motic,BA210T,中国),多功能酶标分析仪(深圳市汇松科技发展有限公司,MB-530,中国)。
1.2 方法
1.2.1 大鼠AP 模型制备、给药方法、取材
20 只SPF 级雄性SD 大鼠经1 周适应性喂养后,根据随机对照原则,分为对照组(腹腔注射生理盐水)、AP 组(腹腔注射20% L-精氨酸溶液)、低剂量GlcNAc + AP 组(腹腔注射50 mg/kg GlcNAc)、高剂量GlcNAc + AP 组(腹腔注射200 mg/kg GlcNAc)。 所有大鼠AP 造模给药前禁食24 h,禁饮8 h。 AP 造模采用方法:按2.5 g/kg 剂量腹腔注射20% L-精氨酸2 次,间隔60 min。 低、高剂量GlcNAc + AP 组造模采用方法:AP 造模前24 h 分别按照50 mg/kg 或200 mg/kg 剂量予以腹腔注射GlcNAc。 24 h 后按2.5 g/kg 剂量腹腔注射20%L-精氨酸2 次,间隔60 min。 48 h 后进行大鼠取材,将大鼠麻醉后固定手术台开腹,取腹主动脉血,于离心机中4℃下,4000 r/min 离心10 min,取上清液,分装于两个1.5 mL 离心管中,-80℃冰箱保存,一份用于检测血清AMY、LPS、TNF-α、IL-1β、IL-6;另一份用于检测MDA、SOD 含量。 取血后再取胰腺组织。 将取好的胰腺组织分为两部分,一部分用4%多聚甲醛溶液固定,制备石蜡切片用于HE 染色和免疫组化;另一部分存放在-80℃冰箱中备用,之后用Western Blot 检测和免疫荧光。
1.2.2 胰腺组织HE 染色
取出用4%多聚甲醛固定的SD 大鼠胰腺组织,将其切成4 μm 的薄片,用不同浓度的乙醇和二甲苯逐级脱水,石蜡包埋,然后在100 倍光镜下检查组织病理学变化。
1.2.3 ELISA 法检测AMY、LPS、SOD、MDA 水平
将保存在-80℃的大鼠血清置于室温解冻,离心,参照各试剂盒说明书进行测定,用酶标仪(MB-530,深圳市汇松科技发展有限公司)分别在450 nm(IL-1β、IL-6、TNF-α、SOD)、532 nm(MDA)、580 nm(LPS)和660 nm(AMY)处检测吸光度。 根据各自的标准曲线计算相应指标的浓度。
1.2.4 Western Blot 检测NRF2、HO-1、PPAR-γ 的表达水平
将存于-80℃的胰腺组织,解冻后加入溶解剂,离心分离上层清液。 采用BCA 法进行蛋白定量。取200 μL 蛋白上清液,进行凝胶电泳后转膜,用1 ×PBST 封闭90 min 后,加入相应抗体(HO-1、NRF2、PPAR-γ、β-actin 抗体,稀释比例分别以1 ∶2000;1 ∶1000;1 ∶3000;1 ∶5000),4℃孵育过夜。 然后加入HRP 标记的二抗(稀释比例1 ∶5000),室温下孵育90 min。 ECL 显色后,采用凝胶成像系统进行图像分析。
1.2.5 M1、M2 极化、PPAR-γ 的免疫荧光
将胰腺组织切片60℃下烘焙12 h 后放入二甲基苯酚溶液1 h,然后分别用100%、95%、85%、75%的乙醇脱水。 将该切片分别在EDTA 缓冲剂(pH =9.0)、0.01 mol/L PBS(pH = 7.2 ~ 7.6)、硼氢化钠溶液、苏丹黑染色溶液、10%的正常人血清/5%的牛血清白处理后,将一抗体(PPAR-γ,CD86 + F4/80,CD206 + F4/80)滴入培养基中置于冰箱中12 h。用50 ~ 100 μL 的抗-兔子免疫球蛋白-IgG 标记的荧光抗体,在37℃下培养60 ~ 90 min,然后甘油封存避光保存,置于荧光显微镜下观察。 采用凝胶成像系统进行图像分析。
1.2.6 免疫组化
将胰腺组织切片60℃下烘焙12 h 后依次脱水,热修复抗原后,加1%高碘酸灭活内源性酶,将一抗体(CD86,CD206)孵育过夜。 用50 ~ 100 μL 抗-兔、兔-IgG 抗体-HRP 多聚体37℃孵育30 min,冲洗后滴加预制好的显色液DAB 工作液50 ~ 100 μL,苏木素复染5 ~ 10 min,蒸馏水冲洗,PBS 返蓝;再次脱水后置于二甲苯10 min,2 次,中性树胶封片、显微镜观察。 用Image-Pro Plus 进行图像分析。
1.3 统计学分析
实验数据和统计过程用GraphPad Prism 9.0 处理,计量资料用平均值± 标准差(±s)表示,多组之间比较采用单因素方差分析,非配对t检验用两组间比较。P< 0.05 表示差异具有显著性。
2 结果
2.1 GlcNAc 下调L-精氨酸诱导的AP 大鼠血清AMY、LPS 水平
L-精氨酸造模后,肉眼观AP 组胰腺较对照组明显水肿,渗出,同时AP 组大鼠血清AMY(8.97 ±0.42 U/mL)、LPS 水平(46.12 ± 3.84 U/L)较对照组(6.63 ± 0.25 U/mL),(22.92 ± 1.19 U/L)明显升高(P< 0.05),表明AP 大鼠造模成功;高剂量GlcNAc + AP 组大鼠血清AMY(7.22 ± 0.32 U/mL)、LPS(27.28 ± 1.26 U/L)与AP 组大鼠相比均明显下降(P< 0.05),同时低剂量GlcNAc + AP 组血清AMY(8.04 ± 0.40 U/mL)无显著性差异,而LPS(32.66 ± 1.77 U/L)明显低于AP 组(P< 0.05)。在大鼠腹腔肉眼观中,低剂量GlcNAc + AP 组和高剂量GlcNAc + AP 组胰腺组织的水肿程度较AP 组明显减轻;而在低剂量GlcNAc + AP 组AMY、LPS水平和高剂量GlcNAc + AP 组无显著性差异(图1)。 综上所述,GlcNAc 可以降低L-精氨酸诱导的AP 大鼠血清AMY、LPS 水平。
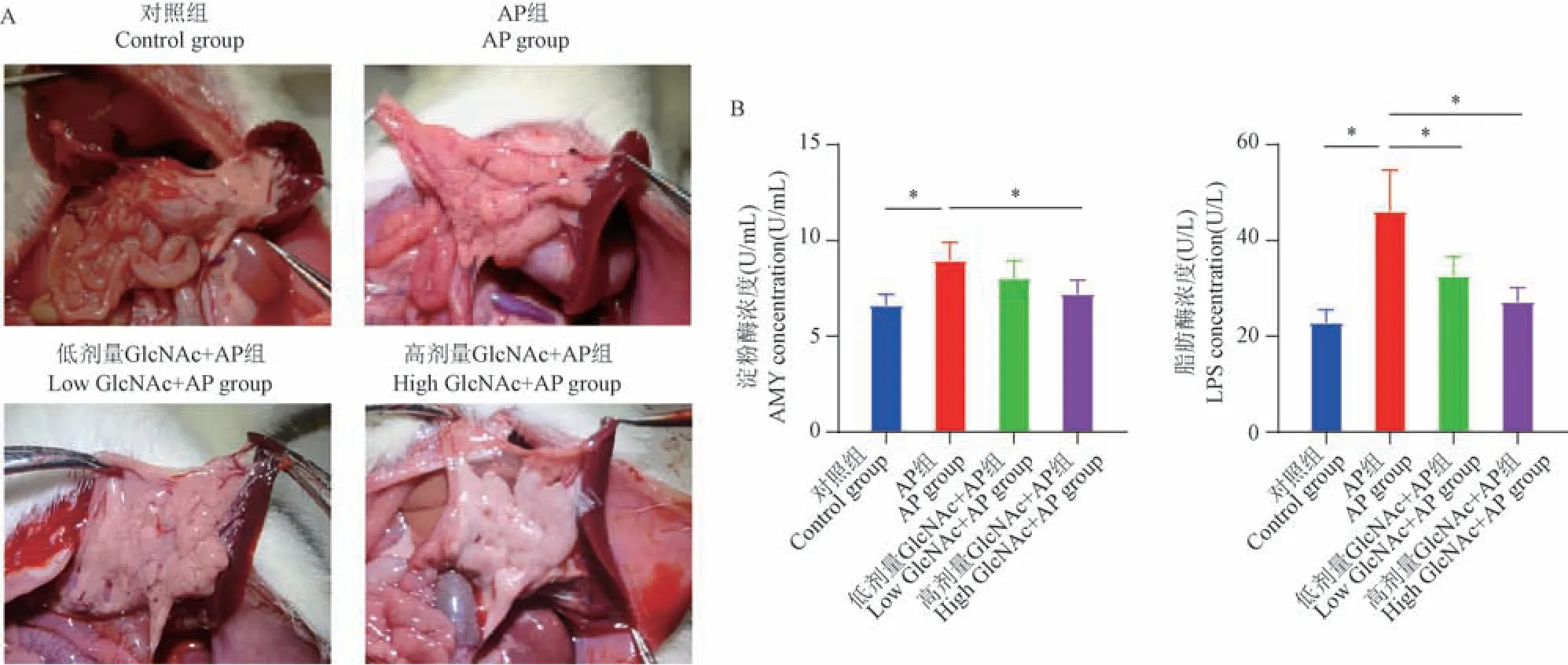
图1 大鼠腹腔肉眼观和血清AMY、LPSNote. A. Abdominal pancreas macroscopic view. B. Serum amylase and lipase concentrations of rats. Compared with AP group, *P < 0.05. (The same in the following figures)Figure 1 Abdominal cavity images of rats and concentration of AMY and LPS
2.2 GlcNAc 减轻L-精氨酸诱导的AP 大鼠胰腺损伤
对照组大鼠在显微镜下可观察到胰腺小叶间清晰,胰腺组织无水肿、坏死、出血等,其周围无明显炎症细胞浸润。 AP 组有明显的胰腺间质水肿、大量炎症细胞浸润聚集、胰腺小叶间模糊、大量胰腺腺泡细胞坏死,未见明显出血。 低剂量GlcNAc +AP 组大鼠可观察到有胰腺间质水肿、中量炎症细胞浸润聚集、胰腺小叶间模糊、腺泡细胞坏死,未见明显出血。 高剂量GlcNAc + AP 组大鼠可观察到有胰腺间质轻度水肿、少量炎症细胞浸润聚集、胰腺小叶间稍模糊、腺泡细胞少量坏死,未见明显出血(图2)。 综上所述,GlcNAc 可以减轻L-精氨酸诱导的AP 大鼠胰腺的损伤。

图2 GlcNAc 对大鼠胰腺组织形态的影响(HE 染色)Note. White arrow. Pancreas hemorrhage. Black arrow. Inflammatory cells infiltrate pancreatic tissue.Figure 2 Effect of GlcNAc on pancreatic histomorphology of rats(HE staining)
2.3 GlcNAc 对AP 大鼠血清炎症因子水平的影响
与对照组炎症因子IL-1β(0.18 ± 0.01 ng/mL)、IL-6(45.81 ± 1.16 pg/mL)、TNF-α(36.13 ±1.73 pg/mL)水平相比,AP 组血清炎症因子IL-1β(0.44 ± 0.01 ng/mL)、IL-6(96.53 ± 2.71 pg/mL)、TNF-α(63.56 ± 1.74 pg/mL)水平明显升高(P<0.05);低剂量GlcNAc + AP 组和高剂量GlcNAc +AP 组与AP 组相比,其血清炎症因子IL-1β、IL-6、TNF-α 水平明显下降(P< 0.05);而低剂量GlcNAc+ AP 组和高剂量GlcNAc + AP 组之间,可以发现高剂量GlcNAc + AP 组血清炎症因子IL-1β(0.29 ±0.01 ng/mL)、IL-6(65.70 ± 2.57 pg/mL)水平较低剂量GlcNAc + AP 组(0.37 ± 0.01 ng/mL,79.18 ±1.86 pg/mL) 明显下降(P< 0.05),而高剂量GlcNAc + AP 组TNF-α(45.31 ± 3.48 pg/mL)仅略低于低剂量GlcNAc + AP 组(53.73 ± 2.13 pg/mL),且无显著性差异(图3)。 总的来说,GlcNAc可明显降低AP 大鼠血清炎症因子水平。
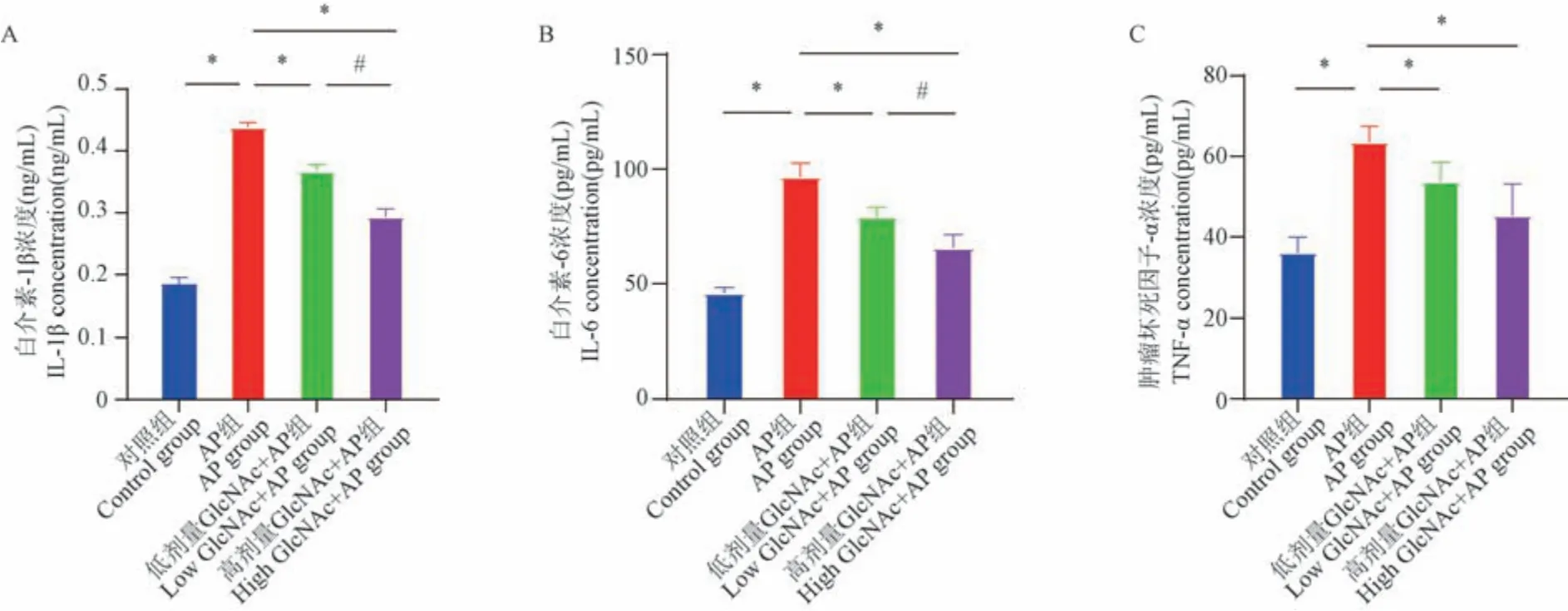
图3 大鼠血清IL-1β、IL-6、和TNF-α 的表达Note. Compared with low GlcNAc + AP group,#P < 0.05. (The same in the following figures)Figure 3 Expression of IL-1β, IL-6 and TNF-α in serum of rats
2.4 GlcNAc 抑制AP 大鼠MDA、SOD 的表达
与对照组MDA(3.99 ± 0.49 nmol/L),SOD(31.89 ± 0.84 nmol/L)相比,AP 组大鼠血清MDA(8.38 ± 0.48 nmol/L)水平明显升高(P< 0.05),而SOD 水平(12.71 ± 1.30 nmol/L)明显下降(P<0.05),表明AP 大鼠机体氧化应激水平明显升高(图4)。 高剂量GlcNAc + AP 组(6.03 ± 0.38 nmol/L)相比于AP 组MDA 水平明显下降(P<0.05),SOD 水平(24.67 ± 1.74 nmol/L)明显升高(P< 0.05),提示GlcNAc 可以显著降低AP 大鼠氧化应激水平。 低剂量GlcNAc + AP 组相比于AP组,MDA 水平(6.59 ± 0.42 nmol/L)明显下降(P<0.05),SOD 水平(18.33 ± 2.29 nmol/L)略高,但都无显著性差异。 同时,高剂量的GlcNAc 似乎比低剂量GlcNAc 更能降低AP 大鼠MDA、升高SOD,但两者并无显著性差异(图4)。 总而言之,GlcNAc 可以明显降低AP 大鼠氧化应激水平。

图4 大鼠血清MDA、SOD 浓度Figure 4 Concentration of MDA and SOD in serum of rats
2.5 GlcNAc 促进AP 大鼠NRF2、HO-1 的表达
相比于对照组,AP 组大鼠NRF2、HO-1 的蛋白表达明显下降(P< 0.05)。 而高剂量GlcNAc + AP组NRF2、HO-1 蛋白表达较AP 组明显升高(P<0.05);同时,在低剂量GlcNAc + AP 组和高剂量GlcNAc + AP 组之间,高剂量GlcNAc + AP 组HO-1蛋白表达略高,但无显著性差异(P> 0.05);综上所述,推断GlcNAc 促进AP 大鼠NRF2/HO-1 轴的激活,抑制氧化应激,减轻AP 大鼠胰腺损伤(图5)。
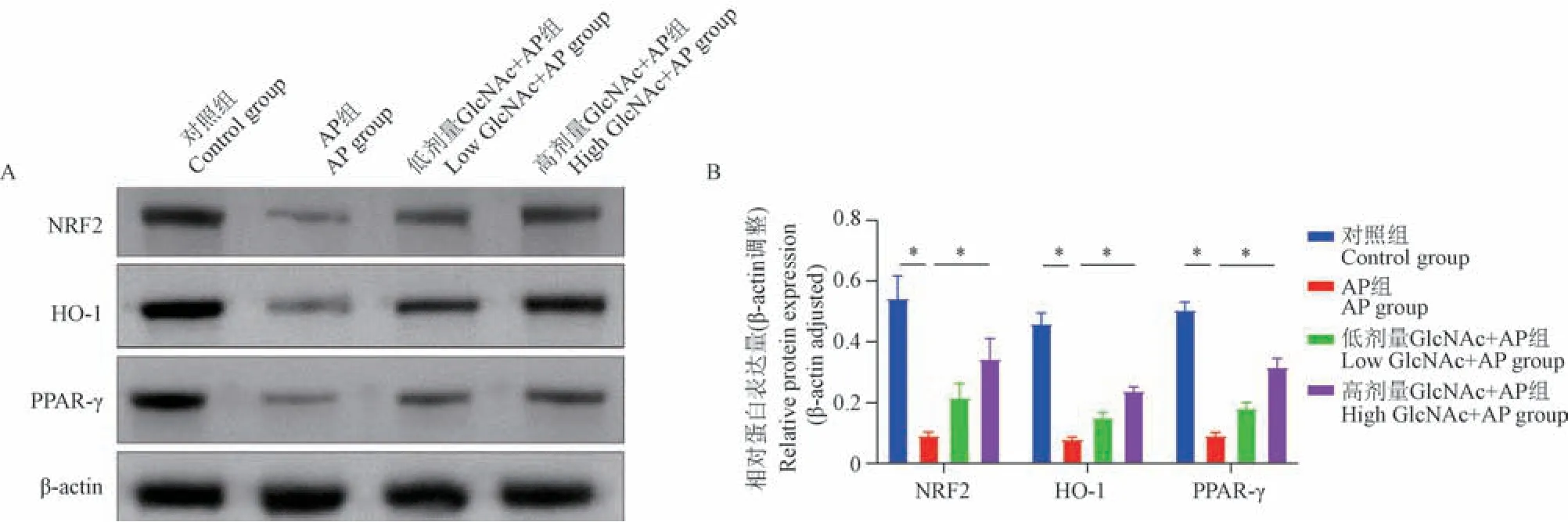
图5 GlcNAc 对大鼠胰腺NRF2、HO-1、PPAR-γ 蛋白质表达水平的影响Note. A. Western Blot of NRF2, HO-1 and PPAR-γ in pancreatic tissue. B. Quantitative and analysis of NRF2, HO-1 and PPAR-γ in pancreatic tissue.Figure 5 Effect of GlcNAc on the proteins expression levels of NRF2, HO-1 and PPAR-γ in pancreas of rats
2.6 GlcNAc 促进AP 大鼠M2 巨噬细胞极化
PPAR-γ 的表达与巨噬细胞极化密切相关[7]。在本实验中,与对照组相比,Western Blot 检测提示AP 组PPAR-γ 蛋白表达明显降低(P< 0.05),同时,高剂量GlcNAc + AP 组PPAR-γ 较AP 组明显升高(P< 0.05)(图5)。 为求进一步验证GlcNAc与巨噬细胞极化的关系,进行免疫荧光和免疫组化验证。 各组大鼠CD86(M1 型巨噬细胞标志物)和CD206(M2 型巨噬细胞标志物)免疫组化显示AP组与对照组相比,CD86 增高,CD206 降低,而无论低剂量GlcNAc + AP 组还是高剂量GlcNAc + AP组都可明显抑制这一现象(图6)。 同时,免疫荧光提示F4/80(巨噬细胞标志物)与CD86、CD206 等存在共定位的现象,表示CD86、CD206 分别代表胰腺组织中的M1 型极化巨噬细胞和M2 型极化巨噬细胞。 AP 组免疫荧光提示CD86 明显升高、CD206 明显下降,提示巨噬细胞向M1 促炎型转化。 而在高剂量GlcNAc + AP 组中,免疫荧光及定量分析提示CD206 明显升高、CD86 明显下降(P< 0.05)。 这结果表明GlcNAc 干预可以促进巨噬细胞向M2 抗炎型转化。 低剂量GlcNAc + AP 组免疫荧光定量提示CD86 明显降低(P< 0.05),但对于CD206 的影响不明显。 同时,高剂量GlcNAc + AP 组相比于低剂量GlcNAc + AP 组,其CD206 定量分析明显升高(图7,图8)(P< 0.05)。 综上所述,GlcNAc 促进AP 大鼠巨噬细胞向M2 型抗炎型转化。

图6 大鼠胰腺CD86、CD206 免疫组化Figure 6 Immunohistochemistry of CD86 and CD206 in rats pancreatic tissue

图7 大鼠胰腺CD86 免疫荧光及定量分析Note. A. Immunofluorescence of pancreatic CD86 in four groups of rats. Green. CD86. Blue. Nucleus. Red. F4/80. B. Quantitative analysis of CD86 immunofluorescence in four groups of rats (ratio of CD86 relative fluorescence intensity to F4/80 relative fluorescence intensity).Figure 7 Immunofluorescence and quantitative analysis of CD86 in rats pancreatic tissue

图8 大鼠胰腺CD206 免疫荧光及定量分析Note. A. Immunofluorescence of pancreatic CD206 in four groups of rats. Green. CD206. Blue. Nucleus. Red. F4/80. B. Quantitative analysis of CD206 immunofluorescence in four groups of rats (ratio of CD206 relative fluorescence intensity to F4/80 relative fluorescence intensity).Figure 8 Immunofluorescence and quantitative analysis of CD206 in rats pancreatic tissue
3 讨论
急性胰腺炎的治疗,临床上多以抑制胰酶、抗炎、止痛、胃肠道减压、静脉营养对症治疗,但仍有部分患者得不到有效的治疗。 因此,寻找治疗AP的手段,仍为重中之重。 通过胰腺炎的病理生理机制研究,减少Ca2+超载、抑制ROS、恢复腺泡细胞自噬、减轻线粒体功能障碍、抑制腺泡细胞和巨噬细胞内胰蛋白酶原过早激活、抑制巨噬细胞M1 型极化和促进巨噬细胞M2 型极化可能是胰腺炎治疗研究的重要着手点。
在本实验中,发现GlcNAc 可明显减轻AP 大鼠氧化应激和胰腺损伤。 对比AP 组,可以发现高剂量GlcNAc + AP 组血清AMY、LPS 水平明显降低,而低剂量GlcNAc + AP 组虽然LPS 水平明显降低,但血清AMY 水平仅略低于AP 组(无显著性差异)。考虑到AMY、LPS 与胰腺炎严重程度并不完全平行,进一步检测了炎症因子(TNF-α、IL-1β、IL-6)的水平。 无论是低剂量GlcNAc + AP 组,还是高剂量GlcNAc + AP 组,其炎症因子(TNF-α、IL-1β、IL-6)都明显下降,这表示GlcNAc 治疗可以减轻AP 大鼠的炎症程度。 在氧化应激相关标志物的Western Blot 检测中发现,相比于AP 组,高剂量GlcNAc +AP 组MDA 水平明显降低,SOD 水平明显升高(P<0.05),而低剂量GlcNAc + AP 组中,MDA 水平仅稍降低,SOD 含量仅稍高于AP 组,且没有显著性差异,这提示低剂量GlcNAc 可能对于L-精氨酸造模的中重度AP 来说,其抑制氧化应激能力较弱。 低剂量GlcNAc 对于AP 的影响,可能需要更为轻型的AP 模型(例如雨蛙肽诱导AP 模型)去进一步探讨其抑制氧化应激能力。
既往的研究中,NRF2/HO-1 通路在众多研究中被证实参与了AP 病情的发生发展,且与氧化应激相关[17-18]。 Shi 等[19]研究表明,LipoxinA4 受体激动剂BML-111 通过NRF2 调节的抗氧化途径改善急性胰腺炎后的肠道紊乱。 Mei 等[20]研究表明由GlcNAc 以β-1,4 糖苷键结合而成的多糖-壳寡糖(COS)可改善胰腺损伤的严重程度,防止肠屏障破坏并减少SAP 中的炎症和氧化损伤。 其主要的保护机制归因于肠道微生物群的重塑以及Nrf2/HO-1通路的调节。 本实验研究了GlcNAc 与NRF2/HO-1通路和氧化应激之间的关系,高剂量GlcNAc + AP组大鼠血清中NRF2、HO-1 的表达明显升高,然而,低剂量GlcNAc + AP 组大鼠血清HO-1、NRF2 表达升高不明显,这可能的原因是低剂量GlcNAc 对于NRF2-HO-1 信号通路的激活能力较弱。 同时,NRF2除了作用于HO-1 这一下游之外,还作用于下游其他基团,如还原型辅酶/醌氧化还原酶(NADPH)、谷胱甘肽过氧化酶4(GPX4)等。 进一步了解GlcNAc对NRF2/HO-1 通路的影响,可以通过增加多个GlcNAc 剂量干预组,同时纳入NADPH、GPX4 等NRF2 其他下游基团进行验证。
对于巨噬细胞M2 型极化和AP 之间的研究,促进巨噬细胞M2 型极化可能是减轻AP 胰腺损伤甚至其他脏器损伤的有效方法。 Taguchi 等[21]研究发现静脉注射一种针对巨噬细胞的新型纳米一氧化碳结合血红蛋白囊泡( CO-bound hemoglobin vesicles,CO-HBVE),可诱导巨噬细胞分化为M2 样表型,从而抑制胰腺中性粒细胞的浸润,减轻胰腺炎所致的肺损伤。 与药物治疗相比,一些特殊的外科技术也可能调节巨噬细胞的极化来治疗AP。 研究表明,在重症AP 大鼠中,腹部穿刺术和引流术可以诱导巨噬细胞极化到M2 型,这可能是由于胰腺炎相关的腹水清除和腹腔炎性环境改善所致[22]。针对M1 极化的实验中,在用表达miRNA-16 的慢病毒转染从AP 大鼠分离的腹腔巨噬细胞后,巨噬细胞的极化从M2 型转变为M1 型,并在功能上激活了CD4+T 细胞,加剧炎症的程度[23]。 此外,最近的报道表明,在小鼠胰腺中,巨噬细胞可能参与诱导腺泡-导管化生(acinar-to-ductal metaplasia,ADM),以及促进胰腺β-细胞再生[24]。
本实验中,首先对胰腺组织进行免疫荧光检测,采用F4/80 标记大鼠胰腺巨噬细胞,然后进行巨噬细胞表型的荧光检测,发现在AP 组可见M1 型极化明显升高,表现为CD206 明显下降,CD86 明显上升(P< 0.05)。 而在高剂量GlcNAc + AP 组中,可以看到M1 型极化明显抑制,M2 型极化明显上升,表现为CD206 明显上升,CD86 明显下降(P<0.05)。 同时,在低剂量GlcNAc + AP 组和高剂量GlcNAc + AP 组的比较中,高剂量GlcNAc + AP 组M2 极化上升更加明显(P< 0.05)。 接着,用Western Blot 对胰腺组织PPAR-γ 的蛋白进行分析,发现AP 组PPAR-γ 蛋白表达明显降低,而应用GlcNAc 干预的低剂量GlcNAc + AP 组和高剂量GlcNAc + AP 组,其PPAR-γ 蛋白表达明显上升(P< 0.05),这也进一步验证了本实验结果。 同时,在对各组大鼠CD86、CD206 免疫组化的检测中,也可以发现GlcNAc 治疗后,大鼠CD206 含量明显升高,CD86 含量明显下降。 这充分证明GlcNAc 治疗促进巨噬细胞M2 极化,减轻AP 大鼠胰腺损伤。
综上所述,在L-精氨酸诱导的AP 大鼠模型中,NRF2/HO-1 信号通路被激活,巨噬细胞表型向促炎型M1 转化,而GlcNAc 治疗可通过抑制NRF2/HO-1 信号通路的激活,促进巨噬细胞表型向抑炎型M2 转化,从而减轻AP。
