过渡金属催化剂的制备及在过硫酸盐高级氧化中的应用研究
2024-01-09唐悦程洁红
唐悦,程洁红
(江苏理工学院 资源与环境工程学院,江苏常州 213001)
目前,随着工业和技术的发展,越来越多的水被污染[1]。部分工业废水中存在着大量的人造高分子物质,如制药废水、农药废水、印染废水和化工废水等[2-5],这些废水中含有的农药、重金属、偶氮染料和抗生素等物质[6-9],具有稳定性好、降解困难和生物降解性低等特点[10],增加了废水处理的难度。
高级氧化法(AOPS)是处理难降解有机化合物的一种有效方法,如臭氧化、光催化、湿式氧化和芬顿氧化是该领域研究最多的技术[11-13]。高级氧化技术利用羟基和硫酸盐自由基可有效处理废水中的有机污染物[14]。在各种AOPS 中,基于硫酸盐自由基的AOPS 更适用于难降解有机物的降解,相比于·OH(1.8~2.7 V),SO4-·(2.5~3.1 V)具有对反应液pH 的依赖性低(pH 值为3~8)、具有强氧化性并且使用寿命长(t1/2= 30~40 μs ,而t1/2(·OH) = 10~3 μs)[15]等优势。且SO4-·更容易通过电子转移与有机污染物发生反应,其在中性或碱性环境中的活性会高于·OH[16]。
目前,SO4-·主要通过热、紫外光、超声或电化学活化过硫酸盐(PS)来获得[17],但耗能较多、设备复杂且运行成本高。相比之下,过渡金属离子活化PS 容易实现,且运行成本低[18],但过渡金属活化过程也存在操作条件受限和效果较低等问题[19]。为解决上述问题,现在的研究集中在制备新型金属催化剂方面,这些新型催化剂是利用过渡金属如Fe2+、Co2+、Cu2+、Ag+、Mn2+、Zn2+来制备,具有结构稳定、pH 使用范围广、催化活性优异且可循环利用等优点,大大提高了活化效率。
本文归纳了利用过渡金属制备催化剂活化过PS 的高级氧化技术的研究现状,概述了影响过渡金属催化剂活化的几种因素,最后进行了总结和展望。
1 活化PS的反应机理
1.1 自由基的产生
Mn+与Mn+1之间的转化是过渡金属与PS反应产生SO4-·的重要途径。过渡金属离子与PS 发生氧化还原反应,给PS一个电子,致使O-O键断裂,生成SO4-·和高价态金属离子,继而高价态金属离子得到SO4-·提供的电子,又生成低价态金属离子,如此反复,不断产生SO4-·降解污染物[20-21]。用反应式表示为:
其中,M代表相应的金属。
此外,过渡金属催化剂活化PS 会产生具有强氧化性的·OH,在PS 活化中,HSO5-通过电子传递,使其分解产生·OH[22],具体如下:
HSO5-+e-→·OH+SO42-
1.2 自由基的氧化降解作用
废水中污染物种类多、含量大且大多数都难降解,而基于硫酸盐的高级氧化工艺是一种很有效的生产羟基和硫酸盐自由基的污染物降解技术。近年来,人们用过渡金属制备的催化剂可以有效活化PS,促进SO4-·与有机物的反应,从而提高污染物的去除率。
常见的有机污染物有芳香类化合物、不饱和烃类化合物以及烷烃、醇、脂和醚类化合物等。相应地,SO4-·与有机污染物的反应机制,总结如下[23-26]:
(1)与芳香类化合物发生电子转移反应:
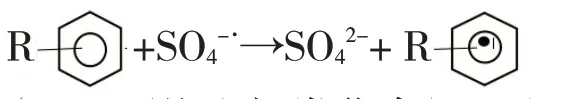
(2)与不饱和烃类化合物发生加成反应:
SO4-·+H2C=CHR →·OSO2OCH2-CHR
(3)与烷烃、醇、脂和醚类化合物发生氢提取反应:
SO4-·+RH →HSO4-·+R·
2 过渡金属制备的催化剂
2.1 不同过渡金属制备的催化剂
用于制备催化剂的过渡金属(Fe2+、Co2+、Cu2+、Ag+、Mn2+、Zn2+)中,铁、锰金属是最廉价的,也是最常见的。Anushree 等[27]首次开发了掺杂过渡金属离子的氧化铁-锰-核壳纳米颗,用于降解溴酚蓝染料;研究表明,在双功能纳米颗粒中,氧化锰用于活化PS,而氧化铁芯用于赋予磁性,使颗粒使用后易于分离并回收利用;并且在催化剂中掺杂银离子后,由于银离子在PS 活化中增强了核壳纳米粒子的反应活性和晶格氧活性,使得染料降解效率最高可达到91%。
除铁、锰外,其他过渡金属制备的催化剂对有机物的降解也有显著的效果。Nguyen等[28]研发了一种新型的绿色纳米催化剂CoO@meso-CN 用于活化过硫酸盐降解亚甲基蓝(MB),CoO@meso-CN 在质量分数为5%时表现出最好的催化性能,其降解MB 的反应速率常数(kobs)为0.264 min-1,该催化剂具有高稳定性,可回收,在催化降解有机污染物方面具有很大的应用潜力。Wen-da等[29]制备了由Cu2+、Co2+或Fe3+组成的不同的金属催化剂,用来活化PS,以处理废水中的有机污染物,并评价了不同金属催化剂的降解效果;结果表明,降解效率由高到低依次为CoO-CuB、Co3O4、CuOCuB、FeO-CuB 、Fe2O3。可见,Co2+在活化PS、降解有机污染物方面有巨大的潜力。
2.2 不同合成方法制备的催化剂
利用这些过渡金属合成催化剂的常见方法有共沉淀法、超声法、水热法和燃烧法等[30]方法。另外,像阴离子表面活性剂等方法,目前相关的研究较少。不同的合成方式会对制备的催化剂产生重要的影响。据报道,Hung 等[31]利用共沉淀法合成了粒径在10~50 nm 的Fe3O4-炭黑纳米结构,并将其用于活化PS,去除海洋沉积物中的多环芳烃(PAHs)。Song 等[32]通过超声和共沉淀法制备了PS 活化的Fe3O4纳米颗粒,用于去除水溶液中的Cr(VI)和三氯生。Zhang等[33]利用水热合成方法,合成出一种可用于降解邻苯二甲酸二丁酯(DBP)的CoO-CuO 双金属催化剂,并对其在室温、常压下的催化性能进行了研究,发现该催化剂在常温、常压下降解DBP 具有良好的稳定性和催化活性。
当然,不同的合成方法对PS 的催化效果也会不一样。Margellou 等人[34]使用阴离子表面活性剂法和燃烧法2 种新型的LaFe1-xCoxO3催化剂,检测不同方法合成的催化剂对PS 降解苯酚的活化性能的影响,结果表明,合成方法影响了钙钛矿的结构特征和催化活性,且表面活性剂法合成的钙钛矿系列材料具有较高的催化活性。
3 影响催化剂活化的条件
3.1 初始pH 对活化的影响
目前,众多研究者颇为关注初始pH 对活化PS 的影响,一般情况下PS 在酸性(pH <3)或强碱(pH>13)溶液中分解速率常数较高[35],并且自由基的种类高度依赖于溶液的pH 值。在pH 为2~7 时,SO4-·是溶液中的主要活性物质。当pH值超过10 时,溶液中·OH 的含量显著增加[36]。这是由于SO4-·在溶液中可与H2O 或OH-反应生成·OH[37-38]。其次,有些金属离子如铁离子只在酸性溶液中稳定存在,在pH >7 时会形成氢氧化物沉淀,从而降低活化性能。Lu 等[39]探索了初始pH 对Fe3O4@MoS2/ PMS 体系中磺胺降解的影响,发现初始pH 为3 时,降解速度最快,当pH升高至9时,降解速度明显减慢。
在用过渡金属催化剂活化PS 降解印染废水时,一般情况下,脱色效率随着pH 的增加而下降。Huang 等[40]则研究了不同pH 值下Co2+/PMS 对2,4-DCP 的去除效果。结果表示,当溶液pH 从3.5 增加到5 时,2,4—DCP 的脱色率明显增强,而当溶液pH 从6 增加到8.4时,脱色率明显下降。可见,在高pH 下,由于Co(OH)2沉淀的形成,催化剂(钴离子)的活性明显降低。Lu 等[41]在Fe2(MoO4)3/PS 降解罗丹明B(RhB)的体系中评估了不同pH 下RhB的降解情况;结果表示,RhB 的降解效率随着pH 值的增加而下降。当初始pH 为3.0时,RhB的降解率最高,几乎达到100%;中性环境下降解率可达84.72%;pH 为11 时降解率可达64.56%。但总的来说,pH 在较宽范围内降解RhB依旧可以表现出较高的催化活性。
此外,pH 值对不同PS的组分也有影响,并且由于活化技术不同,pH 对PS 的活化效果和机理都会不同,还需进一步深入研究。
3.2 温度对活化的影响
一般情况下,温度升高能够促进溶液中的分子热运动,提高反应速率,加速活化[42],且一定范围内温度越高,有机物的降解速率越高,但并非所有体系都这样。Qi等[43]在FeCoNi纳米催化剂活化PS 降解废水中的2,4 二羟基二苯甲酮(BP-1)时,研究了反应温度(15~55 ℃)对BP-1 去除率的影响。研究表明,在15 ℃条件下,30 min 内只有39.1%的BP-1 被去除,而在55℃条件下,BP-1 完全降解。可见,BP-1的降解效率随着反应温度的升高而提高。杨桐飒[44]研究了温度对钴基催化剂活化PS降解四环素废水的影响,研究表明,在25、30、35 ℃时,6 min 内四环素的去除率分别为70.5%、88.3%和95.6%。可见在25~35 ℃时,升高温度可以加速PS 活化。但是在寇晴晴[45]和Huang等[46]的实验中,升高温度,最终的去除率相差不大,说明体系对不同的温度有较高的适应性,温度对PS活化的影响较小。
综上所述,反应体系的温度升高会增强催化剂、PS和有机污染物之间的接触,使得自由基的生成速率增加,有机污染物的去除速率也随之增加,但对个别体系来说,温度对降解有机物的影响作用较小,在室温下进行即可。
3.3 PS投加量和催化剂用量对活化的影响
PS投加量是影响过渡金属活化降解有机污染物的关键因素。研究表明,适当提高PS 用量可以增加有机物的去除率,然而PS投加量过高则会产生淬灭作用,抑制有机物的降解。Xu 等[47]研究了PS 投加量在使用双金属氧化物(Co3V2O8)活化PS降解四环素(TC)废水中的影响,结果表明,当PS投加量从20 mM 增加到30 mM 时,TC 的去除率从75.3%提高到85.3%,反应速率常数(kapp)从0.013 min-1到0.017 min-1,存在明显加速降解过程。继续增加PS的投加量(35~40 mM),对TC的去除率略有提高(由86.6%提高到87.1%),但kapp降至0.015 8 min-1和0.015 7 min-1。Zhang 等[48]在研究磁性Cu/ Fe3O4催化剂活化PS 降解甲基橙(MO)的实验中发现,当初始PS 浓度从1 mM 增加到3 mM 时,MO 的去除率从25.1%提高到94%,但当PS 浓度增加到5 mM 时,MO 的去除率下降到70.9%。Guo 等[49]研究了双金属纳米材料(CoFe2O4/MWCNTs)活化过氧单硫酸盐(PMS)体系对磺胺嘧啶(SDZ)的降解效果,其中,随着PMS 浓度从0.1 mM增加到1.0 mM,SDZ 去除率先增大后减小。PMS 浓度为0.5 mM 时,kobs值最高,SDZ去除率达69.7%。 Zhou 等[50]研究了MnCu 活化Na2S2O8的实验中不同Na2S2O8剂量(50、100、150 mg)对橙II 的降解效率。研究表明:随着Na2S2O8用量从50 mg增加到100 mg,降解率增加;在100 mg 时,降解率达到98%;当投加量增加到150 mg 时,由于PS(Na2S2O8)对SO4-·的自淬灭作用,降解速率降低。
适当剂量的催化剂可以明显提高降解速率,过量的催化剂则会产生淬灭反应,从而影响降解速率。Ma 等[51]研究了Fe3O4-CuO@LAC 催化剂的用量对活化PS 降解废水中苯二酚的影响;研究发现,随着催化剂用量从0.02 g/L 增加到0.1 g/L,对苯二酚的降解速率从0.000 5 M-1·min-1增加到0.011 8 M-1·min-1,降解速率明显提高,这是因为更多的Fe3O4-CuO@LAC 催化剂为其表面活化PS 提供了足够的活性位点。然而,当溶液中催化剂量从0.1 g/L 增加到0.2 g/L 时,降解速率下降到0.006 2 M-1min-1,这可能是由于自由基过多导致自淬反应的发生,是活性位点减少而导致的。Zhang 等[52]对CuFe2O4复合材料活化PDS 降解水中的RhB进行了研究;结果表明,当催化剂用量逐渐增加时,RhB的降解效率逐渐提高;这是由于催化剂质量的增加时候,有效活性位点显著增加,从而增加了催化剂接触PDS 的可能性,生成更多的ROS,提高了RhB 的降解效率。随着催化剂用量从0.3 g/L 增加到0.4 g/L 时,RhB 的降解率仅略有提高,这可能是催化剂在高浓度时容易聚集,在这种情况下活性部位不能被有效利用。
事实上,PS 投加量和催化剂用量之间存在着一定的关系。Rastogi等[53]指出亚铁离子与PS的最佳摩尔比为1∶1,并且随着该比例的增大或减小,活化效率都会降低。大量的实验证明,PS/过渡金属的比例经常为1∶1 和3∶1[54-58],并且与过量的PS相比,过量催化剂的抑制作用更明显[59]。
可见,用过渡金属催化来激活PS 的系统中,适当提高催化剂和PS用量,有利于提高有机物去除率,但过量的PS和催化剂会成为硫酸盐自由基的清除剂,限制硫酸盐自由基的工艺效率。并且两者之间存在一定的比例,寻找最合适的比例可以进一步提高活化效率。
4 结语
目前,过渡金属制备的催化剂由于具有较高的催化活性、结构稳定强且可以多次循环使用等特点在活化PS 领域受到了广泛关注。然而由于催化剂的制备过程复杂,成本高,较难应用于实际,基于已有研究,作者认为仍有许多需要补充和加强的方面,主要有以下三点。
(1)寻找简单高效的合成工艺,开发高效、低成本、简单易得、可重复利用的新型金属催化剂,并且针对后期金属离子的溶出是否会引发二次污染需进一步探索。
(2)将多种金属进行组合,能够使激活效果得到明显提升,应该强化对各个金属比例的研究,并在最小的价格范围内探索各种金属比例的激活效果。
(3)当前大部分实验都局限于实验室模拟,目标物单一,然而实际污水中成分复杂且规模较大,这些技术需在实际废水中做进一步的应用研究。
