水中氯离子去除技术与机理研究进展
2024-01-04张鹏宇李文洋肖麟童冯立明
张鹏宇,李文洋,肖麟童,冯立明
(山东建筑大学材料科学与工程学院,山东济南 250101)
Cl-是氯在自然界中最稳定的存在形式[1],占地球总水量97%的海水是Cl-含量最高的水体,含盐量高达35%,地表水、地下水中也含有一定量的Cl-。此外,矿石开采、食品加工、皮革生产、医药和化工等行业所排放的废水中也含有大量的Cl-。我国人均淡水资源远低于世界平均水平,淡水资源较为匮乏,所以水资源的再生利用对于我国来讲十分重要,为此,我国制定了相应的法规限制各行业污水的排放。按地表水域使用功能要求和废水排放去向,不同场景下含氯废水的排放都应遵守相应的标准。如根据国家《地表水环境质量标准》(GB 3838—2002)规定的氯化物(以Cl-计)排放量,集中式生活饮用水地表水源地补充项目标准限值为250 mg/L;河北省《氯化物排放标准》(DB 13/831—2006)中规定,盐化工产业的氯化物最高排放质量浓度在类别Ι中一级排放限值为300 mg/L;在《污水排入城镇下水道水质标准》(GB/T 31962—2015)中规定,污水排放氯化物质量浓度不得大于500 mg/L,甚至有些地方性法规要求排放质量浓度小于400 mg/L,可见国家对控制污水中Cl-浓度的重视。
在工业发展迅速、废水排放量日益增加的严峻背景下,选择适合于特定环境下对水中除氯的方法具有急迫性和重要性。由于各种工业活动和对海水的直接利用,时刻都有大量含Cl-的废水产生;在沿海地区、盐碱地区地表水及地下水中,天然存在的Cl-含量很高,若不加处理将对生产、生活造成不良影响。工业用水中含量过高的Cl-会加速工业设施的腐蚀破坏[2-7];建筑施工用水Cl-含量过高,将会加速钢筋腐蚀,影响施工质量,进而影响建筑物安全;饮用水中过高含量的Cl-会对人体造成一定损害;如果科学试验用水中的Cl-含量过高,会影响试验准确性,甚至会致使实验室事故。由此可见,无论是工业生产用水还是生活、试验用水,控制Cl-含量具有重要意义。因此,寻求高效去除Cl-的方法,降低水中Cl-含量,既能够提高工业用水回用率,有效缓解我国淡水资源短缺的压力,又可以满足人民对水质的不同需求。目前常用的Cl-的去除方法有化学沉淀法、吸附法、分离法、氧化法等[8-9]。本文旨在总结常用去除含有Cl-水体中Cl-的方法机理及优缺点,提出适配的水中除氯方法,为水中除氯方法的深入研究及工业化应用提供参考。
1 水中Cl-的去除方法研究进展及综合应用
水中去除Cl-的主要方法如表1所示。

表1 水中除氯方法分类Tab.1 Classification of Dechlorination Methods in Water
1.1 化学沉淀法
化学沉淀法是Cl-与其他离子或者化合物进行反应,生成难溶性氯化物或者沉淀达到去除Cl-的目的[10-11]。化学沉淀法除氯通常用于Cl-浓度较高的废水,处理周期短、操作简单、见效快,但是沉淀剂价格通常较高,使得化学沉淀法除氯的成本偏高,推广应用受到局限。化学沉淀法中应用较多的有钙铝盐沉淀法、氯化亚铜法、硝酸银法等。
钙铝盐沉淀法又称超高石灰铝法,是化学沉淀法中应用最广泛的一种方法,且因操作简单、成本较低、去除率高等优点深受科研工作者的喜爱并被广泛研究。钙铝盐沉淀法是向含氯废水中加入一定比例的钙盐和铝酸盐,生成一种难溶性的弗里德尔氏盐沉淀[12-13],以此达到去除Cl-的目的。目前,常用的钙盐为CaO,常用的铝酸盐为NaAlO2[14-17]。钙铝盐沉淀法整个过程的具体反应方程如式(1)~式(5)。
CaO+H2O → Ca(OH)2
(1)
NaAlO2+2H2O → Al(OH)3+Na++OH-
(2)
4Ca(OH)2+2Al(OH)3→ Ca4Al2(OH)14↓
(3)
Ca4Al2(OH)14+2Cl-→ Ca4Al2Cl2(OH)12↓+2OH-
(4)

(5)
以选择的钙盐是CaO为例,CaO和NaAlO2在水中与水反应,分别生成了Ca(OH)2和Al(OH)3,然后两者在碱性环境下继续反应生成Ca2Al2(OH)14,而Ca2Al2(OH)14的沉淀平衡常数为1×10-25,难溶于水,可以与水中的Cl-进行反应,生成一种沉淀平衡常数更小的氯铝酸钙沉淀[16],即Ca4Al2Cl2(OH)12。Ca2Al2(OH)14以[Ca2Al(OH)6]+为主体层,OH-为层间阴离子,其与Cl-反应生成Ca4Al2Cl2(OH)12,模型如图1所示。

图1 Ca2Al2(OH)14结合Cl-的过程Fig.1 Process of Ca2Al2(OH)14 Bonding Cl-
值得注意的是,CaO的NaAlO2的投加比例需要严格控制,如果NaAlO2过量,结合Cl-生成的Ca4Al2Cl2(OH)12则会再度参与反应,释放出已经吸收的Cl-,导致去除效率降低。唐宝玲等[17]针对废水中高浓度Cl-的去除进行试验,对比例、时间、投加量等因素对吸附效率的影响进行深入研究,结果表明,n(Al3+)∶n(Ca2+)为1∶3.3、搅拌时间为30 min时的去除效果最佳,最终可使Cl-的质量浓度降到400 mg/L以下。但研究的局限在于该试验在Cl-质量浓度低于10 000 mg/L的条件下进行[18-20],另外引入的Al3+也需要进一步处理。该方法去除废水中的Cl-具有环保、原料易得、操作简便的优点,其主要成本支出是用于原材料,相比之下,其原料价格也较低廉,且与Cl-反应后生成的沉淀物能吸附废水中的重金属离子,所以可将沉淀物进行煅烧后回收处理。该方法可以应用于大体积的废水处理,具有很好的工业应用前景和深入研究的价值。
氯化亚铜法是利用Cl-与Cu+进行反应生成CuCl沉淀的原理来去除Cl-。比如铜、锌粉法,一般应用在酸性镀铜溶液中除氯,铜粉法主要进行反应如式(6)~式(7)。锌粉法处理Cl-的机理的研究仍比较模糊,但目前主要的观点是锌粉将Cu2+还原成Cu+,Cu+与Cl-生成CuCl沉淀,同样如式(7)。
Cu+Cu2+→ 2Cu+
(6)
2Cl-+Cu2++Cu → 2CuCl↓
(7)
郭崇武[21]利用这个方法对酸性镀铜废液中的Cl-进行去除,加入铜粉时去除效率可达到58.9%,加入锌粉时去除效率为47.0%。该方法与Cl-反应迅速,原料易得,方法简便,但对Cl-的去除效率偏低,且成本昂贵。过量的铜粉投入可能会使废水中金属Cu2+的含量增多,所以控制添加量尤为重要。此方法通常应用于小规模低浓度的含氯废水的处理。
硝酸银法是利用Cl-与银离子反应生成不溶于水的氯化银沉淀。由于硝酸银沉淀剂价格昂贵,仅用于水质中取样检测Cl-含量,不适于工业化去除Cl-[22]。
化学沉淀法反应迅速、反应过程简单、操作容易,开发成本低的沉淀剂是水中去氯的重要方向,具有广阔的应用前景。
1.2 吸附法
吸附法一般是采用离子交换剂与水中的Cl-交换,以交换吸附的方式固定Cl-[23],但交换离子量有限,很容易达到饱和,交换剂需要再生利用,此方法多用于小水量废水的Cl-的去除处理。吸附法中常用的有离子交换树脂法[24]、水滑石法、改性粉煤灰法、电吸附法等。
离子交换树脂具有优异的离子交换作用,尤其是717型硫酸根阴离子交换树脂和201×7型离子交换树脂应用较广,能对Cl-进行稳定吸附,其成本在7 000元/t左右。据报道[25],201×7型离子交换树的再生利用率可高达83.40%,可以大大降低成本。离子交换树脂不仅可以应用于废水中的Cl-去除,还能作为建筑材料的吸氯添加剂使用。Qu等[26]利用SBAE树脂(强碱阴离子交换树脂),将它添加到钢筋混凝土中,所制备的砂浆能有效地吸附砂浆内部的Cl-,从而达到长效防腐效果,延长混凝土使用寿命。离子交换树脂法去除Cl-一般适用于Cl-浓度较低的情况,而且需要考虑树脂的再生费用。
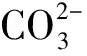
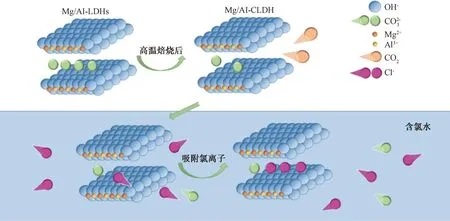
图2 焙烧水滑石对Cl-的吸附过程Fig.2 Adsorption Process of Calcined Hydrotalcite for Cl-
粉煤灰是一种工业废弃物,具有较强的可改性能力,且本身疏松多孔,可作为吸附剂使用。粉煤灰的主要成分为石英(SiO2)和莫来石(3Al2O3·2SiO2),改性后Al-O键和Si-O键打开,增加Cl-与硅、铝离子交换的机会,从而可以有效固定Cl-。此外,改性后的粉煤灰其表面的吸附位点增多,更能有效地吸附Cl-。对粉煤灰进行改性早已成为了粉煤灰吸附领域的热点,刘凌寒等[29]将改性的粉煤灰用于脱硫废水中除氯,最佳投入量为25 g/L,反应约280 min达到平衡,对Cl-的吸附率达到56%。施云芬等[30]利用类水滑石和改性粉煤灰协同在脱硫废水中除氯,类水滑石与改性粉煤灰的质量比为2∶1,对Cl-的去除率可达到88.89%。粉煤灰法是一种较为理想的废水除氯方法,以“废”治“废”,并且原料易得、成本低廉,价格在200元/t左右,跟其他添加剂协同使用可能会有较好的效果。同时,粉煤灰也含有一些微量金属元素,如As、Se、Cd等,在使用过程中粉煤灰中的微量元素可能浸出,导致环境污染。粉煤灰法在国内主要应用于脱硫废水和重金属废水中的污染物处理。因为实际的工业废水中组分复杂,各种离子之间可相互影响,处理的效果会大大降低,现阶段的研究主要在模拟废水中进行。因此,继续深入研究粉煤灰对实际废水中Cl-的吸附具有重要意义。一般可以通过高温、助溶剂、发泡剂等手段对粉煤灰进行改性,使其能够在实际废水中对Cl-进行有效的吸附。
电吸附法是一种基于静电吸附原理的脱盐方法,主要用于水质的净化和淡化。主要采用活性炭作为电极,具有良好的导电性和一定的吸附能力。在两电极上施加电压,溶液中的正负离子在电场力和浓度梯度的驱动下向两极移动,吸附在溶液与电极的表面形成双电层电容,达到去除Cl-的目的。该方法对废水中Cl-的处理效果主要取决于电容的大小。王红兵[31]利用电吸附原理,选用活性炭为电极材料,在水处理过程中有效脱盐,并对电压、盐溶液浓度、流速等因素进行了试验研究,最终活性炭电极可达到的最大吸附容量为5.6 mg/g。电吸附法不仅能够吸附盐离子,而且广泛用于吸附水质中的各种有害物质。科研人员[32]利用电吸附活性炭,对水中的医用高分子污染物进行去除,研究发现活性炭通电压后的吸附容量比没通电压时提高了44%。电吸附法虽然能耗较高,但处理过程不发生化学反应,可以避免生成二次污染物,并且效果良好,是一种非常有前景且具有成本效益的方法,适合用于农业污水、地下水处理、回用水净化等。电吸附法电极材料的选择能决定其吸附能力,所以研发一种新型高效的电极材料迫在眉睫。
1.3 分离法
分离法是采用物理或者物理化学方法,使Cl-以氯化物形式从水中分离出来,以达到Cl-脱离水的目的。分离法对氯化物去除效率较高,但成本也偏高,需要专用设备,目前工业化应用的主要有蒸发浓缩法、膜分离法等。
蒸发浓缩法是将不含可挥发溶质的水分子沸腾汽化、冷凝,使水分子与盐分离,该方法主要用于高纯水制备及高氯盐水处理[33-34]。通过多级蒸馏可以获得高纯度蒸馏水,用于科研需要。对于高氯盐水,通过蒸馏既可获得蒸馏水用于生产,又可获得氯化物盐,实现盐、水分离,如将Cl-从多晶硅产生的高氯废水中进行分离,多次地蒸发且循环利用,将Cl-以结晶盐的形式排出体系外,实现水、盐的二次利用。蒸发浓缩法工艺简单、效率较高,但是长期蒸馏导致高氯盐溶液对设备的腐蚀加剧,受电费、蒸汽、不同的处理设备等因素的影响,处理废水的成本在50元/m3左右,耗能和成本较高,限制了大规模工业应用。
膜分离法在工业污水处理和纯水制备中应用前景广阔,特别是随着膜材料、膜技术的快速发展,极大带动了膜分离法在Cl-的去除、脱盐领域的应用,如纯水制备、废水处理,特别是海水淡化领域,前景广阔。但该方法由于膜对水质要求高,需要对水进行预处理,工序复杂,主要包括预过滤、预吸附、氧化、絮凝、还原等前处理工序,以及对水中的其他组分进行分离[35-36],如图3所示。目前膜分离技术在海水淡化方面应用广泛,具有分离效果好、能耗低等优点,该方法成本包括电费、树脂费、药剂费和滤芯的清洗或者更换维护的费用,处理废水的成本在40元/m3左右。但是在Cl-浓度较高的环境下,由于渗透压过高,难以应用;同时,废水中的其他杂质会对膜层造成一定的污染和损坏,从而限制了其应用。分离后产生的高浓度盐水如何处理也是难题。

图3 渗透膜法除氯工艺Fig.3 Process of Chlorine Removal by Osmotic Membrane Method
1.4 氧化法
氧化法是利用电解、电渗析、还原等方式将Cl-从溶液中去除,主要包括电解法、氧化剂法、电渗析法等。
电解法除氯的原理是将含有Cl-的水体通电,电解槽产生电位差,水体中的阴离子向阳极移动发生还原反应,Cl-在阳极被氧化,如图4所示。但是阳极电位很正,如果水体中的其他离子或杂质含量较多,则会夹杂着很多副反应,所以一般情况下很少应用直接电解法去除复杂水体中的Cl-。并且电解法的成本较高,不建议处理大水量水体,通常在预处理后采用电解法二次处理。氧化剂法是通过与Cl-发生氧化还原反应将Cl-去除的方法。添加氧化剂将Cl-氧化为气态,从而达到去除Cl-的效果。添加氧化剂法在处理废水中极少应用,原则上可行,但是存在诸多的问题。

图4 电解法去除Cl-的工作原理Fig.4 Working Principle of Electrolytic Process for Dechlorination
电渗析法除氯的原理是以电能为动力,离子交换膜为渗透膜,通电使阴、阳离子分别向阳极、阴极移动,由于渗透膜只能通过阴离子或者是阳离子,从而使阴、阳离子分离,实现Cl-的去除。闫虎祥等[37]针对高浓度Cl-采用电渗析工艺,对废水中Cl-的去除率高达85%以上,处理后的Cl-质量浓度降至600 mg/L以下。电解法处理废水操作简单,无污染,且生成OH-可以与废水中的有机物进行反应,有利于后续处理,但是存在能耗高、成本高等缺点,常在废水预处理后应用或者小规模的污水处理。
1.5 各除氯方法综合应用
各种Cl-的去除技术具有不同的特点,适用的水质也不相同,应根据用水规模、水质要求、运行成本控制等方面综合考虑。几种常用Cl-的去除方法优缺点如表2所示。

表2 水中除氯方法对比Tab.2 Comparison of Dechlorination Methods for Wastewater Treatment
由此可见,每种Cl-的去除方法原理、效果、适合的水质不同,如何发挥各种方法的优势,形成组合技术,是值得探讨的问题。总结各方法的特点和发展方向、不同的除氯方法可形成组合技术如下。
(1)沉淀法、氧化剂氧化等化学法除氯,设备简单、效率高,对高浓度含氯水除氯具有显著优势,但试剂消耗大,运行成本高,而且为了有效降低水中Cl-浓度,必须投放过量的沉淀剂或者氧化剂,会对水质带来不良影响,尤其是导致全盐量大幅度提高。因此,开发用量小、效率高的沉淀剂与氧化剂是该领域重要研究方向。化学法处理后的清水可以采用膜处理法进一步净化处理,实现水的高效利用。
(2)膜分离法对于低盐水去除Cl-的优势突出,适合规模化生产,经浓缩后的高盐水可以结合蒸发浓缩法、电解法等进一步处理,实现水及金属等物质的资源化利用,在工业废水处理中是实现废水闭路循环、“零排放”的重要途径。
(3)离子交换树脂、水滑石及粉煤灰受交换容量的限制,仅适合于低氯、低盐水的净化处理,但离子交换树脂与反渗透膜法组合处理,在高纯去离子水制备、重金属回收利用等方面优势突出。反渗透后的淡水经离子交换树脂进一步处理,可以有效脱盐,获得高纯水;反渗透后的浓水经离子交换树脂选择性交换吸附,可以富集重金属离子,实现资源化利用。
2 常见含氯水体Cl-的去除方法及综合应用
为了面向具体水体成分的处理方法、耦合技术选择,提供更有益的技术依据,以下总结了常见典型水体的主要组成数据,并针对几类典型含Cl-的水体特征及处理排放要求,介绍了相关脱氯技术研究、应用进展。最后,为相关技术及耦合方法的适用性、待提升之处给出了建议,对相关水体适用的处理技术进行了总结。
2.1 煤化工高盐氯水Cl-的去除
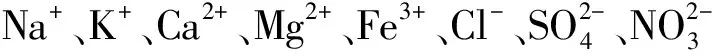

表3 煤化工产业废水主要成分及含量Tab.3 Main Components and Contents of Coal Chemical Industry Wastewater
考虑到煤化工高盐废水中的盐离子质量浓度比较高,通常可达3 000~15 000 mg/L[38]。如果直接将废水进行蒸发浓缩,大量的含氯废水需要很大的能耗和较长的处理时间。如果先将含氯废水进行浓缩,然后集中对浓缩盐水进行蒸发结晶,则会有较好的效果,虽然增加设备会提高成本,但是其Cl-的去除效率会大大提高,且长效配合应用会有良好的成效。对含氯废水进行浓缩常用的方法是离子交换法,一般使用离子交换膜或者离子交换柱将含氯水进行处理[39],得到浓缩高氯盐水和低氯盐水,再将高氯盐水配合应用蒸发浓缩法,使Cl-析出并结晶。高氯盐废水最后转化为低盐废水、水蒸气、固体盐结晶。具体流程如图5所示。而低氯盐水如果达到排放标准可以直接排放,如果氯含量仍然超标,则可以利用离子交换树脂或者水滑石法等再处理。国内有多个煤化工高盐处理项目采用了多种工艺技术组合处理Cl-,如久泰能源(准格尔)煤制甲醇项目采用了机械压缩蒸发、自然蒸发、多效蒸发等工艺技术的一种或几种工艺组合[40]。煤制甲醇项目主要处理工艺为高效澄清池+V型滤池+超滤+钠床+阳床+反渗透,这样不仅可以有效地对Cl-进行去除,同时还能广泛地去除其他盐离子,但是处理后得到的混合盐离子没有市场价值,通常进行填埋处理。国家能源投资集团新疆化工有限公司在高氯盐水的处理上取得较大的进展,通过分步结晶的方式,可以分步得到较为纯净的各种盐离子,如氯化钠、硫酸钠等,并且对Cl-的去除效率较高,基本可以达到高盐废水的零排放标准,平均废水的处理费用约为10.5元/m3。
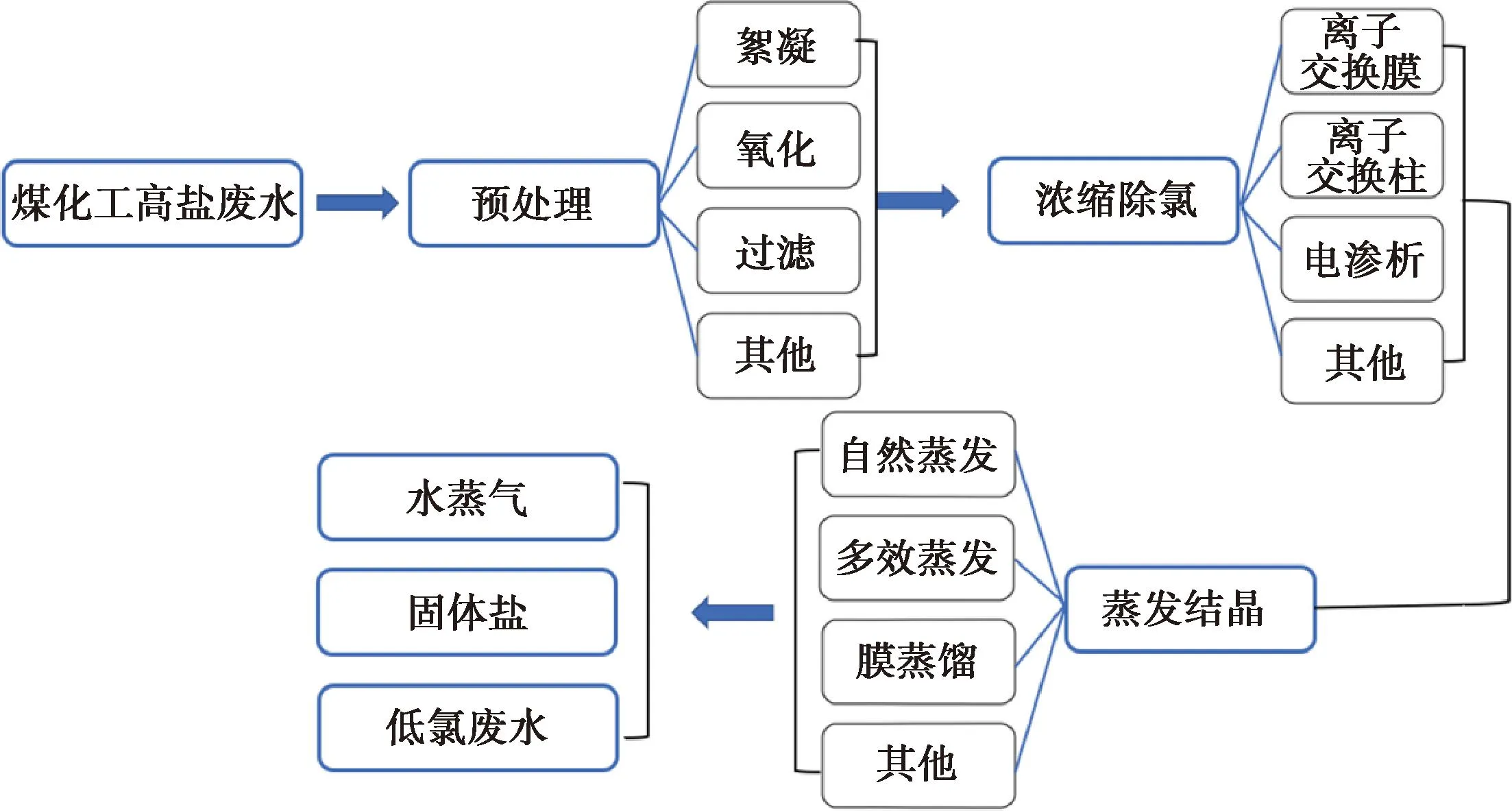
图5 煤化工高盐废水处理流程Fig.5 High Salt Wastewater Treatment Process in Coal Chemical Industry
2.2 电镀含氯废水Cl-的去除
电镀废水中Cl-主要来源于电镀的3个环节:前处理、电镀、后处理[41]。在镀前处理中需要用到盐酸等无机酸来清洗镀件表面,电镀过程中使用的氯化镍、氯化锌等氯化物,以及镀后处理使用氯酸盐的钝化液等都会将Cl-引入到废水中。以山东某机械工具厂处理电镀废水的方案为例,该厂采用先分质分流预处理进行浓缩,最后进行蒸发结晶[42]。首先通过生化系统对废水内的有机物进行去除,防止污染物对膜浓缩系统造成堵塞。处理后的废水进入到膜浓缩装置,通过三段浓缩处理进行脱盐,通过三段的浓缩处理,整体的回收率可以达到90%以上。最后,浓缩后的废液用蒸汽压缩机蒸发,使用全自动离心机进行离心出盐。最终经处理的废水达到了零排放项目的要求,总运行成本约为48.5元/m3,略高于同类废水的处理标准。
电镀含Cl-废水中Cl-的去除可应用的方法还有很多,但同时也要面临各方法的弊端,如果想要达到较好的处理效果,同时想要降低成本,使用各方法的组合技术是必然的。煤化工高盐废水Cl-去除的组合技术同样也可应用于电镀含Cl-废水中Cl-的去除处理,但相对于煤化工高盐废水,电镀废水中的盐离子种类较少且已知,可以使用化学添加剂对Cl-和其他盐离子进行准确地去除。将含氯废水用化学沉淀法处理后,再使用离子交换树脂法或膜分离法再次处理可能会有更好的效果。
2.3 海水淡化
随着水资源的匮乏,积极开发海水淡化技术可以有效缓解水资源短缺的压力。Cl-作为海洋中含量最高的盐离子,在淡化过程中势必作为重点脱除对象。海水主要的组成成分如表4所示。常见的海水淡化的技术大致有蒸馏法、电渗析法、反渗透法(膜分离法)等[43]。

表4 海水中主要成分及含量Tab.4 Main Components and Contents in Sea Water
化学沉淀法和离子交换法不适用于海水中脱盐、除氯。海水是一个Cl-含量非常高且庞大的水体,任何使用添加剂的Cl-去除方法效果有限,并可能对水体进行污染。通过蒸馏法处理过的海水,得到的淡水质量优异,但需要消耗大量能量。电渗析法则是通过分离膜技术,使用离子交换膜将海水分为低浓度盐水和高浓度盐水。反渗透法通过渗透膜淡化海水,经济环保。此外,海水具有一定的腐蚀性,可对设备造成破坏,渗透膜价格昂贵,且3~5年就需要更换一次,并且容易损坏,所以目前海水淡化主要以蒸发浓缩法为主。目前的关键仍然是提高海水淡化技术,降低淡化成本。某沿海钢铁企业探索并建设了海水淡化浓盐水综合利用中试生产线[44],该厂海水淡化装置技术比较领先,且运行平稳。采用热法低温多效蒸馏工艺,充分利用钢铁厂的蒸汽对海水进行加热蒸馏,得到蒸馏水和浓缩海水,再将浓缩海水通过反渗透浓缩技术继续处理,最终可以将氯化钠的质量浓度浓缩为746 000 mg/L左右。该方法需要较高的能耗,利用钢铁厂所富有的余热进行对海水进行处理可有效地降低成本。
3 展望
现阶段的环保政策对水中Cl-含量进行了更加严格的管控,深度处理含有Cl-的水体意义重大。对处理水中除氯的方法工艺进行科学研究,既能有利于水资源的再生利用,又能缓解环境压力,符合可持续发展观念。现存的各种除氯技术大部分都处于实验室研究阶段,且在适应性方面都存在一定的局限性,主要应用于中小水量除氯处理。若要在大水量水体中进行除氯处理,需将改善Cl-的处理效果作为研究重点,兼顾节约成本和环保意识,而后针对各类水的具体情况匹配最佳的除氯工艺方法,形成组合技术,最终建立起一套完整的除氯标准,朝着低成本、高效率且更环保的方向发展。总之,随着工业科技的发展和科研工作者的努力,水中Cl-去除的工艺方法也会不断进步。
