踝上截骨术治疗内翻型踝关节骨关节炎的进展
2024-01-04吕林建王凤玲段小军
吕林建,王凤玲,段小军
(陆军军医大学第一附属医院关节外科,重庆 400038)
踝关节骨关节炎(osteoarthritis,OA)发病率约为1%[1],尽管发病率比膝关节、髋关节更低,但是患者总数并不少,且通常有外伤史。踝关节OA的早期治疗包括药物对症、理疗和关节腔注射等,终末期治疗中关节融合术的近期疗效可靠,但是关节功能部分缺失以及远期邻近关节退变,均使该治疗措施不够完美。关节置换术保留了关节屈伸活动,但是远期假体松动使得该技术不太适用于运动量较大的患者。因此,对于中期踝关节OA,采用踝上截骨(supramalleolar osteotomy,SMOT)和调整软组织平衡的联合手术,有望保留关节功能,近年来在足踝外科和运动医学领域受到高度关注[2]。
踝关节解剖特性以及踝关节内翻、跖屈肌力强于外翻、背伸肌力等综合因素,导致踝关节OA内翻畸形远多于外翻畸形[3]。踝关节内翻畸形时,踝关节应力中心点将内移,加速局部的软骨退变。SMOT的治疗原理为:在胫骨远端截骨,调整踝关节负重力线,使得软骨质量较好的区域承受较大应力,同时减轻软骨缺损区域的负重应力,最终减缓OA发展的进程,甚至使部分患者实现病程逆转[4]。
1 疾病分类与分期
为了便于规划手术治疗和患者随访评估,需要对踝关节OA进行分类。负重位踝关节正位X线片是目前主要的分类与分期依据,可首先通过该检查判断踝关节是否存在内翻和外翻畸形。1995年,Takakura等[5-6]制定的踝关节内翻型OA的分期也是依据该检查而确定,具体是将踝关节内翻型OA分为4期,1期:未出现关节间隙变化,仅有硬化骨和骨赘形成;2期:内侧间沟狭窄;3期:内踝间隙严重狭窄,进展到距骨内侧穹隆与胫骨软骨下骨的接触;4期:全关节间隙狭窄,以及关节两侧软骨下骨广泛接触。3期可进一步分为两个亚型:3a期指距骨与胫骨的软骨下骨接触局限在内侧间沟;3b期指接触面已波及负重的胫距关节间隙。
2 手术适应证
因创伤或者退变导致踝关节力线异常,关节间隙不平行,保守治疗3~6个月仍存在局部疼痛可以考虑SMOT。目前具体适应证尚存在争议,SMOT通常适用于2期或者3a期踝关节OA伴内翻畸形患者,1期或者3b期个案也有报道[6-7]。Colin等[8]认为术前患者行走在相反倾斜度的路面可以缓解局部疼痛,是提示手术疗效较满意的表现。SMOT分为胫骨远端的开放性截骨和闭合性截骨,是否需要同期实施腓骨远端截骨,需要根据病情而定[4]。
当胫距关节面软骨损伤范围超过1/3负重面,不适宜截骨术[2]。因神经系统异常、结缔组织疾病或者感染导致的继发病变不在此讨论中。
3 术前检查
术前检查主要包括负重下踝关节正侧位X线片、后足力线位X线片;核磁共振检查有助于判断关节软骨损伤部位与程度,临近关节有无退变;踝关节三维CT重建可以准确判断是否存在骨赘及其部位。依靠CT数据还可以制备个体化3D打印截骨导板,从而更好地进行个体化精准手术治疗[1]。Beijk等[9]认为负重位的CT分析可能会更真实地反映患者运动状态下的后踝力线。
术前通过负重X线片可常规测定胫骨远端关节面(tibial ankle surface,TAS)角、胫距关节面(talar tilt,TT)角、胫骨侧面关节(tibial lateral surface,TLS)角[4]。TAS即胫骨轴线与胫骨远端关节面的内侧夹角,TT即胫骨远端关节面及距骨关节面之间的夹角,TLS即侧位X线上胫骨轴线与胫骨远端关节面的夹角[10](见图1)。从而规划截骨部位、截骨后撑开角度或者去除的楔形骨块角度。
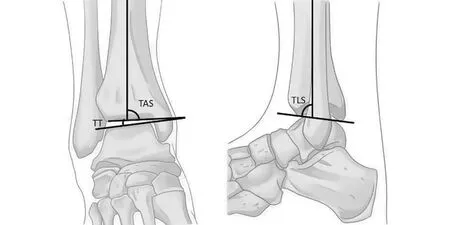
图1 术前角度测量示意图
4 外科技术
手术体位:仰卧位,术区同侧臀部稍垫高,大腿上段使用气囊止血带[1,7]。熟悉关节镜技术的医生通常对踝关节OA患者先实施关节镜探查术,确认是否适宜进行SMOT,然后进行清理术。关节镜清理术中小的骨赘可以在关节镜下切除,大的骨赘也可以在截骨时处理。是否有必要对关节软骨损伤进行微骨折处理,尚存在争议。微骨折是关节软骨治疗的常规术式,机理是诱导骨髓干细胞和生长因子在软骨缺损区域聚集,从而进行组织修复。手术技巧:关节镜下去除损伤和不稳定的关节软骨,然后在软骨下骨表面使用专用尖锥打击形成骨洞,间距3~4 mm,深度2~4 mm。Kim等[11]在术后二次关节镜探查发现,微骨折处理后的创面较术前有明显好转。但是Ahn等[2]术后二次关节镜探查发现,未进行微骨折处理后的创面也较术前有明显好转。笔者认为力线调整是关键,内踝应力改善后即可以出现软骨再生表现,局部是否有必要进行微骨折等处理尚待进一步对照性研究。
截骨术通常分为开放截骨和闭合截骨。开放截骨通过撑开截骨面来调整力线,从而较好地保留了肢体长度,但是撑开角度过大时,切口软组织张力将显著性增加,容易出现皮肤切口并发症。为了减少对局部血供的破坏,应减少骨膜剥离。术中在截骨部位首先钻入1.6~2.0 mm克氏针2~3枚,C型臂透视确认截骨线满意,然后在截骨线钻多个小孔,再用骨刀连接,延伸截骨深度,也可以直接使用摆锯截骨。术中注意避免损伤邻近组织和截骨产生的热损伤。术中还应注意保留截骨对侧的皮质骨,在撑开截骨面时利用骨刀逐步缓慢地进行操作,避免对侧皮质骨折,使截骨部位更稳定[4,12]。闭合截骨是通过去除截骨部位的楔形骨块来实现,截骨面的愈合速度较开放截骨更快,皮肤切口软组织张力不会增加,因此切口愈合不良发生率较低,但是该术式容易导致肢体短缩、肌肉张力下降、踝关节外翻肌力减弱等不足。
3D打印技术促进了足踝截骨术的精准治疗,已在临床逐步试用[1]。依据患者术前CT数据制备的病灶模型可用于术前手术演练、医患治疗沟通等,术中依据个体化截骨导板精准定位,可以节约手术时间和减少术中透视次数,使用目标垫块更可以协助术中判断,甚至还可以制备个体化的金属内植物,强化支撑截骨间隙和固定截骨部位。
4.1 截骨技术 目前主流手术是胫骨远端的开放截骨。切口选择:大部分选择踝关节内侧切口,为避免内植物压迫切口出现并发症,通常切口中央可以向前方弧形凸起,少数选择踝关节前方切口入路。截骨方法:早期选择的胫骨远端截骨线多位于内踝尖的近端4~5 cm,呈水平样,近期多选择倾斜的截骨线,内侧近端截骨部位不变,远端朝向下胫腓联合韧带的上缘(关节线上1.5~2.0 cm),该截骨的骨面为松质骨,且面积较大更容易愈合。Hintermann等[13]认为截骨分为踝上截骨(截骨线位于踝关节上方)、踝下截骨(截骨线位于踝关节下方)、关节内截骨(截骨线朝向关节软骨面),根据畸形特点来选择,可以更好地恢复患者局部的病理生理状态。也有人未进行常规腓骨截骨,使得手术更容易完成,节约手术时间和减少创伤[6,14]。Kim等[4]报道,腓骨截骨与否的两组患者术后随访采用美国足踝外科协会(American orthopaedic foot and ankle society,AOFAS)评分评价后踝功能和疼痛视觉模拟评分(visual analog scale,VAS),结果均较术前明显改善,但两组间比较差异无统计学意义。Ahn等[14]发现SMOT后不做腓骨截骨,常常在负重位X线片上观察到下胫腓联合有增宽表现。而Liang等[15]显示,胫骨联合腓骨截骨对于改善胫距关节面夹角等影像学数据更有帮助,当合并腓骨远端畸形、长度异常或内翻角度超过15 °,单纯实施胫骨截骨达到目标力线存在困难,普遍认为应该加做腓骨截骨,其截骨线位于下胫腓联合韧带近端。除了在冠状面调整角度外,根据患者病情,需要关注是否有必要对矢状位力线进行调整,在截骨区域前方或后方撑开不同角度即可对矢状位力线进行调整。
Beijk等[9]为了明确最适宜的目标矫正角度,分析了33篇病例报道(涉及922个踝关节)后,很遗憾未能总结出具体的最佳矫正角度,不过在总结治疗膝关节OA的胫骨高位截骨术中为踝上截骨术提供了较多经验。他认为通常TAS角术后应当较正常值增加3 °,以避免术后丢失角度导致畸形复发。基于此,近期大部分文献的目标值为93 °~95 °[14]。然而过度的外翻矫正,也将导致外踝出现骨性撞击和局部疼痛。
4.2 固定与植骨 截骨后局部固定首选钢板螺钉内固定,在胫骨远端使用内踝钢板,截骨线两侧各使用3枚螺钉,也有钢板放置前方的报道。腓骨截骨部位首选在腓骨外侧进行钢板螺钉固定,也有使用克氏针固定的报道。Horn等[16]使用多轴环形外固定架进行截骨部位的固定,术后可以对畸形进行持续调整,直至达到预期目标。该技术尤其适用于严重的多平面畸形,涉及软组织平衡或者属于局部感染后遗症的病例。开放截骨后形成的骨缺损通常建议植骨,自体骨与异体骨均可以使用,目前无两者疗效差异的文献报道。
4.3 合并症的处理 (1)踝关节不稳:患者存在外伤史的情况并不少见,是否需要对踝关节韧带损伤进行同期处理尚存在争议。通常认为,对于轻度的踝关节不稳,实施SMOT即可缓解局部疼痛,不需要常规进行外踝韧带修复或者重建。而另外文献认为[2],实施SMOT后应该再次术中评估,若外踝不稳,则需要同期实施外踝距腓前韧带修复术(例如Broström-Gould术式),从而增强踝关节稳定性,避免再次受伤。(2)后踝力线异常:由于影响后踝力线的因素较多,因此当SMOT实施后术中应再次评估后踝力线,必要时考虑跟骨截骨术或者距下关节融合术进一步调整后踝力线。若存在内侧足弓异常,需要同期处理跟骨和调整内侧跖列力线[13,17]。(3)跟腱挛缩:建议采用经皮微创松解延长术,恢复跖行足状态[18]。
5 术后康复
术后早期下肢肌肉收缩锻炼、直腿抬高,术后石膏托固定踝关节功能位,免负重6周,然后复查摄片,指导患者以不痛为前提,在行走靴保护下逐渐负重行走直至骨性愈合,期间可以主动或者被动的间断屈伸活动踝关节[4]。闭合截骨术后康复措施的报道较少,可以参考开放截骨方案。
6 疗效和预后
SMOT术后患者局部的VAS和AOFAS评分均较术前显著性改善,AOFAS可以提高至少20分,其中部分患者的术后影像学表现不尽如人意,但是患者对其疗效仍感到满意。患者术后TAS、TT角度比术前有显著改善[19-20],不过手术前、后踝关节屈伸活动范围是否存在变化,目前意见不统一。Kim等[21]的研究中部分病例术后出现持续性疼痛,二次关节镜手术观察到关节腔出现软组织撞击、滑膜增生等,清理术后患者疼痛有所缓解。Tanaka等[6]认为当软骨损伤达到3b时,手术疗效较3a更差。Lee等[22]认为当TT角度>9.5 °时,其手术疗效较低于4 °时更差,建议手术患者TT角度不宜超过7.3 °。但Colin等[8]认为TT角度与术后临床疗效并无相关性。而Kim等[11]则认为关节软骨损伤程度与手术疗效存在相关性。
Xue等[23]分析文献,患者TAS角由术前84.2 °提高到91.5 °,TLS角由术前79.7 °提高到82.2 °,TT角由术前9.6 °改善到4.8 °,结果数据差异有统计学意义(P<0.01);AOFAS由术前54分提高到80分,VAS由术前5.8分改善到2.5分(P<0.01);并发症包括感染1.3%,延迟骨愈合2.5%,血肿、疼痛、关节纤维化、跗骨窦综合征等6.1%,其中1例静脉血栓,1例内固定断裂;手术治疗失败的主要原因是踝关节OA在术后仍逐渐进展。笔者认为SMOT可以有效调整踝关节力线,是治疗中期踝关节OA的可靠手术,但需要警惕该术式仍存在一定的并发症,难以完全让踝关节疼痛消失。Butler等[24]进行meta分析也获得类似的结论,随访失败率6.8%。研究认为SMOT治疗中期踝关节OA安全有效,该手术可以较好地延缓病程,推迟关节融合或者置换的时间,由于总体随访时间偏短,尚不明确术后对下肢邻近关节的远期影响。
7 展 望
对于踝关节间隙非均匀性狭窄的中期OA,SMOT术是一种有效的术式,对缓解患者局部疼痛和改善功能有显著意义,值得推广应用。未来还需临床多中心协同研究,对于明确最佳的截骨部位及其程度、最佳固定方式以及辅助手术的适应证,准确了解预后将产生积极作用,从而促进临床规范化开展此手术。
