高收率人凝血酶原复合物生产工艺优化
2024-01-04赵良超李冠军马小伟赵东生王明华宋博
赵良超 李冠军 马小伟 赵东生 王明华 宋博
(华兰生物工程股份有限公司,河南 新乡 453003)
人凝血酶原复合物(human prothrombin complex concentrates,PCC)是从健康人血浆中分离纯化的一种促进血液凝固的血浆蛋白制剂,PCC 中发挥功能的主要是人凝血因子Ⅱ、Ⅶ、Ⅸ、Ⅹ(FⅡ、FⅦ、FⅨ、FⅩ)4 种维生素K 依赖的凝血因子,4 种因子均为肝脏合成的糖蛋白。由于4 种因子的等电点(4.1~4.6)和相对分子质量(54 000~70 000Da)等理化性质极为相似,使用常规纯化方法难以将之分离,一般将其作为一个整体制备[1]。PCC 主要用于治疗先天性和获得性FⅡ、FⅦ、FⅨ、FⅩ缺乏证包括:1)FⅡ、FⅦ、FⅨ、FⅩ缺乏症包括乙型血友病,2)抗凝剂过量、维生素K 缺乏症,3)因肝病导致的凝血机制紊乱,4)各种原因所致的凝血酶原时间延长而拟做外科手术患者,5)治疗已产生因子Ⅷ抑制物的甲型血友病患者的出血症状,6)逆转香豆素类抗凝剂诱导的出血。因为PCC 的适应证主要与FⅨ的含量有关,所以通常以FⅨ的效价来计算PCC 的收率,FⅨ的比活性来衡量PCC 的纯度。
目前大多数生产厂家使用二乙基氨基乙基-葡聚糖A50(DEAE Sephadex A50)凝胶两步法进行PCC 制备,且许多厂家在第一步吸附时使用批式凝胶吸附罐[2],其典型工艺为:在凝胶吸附罐中对DEAE Sephadex A50 凝胶进行平衡,从除去冷沉淀的人血浆上清液中提取PCC 粗品,用低离子强度的缓冲液除去吸附能力较弱的杂质蛋白和黏附的其他成分,然后增加缓冲液的离子强度洗脱目标蛋白,通过超滤透析除去小分子杂质,获得PCC,然后再通过S/D 病毒灭活以及第二步纯化得到最终产品。但由于不同厂家采用的工艺参数不同,如:凝胶用量、平衡液、洗涤液、洗脱液配方或者超滤等步骤,所得产品的因子收率不同,甚至有些工艺只能得到三因子PCC(3F-PCC),这种PCC 制品因FⅦ含量低,在治疗上文所述适应证:1)各种原因所致的凝血酶原时间延长而拟做外科手术患者,2)治疗已产生因子Ⅷ抑制物的甲型血友病患者的出血症状,3)逆转香豆素类抗凝剂诱导的出血时效果不如四因子人凝血酶原复合物(4F-PCC)。因此,PCC 中具备一定含量的FⅦ将会提高产品对上述适应证的疗效。
本文通过对PCC 制备的各步骤的研究,如:在吸附步骤提高了4 种凝血因子的收率,洗涤步骤减少了FⅦ的损失并有效去除了杂质蛋白,洗脱步骤提高了产品的比活性,超滤步骤保护了凝血因子效价活性,最终得到成品收率约为62~63 万IU/吨血浆,比活性符合国家药典标准,4 种凝血因子比例较为均衡的4F-PCC 产品。
1 材料与方法
1.1 材料与设备 健康人血浆[华兰生物工程股份有限公司下属的浆站(批号T202301018)]质量符合药典规定。DEAE Sephadex A50 凝胶购自GE Healthcare 公司(货号02-0047-01)。分析仪器,全自动凝血仪由法国STAGO 公司提供,仪器型号为STA-Compact Max,紫外分光光度计由日本岛津公司提供,仪器型号为UV-1900,血凝仪由北京普利生仪器有限公司提供,仪器型号为C2000-4。
1.2 检测方法 1)蛋白浓度检测方法依据«中国药典»2020 版三部通则0731 蛋白质含量测定方法,第三法“双缩脲法”进行测定。2)效价检测方法依据«中国药典»2020 版三部通则3517~3520,使用FⅡ、FⅦ、FⅨ、FⅩ乏浆为基质血浆,采用一期法测定供试样品中FⅡ、FⅦ、FⅨ、FⅩ的效价。3)活化的凝血因子活性检查依据«中国药典»2020 版三部通则3423,加适量稀释剂溶解至FⅨ20IU/mL 进行检定,应符合规定。
1.3 实验设计 实验设计(DOE)是研究正确的设计实验计划和分析实验数据的理论和方法,通过改变过程的输入因素,观察其相应的输出响应的变化,从而获取这个过程的知识,确定各个输入因素的重要性以及各个输入因素如何影响输出响应,并如何达到最优化过程的目的[3]。
DOE 包括正交实验和析因实验,正交实验是处理复杂系统多因素、多水平的一种科学方法。析因实验是研究两个或多个变动着的因素的有效方法,一般设计的实验都为2 水平实验(2k实验)加中心点的实验方案。DOE 实验设计,无论是正交实验还是析因实验,实现重复实验的一种巧妙的方法为选取“中心点”进行重复实验。选取“中心点”并在此安排重复实验的好处,主要是为了进行完全相同条件下的重复,因而可以实验检测出随机误差。
1.4 实验方法
1.4.1 吸附试验 吸附体系包括凝胶与血浆两部分。经评估,我们剔除了可能对血浆产生影响的两项因素:血浆pH 值和血浆电导率,因为对这两项因素的调整可能对提取PCC后的血浆造成影响,进而影响下游产品。另外,我们认为凝胶电导率和pH 值的改变对整个体系的pH 值和电导率的影响很小,因为凝胶仅占整个体系的1.2‰~2.5‰。因此,我们选取凝胶pH 值、吸附时间和凝胶加量作为考察因素,因凝胶加量与pH 可考察的梯度水平较多,为节约实验时间和成本,制定三因素三水平正交实验方案见表1,以FⅨ收率为评价指标,采用Minitab 17 软件进行析因分析,进行初步筛选,确定主要影响因素后,再对多个梯度进行考察,同时验证正交实验结果。
依据上述正交实验结果,确定凝胶加量主要吸附收率主要影响参数。凝胶加量分别按照1.2、1.5、1.7、2.0、2.3、2.5 g/L,于pH=7.6 条件下吸附40min,以FⅦ和FⅨ收率为评价指标进行单因素实验,验证正交实验结果的同时,对凝胶加量的限度范围进行进一步考察。

试验序号吸附时间(min)pH 值 凝胶加量(g/L 血浆)1 607.81.4 507.62 3 607.22 4 507.81.7 5 407.82 6 607.61.7 7 407.61.4 8 407.21.7 9 507.21.4 2
1.4.2 洗涤试验 影响洗涤的主要因素有洗涤液的电导率(主要与NaCl 浓度有关),洗涤的次数以及洗涤的倍数有关,使用minitab 17 软件进行实验设计,选取NaCl 浓度0.175 mol/L、洗涤次数5 次、洗涤倍数2 倍作为中心点进行3次重复实验,考察洗涤液NaCl 浓度、洗涤次数、洗涤倍数对收率、蛋白浓度的影响,评价洗涤效果(表2)。
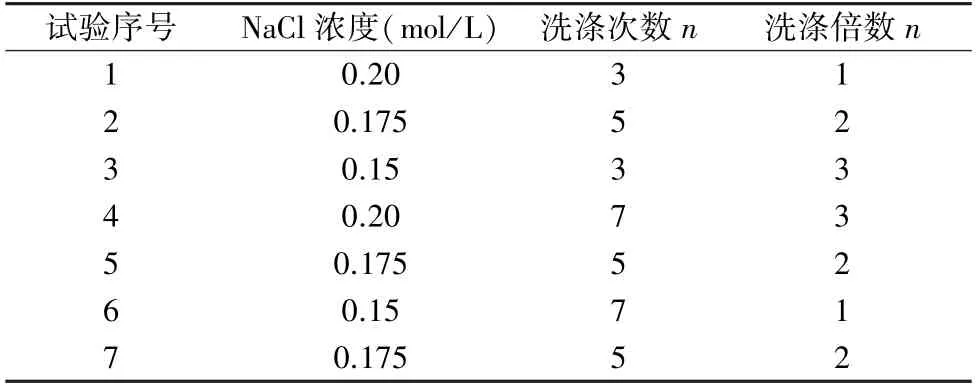
试验序号NaCl 浓度(mol/L) 洗涤次数n洗涤倍数n 1 0.2031 0.17552 3 0.1533 4 0.2073 5 0.17552 6 0.1571 7 0.17552 2
1.4.3 洗脱试验 影响洗脱的因素主要有电导率、洗脱次数、洗脱的倍数有关,考虑到常用洗脱液NaCl 浓度范围为0.5~2.0 mol/L,NaCl 浓度水平较高,浓度范围跨度较大,为初步考察洗脱条件,选取了0.5、1.0、1.5、2.0 4 个NaCl 浓度水平,设置了洗脱的倍数均为1,洗脱次数为3 次和5 次进行考察,通过二因素正交实验(表3)考察洗脱液中NaCl 浓度以及洗脱次数对收率的影响,评价洗脱效果。
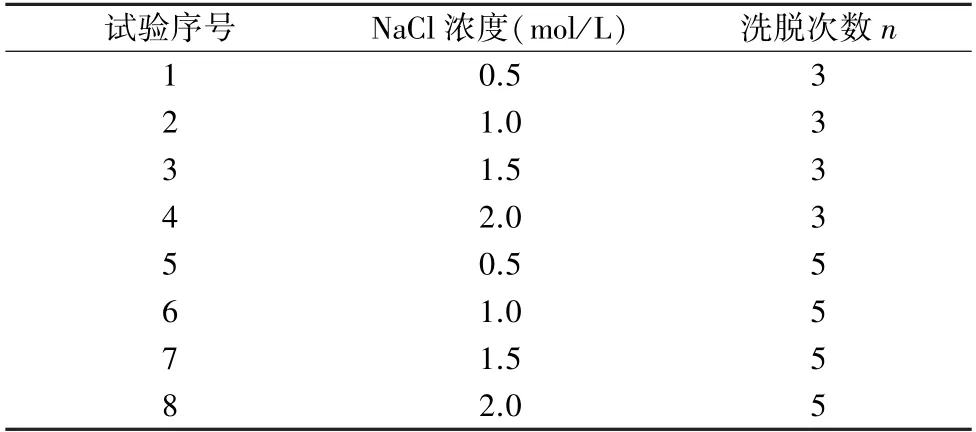
试验序号NaCl 浓度(mol/L)洗脱次数n 1 0.53 1.03 3 1.53 4 2.03 5 0.55 6 1.05 7 1.55 8 2.05 2
1.4.4 超滤试验 选取了常用的两种保护剂肝素和NaCl,以肝素添加量35IU/L 血浆、NaCl 添加量0.1mol/L 为中心点进行重复实验,设计析因实验对超滤步骤进行研究,以FⅨ收率为评价标准,评估保护剂的作用,试验方案见表4。

试验序号肝素(IU/L 血浆)NaCl(mol/L)1 0 0.07 350.1 3 350.1 4 700.13 5 350.1 6 0 0.13 2 7 700.07
2 结果
2.1 吸附试验结果 使用minitab 17 软件进行分析,分析结果见表5,依据实验数据绘制等值线图如图1、图2 所示。

图1 pH 值、凝胶量对吸附收率的影响

图2 时间、凝胶量对吸附收率的影响

项效应系数系数标准误差T 值P 值 方差膨胀因子常量/0.552 81 0.009 74 56.74 0.000 pH 值0.078 2 0.039 10 0.015 30 2.560.125 1.75凝胶量0.213 8 0.106 90 0.014 50 7.380.018 1.52时间-0.019 7-0.009 90 0.014 50-0.68 0.566 1.52 pH 值∗凝胶量0.028 5 0.014 30 0.020 50 0.700.558 2.13 pH 值∗时间 0.030 7 0.015 40 0.020 50 0.750.531 2.13凝胶量∗时间 0.092 1 0.046 00 0.023 30 1.970.187 2.63
由表5、图1、图2 得知,只有当凝胶用量较为充足的时候才能得到较高的收率。可见凝胶用量较pH 值和吸附时间是影响吸附收率的重要因素。
在确定了凝胶用量为主要影响因素之后,针对凝胶用量的使用范围进行了单因素实验进行考察,从图3 的试验结果可以看出,当凝胶加量>2.3g/L 时,FⅨ收率仍有较大的上升幅度。另外具有一定应用意义的是,随着凝胶用量的不断上升,FⅦ效价也不断上升,其上升幅度甚至超过FⅨ效价,如图4 所示。

图3 FⅨ收率折线图

图4 凝胶用量与FⅦ:FⅨ比例的关系
2.2 洗涤试验结果 经试验发现,洗涤液中FⅦ效价较高,而FⅡ、FⅨ、FⅩ几乎不存在于洗涤液中,证明FⅦ最容易在洗涤的过程中损失。而洗涤步骤为关键的去除杂质步骤,洗涤液中蛋白浓度越高,最终产品的比活性也会越高。依据表6 试验数据,针对洗涤液中FⅦ和蛋白浓度使用minitab 17 进行分析如图5、6 所示。
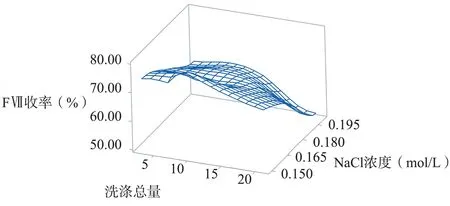
图5 FⅦ收率与NaCl 的浓度,洗涤总量的曲面图
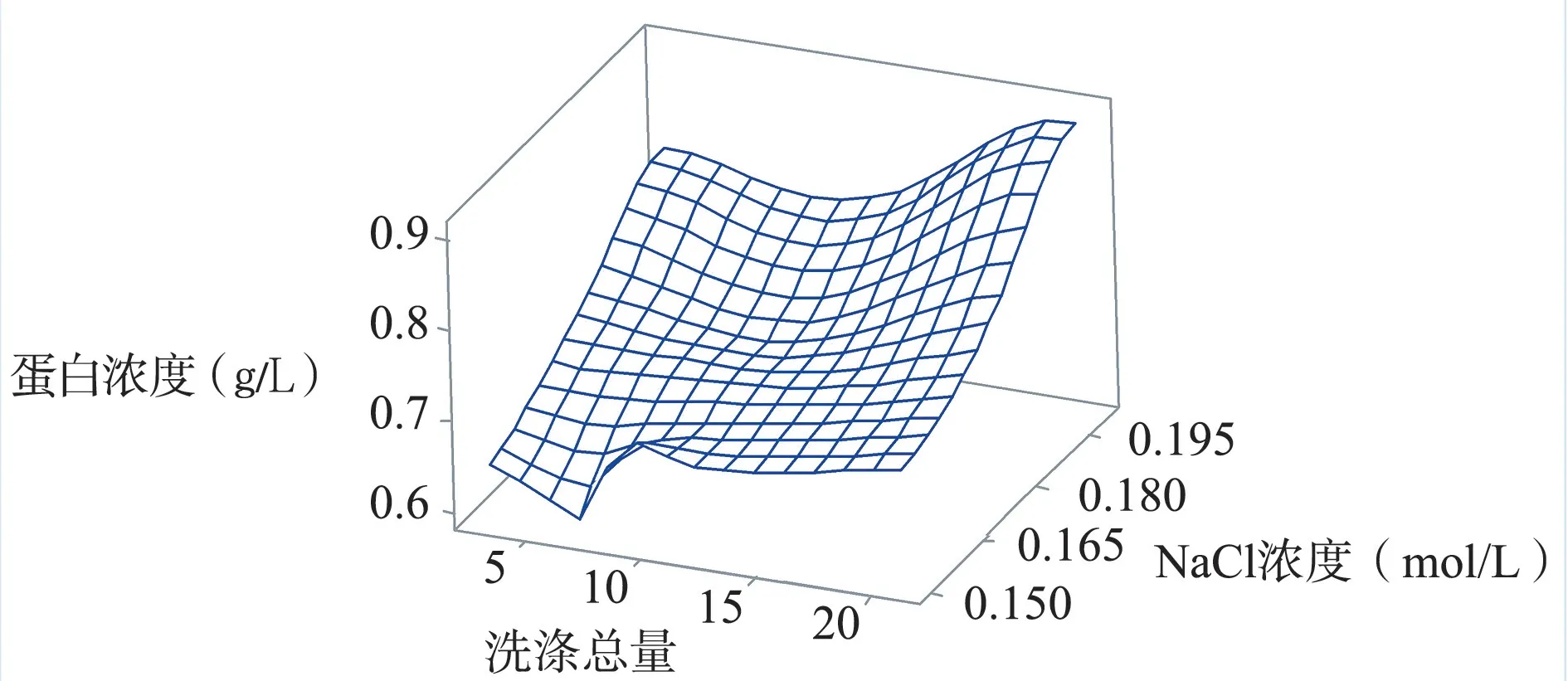
图6 蛋白浓度与NaCl 的浓度,洗涤总量的曲面图
从分析结果来看,FⅦ效价收率与蛋白浓度似乎是相互矛盾的两个响应,很难使两者同时达到较优的情况。

试验序号NaCl 浓度(mol/L)洗涤次数(n)洗涤用量(n)洗涤总量(次数×用量)FⅦ收率(%)蛋白浓度(g/L)10.2031362.360.8 20.175521067.480.7 30.1533978.960.7 40.20732150.830.9 50.175521066.920.7 60.1571774.350.6 70.175521067.420.7
2.3 洗脱试验结果 经试验研究发现,使用含有NaCl 浓度为0.5~2.0 mol/L 进行洗脱时,洗脱3 次以上均可以保证四种凝血因子均被充分回收,实验结果见表7。
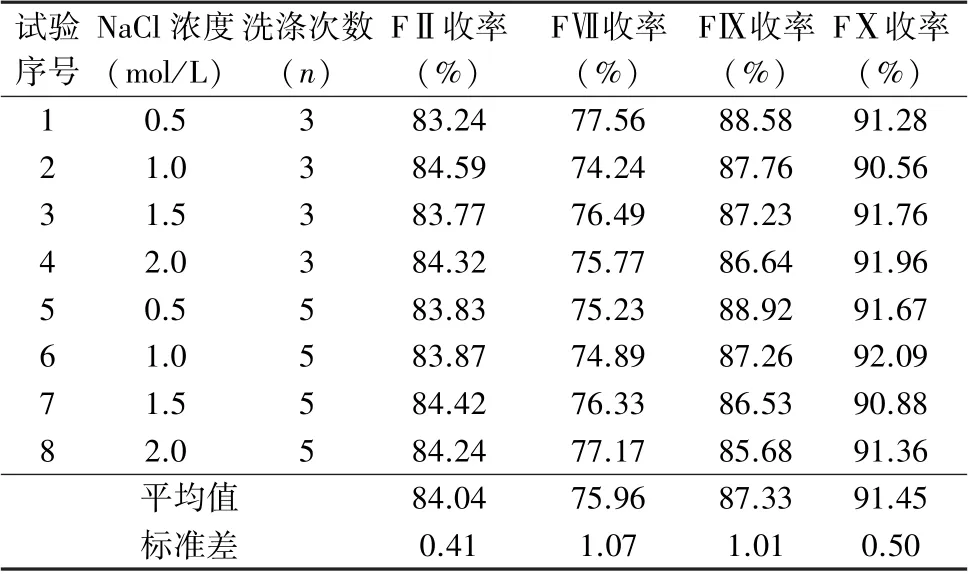
试验序号NaCl 浓度(mol/L)洗涤次数(n)FⅡ收率(%)FⅦ收率(%)FⅨ收率(%)FⅩ收率(%)10.5383.2477.5688.5891.28 21.0384.5974.2487.7690.56 31.5383.7776.4987.2391.76 42.0384.3275.7786.6491.96 50.5583.8375.2388.9291.67 61.0583.8774.8987.2692.09 71.5584.4276.3386.5390.88 82.0584.2477.1785.6891.36平均值84.0475.9687.3391.45标准差0.411.071.010.50
2.4 超滤试验结果 使用minitab 17 分析试验结果如图7所示,从图7 可以看出适量的保护剂可以对凝血因子的效价形成保护作用,活化的凝血因子活性检查符合药典规定。

图7 收率与肝素,NaCl 的曲面图
3 讨论
吸附:从试验结果可以看出,吸附步骤的凝胶使用量是影响人凝血酶原复合物收率的显著因素,而且我们的研究与Heystek 等[4]的研究基本一致,只是在凝胶用量>2.3 g/L 时,我们研究发现收率仍会显著上升,而Heystek 等的研究表示凝胶的吸附能力已经趋于饱和。另外,当凝胶用量越大时洗脱的蛋白浓度越高,所以其结论趋向于使用1.5 g/L 的凝胶。但随着研究发现,后续工艺可以达到洗涤或者分离杂质蛋白的目的。因此,在保证最终产品质量符合药典规定的前提下,适当提高凝胶的使用量是适用的。
另外,我们还研究了FⅦ效价与凝胶使用量之间的关系,从试验结果(图4)我们可以看出,FⅦ效价也是随凝胶用量的增加而增加的,其增加的幅度甚至快于FⅨ效价,尤其是在凝胶用量>1.5g/L 血浆时。据分析,可能是因为当凝胶用量<1.5g/L 时,血浆中FⅨ浓度较高,随着凝胶用量的增加,FⅨ被大量吸附而导致血浆中的浓度降低,相对吸附能力较弱的FⅦ因浓度相对较高的优势在竞争性吸附的过程中占据了上风,所以随着凝胶用量的继续增加至1.5g/L 血浆以上时,被吸附的FⅦ的量高于FⅨ,后续解析下来的FⅦ效价也随之提高。我们的研究为制造因子比例均衡的人凝血酶原复合物提供了研究基础。
洗涤:洗涤效果与最终产品的杂质含量有关,洗涤液NaCl 浓度越高,洗掉的杂质蛋白越多。但NaCl 浓度过高会导致FⅦ损失较大,甚至只能得到3F-PCC。目前依据PCC中FⅦ的含量,将PCC 划分为三因子PCC(3F-PCC)和四因子PCC(4F-PCC),近年来,许多文献研究表明4F-PCC 优于3F-PCC,由于在某些适应证上的疗效更加优秀,如:Luca等[5]的研究表明,4F-PCC 使用最小的剂量既可以完成香豆素类抗凝剂(如华法林)过量导致的国际标准化比值(INR)升高的逆转,而3F-PCC 所需的剂量较大。Megan 等[6]的研究比较了4F-PCC 在治疗服用Ⅹa 抑制剂的颅内出血病人的INR 逆转情况。Muhammad 等[7]的研究表明在外伤性凝血病(COT)的应用中4F-PCC 逆转更快,INR 修正率更高。李泽坤等[8]儿童血友病A 免疫耐受诱导过程中旁路止血的治疗中,对于中轻度治疗以及预防治疗均显示有效性和安全性。所以市场对于4F-PCC 的需求逐步扩大,我国最近批准进行临床研究并上市的PCC 产品均为4F-PCC[9-10]。虽然国内不少厂家4F-PCC 产品陆续上市,但PCC 仍处于供应短缺状态。
Steinbuch 等[11]的研究表明,洗涤液对多种蛋白具有富集作用,且对FⅦ也有数倍的富集作用。这点与我们的研究结果一致,在我们所研究的洗涤液NaCl 浓度范围之内,合理应用了批式洗涤的特点,精心进行DOE 试验设计,发现了某些“异常”的情况,这可能是“少量多次”这种原则反向应用。虽然并未打破“洗涤液NaCl 浓度越高,FⅦ的收率越低”的趋势。但是也为开发者提供了一些思路。
另外考虑到洗涤液对FⅦ的富集作用和绝大多数PCC中都会含有一定量的FⅦa(活化的凝血因子Ⅶ)[12-13],那么过度的降低洗涤液NaCl 浓度,是否会导致FⅦa 富集? 而这些FⅦa 究竟是来源于血浆采集过程中,还是源于制备过程中[14-15]? 这些问题虽然不是本文要讨论的,但也是对于PCC安全性来说相当重要的问题。
洗脱:依据本文的实验结果,洗脱液的NaCl 浓度在0.5~2.0 mol/L 时,洗脱3 次以上,4 种凝血因子均可以被充分洗脱。那么,在此范围之内,适当选择NaCl 浓度较低的洗脱液,应当可以避免收集一些较难以洗脱的杂质蛋白,提高产品的比活性。
超滤:从本文的研究结果来看,超滤过程的控制对于凝血因子的影响是显而易见的。虽然实验结果显示加入肝素钠作为保护剂对凝血因子效价有益[16],但是我们尚不能判断是保护剂抑制了凝血因子活化,还是保护剂防止了凝血因子失活。有研究者的观点认为FⅦa 在肝素存在的情况下被抗凝血酶抑制,但抑制过程是如此的缓慢,以至于可能存在很小的生理意义[17]。本文也认为保护剂可能并非抑制了凝血因子活化,而是防止了失活。因为某些PCC 产品不含肝素也并未表现出成品检测时“活化的凝血因子活性检查”指标明显异常。
综上所述,选用DEAE-Sephadex A50 凝胶,先用平衡液将凝胶平衡至pH7.6,然后按血浆重量1.7~2.5 g/L 加入去除冷沉淀的血浆中吸附40 min。用3 倍凝胶体积的NaCl 浓度为0.150~0.175 mol/L 的洗涤液洗涤吸附后的凝胶3 次,然后用NaCl 浓度为0.5~2.0 mol/L 的洗脱液洗脱3~5 次。超滤透析时使用肝素保护剂35IU,NaCl 0.1 mol/L 对产品进行保护,最终产品收率可达到62~63 万IU/吨血浆,收率较高,适合PCC 的工业化生产。
利益冲突:所有作者均声明不存在利益冲突。
