CO2吸附分离材料的研究进展*
2024-01-03云日娜罗明检
云日娜,罗明检
(东北石油大学 化学化工学院,黑龙江 大庆 163318)
随着全球经济的飞速发展和人口不断增长,CO2的排放量逐年增加,截至2020年全球大气CO2质量浓度已高达412 mg/L,CO2的排放已经成为全球气候变暖的重要原因,实施低碳减排战略迫在眉睫[1]。中国提出力争2030年前实现CO2排放达到峰值(即“碳达峰”)、2060年前实现“碳中和”的“双碳”目标,控制CO2的排放量已经成为当前最为关注的问题[2]。CO2捕集、利用与封存(CO2Capture,Utilization and Storage,CCUS)技术是大幅减少CO2排放,减缓气候恶化,实现可持续发展的主要技术手段,在未来几十年极具发展前景[3]。
将CO2从混合气体中分离是实现CO2利用和封存的前提。CO2常用的分离捕集方法包括吸收法、吸附法、深冷分离法和膜分离法等。吸收法目前在工业上广泛应用,一般在加压条件下利用醇胺类有机溶剂选择性吸收混合气体中的CO2,再通过降压、加热等手段将CO2解吸。吸收法存在溶剂的挥发损失,吸收剂有腐蚀性,过程能耗大等问题。深冷分离法在低温、加压条件下将CO2液化冷凝,实现与难凝组分的分离。深冷分离法不腐蚀设备,且冷凝后产生的CO2便于运输,但压缩和降温过程的能耗大,操作成本较高,并且低温条件下CO2以固体形式析出,容易堵塞管路,影响生产的平稳运行。膜分离法利用CO2与其他分子选择透过性速度不同分离CO2,具有无相变、操作简单等优点,能耗较其他方法低,但是分离效率和产品纯度较低。吸附分离法利用吸附材料对CO2的选择性吸附分离CO2,工艺过程比较简单,吸附剂损失量低,能耗较低,符合绿色环保的发展理念,并且潜在的吸附材料种类多,是目前CO2分离捕集的研究重点。
高效吸附剂是吸附分离技术的核心。沸石分子筛、金属有机骨架、碳基材料等多孔材料都具有高效分离捕集CO2的潜力。作者对这些材料在CO2吸附分离中的应用进行了详细综述,并对其应用前景进行了总结与展望。
1 分子筛材料
沸石分子筛是传统的吸附分离材料,由于其自身的优异性质,至今仍是应用最广泛、研究最深入的吸附剂。分子筛晶体内具有较强的极性和静电场,可以选择性吸附极性分子或易极化分子。虽然CO2分子偶极矩为零,但是具有较强极性的四极矩,因此CO2可以与沸石分子筛的阳离子具有强烈的相互作用,有利于其在沸石上的吸附[4]。此外,CO2临界温度为31.2 ℃,很低的压力下就能在分子筛的微孔内进行微孔填充。因此,对于CO2与其他小分子组成的混合气体来说,CO2分子优先在分子筛吸附,可以实现含CO2混合气体的分离,并且分子筛还具有以下特点。(1)通过简单离子交换的方式可调变孔径尺寸与酸碱性质;(2)通过调变合成原料的配比可在一定范围内调变分子筛的硅铝比,从而改变表面极性和电场,合成比表面积大、孔径分布均匀的分子筛;(3)通过原位封装等手段可引入能够与气体分子选择性配位的不饱和金属中心,从而提高吸附分离的选择性。分子筛及改性的分子筛材料在CO2吸附分离中具有广泛的研究和应用。
1.1 分子筛的CO2吸附性能
蒋文彬等[5]以经酸化处理后的凹凸棒石黏土(以下简称凹土)为硅源,铝酸钠为铝源,利用水热法合成13X分子筛。由于凹土中含有质量分数为1.67%的K2O,在沸石骨架中引入了K+。K+的引入使合成的13X分子筛的CO2吸附选择性比商品13X大幅度提高,由6.29提高至14.53,并且保持了3.32 mmol/g的CO2吸附量。Kongnoo等[6]以棕榈油厂粉煤灰为原料,采用碱熔法合成了13X沸石,对13X沸石产品进行酸活化,增加了沸石的中孔体积以增强其CO2吸附能力,将CO2吸附量提高至6.42 mmol/g。Krachuamram等[7]采用硅酸钠溶液+Al(OH)3和硅酸钠粉末+偏铝酸钠2种原料搭配合成NaX分子筛,并用十六烷基三甲基溴化铵和庚烷进行修饰。总体上,第二种原料搭配的NaX分子筛性能更好,在303 K下对CO2的吸附量为5.08 mmol/g,CO2相对N2的选择性为116。孙锋等[8]以水热法合成NaY型沸石吸附剂,并用溴化钠浸渍法对沸石进行改性,25 ℃时CO2吸附量为3.74 mmol/g,改性后吸附剂的CO2吸附量为4.05 mmol/g,相较于未改性的吸附剂性能提升了8.4%。Hwang等[9]采用碱熔法和水热合成法合成了4A型沸石,比表面积、孔体积和商业沸石相当,显示出对CO2的高吸附能力。将4A沸石作为骨结构进行材料改性,改性后的沸石吸附量为5.9 mmol/g。鲁景山等[10]采用外加晶种的方法,四丙基氢氧化铵(TPAOH)为模板剂合成了自堆积ZSM-5分子筛。n(TPAOH)∶n(SiO2)∶n(Al2O3)=4.5∶15∶1,w(晶种)=3%,t=170 ℃,晶化2 h,合成分子筛的CO2吸附量比商品ZSM-5分子筛提高13%,CO2吸附量为1.13 mmol/g。Wahono等[11]用不同浓度盐酸处理天然丝光沸石-斜发沸石,脱铝过程中方解石晶相基本被脱除,微孔和介孔的比表面积和孔体积均有所增大,CO2吸附量提高。
总体上,用于CO2吸附的分子筛主要是微孔分子筛。这是因为CO2临界温度为31.2 ℃,可在25 ℃附近填充到微孔内。实际上,CO2吸附量的测定多在10~30 ℃、(100~400)kPa下进行。分子筛的CO2吸附量主要取决于分子筛的孔体积,MFI结构的13X、Y分子筛的理论孔体积分数为27.4%,LTA结构的A型分子筛的理论孔体积分数为21.4%,因此,CO2吸附量均较高;MFI结构的ZSM-5的理论孔体积分数为9.8%,MOR结构的丝光沸石的理论孔体积分数为12.3%,HEU结构的斜发沸石的理论孔体积分数为9.4%,因此,这些分子筛的CO2吸附量均较低。增加介孔体积和总孔体积也有利于CO2吸附能力的提高[6],尤其是酸化处理后,主要是由于介孔表面提供了吸附位。较高压力条件下,CO2可在介孔内发生毛细管凝聚,因此介孔材料的CO2吸附量在加压条件下可大幅度提高。例如,将压力由0.2 MPa提高至3.0 MPa,CO2在HCl处理过的天然丝光沸石-斜发沸石上的吸附量可由1.35 mmol/g提高至5.20 mmol/g[11]。
1.2 分子筛的有机胺改性
CO2是一种酸性气体,对分子筛表面进行功能化处理,提高分子筛与CO2的相互作用,也是提高分子筛CO2吸附量和吸附选择性的重要方法。
有机胺类材料的胺基可提供电子,具有一定碱性,有机胺功能化可改进分子筛的CO2吸附能力。张中正等[12]采用浸渍法将聚乙烯亚胺(PEI)负载到介孔KIT-6分子筛的表面,功能化后CO2的吸附量和选择性比功能化前分别提高6.0、7.2倍,改性后的吸附剂在378 K条件下可完全再生。李誉等[13]研究了用3-胺丙基三甲氧基硅烷(APTES)、四乙烯五胺(TEPA)和PEI改性的ZSM-5/MCM-48复合微/介孔分子筛的CO2吸附性能、吸附量均随负载有机胺量的增大先增大后降低,3种改性剂的最大吸附量分别为1.58、4.97和3.28 mmol/L,APTES和TEPA混合使用时吸附量为5.82 mmol/L,最佳吸附温度均为60 ℃。Madden等[14]采用APTES和TEPA对β分子筛进行改性,CO2分压为0.015 MPa时,质量分数为25% APTES改性样品的CO2吸附量为4.7 mmol/L;总体上,改性后的CO2-TPD峰约在100 ℃。Kwon等[15]研究了含水条件下—OH、—NH2和—COOH等基团对β分子筛CO2吸附性能的影响,发现苄胺官能团化增强了沸石的疏水性,阻碍了对H2O的吸附,在25 ℃、10.5 kPa条件下苄胺官能团化后CO2的吸附量可由0.86 mmol/g提高至1.28 mmol/g。郭萌等[16]将三乙烯四胺(TETA)聚合得到超支链聚合物(HBP),并将其浸渍到SBA-15分子筛和SBA-15/氧化石墨烯(GO)上,t=75 ℃,SBA-15-HBP和SBA-15/GO-HBP的CO2吸附量为1.0和1.5 mmol/g。
常规分子筛对CO2的吸附为物理吸附,有机胺改性后物理吸附转化为化学吸附为主,有利于吸附量和吸附选择性的提高。但是,由于化学吸附作用力增强,有机胺改性后最佳吸附温度一般提高至60~100 ℃[12-14,16],脱附温度也相应提高,必然提高脱附再生的能耗。在烟道气的分离过程中,由于烟道气温度较高,有机胺改性分子筛的高温性能可成为其应用中的优势。
1.3 分子筛的疏水改性
CO2混合气体中一般有水的存在。水是强极性分子,将优先吸附在分子筛表面,从而降低CO2吸附性能。对分子筛表面进行疏水改性可提高对CO2的吸附量和吸附选择性。分子筛与有机高分子复合材料可提高吸附过程中的抗水性。
Chi等[17]提出了在聚丙烯酸酯基(PA)微珠中原位生长分子筛的方法,制备用于燃烧后烟气中CO2捕集的NaY@PA复合材料。与纯净NaY相比,NaY@PA复合材料对CO2吸附量提高了17.9%,CO2吸附量为3.435 mmol/g,对H2O的吸附量降低了36.6%。为了进一步降低水的吸收,在NaY@PA表面包裹金属有机骨架材料ZIF-8,合成了具有双分子层复合结构的NaY-ZIF@PA材料。NaY-ZIF@PA的H2O吸附量降低了54.8%,CO2吸附量为2.624 mmol/g,保证了高效的CO2吸附。
2 金属有机骨架材料
金属有机骨架材料(MOFs)是由有机配体和金属离子或团簇通过配位键自组装形成的具有分子内孔隙的有机-无机杂化材料。MOFs材料大多具有化学性质稳定、孔隙率高、比表面积大、密度低和孔道可调节等特点[18-21]。并且,多种MOFs材料在经活化处理后可展现出配位不饱和的活性金属位点[22-24],可以设计成特定化学或物理性质的功能材料[25-26]。除了结构可调性高以外,MOFs材料在比表面积方面也显著优于分子筛,比表面积最高为7 310 m2/g[27]。一直以来都认为MOFs材料的骨架刚性不变,而柔性MOFs的发现,打破了对这一概念的认知[28]。柔性MOFs受外界温度和压力的影响会出现特有的两步吸附阶梯现象。一定温度下,达到开口压力吸附曲线会明显上升,未达到该压力时不会发生吸附现象,对于不同的气体分子来说,由于表面作用的不同会对应不同的开口压力,因此柔性MOFs材料可用于开口压力不同的N2、CO2、CH4的吸附分离[29]。
Liang等[30]通过水热法制得具有多种高密度活性位的Cu(Ⅱ)金属有机骨架材料FJI-H14,该材料具有很好的耐酸碱性能,298 K,0.1 MPa条件下CO2吸附量为171 cm3/cm3(146 cm3/g)。并且,FJI-H14可催化模拟烟道气(80 ℃,0.085 MPa N2,0.015 MPa CO2)中的CO2与环氧化合物反应转化为环状碳酸盐,吸附-催化的协同效应进一步提高了该材料的应用潜力。Park等[31]报道了Zn-MOF(PCN-123)材料,该材料可在紫外或加热条件下发生异构化反应,实现CO2吸附能力的调控。t=25 ℃,PCN-123的CO2吸附量为22.9 cm3/g;采用紫外线照射处理1 h后,单晶测试表明有机配体异构化为顺式结构,吸附量下降至16.8 cm3/g;再通过60 ℃热处理20 h后有机配体又异构化为反式结构,CO2的吸附量升至26.4 cm3/g。Zhou等[32]采用一步合成法成功制备了双金属MIL-101(Cr,Mg)材料,掺杂的Mg均匀分散在晶体材料中,Mg2+与对苯二甲酸的羧基反应形成了Mg—O。掺杂的Mg2+不仅提高了材料的水稳定性,而且相比于纯的MIL-101(Cr)材料其CO2吸附性能提高了大约40%(298 K和0.1 MPa条件下3.28 mmol/g),CO2/N2选择性提高4倍。杨萍等[33]以Mg、Ni为中心金属、十二烷基苯磺酸钠(SDBS)为模板剂,采用溶剂热法合成了不同组成的HP-MOF-74(MgxNi1-x)样品,在273 K和100 kPa的条件下,HP-MOF-74(Mg0.50Ni0.50)的CO2吸附量为4.864 mmol/g,HP-MOF-74(Mg0.25Ni0.75)的CO2选择性为2 263,吸附量和选择性均优于传统Mg-MOF-74。Lei等[34]改变冷凝回流温度制备了系列MOF-74(Ni)材料,丰富的Ni2+及微孔使CO2吸附量为8.29 mmol/g,远高于已报道的MOF-74-Ni、UTSA-16和DA-CMP-1等材料。Li等[35]合成了具有多种吸附位点(μ—OH,N—H,N—N和H—C)的MOFs-303(Al),该材料CO2吸附量为5.10 mmol/g,循环使用50次后依然保持良好的吸附能力,可用于CO2-N2、CO2-CH4的分离。Nandi等[36]利用单一小分子配体(4-吡啶羧酸镍)制备了孔径为0.35和0.48 nm的超微孔MOF Ni-4Pyc,该材料的CO2/H2选择性为285,1 MPa和298 K下的CO2吸附量为8.2 mmol/g,CO2扩散系数为13X的2倍。
Shen等[37]在25 ℃条件下合成了柱层状的金属有机骨架材料dptz-CuGeF6,这种材料具有0.525 nm的超微孔,孔径分布窄,0.015 MPa和0.1 MPa下CO2吸附量分别达2.17和3.23 mmol/g,并且,dptz-CuGeF6具有很好的抗湿及抗强极性溶剂性能。
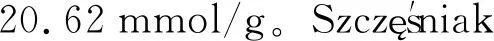
MOFs材料种类多,吸附容量大,但同样也存在很多缺点,例如合成金属有机骨架材料的有机配体价格昂贵,依靠配位键组装的MOFs材料的热/水热稳定性差,很大程度上限制了MOFs材料的工业应用。为了获得理想的气体吸附材料,MOFs材料还需要从以下方面进一步开展研究。(1)通过改变有机配体分子的长度和官能团调节孔径和孔道尺寸[40-41];(2)对金属中心或有机配体进行功能化修饰,在孔道中引入功能性位点[42-43];(3)增加MOFs材料骨架结构中开放的金属位点数量[44-46];(4)制备柔性MOFs材料。这些手段可提高MOFs材料的酸碱稳定性、热稳定性以及目标气体的吸附量和吸附选择性。
3 碳基材料
碳基材料具有比表面积大、微孔结构丰富、耐酸碱性强和化学性能稳定等特性,在气体的吸附和储存中得到了广泛的应用[47],用于CO2捕集也有如下独特的优势[48]。(1)碳基材料对水蒸气不敏感,水蒸气不会影响CO2在碳基材料上的吸附,对处理工业烟气有重大意义;(2)碳基材料热效应低,容易再生,能有效降低吸附过程的能耗;(3)碳基材料的制备成本较低,利于大规模的工业化生产;(4)碳基材料可以通过表面功能团改性提高吸附性能。目前,活性炭、碳分子筛、活性碳纤维等传统碳基材料均已经在工业上应用于CO2的吸附;新型碳基吸附材料,包括球形活性炭、石墨烯、掺杂多孔碳、有序多孔碳、碳纳米管及其他碳基材料也在研究开发中。碳基材料的研究主要集中在提高CO2吸附量、CO2选择性及再生性能,改进的方式主要有调控其孔道结构和表面改性等。
3.1 活性炭
活性炭主要由碳元素构成,同时还有少量的氢、氯、硫、氮等异质元素和灰分,常为黑色粉末、颗粒、块状的固体无定型多孔碳材料,通常通过煤、果壳、石油沥青等含碳物质经过预处理、炭化、活化等步骤制备得到[49]。低温炭化及高温活化是制备活性炭的核心工艺[50]。碳化过程产生的无孔材料不适用于吸附,所以一定要进行活化处理。作为优异的吸附材料,可以通过水分、灰分含量测定、粒径分布、碘吸附值、表观密度等方面的测定结果评估活性炭的品质。活性炭按原料来源分为植物类活性炭(如椰壳、木质素、纤维素等)、矿物类活性炭(如煤、石油等)和有机类活性炭(如橡胶、蔗糖等)。
Li等[51]以稻壳炭作为原料,KOH为活化剂,制得孔径小于0.7 nm或1 nm的微孔活性炭,样品在0 ℃、CO2吸附量分压为0.01和0.1 MPa时的吸附量分别为2.11和6.24 mmol/g。Ganesh等[52]以油棕空果串为原料,先水热法处理再用KOH活化得到活性炭,样品的比表面积为2 510 m2/g,微孔体积为0.55 cm3/g,在25 ℃和0.1 MPa条件下的CO2吸附量为3.71 mmol/g,且重复使用10次不损失吸附容量。宋雪等[53]分别用碱金属(K)、碱土金属(Ca、Mg)和重金属(Fe、Cu、Ag)对椰壳活性炭进行改性,对比改性前后活性炭的CO2/CH4吸附分离性能,发现金属离子改性后活性炭的比表面积、总孔体积和微孔体积下降,中孔体积增大。金属离子改性使活性炭的表面极性提高,有利于CO2的吸附量提高和CH4的吸附量降低,CO2/CH4分离因子可提高约30%。Ning等[54]研究了利用K2CO3改性的微波椰壳活性炭,发现改性后K2O的作用以及介孔的增加,大幅提高了吸附剂对CO2的吸附量,CO2/CH4的分离系数可提高至7.42,高于多数报道的活性炭的CO2/CH4分离系数。Luo等[55]以酒糟为原料制备活性炭,并研究了KOH、K2CO3、KHCO3、K3PO4和NaOH的活化效果。KOH的活化效果最好,比表面积和微孔体积随KOH用量的增加和活化温度的提高而增大,最大为2 950 m2/g和1.63 cm3/g。KOH与活性炭质量比为0.5,700 ℃条件下活化样品的CO2吸附容量最大,0.1 MPa条件下,273.15和298.15 K下分别为6.34和4.26 mmol/g。除了碱及碱金属盐改性,周绪忠等[56]将活性炭在乙醇胺中进行浸渍改性,改性后的CO2吸附量为4.165 mmol/g,是改性前的4.4倍。
活性炭的CO2吸附量主要取决于微孔表面积和微孔体积,对活性炭进行活性,促进微孔结构的形成是研究的重点;同时,改性组分与CO2的相互作用也有利于活性炭CO2吸附选择性的提高。
3.2 石墨烯
石墨烯(Graphene)是由sp2杂化的C原子构成的二维网格结构物质,仅具有单原子层厚度,是世界上最薄的材料,因此被称为“超级膜”[57]。石墨烯具有良好的机械性能和化学稳定性、高不渗透性、较大的比表面积,因此在膜分离和吸附分离领域均有较大的应用潜力。由于芳香环上致密的电子密度会阻止气体穿过,任何气体都无法穿过完美结构的石墨烯[58]。所以,需要在石墨烯上“造孔”获得多孔石墨烯,解决气体选择性穿过石墨烯的问题。“造孔”过程中需要调控石墨烯的层数、孔的大小、形状、分布及对孔道进行功能化处理,使不同种类的气体分子以不同的速率穿过,从而达到分离混合气体的目的。
杨志远等[59]以石墨粉(G)为原料,采用改进Hummers法制备氧化石墨(GO),通过热剥离及KOH活化制备出类石墨烯多孔材料(GPM),20 ℃、3 MPa条件下CO2、CH4和N2饱和吸附量分别为33.13、11.45和7.80 mmol/g,CH4/N2、CH4/CO2、CO2/N2的分离系数依次为2.86、1.93、5.54。Haque等[60]合成了氮原子摩尔分数7.67%和4.33%的氮掺杂石墨烯材料,比表面积为278 m2/g,在25 ℃、0.1 MPa条件下对CO2的吸附量为4.43 mmol/g,CO2/N2选择性为42。
除了活性炭和石墨烯,碳纳米管、活性碳纤维等材料在CO2吸附分离中也有广泛研究。在这些碳材料中,活性炭具有原料易得,制备和活化工艺成熟,成本低等优点,在工业应用中具有良好的应用前景。石墨烯、碳纳米管等材料虽然具有良好的性能,但由于不易于大规模制备,成本高,短期内难以实现工业应用。
4 结束语
含有高浓度CO2的混合气体主要有烟道气、合成气和天然气,这几类混合气体中CO2之外的典型组分分别为N2、H2和CH4。因此,吸附材料应该对CO2和N2、CO2和H2或者CO2和CH4的吸附能力有显著差异才能完成吸附分离。
(1)CO2临界温度为31.2 ℃,临界压力为7.38 MPa。以微孔材料为吸附剂时,约25 ℃ CO2在较低压力下就能填充到微孔材料的孔腔;N2、H2和CH4等临界温度低,常规微孔材料在约25 ℃对其吸附量相对较低。因此,含有微孔的分子筛、MOFs、活性炭等多孔材料均具有吸附分离CO2的潜力,提高微孔体积是改进这些材料CO2吸附分离能力的关键。此外,较低温度和加压条件下CO2可在介孔内发生毛细管凝聚。因此,增加介孔体积也是提高CO2吸附分离能力的手段,介孔吸附材料在合成气、天然气等含CO2的高压混合气体的分离中具有潜力。
(2)CO2是酸性气体,与碱性位作用力强。因此,对多孔材料进行胺基功能化,利用CO2与胺基功能化材料的化学作用可提高CO2的吸附容量及吸附选择性。胺基功能化材料化学吸附CO2后需要在较高温度才能再生,其用于分离温度较高的烟道气中的CO2更有优势。
(3)一般使用CO2-N2、CO2-H2和CO2-CH4作为模拟组分研究吸附材料的CO2分离性能,实际混合气体中还含有以H2O为代表的极性组分及其他重组分(例如天然气中的C2、C3组分)。因此,吸附剂走向CO2分离工业应用的过程中还需要考虑这些组分的影响。
(4)分子筛和MOFs及改性后的材料具有催化CO2转化的作用,可以在吸附分离的同时直接将CO2转化为化学品,是未来研究中的重要方向。
此外,CO2的吸附分离属于大规模生产过程,吸附剂的生产成本、稳定性、寿命、强度等是吸附剂工业应用需要考虑的问题。因此,生产工艺成熟,成本较低的分子筛和活性炭更具工业应用前景;MOFs、石墨烯、碳纳米材料等尽管已经展现出良好的性能,但还需要进一步解决生产成本、稳定性等问题,才能具备规模化分离CO2的价值。