铁基纳米粒子氧还原电催化剂的研究进展*
2024-01-03邓方健王明笛
邓方健,王明笛
(东北石油大学 化学化工学院,黑龙江 大庆 163318)
随着社会的不断发展,人类对能源的需求量日益增大,由于地球化石能源存在不可再生性,为促进可再生能源的开发和应用,现阶段已经研发出很多先进的电化学转换装置,其中包含燃料电池和金属-空气电池,因其具有能量转化高效、性能安全、污染程度低等特点,广泛应用于新能源领域[1-2]。氧还原反应(Oxygen reduction reaction,ORR)就是这些能源转化装置中的阴极反应,但动力学缓慢是制约其性能的关键因素。为解决这一难题,研究人员仍在不断探索氧还原电催化剂的发展,现已得到认可的贵金属及其衍生物催化剂包括Pt/C、RuO2、Ir等[3]。尽管贵金属催化剂表现出优越的性能,但是高成本、稀缺性和低稳定性阻碍了其实际应用,减缓了大规模商业化的步伐[4]。因此,开发低成本、高活性、高稳定性、长寿命的氧还原电催化剂已经成为了目前燃料电池发展的热点。铁基催化剂由于铁元素在地球储量大、成本低而备受青睐,在目前研究的催化剂中,碳载体上的氮配位铁基催化剂最有前途[5]。作者介绍了ORR的机理,从含铁化合物氧还原电催化剂、铁基杂原子掺杂氧还原电催化剂等方面综述了铁基纳米粒子氧还原电催化剂的研究现状,并总结了提升氧还原电催化剂活性、稳定性的方法及展望未来发展趋势。
1 ORR机理
在由电催化方式实现能源转换的过程中,以燃料电池为代表的能源转换装置,其阴极反应通常为ORR。对ORR机理的探讨直接影响催化剂对ORR的活性以及研发成本。ORR的电子转移途径,见图1[6]。
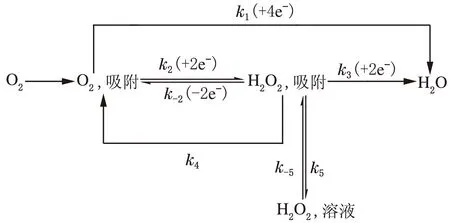
图1 ORR途径示意图
在酸性介质中,Pt基电极上的ORR反应主要产物是水;当Pt电极表面有强吸附阴离子、氢原子、惰性金属原子或有机物时,部分氧气也可在电极表面不完全生成H2O2。
在酸性条件下,4e-转移的ORR见式(1)。

(1)
在碱性条件下,4e-转移的ORR见式(2)。

(2)
具体的反应路径见式(3)~(7),其中式(4)~(7)分别对应4e-转移过程[7]。

(3)

(4)

(5)

(6)

(7)
在碱性条件下2e-转移的ORR见式(8)~(9)[8]。
(8)

(9)
在酸性条件下2e-转移的ORR见式(10)~(13)[9]。
(10)
(11)
(12)

(13)
式中:*为活性位点吸附位置。
2e-途径即氧气部分被还原为H2O2的过程不可避免,这与催化剂自身的性质有关。4e-转移反应是燃料电池高效能量转化的主要途径,氧气得到4个电子直接生成OH-,无其他中间产物。相比之下,2e-转移反应过程会生成H2O2中间产物,而且H2O2具有一定的腐蚀作用,会破坏质子交换膜,大大缩短燃料电池寿命,影响电池的稳定运行。因此,ORR催化剂要对4e-转移途径具有很高的选择性才能实现高效催化[10-11]。
2 含铁化合物氧还原电催化剂
目前,除广泛使用的Pt/C等贵金属催化剂之外,在储量众多而价格低廉的非贵金属催化剂中,催化性能优异的铁基催化剂因其在碱性条件下接近甚至优于Pt/C催化剂的性能而被广泛关注和研究,有望取代Pt/C等贵金属催化剂成为具有广阔发展前景的ORR电催化剂。在所有可用的非贵金属替代品中,铁基催化剂具有低成本、高电导率及碳载体与其他组分之间的诱导协同作用等优点受到广泛研究[12]。其中铁元素的存在状态为含铁化合物、铁单原子、铁合金、其他铁基复合物等。
2.1 含铁碳化物
Fe/Fe3C催化剂具有良好的氧还原催化活性,主要是由富含碳的前驱体与含铁化合物热解制备而成。热解产物为包覆在碳基体中的含铁颗粒,含铁粒子与碳基体之间的相互作用导致C的能态显著下降,电子从Fe转移到C,从而导致ORR活性增加。此外,包覆着含铁颗粒的碳壳增强了催化剂的整体稳定性[13]。
Zhang等[14]采用无模板缩聚热解法合成了铁氮共掺空心碳球催化剂(Fe-M/G/H)。以三聚氰胺、d-葡萄糖、六亚甲基四胺为原料,缩聚得到高氮碳球。通过热解制备了含Fe-Nx和Fe3C的空心微球。空心微球结构不仅暴露出更多的活性位点,而且促进了O2的传质。Fe-M/G/H在碱性介质中具有较高的极限电流密度(5.09 mA/cm2)和半波电位(0.80 V),具有较好的ORR性能,近似商用Pt/C。

2.2 含铁氮化物
纯Fe3N无法作为ORR的活性位点,一般需要与Fe-N-C活性位点产生耦合,利用纳米Fe3N与碳骨架中Fe-N-C位点的协同作用,从而产生良好的ORR性能。与其他化合物不同,含铁氮化物中的氮原子以空隙填充的方式嵌入铁晶格中,形成的间充型Fe3N纳米粒子一般具有较高的导电性、稳定性。
Xue等[15]以核桃壳为前驱体,随后经铁离子掺入和NH3气氛中热解,制备了一种Fe3N纳米颗粒和Fe-N-C活性位点共存的高活性ORR电催化剂(Fe3N/Fe-N-C)。通过一系列表征强有力地证明了Fe3N纳米颗粒与Fe-N-C活性位点的共存,Fe3N纳米粒子与掺氮碳骨架中Fe-N-C位点的协同作用,使其具有良好的ORR性能。Fe3N/Fe-N-C-900具有良好的起始电位和半波电位;具有更小的Tafel斜率(70 mV/dec),优于Pt/C的Tafel斜率(82 mV/dec);在稳定性测试中,表现出较好的长期稳定性和优异的抗甲醇能力,综合性能优于Pt/C。
将Fe3N纳米颗粒固定在CN载体框架中,使合成的含Fe3N纳米粒子的催化剂产生更多的活性位点。载体为碳材料,N的电负性大于C,说明N的得电子能力强,会从C上得到电子,致使碳材料上分布大量正电荷,有利于增强氧分子的吸附并产生可以活化氧分子的活性位,促进了扩散动力学,使氧还原性能、材料导电性、稳定性能大大提升。
2.3 含铁硫化物
迄今为止,Fe-N-C类电催化剂一般是将含铁盐和含氮前驱物与碳底物随机混合热处理而成。尽管热解过程简单,但部分Fe3C活性位点受到厚碳层的聚集和覆盖,再加上由于高温过程中Fe团聚和Fe3C的稳定性差,导致金属-空气电池的ORR效率较低,因此需要开发新的Fe相与其他Fe相(如Fe硫化物)的掺入研究。
Mmako等[16]采用热解和热退火方法合成了具有良好ORR活性的氯、硫共掺杂碳纳米管(SClCNTs)。通过在噻吩中对ClCNTs进行热退火,将FeS2纳米颗粒加载到ClCNTs表面。在ClCNTs中加入硫后,CV曲线可以观察到ORR峰显著增强,ORR活性大大增强,这归因FeS2纳米颗粒牢固地结合在ClCNTs表面。
有研究表明,在还原氧化石墨烯(rGO)内嵌入FeS2和FeS,耐久性均有明显提升。动力学研究表明,rGO内嵌入FeS2的氧还原过程主要通过4e-途径发生,FeS2中所具有的S—S在ORR 4e-途径中发挥主要作用,但rGO内引入FeS的氧还原过程主要通过混合途径发生,即2e-和4e-途径[17]。也有例外,如FeS@C具有优异的电催化ORR性能,在碱性介质中,半波电位达到0.80 V,属于完全4e-途径[18]。碳材料容易被杂原子掺杂以提高其性能和催化活性,S原子容易诱导邻近的C原子和N原子极化,有助于增强ORR活性。S/N共掺杂碳层增强了电导率和耐久性,与FeS的协同作用,共同促进了ORR性能。
2.4 含铁磷化物
为了满足实际应用要求,还需要合理设计出更多的铁基物种提高现有催化剂的活性。其中,P掺杂Fe-N-C材料备受关注。因为P不仅在3p轨道上拥有孤对电子,给相邻的C传递相当高的正电荷密度,引起碳晶格的不对称自旋密度的变化,且还具有空的3d轨道容纳O2的孤对电子[19]。P的引入与Fe和N产生协同效应,通过Fe与P之间的相互作用提高掺杂水平;与Fe形成Fe—P,可作为氧还原催化的活性组分,例如常见的FeP和Fe2P纳米颗粒。
Wang等[20]采用微乳液模板法首次合成了类似杨梅的聚苯胺纳米球(PANI-NS)。在水热处理过程中,Fe被嵌入PANI-NS中,进行热解得到嵌有Fe2P纳米粒子的杨梅状N/P富集碳纳米球(Fe2P/NPCs)。电化学测试结果表明,Fe2P/NPCs表现出优异的ORR电催化活性,半波电位为0.82 V,极限电流密度为5.58 mA/cm2,与商业Pt/C相当,具有良好的持续稳定性和更高的甲醇耐受性,经4 000圈CV循环,半波电位仅衰减14 mV。其氧还原性能优异的原因在于,Fe2P/NPCs具有丰富的Fe2P纳米粒子,可作为ORR的活性位点。
非金属P是一种具有丰富价电子的元素,有助于调节金属的电子结构,易吸引邻近金属的电子,改善含氧物种在金属表面的吸附情况。在高温条件下,P容易与金属成键,形成FeP或Fe2P等纳米粒子,易形成碳载体包覆结构,为活性中心提供更多附着位点,而且经常与Fe-Nx活性位点起协同作用,共同促进ORR。
2.5 含铁氧化物
由Fe3O4纳米颗粒负载在碳材料上组成的杂化材料,是一种具有高效活性的ORR电催化剂。Fe3O4纳米颗粒的形成,大多依赖于载体的多孔结构,该结构不仅影响Fe3O4纳米颗粒的传质和活性位点,对其成核也具有很大影响[21]。通过密度泛函理论(DFT)计算表明,在Fe3O4基团的支持下,Fe-N-C对O2的吸附更强,这可能会增加氧还原过程的反应物浓度,能够提高整体活性[22]。
Ajmal等[23]采用单步微波辅助策略将Fe3O4纳米颗粒加载到多壁碳纳米管上(Fe3O4@CNTs),同时合成对比样Fe3O4和CNTs。电化学测试结果表明,与Fe3O4和Pt/C催化剂相比,制备的Fe3O4@CNTs的半波电位分别正移了240 mV和20 mV,表现出优异的循环稳定性和甲醇耐受性。Fe3O4@CNTs氧还原活性的提高可归因于CNTs与Fe3O4纳米颗粒之间的协同作用。
纯Fe3O4纳米颗粒在电池反应中导电性、稳定性都很差,在目前的研究中,大多采用碳材料负载Fe3O4纳米颗粒,一方面,可以防止Fe3O4在电解液中溶解,以增强稳定性;另一方面,使其暴露更多的活性位点(Fe3O4和Fe-Nx),以提高ORR效率。
3 铁基杂原子掺杂氧还原电催化剂
由机理可知,ORR过程主要分为一步4e-途径和两步2e-途径,从能量转换效率及电池寿命考虑,应尽量避免H2O2的生成,即尽量避免2e-反应过程。ORR电子转移的数目主要取决于催化剂,因此研发高效催化剂是当前研究热点。非金属杂原子(N、P、S、B)掺杂的碳材料具有良好的催化活性、稳定性、抗甲醇能力等优点,这可明显改善多孔碳材料的表面化学活性和反应稳定性,与C或N之间能形成多种杂化键,形成新的活性位点,有效调节电子结构,提高材料导电性,增强氧还原催化活性。因此,利用B、P、S等杂原子进行掺杂可以作为提高阴极ORR性能的一个重要方法。
3.1 硼掺杂
碳的电负性为2.55,硼的电负性为2.04,B相对C是缺电子原子,将B引入C的晶格中,会破坏C sp2杂化结构的对称性和自旋密度,即B可以作为电子受体促使C发生费米能级转移,有助于降低禁带宽度,可以改变碳材料的电荷分布,从而改善碳材料的表面润湿性、导电性及催化活性。许多研究表明,硼氮共掺杂的碳材料中,B、N、C之间会形成多种杂化键,使其具有独特的电子性能,有可能形成新的B-N-C活性位点,也可能形成BC3以增强碳载体的导电性,从而增强氧还原性能。

与单掺杂相比,杂原子的二元掺杂能形成更独特的电子结构。N的电负性大于C,而B的电负性小于C。2种元素掺杂在一起,由于协同作用,会产生更多的催化活性位点,使二元掺杂碳纳米材料的催化性能优于单掺杂碳纳米材料。
3.2 磷掺杂

Li等[25]开发了一种新型的Fe-N-C电催化剂,其中Fe-Nx活性位点被P原子修饰。在酸性电解液中,其半波电位达到0.858 V,与未掺杂P的材料相比,半波电位提高了23 mV。DFT计算表明,P掺杂可以降低决速步骤的热力学过电位,从而提高氧还原催化活性。
更多的研究结果表明,P具有更为优异的氧还原活性。P的最外层有5个电子,说明P具有较强的电子流动性,当P与C耦合后,极易形成C—P,能够加速碳材料的石墨化程度,提高稳定性的同时暴露出材料更多的缺陷,这种特性使P掺杂成为优化材料催化活性的常见方式。但是过多引入P则会降低材料2e-ORR途径,少量P的存在会促进吡咯N的形成,从而提高了2e-ORR途径的选择性。
3.3 硫掺杂
近年来,在Fe-N-C材料中掺杂S被证明是提高酸性介质中ORR活性的有效策略。然而,S原子只能掺杂在碳材料的边缘或缺陷处,这可能限制了S修饰的Fe-Nx活性中心基团的数量。虽然引入S原子有部分局限性,但会使材料中吡啶N、石墨N及Fe-Nx活性中心的含量增多,而且噻吩S能够提高材料的导电能力,增加材料缺陷,调整材料的酸碱性,改变碳载体的电子结构,使过电位降低,促进O2的吸附,有利于ORR的发生。
Ma等[26]合成了一种具有分层多孔结构的S掺杂Fe-N-C催化剂。结果表明,Fe-N-C的大孔和中孔结构在ORR过程中显著增加了Fe-N4活性位点的数量,并为Fe-N-C的微观结构和纳米结构的结合提供了理想的亲氧/疏水表面,促进了ORR过程中O2的运输。碳骨架中的S掺杂提高了单个Fe-N4组分的内在活性。将其应用于锌空气电池中,其功率密度达到453 mW/cm2。

4 结束语
对铁基纳米粒子氧还原电催化剂中Fe颗粒组成形式、活性中心的存在方式及二者之间相互作用的最新研究进展进行了介绍和讨论。从中发现传统的Fe NPs-N-C系列催化剂未经改性,其氧还原活性不佳,目前常用的提升催化剂氧还原活性的方法是掺入杂原子(B、S、P)改变电子结构,或者使Fe纳米颗粒变成化合物的形式。Fe颗粒存在的形式有很多种,例如碳化物、氮化物、磷化物等,但是各种含铁化合物,其自身并不具有强大的氧还原活性,容易团聚、稳定性差。因此,需要含铁化合物与Fe-Nx活性中心共存且发生协同作用。当引入杂原子时,杂原子并不一定与金属成键,很可能仅与碳载体成键,无法形成铁化合物,但是形成的杂原子掺杂的碳载体,可以增加催化剂的导电性,也可以提供氧还原活性位点。引入适量杂原子的方法是当前解决Fe纳米粒子催化剂稳定性差、活性低的最优解决办法,也是Fe基纳米粒子催化剂能成功应用于金属-空气电池的关键手段。但该类型催化剂仍存在含铁化合物颗粒易从载体脱落的问题,因此,有效形成碳层包覆结构稳定纳米颗粒以增强其氧还原性能,成为接下来亟需解决的问题。