体外冲击波治疗骨折愈合的疗效及炎症因子变化动态研究
2024-01-01赵兴东林牧陈明勇赵学平刘木波马庆庆
赵兴东 林牧 陈明勇 赵学平 刘木波 马庆庆△
(1.贵州航天医院骨科,贵州 遵义 563000;2.贵州航天医院中心实验室,贵州 遵义 563000)
在创伤骨科治疗中,患者行骨折术后常出现肢功能障碍、骨延迟愈合,甚至骨不愈合等并发症。此症状一直被视为常见的、较难有效治疗的难题,是目前临床研究的热点之一[1]。体外冲击波疗法(ESWT)为近30年应用于骨科领域的新方法,研究证明其具有明确的促进血管生成、抗炎、镇痛、诱导成骨、激活损伤修复的作用,改善关节功能,也正因为这些生物学特性才在骨科领域得到广泛应用,它在促进骨折愈合方面的研究一直是热点[2]。本文探讨体外冲击波治疗骨折愈合的疗效及炎症因子变化动态,旨在探究体外冲击波对骨折愈合的临床疗效和作用机制进行探究,以期为提高临床骨科治疗提供参考依据。
1 资料与方法
1.1一般资料 选取2019年7月至2021年10月于本院收治的无软组织缺损的闭合桡骨远段骨折内固定术后患者80例,随机分为体外超声组和对照组,各40例。体外超声组中男18例,女22例,平均年龄(56.33±2.48)岁,平均体质量(22.18±2.00)kg/m2,平均手术时间(78.66±6.03)min,平均术中出血量(30.47±2.19)ml;对照组中男21例,女19例,平均年龄(56.10±1.49)岁,平均体质量(22.09±1.48)kg/m2,平均手术时间(78.39±5.10)min,平均术中出血量(30.76±1.49)ml。纳入标准:年龄18~78岁;符合闭合桡骨远段骨折的诊断标准,且顺利完成内固定术;确定为新鲜骨折;患者知情同意,生命体征稳定;本医院伦理委员会批准了此次研究;具有完整的临床资料。排除标准:手术禁忌症患者;肿瘤、转移瘤、结核患者;备孕期、妊娠与哺乳期妇女;合并高危传染性疾病者。两组患者的一般资料对比无显著差异(P>0.05)。
1.2方法 所有患者均进行骨折手术,术前常规药物治疗及对症处理,对其进行常规石膏固定处理。待患者符合手术条件时,对其进行切开复位内固定术,切口位于桡掌侧。体外超声组采用体外冲击波治疗(强度2.5 bar,10Hz,根据患者对疼痛承受情况选择相应治疗量1 000~3 000/次),根据骨折部位、断端间隙和横截面积的大小等因素综合考虑,施行治疗参数个体化。依据骨骼的粗细及强度,术后第9天开始治疗,每隔3 d冲击治疗一次,6次为一个疗程(C型臂下定位骨折线,避开内置物,于腕部桡侧选择治疗位置2~3点)。对照组:不给予体外冲击波治疗。所有病例术后其余治疗均相同,在术后24 h内对其进行规范预防感染治疗,定时对其切口进行清洁换药,并指导其进行康复锻炼。
1.3观察指标 治疗后24周,比较两组患者疗效;记录两组治疗后24周出现的并发症情况;所有患者在治疗后4周与治疗后24周,采用酶联免疫法检测血清IL-6及IL-13等炎性因子表达变化情况;记录两组患者的骨折愈合时间。
2 结 果
2.1两组患者总有效率对比 治疗后24周,体外超声组的总有效率100.0%(治愈34例,显效3例,有效3例)高于对照组的90.0%(治愈24例,显效6例,有效6例,无效4例)(χ2=4.211,P<0.05)。
2.2两组患者并发症发生情况对比 治疗后24周,体外超声组发生骨质疏松1例,并发症发生率3.3%;对照组发生骨质疏松5例,骨延迟愈合1例,并发症发生率15.0%。体外超声组并发症发生率低于对照组(χ2=3.914,P<0.05)。
2.3两组患者骨折愈合时间对比 体外超声组的骨折愈合时间(10.33±1.38)周少于对照组的(13.29±1.09)周(t=10.646,P<0.05)。
2.4两组患者血清IL-6及IL-13变化对比 体外超声组治疗后4周与治疗后24周的血清IL-6及IL-13水平均明显少于对照组(P<0.05)。见表1。
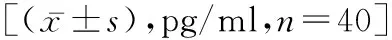
表1 两组治疗后不同时间点的血清IL-6及IL-13变化对比
3 讨 论
目前体外冲击波疗法已在骨肌疾病临床治疗领域广泛应用,尤其在骨延迟愈合及骨不愈合方面的得到了广泛的应用。研究证实体外冲击波疗法具有机械效应、空化效应、热效应等物理学特性,由此产生了一系列的生物学效应,以达到高密度组织裂解作用,扩张血管和血管再生作用,从而达到促进组织损伤修复重建作用[3]。本文结果显示,治疗后24周体外超声组的总有效率高于对照组(P<0.05);体外超声组的骨折愈合时间都少于对照组(P<0.05),表明体外冲击波疗法在闭合桡骨远段骨折内固定术后的应用能提高治疗效果,促进患者骨折愈合。特别是体外冲击波疗法可通过机械传导将脉冲能量直接作用于骨组织和骨周围软组织,造成点状骨膜下出血及陈旧骨痂微骨折,再通过反复刺激以引发骨折炎性反应,从而释放各类炎性因子及生长因子。同时体外冲击波疗法可增强骨髓间充质干细胞分泌及增殖活性,以利于血管新生及成骨方向分化,促进成骨细胞活化和黏附,并抑制其脂肪方向分化,从而有利于新骨生成[4]。
本文结果显示,体外超声组治疗后24周的并发症发生率少于对照组(P<0.05),表明体外冲击波疗法在闭合桡骨远段骨折内固定术后的应用能减少并发症的发生。可能是因为早期应用体外冲击波治疗有利于通过机械效应减轻肌腱黏连,减少瘢痕形成,促进软组织肿胀消退,从而促进功能的早期康复,进而减少骨质疏松、骨延迟愈合并发症的发生。
白细胞介素-6(IL-6)是维持体内平衡的原型细胞因子,当通过感染或组织损伤破坏体内平衡时,IL-6立即产生并通过激活急性期和免疫应答有助于宿主防御这种紧急应激[5]。白细胞介素13(IL-13)是一种多功能T辅助2型(Th2)细胞因子,可以减少炎症反应[6]。IL-13可通过抑制单核细胞释放炎性因子,控制炎症反应。上述炎性因子在机体创伤后均出现不同程度的改变并发挥其功能,是目前研究的热点问题,而这些功能同样对骨折创伤愈合过程具有不可或缺的重要作用[7]。体外冲击波疗法的最终效应是通过作用于干细胞、内皮细胞、成骨细胞及炎细胞等黏附、 增殖及分化阶段而发挥作用[8]。本文结果显示,体外超声组治疗后4周与治疗后24周的血清IL-6及IL-13水平都明显少于对照组(P<0.05),也表明将体外冲击波作用于骨折内固定术后早期治疗,以达到调节炎性细胞因子来实现的合成代谢和分解代谢的平衡促进恢复骨动态平衡。
综上,通过体外冲击波疗法应用于闭合桡骨远段骨折内固定术后,能减少并发症的发生,还可有效调节炎症因子动态变化情况,从而能提高治疗效果,促进患者骨折愈合。
