肝豆状核变性并发肝性脊髓病5例临床分析及文献复习
2023-12-18王佳炜方明娟刘力生杨任民胡文彬
王佳炜, 方明娟, 刘力生, 王 训, 杨任民, 胡文彬
肝豆状核变性(hepatolenticular degeneration,HLD)是一种常染色体隐性遗传铜代谢障碍疾病,临床以肝脏和神经系统受损为主要表现。50%~80%的患者以肝脏损害为首发或主要症状[1],因肝硬化就诊的HLD 患者达35%~45%[2]。肝损伤后造成的物质代谢紊乱不仅影响到脑,还会影响到脊髓和周围神经,出现肝性脊髓病(hepatic myelopathy,HM)[3]。HLD 并发HM(HLD-HM)的临床报道甚少。现回顾性研究安徽中医药大学神经病学研究所附属医院2018年1月—2023年2月收治的5 例HLD-HM患者病例资料,总结其临床特点及预后,并复习国内外文献报道病例,以提高各科医师对本病的认识。
1 对象与方法
1.1 研究对象
2018年1月—2023年2月在安徽中医药大学神经病学研究所附属医院住院HLD 患者中,选出并发HM 的患者。HLD 和HM 的诊断分别参考《中国肝豆状核变性诊治指南2021》[4]和《肝性脊髓病的研究进展》[5],且入组患者均无饮酒史及病毒性肝炎病史。本研究为回顾性病例系列分析,已通过安徽中医药大学神经病学研究所附属医院伦理委员会批准,并获得了患者家属的知情同意。
1.2 方法
1.2.1 资料收集 回顾性采集HLD-HM 患者临床资料,包括一般情况、病史、体格检查;实验室检查包括血常规、肝功能、凝血功能、铜生化、血氨及ATP7B基因等指标;影像学检查包括腹部彩超(肝胆胰脾肾、门静脉系统)、角膜K-F 环、肝脏CT/MRI、脊髓MRI 和头部MRI 等;神经电生理检查包括肌电图和脑电图;对治疗和临床结局进行回访及总结,并复习国内外相关文献。
2 结 果
2.1 一般情况 2018年1月—2023年2月在安徽中医药大学神经病学研究所附属医院住院的HLD患者共5 518例,并发HM共5例。5例HLD-HM患者中男性4 例,女性1 例;HLD 发病年龄10~31 岁,HLD 病程12~264 个月;出现HM年龄16~32 岁,HM病程2~60个月,3例患者HM症状在HLD发病后1年出现,2 例患者在HLD 发病后17年出现HM 症状。肝型1例,肝脑型4例,3例患者有经颈静脉肝内门体分流术(TIPS)病史;Child-Pugh 分级:3 例为B 级,2例为C级(见表1)。
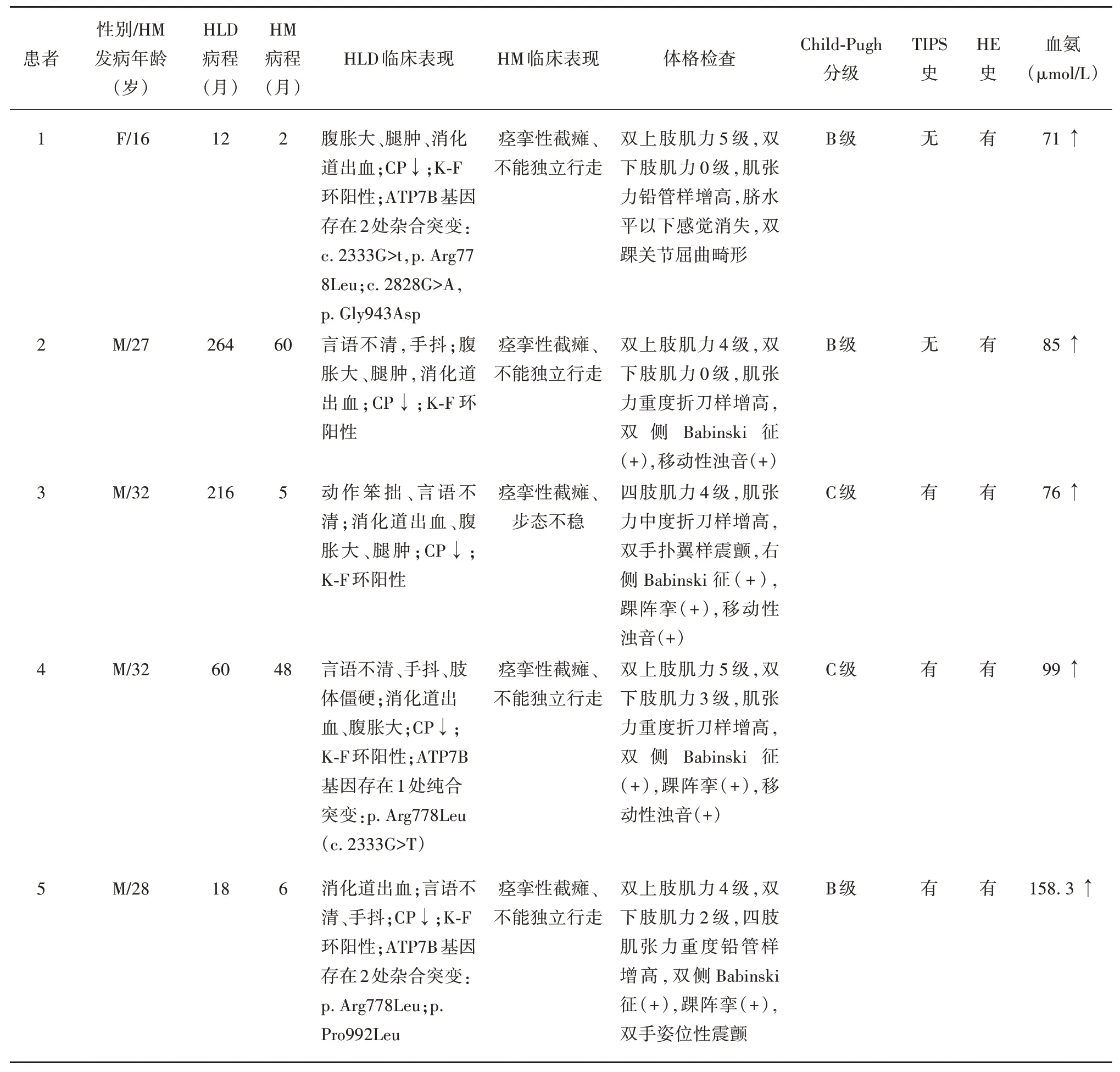
表1 肝豆状核变性并发肝性脊髓病5例临床资料
2.2 临床表现 HLD 临床表现:5 例患者在发病过程中均有脾大、低蛋白血症、腹腔积液、消化道出血及肝性脑病(hepatic encephalopathy,HE)等肝硬化表现;3 例患者因检查发现“脾大”,1 例患者在外院行脾切除术时诊断为HLD,2 例患者在脾切除术后渐出现肢体僵硬、双上肢不自主抖动等锥体外系症状;2 例患者以腹胀大、腿肿为主要表现;1 例患者以动作笨拙、言语不清等神经系统症状为主要表现。
HM 临床表现:3例患者因消化道出血行TIPS 治疗后渐出现双下肢僵硬、无力,影响行走。2 例患者不能独自站立和行走。5 例患者查体均有双下肢肌力明显减退,其中2 例患者双下肢肌力为0 级;双下肢肌张力均呈中重度铅管样/折刀样增高,双侧膝腱反射亢进,双侧踝阵挛阳性,双侧Babinski 征阳性(见表1)。
2.3 实验室检查结果 5 例患者均存在不同程度的贫血(最低者Hb 34 g/L);5例患者Alb均明显减低(最低者Alb 16.5 g/L)、总胆红素轻微升高、血氨明显升高;铜生化中血清铜、铜蓝蛋白及铜氧化酶明显减低;5 例患者凝血功能均不同程度地异常;5例患者的血肝炎病毒学指标均为阴性(见表2)。

表2 肝豆状核变性并发肝性脊髓病5例临床资料
2.4 影像学检查和电生理检查结果 5 例患者的腹部B 超均发现肝硬化,3 例患者腹部B 超发现腹腔积液;5 例患者的门静脉B 超发现门静脉增宽;1例患者肝脏CT示侧支循环形成;2例患者肝脏MRI示肝脏内信号不均,形态欠佳,食管胃底静脉曲张;4 例患者头部MRI 示脑干、双侧基底节区异常信号;2 例患者脊髓MRI 示胸髓信号不均,斑片状异常信号灶;5例患者角膜K-F环均为阳性;3例患者肌电图双腓总神经、双胫神经各段CMAP 潜伏期延长,双腓肠神经SNAP潜伏期延长,双胫神经H反射潜伏期延长;4 例患者脑电图示背景θ、δ 波增多,背景脑电明显变慢(见表2)。
2.5 治疗及转归 5 例患者均予以低铜低蛋白软食,根据患者体重,予以二巯丙磺酸钠20~30 mg/kg 联合肝豆片排铜,促肝细胞生长素保肝,精氨酸谷氨酸注射液或/和门冬氨酸鸟氨酸联合支链氨基酸静脉注射、乳果糖口服、白醋灌肠改善氨代谢,胞磷胆碱活化脑代谢,甲钴胺营养神经等。针对患者贫血,予以纠正贫血,其中1 例予以多次输注悬浮红细胞纠正贫血。并定期予以输注白蛋白纠正低蛋白血症及消胸腔积液/腹水。出院后继续服用青霉胺排铜,门冬氨酸鸟氨酸颗粒及利福昔明改善氨代谢等。
1 例患者在住院期间因上消化道出血死亡。2 例患者症状持续加重,于外院行“肝移植”治疗,其中1 例患者临床症状好转。2 例TIPS 史患者转外科行血管内支架内限流术治疗。除1 例患者死亡外,另4 例患者高氨血症、贫血、低蛋白血症、腹水及肌力均得到不同程度的改善。
3 讨 论
HM 是继发于慢性肝病的一种较为罕见的神经系统并发症,临床以缓慢进行性、对称性的痉挛性截瘫为主要表现[6]。杨明芝[7]统计562例HM的病因发现,仅有4 例患者合并HLD。通过PubMed、中国知网等数据库对HLD-HM进行了文献检索,共收集7例HLD-HM 报道病例(包括本院1 例)。2018年1月—2023年2月,笔者单位共收治5 518例HLD患者,统计发现合并HM 者共5例,其患病率约为9.06/万,男女比例为4∶1,发病年龄16~32 岁,HM 多在HLD 发病后10月~17年确诊。国内首例HLD-HM 病例由我院杨任民教授于1991年报道,并认为早期积极地治疗,半数以上患者有恢复的可能[8]。
HLD-HM 的发病机制尚未完全阐明。结合文献复习及本研究5 例患者,考虑其发病为铜中毒、氨中毒、营养缺乏和血流动力学改变等多种因素共同作用的结果。HLD 患者体内过多的铜沉积在脊髓,可直接导致脊髓病变[9]。孙刚等人[10]发现体内铜过度升高,会加速氧与有机物的氧化反应,使脂质过氧化,进而加重脊髓损伤。除了铜中毒外,TIPS和高氨血症也是HM 形成的主要因素[11]。研究发现[12]20%~50%的TIPS 术患者会在TIPS 术后4年出现HM 症状,但本组3 例TIPS 术患者在术后2~12月出现症状。中枢神经系统对氧的利用受血氨水平的影响,血氨增高可以造成神经系统功能减退[13]。肝功能受损导致对毒性物质的解毒能力下降,和侧支循环的开放引起门体分流导致大量的有毒物质不经过肝脏解毒,含氮产物等有毒物质直接进入体循环,并在体内积聚,有毒物质可透过血脑屏障对脑、脊髓进行损伤,最终诱发HM[14,15]。本组5 例和侯志峰[9]报道的2 例患者均有高氨血症,其中2 例患者病程较长,其间反复出现血氨轻度升高,患者逐渐出现下肢无力及僵硬感等症状,与文献[11]报道相符,即血氨水平与HM 病情轻重程度不平行。HM 的临床过程分为神经症状前期、肝性脑病期和脊髓病期。但本研究中2 例患者先出现脊髓损伤症状/体征,后出现意识模糊,由此认为HLD肝硬化后出现HM 与HE无明确先后关系,但与血氨水平持续偏高有关,血氨水平持续偏高的患者脊髓损伤症状偏重。因此,我们推测HE与HM之间存在一定的关联性。
监测血氨水平对诊断及治疗HM 有一定的价值,但导致HM 的因素绝非仅仅是血氨升高。HLDHM 患者多以脾大、消化道出血为首要表现,与文献[9,16,17]报道一致。但与既往文献报道不同的是,本研究中5 例患者均存在一定程度贫血、低蛋白血症及门静脉高压,严重者Hb 低至34 g/L,Alb 低至16.5 g/L。张俊峰[18]研究发现贫血患者的VitB12水平下降,VitB12等B 族维生素缺乏,可引起脊髓及周围神经损伤。在本组3 例患者肌电图提示神经源性损害,考虑除了与铜沉积损伤有关外,营养物质的缺乏也是原因之一。另有研究发现[19]中重度贫血可以导致血管的平均血流速度增快、低蛋白血症使血液携氧能力不足、门静脉高压时血流动力学改变,以上因素均可导致脊髓的血液供应不够充分,逐渐出现缺血缺氧及局部营养障碍,最终导致HM[5]。由此推测贫血、低蛋白血症和门静脉高压与HM 的发生有直接关系。
针对原发疾病的治疗以促进肝损害及脊髓功能的修复,是改善HM 临床症状和预后的关键[20]。赵玉红及贾淑培等人[16,17]分别对HLD-HM 患者予以排铜、保肝及对症等治疗后,患者双下肢肌力恢复,可独立下床行走。本组1 例患者予以排铜及降血氨治疗后,其双下肢肌力有所改善,并能短距离地行走,但随访2年后,该患者因上消化道出血而死亡。与日本一学者[21]报道一致,认为HM 早期病理机制是脊髓脱髓鞘改变,及时控制血氨,可逆转患者的临床症状。赵洪伟[22]对TIPS术后的HM 患者行支架内限流术治疗后随访,发现大部分患者的血氨明显下降、肌力提高、HE 发作程度减小及生活能力较前有所改善。本组2例TIPS术患者再次入外科行血管内支架内限流术治疗,1 例患者血氨恢复至正常范围,肌力改善;另1 例患者目前是术后半个月,复查血氨恢复至正常,HM症状未见明显改善。肝移植后临床症状改善程度与HM 病程有关,如果早期进行肝移植,HM患者的临床症状可以恢复,但对晚期患者的作用不大[23],可能与疾病晚期脊髓轴突丧失有关[24]。本研究中2 例患者行肝移植治疗,其中1 例发病后2 个月即行肝移植术治疗,术后临床症状改善;而发病5年后行肝移植术治疗的患者,除血氨等肝损伤指标恢复正常外,神经系统症状无明显改善。
早期诊断和及时治疗对预防HLD 肝损伤和神经精神症状的出现或/和加重等至关重要[25]。由本研究得知,HLD 肝损害程度与HM 的预后密切相关,大部分HLD-HM 病情均有不同程度的改善,其原因:(1)排铜及护肝治疗后,肝损害可以向好的方向转化[1,2];(2)沉积在脊髓的铜得以排出后,减少了氧与有机物的氧化反应,进而减轻脊髓损伤[9,10]。但由于本研究是回顾性研究,病例数较少,且部分病例缺少详细的体格检查记录以及电生理检查,缺少客观指标作为预后评估。因此,我们准备在今后诊治HLDHM 患者过程中完善检查,为进一步研究HLD-HM临床特点及治疗提供依据。
综上所述,HLD-HM 患病率较低,多为男性,临床缺少特异性表现,临床医生对该病的认识相对不足,故容易被误诊和漏诊。目前,HLD-HM 的原因尚不清楚,仍需进一步研究。临床缺少治疗HLD-HM的有效方案,预后较差。因此,各科临床医生应重视HLD 的诊断、治疗,防止肝损伤进展;在接诊不明原因的肝硬化、脾大的患者时,可考虑行铜代谢指标检查,并谨慎评估TIPS 术的适应证,对预防HLD 并发HM有重要意义。
伦理学声明:本研究方案经由安徽中医药大学神经病学研究所附属医院伦理委员会审批[批号:2023伦字(03)号],患者及家属均签署知情同意书。
利益冲突声明:所有作者均声明不存在任何利益冲突。
作者贡献声明:王佳炜负责论文设计、起草论文;方明娟、刘力生负责临床资料收集、绘制图表;王训负责论文修改;杨任民对论文中病例的入组整体把关;胡文彬负责拟定写作思路、指导撰写文章并最后定稿。
