软骨肉瘤的18F-FDG PET/CT 征象
2023-12-13宋乐韦峰庄洪卿韩嵩博张卫方
宋乐,韦峰,庄洪卿,韩嵩博,张卫方*
1.北京大学第三医院核医学科,北京 100191;2.北京大学第三医院骨科,北京 100191;3.北京大学第三医院肿瘤放疗科,北京 100191;4.北京大学第三医院放射科,北京 100191;*通信作者 张卫方 tsy1997@126.com
软骨肉瘤居常见恶性骨肿瘤第3位[1],好发于四肢及骨盆,常导致患者局部肿胀、疼痛。软骨肉瘤90%以上为普通型,大部分组织学分化较好,局部复发或转移风险较低。组织学分化是软骨肉瘤治疗决策和预后评估的重要指标[2]。但软骨肉瘤组织分化具有异质性,穿刺活检可能难以反映肿瘤的整体分化,导致低估肿瘤的分级,影响后续治疗[3]。影像学检查可以反映病理分化,指导穿刺活检,对于软骨肉瘤的诊治有重要价值[4-6]。目前应用CT及MRI评估软骨肉瘤的报道较多,但部分病变缺乏特征性影像表现而难以诊断[7-8]。18F-FDG PET/CT已经广泛用于恶性肿瘤的评估[9-11],但关于软骨肉瘤的研究较少,且多为个案报道。本文总结软骨肉瘤的18F-FDG PET/CT表现,旨在加强对本病的认识,更好地指导临床诊治。
1 资料与方法
1.1 研究对象 回顾性收集2012年10月—2021年12月北京大学第三医院21例软骨肉瘤患者的PET/CT及临床资料。男11例,女10例,年龄29~82岁,平均(50.8±15.5)岁。未经治疗的初诊病变14例,术后复发病变7例。临床表现:颈肩、腰腿或胸壁疼痛15例,四肢感觉异常、乏力或活动受限4例,局部触及包块7例。1例患者有乳腺癌病史。所有患者经穿刺或手术获得组织病理学诊断。病理亚型:普通型8例,其中高分化3例,中分化4例,低分化1例;少见病理亚型8例,包括间叶性5例,透明细胞、黏液样、去分化各1例;病理分型及分化程度不明5例。本研究经本院伦理委员会批准(LM2022574),豁免患者知情同意。
1.2 仪器与方法 患者禁食6 h以上,空腹血糖低于11.1 mmol/L。按照3.7~5.5 MBq/kg静脉注射18F-FDG(北京原子高科股份有限公司,放化纯>95%)60 min后,采用Siemens Biograph 64 PET/CT进行局部或躯干扫描。CT采集参数:管电压120 kV,有效管电流100 mAs,螺距0.9。CT图像重建参数:层厚3 mm,层间距2 mm,卷积核B30f。PET采集3个(局部)或5~6(颅底至股骨中段)个床位,每个床位采集2 min,True X方法重建,迭代3次,子集21,高斯滤波,半峰宽5.0,放大倍数1.4。
1.3 图像分析 由2名主治医师及以上核医学医师独立阅览PET/CT图像,意见不同时经协商达成一致。应用北京麦迪克斯影像工作站进行病变征象分析及数据测量。重点总结骨骼病变的发生部位、数目、CT征象及18F-FDG代谢特点:包括骨质破坏类型(溶骨性、成骨性)、病变边缘(模糊、清晰、硬化缘)、骨皮质中断、骨膜反应、肿瘤基质(钙化、骨样高密度,液性低密度)、软组织肿块;放射性摄取是否均匀,内部有无放射性减低或缺损区。分析骨外病变的分布及代谢情况。于PET/CT融合图像测量病变最大标准化摄取值(SUVmax)及最大径线。对于多发骨病变患者,选择经病理证实的病变进行分析、测量及统计学处理。
1.4 统计学方法 利用SPSS 21.0软件,符合正态分布的计量资料以±s表示;不符合正态分布的计量资料以M(Q1,Q3)表示,组间比较采用Mann-WhitneyU检验。计数资料以例数(%)表示。应用Spearman相关分析病变SUVmax与肿瘤大小的相关性。P<0.05表示差异有统计学意义。
2 结果
2.1 病变分布 患者行躯干扫描17例,局部扫描4例。12例检出单发病变,位于脊柱7例,其中颈椎3例、胸椎2例、腰椎2例;肋骨2例,髂骨、股骨、掌骨各1例。9例检出多发病变,其中6例检出骨外病变,包括肺结节(4例)、肝脏、胰腺、肾上腺、胸膜、腹盆腔、腰大肌、椎管等。7例高、中分化普通型软骨肉瘤中,单发病变6例,多发病变1例。5例间叶性软骨肉瘤中,单发病变2例,多发病变3例。3例其他亚型(透明细胞、黏液样、去分化)软骨肉瘤均为多发病变。
2.2 CT表现 14例初诊病例中,躯干扫描12例,局部扫描2例,发现单发骨病变9例,其中溶骨性破坏7例(图1),边缘均未见硬化缘,未见骨质破坏2例(图2);9例均有软组织肿块,大小不一;9例均见钙化密度影(图1、2),呈点状、片状、不规则、块状等,形态及数目差异显著;2例伴有骨化影(图2)。5例多发骨病变,均见钙化灶(图3),其中1例透明细胞软骨肉瘤可见多发溶骨性破坏,较大病变内部见大量钙化密度影,部分见硬化缘(图4);1例黏液样软骨肉瘤见骨膜反应。7例术后病例中,躯干扫描5例,局部扫描2例,发现术区局部软组织肿块影6例;多发骨病变4例,单发2例;5例见钙化密度影,2例未见。部分骨外病变包括肺结节、胰腺等可见钙化灶(图3)。

图1 女,39岁,颈椎间叶性软骨肉瘤。PET MIP图示颈椎代谢活跃灶(箭,A);横轴位CT示C4椎体及左侧附件溶骨性破坏,内见多发钙化灶(箭,B); PET/CT融合图像示病变代谢不均匀增高,SUVmax 7.31(箭,C)
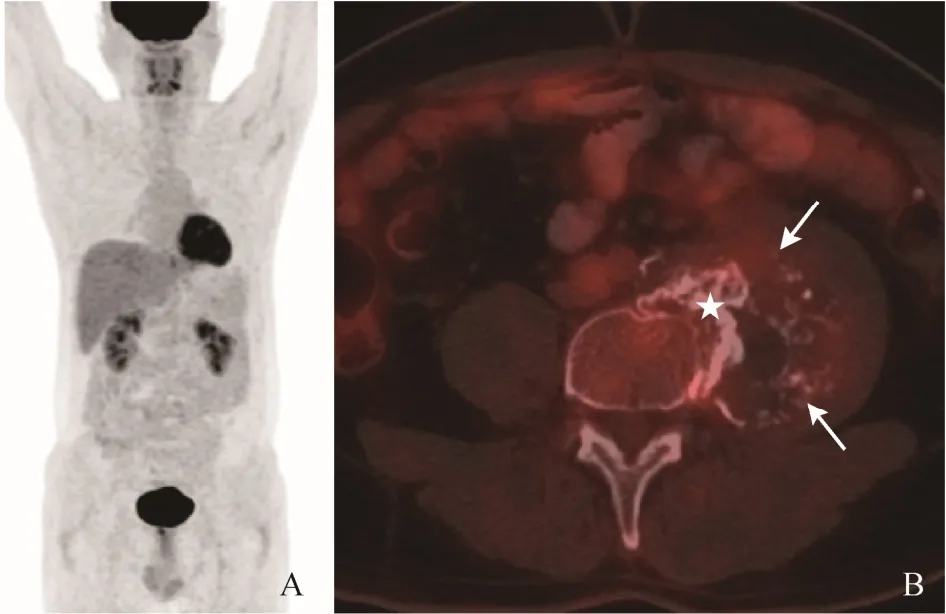
图2 男,40岁,腰椎普通型高分化软骨肉瘤。PET MIP图像未见异常放射性浓聚灶(A); PET/CT融合图像示腰4左侧软组织肿块,伴内部多发钙化灶(箭,B),边缘代谢不均匀轻度增高,SUVmax 1.70,腰4未见明确骨质破坏,周围见骨样密度影(星号)

图3 女,45岁,间叶性软骨肉瘤多发转移。PET MIP图示全身骨、胸腹部多发18F-FDG代谢增高灶,部分病变呈环状(箭,A);PET/CT融合图像示右侧股骨旁软组织肿块,伴钙化灶(箭,B),肿块边缘代谢增高,SUVmax 10.51;PET/CT融合图像示胰腺尾部肿块,伴钙化灶,代谢增高,SUVmax 3.60(箭,C)

图4 男,31岁,透明细胞软骨肉瘤。PET MIP图示脊柱、肋骨、左侧股骨多发18F-FDG代谢增高灶(箭,A);CT(B)及PET/CT(C)融合图像示颈胸椎多发骨质破坏灶,颈2破坏为著,伴内部大量钙化影(箭),代谢不均匀增高,SUVmax 3.01,胸1椎体病理性骨折,后部代谢稍高,SUVmax 1.96(星号),颈5及胸3病变代谢不活跃(箭头),后者伴硬化缘
2.3 代谢特点 21个骨病变(12例单发,9例多发者各取1个病理证实的病变)18F-FDG代谢不同程度增高,大部分代谢不均匀,体积较大者尤著,呈边缘和(或)间隔代谢增高(图2~4)。高代谢位于钙化和(或)软组织密度区,分布未见显著规律。同一患者的多发骨病变之间18F-FDG代谢亦有不同程度差异(图4)。21例骨病变中位SUVmax 5.80(3.52,10.20),中位长径5.73(4.83,12.36)cm,两者无相关(r=0.089,P=0.701)。按照病理分化程度,软骨肉瘤分为2组:高-中分化组8例(普通型高分化3例,中分化4例,透明细胞1例);低分化组8例(间叶性5例,普通型、黏液样、去分化各1例)。高-中分化与低分化软骨肉瘤中位SUVmax分别为3.52(3.09,5.33)、9.02(6.52,16.86),差异有统计学意义(Z=-3.151,P=0.001)。骨外病变代谢不同程度增高,较大者代谢不均匀。
3 讨论
3.1 病理与临床特点 软骨肉瘤病理亚型较多,分化异质性显著。本组高、中分化普通型软骨肉瘤大部分(6/7)为单发病变,未见转移;其他少见亚型的软骨肉瘤大部分为多发病变,常见累及部位是骨骼、肺部、肝脏、胰腺、肌肉等。
3.2 CT表现 软骨肉瘤初诊病例大部分可见溶骨性破坏,伴软组织肿块,内部见数量不等、形态各异的钙化密度影。复发性软骨肉瘤大部分亦见软组织肿块与内部钙化影。CT表现与既往报道相符[13-14],需要与脊索瘤等疾病鉴别[15]。本组1例黏液样软骨肉瘤累及肩胛骨、肱骨,伴肩胛骨放射状骨膜反应。骨膜反应相对少见,并非软骨肉瘤特异性征象,但可以作为软骨肉瘤与软骨瘤的鉴别要点之一[16]。透明细胞软骨肉瘤罕见,好发于长骨干骺端,属于高分化肿瘤,较少出现转移[17-19]。本组1例透明细胞软骨肉瘤为多发骨病变,呈溶骨性破坏,较大病变内部见钙化影,部分病变边缘硬化。本组4例软骨肉瘤可疑继发于骨软骨瘤恶变,其中2例呈骨旁软组织肿块而未见骨质破坏,1例病变内部可见骨化影,1例见多部位骨软骨瘤。部分骨骼、肺脏、胰腺转移瘤可见钙化灶。
3.318F-FDG代谢特点 软骨肉瘤18F-FDG代谢具有三不均匀的特点:①单个病变代谢欠均匀,体积较大者尤著,高代谢多位于病变边缘和间隔,与钙化灶的分布未见明确相关。Ghafoor等[20]报道软骨肉瘤钙化区域18F-FDG摄取可以与周围软组织一致,亦可减低甚至缺损。②同一患者的多发骨病变间18F-FDG代谢亦有不同程度差异。③不同患者间软骨肉瘤18F-FDG代谢差异显著,与病理分化程度相关,与病变大小无相关性。本组高、中分化软骨肉瘤SUVmax(中位值3.52)明显低于低分化组(中位值9.02),与文献报道大致相符。Annovazzi等[2]分析95例软骨源性肿瘤,发现以SUVmax 3.7为阈值,PET/CT鉴别高分化、中低分化软骨肉瘤的敏感度、特异度分别为83%、84%。肿瘤病理学分级越高,SUVmax越大,亦适用于复发性软骨肉瘤[21]。因而,PET/CT可以指导软骨肉瘤穿刺活检部位的选择,提高病理诊断的阳性率,甚至影响病变分期。
3.4 本研究的局限性 纳入病例数目较少,并且4例行局部PET/CT显像,可能会漏诊扫描视野以外的转移病变。部分病例的病理诊断基于穿刺标本而非术后组织,可能无法全面反映肿瘤的组织分化。
总之,软骨肉瘤大部分呈溶骨性破坏,伴软组织肿块及钙化影,摄取18F-FDG不同程度增高,与病理学分级相关。
