经皮脊柱内窥镜下腰椎间盘切除术及镜下治疗复杂移位型腰椎间盘突出症的研究进展
2023-12-13董智瑞贺欢欣赵明东
王 京 董智瑞 贺欢欣 赵明东
(复旦大学附属金山医院骨科 上海 201508)
腰椎间盘突出症(lumbar disc herniation,LDH)即腰椎间盘各部分发生退行性变后,在外力作用下,纤维环破裂,其内容物造成了神经压迫,引起疼痛、神经功能障碍等临床症状[1]。随着社会人口结构变化和工作压力增大,LDH 发病率逐渐增高[2]。目前经皮脊柱内窥镜下腰椎间盘除术(percutaneous endoscopic lumbar discectomy,PELD)是外科治疗LDH 的最先进的术式,其凭借卓越的微创性,深受脊柱外科医师重视,并随着技术的进步和镜下工具的改进,PELD 术式的手术适应证不断地拓展[3]。但椎间盘内容物可发生局部移位,其中部分复杂移位类型的LDH 经皮脊柱内窥镜下手术难度较高,可能存在减压不彻底、医源性脊柱不稳、神经损伤等问题。本文基于近年来的文献,对PELD 技术及镜下治疗复杂移位型腰椎间盘突出症的研究进展进行综述。
PELD 的定义旧指经皮椎间孔镜下椎间盘摘除术,即通过椎间孔入路到达责任节段,处理相关病灶。后因椎间孔入路解决临床工作中的实际问题具有局限性,Ruetten[4]提出了椎板间入路术式,拓展了PELD 术式范围。故对PELD 而言,“椎间孔镜”较为狭义,更倾向使用“脊柱内窥镜”概念。PELD 术式可被认为是显微镜下腰椎间盘切除术的替代方案[5],且创口更小,适用于各种类型的LDH。
PELD 的不同术式
椎间孔入路经皮脊柱内窥镜下经椎间孔椎间盘切除术(percutaneous endoscopic transforaminal discectomy,PETD)(入路示意图如图1 所示,用Visible Body 软件制图)始于20 世纪末期,即Yeung和Hoogland 等开发的Yeung 脊柱内窥镜系统(yeung endoscopic spine system,YESS)和经椎间孔内窥镜脊柱系统(transforaminal endoscopic spine system,TESSYS)和衍生后的改良术式。YESS 技术经过安全三角进入椎间盘内,通过工作通道置入内镜和器械,在直视下由椎间盘内向外切除髓核组织,是一种间接椎间盘减压技术。但有时受限于生理解剖入路,难以取出椎管内的椎间盘,对中央椎管狭窄、侧隐窝狭窄、椎间孔狭窄及髓核突出患者的运用有所限制。TESSYS 技术则在YESS 基础上进一步发展,由安全三角入路改为关节突穿刺入路并行椎间孔成型,直接对病变部位由外向内操作,并降低穿刺、置管损伤出行神经根和背根神经节的风险,不过仍存在损伤椎管内血管、走行神经根和硬膜囊的可能。
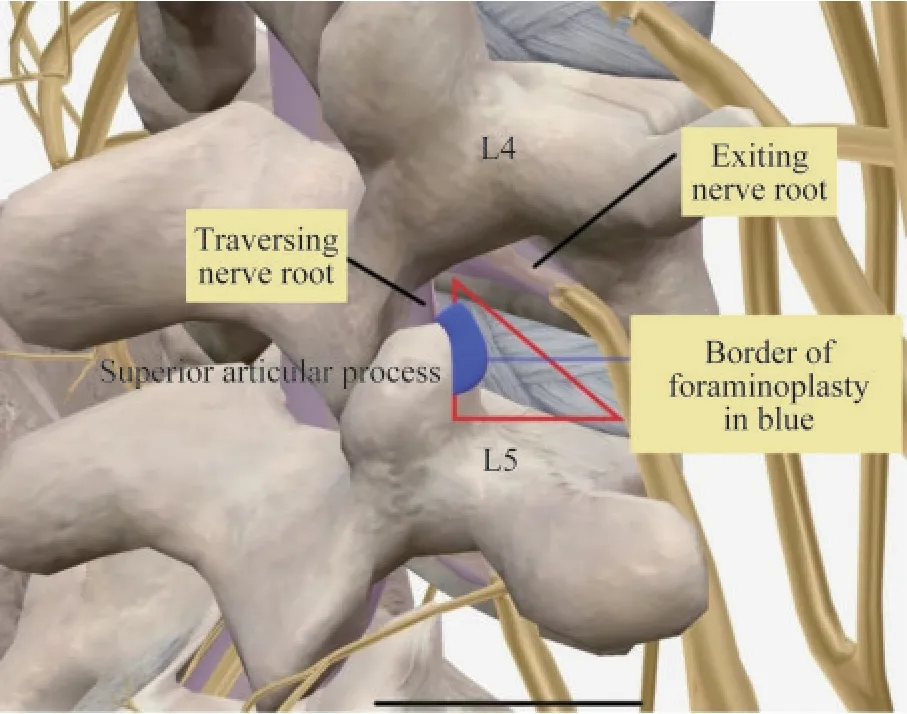
图1 PETD 术式的入路解剖Fig 1 Approach anatomy of the PETD procedure
YESS 技术操作较易,职业射线暴露低,但减压效果较差,且操作损伤神经的风险较大;TESSYS技术适应证较广,并能对神经根充分减压,不过传统TESSYS 技术常需多次穿刺、定位,所需时间较长从而导致医患双方暴露风险增大,且多次穿刺可能会增加损伤椎管内血管神经风险。此外,退行性病变需更大范围椎间孔成形,故而衍生一些针对椎间孔成形和穿刺定位的改良技术,如椎间孔镜靶向技术、BEIS 技术、改良椎间孔入路、MaxMore 技术(改用螺旋骨钻,可保护神经)、TESSYS-ISEE 技术[6]、全可视化内窥镜技术[7]。
椎板间入路经皮脊柱内窥镜下经椎板间椎间盘切除术(percutaneous endoscopic interlaminar discectomy,PEID)(入路示意图如图2 所示)作为PETD 术式的重要补充,与显微内镜下椎间盘切除术一样,都从后方入路,这是脊柱外科医师所熟悉的,其学习曲线较低平,具有穿刺快、暴露时间短等优点。

图2 PEID 术式的入路解剖Fig 2 Approach anatomy of PETD procedure
PEID 术式需穿黄韧带进入椎管内,而黄韧带是阻止椎管内瘢痕形成[8]和维持腰椎节段稳定的重要结构,保存黄韧带可能有利于腰椎节段的长期稳定和预防术后粘连,其突破技术是临床难点。在PEID 术式中,Chung 等[9]研究比较采用传统开放突破黄韧带和剥离黄韧带两种方式,两组术后随访临床结果相似。突破组通过内窥镜剪和手术镊切开黄韧带,其缺损为3~5 mm,而剥离组通过钝性分离器和手术剪剥离黄韧带,剥离后的黄韧带的弹性与本身近似,其缺损可忽略不计。但就并发症而言,突破组出现1 例硬膜囊撕裂,且缺口黏连可能影响翻修手术,而剥离组可能因为存在视野盲区而出现2 例无症状椎间盘(intervertebral disc,IVD)内容物丢失和1 例踝关节足底屈曲短暂无力。故在选择处理黄韧带的方式时,应考虑每种方法的潜在优点和缺点。
L5~S1 节段椎间孔较为狭窄且髂骨较高,而椎间隙较宽,PEID 较适合治疗此节段LDH,也适用治疗钙化LDH[10-11]。传统PEID 术式一般行全麻,可能存在围术期神经认知功能障碍(perioperative neurocognitive disorders,PND)。Guan 等[12]回顾性研究局麻下行PEID 的可行性,其研究表明局麻下行PEID,疼痛控制良好,PND 发生风险低,恢复更快,住院费用更低,进一步拓宽了PEID 术式的适应证。不过需要注意的是,亚洲人的椎间隙较欧美人窄一些,有时需要椎板成形。目前主要有单通道和双通道两种技术[13-14],均表现出良好的临床预后结果,这两种技术的选择方式主要取决于术者的倾向和熟练程度。
并发症及术式选择PELD 术式治疗LDH 效果显著,不过仍然存在一些术后并发症,如感染、椎管内出血、硬脊膜撕裂、神经根损伤致感觉障碍、器械折断、复发、腹腔内脏器损伤和腹膜后血肿,还可发生癫痫(可能和硬膜外压力增高有关)、工作通道置入失败等少见并发症[15]。目前,有学者研究内窥镜下取出硬脊膜内IVD,并用硬膜补片和明胶海绵修复硬脊膜[16],对指导治疗内镜下治疗硬脊膜内的LDH 有一定借鉴意义。脊柱外科医师术前应明确病史、仔细查体,在深刻理解解剖结构的基础上仔细穿刺定位,并严格把握适应证,谨慎操作,做到个体化精细管理患者。
就术式的选择而言,并非仅凭术者偏好及髂骨和椎间隙的解剖关系。Choi 等[17]研究发现,PETD术式适合肩型、中央型和复发性LDH,而PEID 适合腋型LDH,还可用于治疗IVD 内容物移位的LDH。PETD 术式入路可处理相关路径狭窄的问题,且行局麻即可,较为安全。PEID 术式经椎板间入路,工作通道可在椎板间移动从而充分探查减压,且学习曲线低平、手术时间及职业暴露时间较PETD 短,但会损伤椎旁肌和脊柱后方韧带复合体(posterior ligamentous complex,PLC),且术中可存在硬膜囊牵拉和根性疼痛,容易导致术后出现下肢感觉异常。基于既往文献,我们总结了两种手术入路的区别(表1),外科医师可酌情采用。
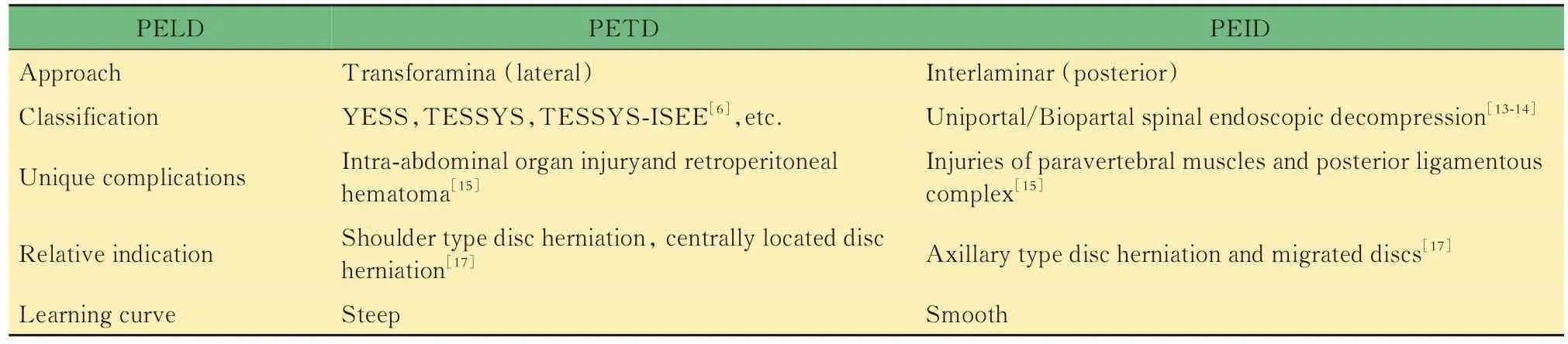
表1 PELD 的简要总结:PETD 与PEIDTab 1 A brief summary of PELD:PETD vs. PEID
移位型LDH移位型LDH 即IVD 内容物(如髓核、软骨终板、纤维环组织等)经纤维环裂隙,在矢状面或水平面上移位[18],压迫或刺激神经产生相应临床症状。因经皮脊柱内窥镜下治疗轻度移位型LDH 在临床实际工作中较易完成,故本篇综述重点介绍复杂移位型LDH 和近年来PELD 术式治疗复杂移位型LDH 的研究进展。
水平面上复杂移位型LDHIVD 内容物可根据水平面上移位的位置,将LDH 分为中央管型LDH(central lumbar disc herniation,CLDH)、后外侧型 LDH(posterolatera lumbar disc herniation,CLDH)和极外侧型LDH(far lateral lumbar disc herniation,FLDH)。PELD 术式治疗中央管型和后外侧型LDH 较为容易,而较难处理FLDH(水平面上复杂移位型LDH)。FLDH 首先由Abdullah 等[19]报道,发生率较低,约1.0%~11.7%,好发于腰4~5椎体,FLDH 还可进一步分为椎间孔内型(I 型)、椎间孔外型(Ⅱ型)和混合型(Ⅲ型)[20](图3)。
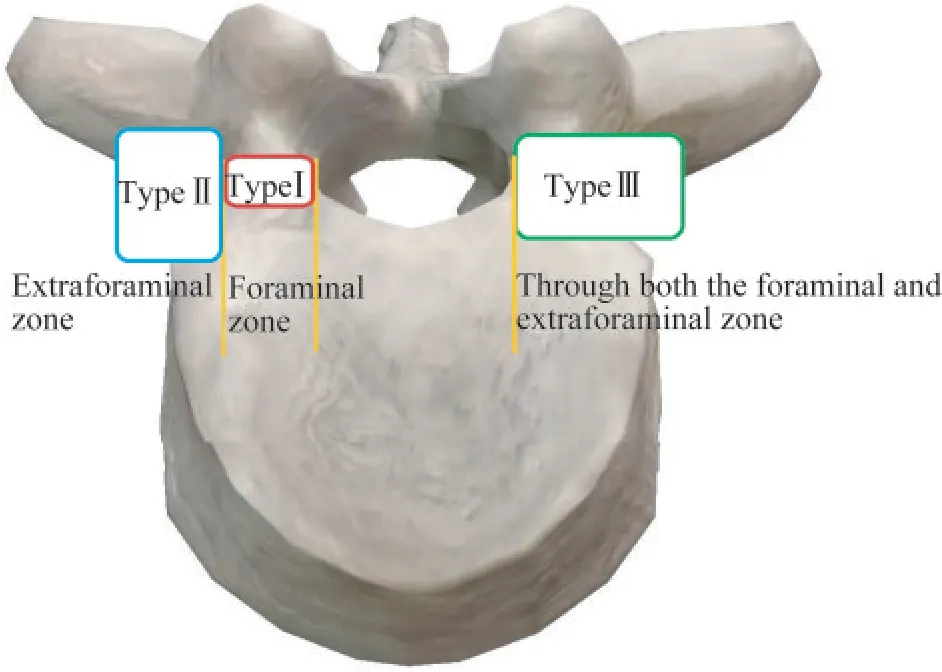
图3 FLDH 分类Fig 3 Classification of FLDH
PELD 治疗FLDHFLDH 可直接压迫背根神经节,产生难以忍受的疼痛,并可能造成不可逆的神经损伤,故多主张采取手术治疗。而治疗上具有挑战性的Ⅲ型FLDH,即移位的IVD 由椎间孔延伸到椎间孔外,经常被忽视和误诊[21],这类情况往往需要更大的减压范围。对于FLDH 可以通过远外侧的横突间入路、经外侧和旁正中等切口进行手术治疗,如:Wiltse 间隙入路术式可保持小关节和峡部完整,但椎间孔内侧难以触及;显微镜下通道LDH切除术(如EF-MAPN[22]、EL-MAPN[23])是一种微创方法,可不损伤小关节或关节间部;PETD 术式比显微镜下通道LDH 切除术更加微创,可经传统安全三角定位方式到达责任间隙进行内部减压,对正常生理结构损伤更小。对于Ⅲ型FLDH, Fiorenza等[24]采 取 了 TOIO (transforaminal outside-in outside)方式,提出采用不完全垂直的通道轨迹接近椎间孔,可进一步降低神经损伤风险。第一步将工作通道置入邻近下椎弓根上、内侧缘的硬膜外间隙。第二步则内外移动手柄并同时旋转工作通道,使开口面向下椎弓根的上表面,旋转的过程中可使出口神经稍微侧向移动,但并未出现神经损伤。PETD 术式处理FLDH 充满了挑战,尤其是L5~S1节段,其安全入路受高髂骨限制,关于FLDH 的经皮脊柱内窥镜下治疗仍需进一步探索。
矢状面上复杂移位型LDHDaghighi 等[25]研究发现,高达72.2%的LDH 患者的IVD 在矢状面上向尾端移位,27.8%则向头端移位,但随着年龄的增长,向头端移行比例显著增加。目前存在矢状面分级系统,而仍无有效的水平面或冠状面分级。Lee 等[26]基于MRI 对移位型LDH 进行分级,将IVD内容物移位位置在腰椎矢状面上分为经典的4 个区:IVD 内容物向头端移位至上椎弓根下缘以下3 mm 和上椎弓根下缘之间,即到达1 区,或向尾端移动至从下椎弓根中部到下椎弓根下缘,即到达4区,并认为IVD 内容物移位至1 区和4 区的行内窥镜技术治疗效果不佳,宜行开放术式,而对于IVD内容物移位至从上椎弓根下缘至上椎弓根下缘以下3 mm(即2 区)或从下椎体上缘到下椎弓根中心(即3 区)的LDH 治疗较为容易。
若IVD 内容物向头尾两端移位到达椎弓根下缘,则超出经典4 区范围。Ann 等[27]提出新6 级分类系统,且对经典的1、2 区界限和3、4 区界限进行了新的划分。本文基于IVD 内容物移位的经典4 区分类,参考Zhao 等[28]在经典4 区之外新定义了5 区、6 区标准,总结PELD 术式治疗矢状面上复杂移位型LDH(图4),即IVD 内容物在矢状面上移位至1、4、5、6 区。
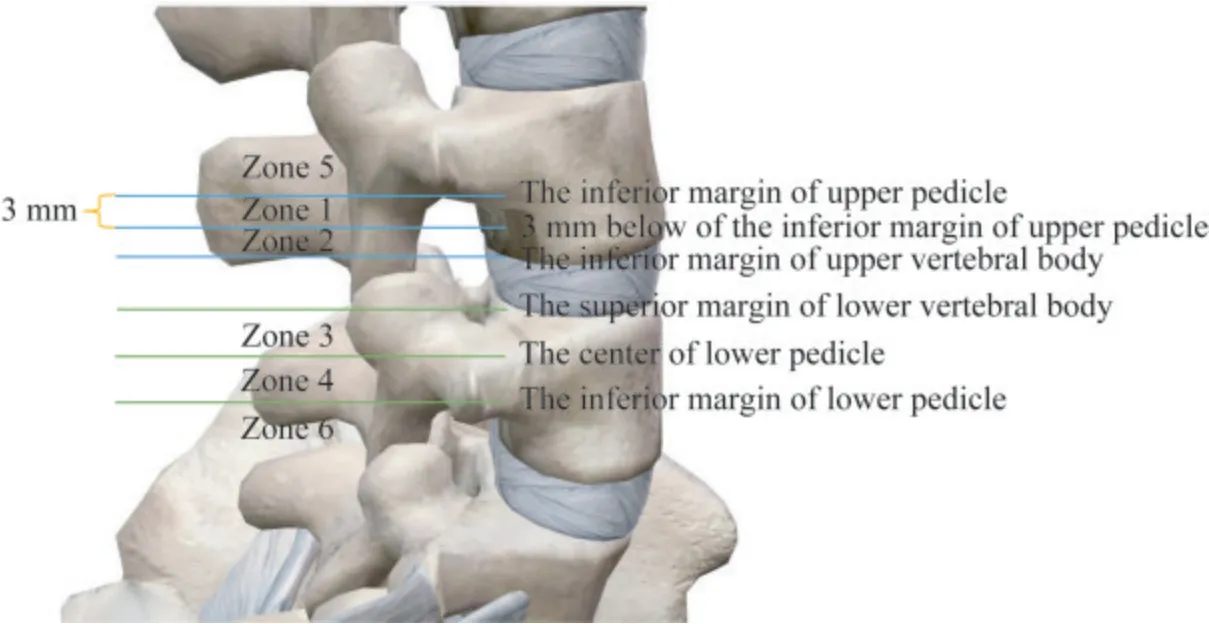
图4 矢状面上复杂移位型LDH 分类Fig 4 Classification of complex migrated LDH in the sagittal plane
PELD 治疗矢状面上复杂移位型LDH
1、4 区移位型LDH早期的器械灵活性低,术中操作受限,在1、4 区移位型LDH 的手术中有较大的IVD 内容物丢失风险,有时需要较大面积的骨切除,可能导致术后脊柱不稳。但随着技术的发展和工具的进步,如柔性钳、超声骨刀等的运用,PELD术式治疗复杂移位型LDH 的适应证范围扩大了。不少学者使用PELD 术式对IVD 移位到达1、4 区的治疗,提供了宝贵经验。
Huang 等[29]比较了两种术式治疗L4~5 节段IVD 内容物向尾端移位至4 区的LDH,研究发现两种术式治疗均安全有效,不过在取出IVD 满意程度、手术时间和透视时间方面,PEID 优于PTED,但PEID 更容易导致术后感觉异常。Wu 等[30]开展的小型前瞻研究发现,PELD 术式治疗IVD 移位至1、4 区患者安全有效。对L4~5 以上节段移位至1、4区或L4~5 节段向头端移位至1 区,采用PETD 术式,而当IVD 内容物在L4~L5 节段向尾端移位至4区或L5~S1 节段向头段移位至1、4 区,PEID 术式可作为更好的选择。
针对解剖入路障碍问题,改良术式有椎弓根入路[31]、对侧椎间孔入路[32]、椎弓根上入路[33]、跨关节突和椎弓根的复合体入路[34]。还有有学者尝试经改良的椎板入路[35]治疗IVD 移位至1 区或4 区的LDH 患者。相较于PEID 术式需要切除一定的椎板达到责任病灶,经椎板入路可以结合使用全程可视化内窥镜,先将环钻直接对准移位的IVD 在椎板上的投影,再垂直椎板行钻孔开窗,为直接到达责任病灶提供新的选择。优点是对椎旁肌肉和小关节的损伤很小,还避免了椎板切除术和黄韧带切除术,但此式对定位要求高,且有一定硬脊膜撕裂风险。
5、6 区移位型LDH目前,对IVD 移位到达5、6区的LDH 患者治疗仍充满挑战。L4~5 解剖特征:椎间孔较大;IVD 高度高于椎板间隙。Liu 等[36]认为:L4~5 节段IVD 内容物到达上位椎弓根下缘,即到达5 区,首选PETD 术式,若存在多份IVD 内容物则可做椎间孔成形;IVD 下移到达下位椎弓根下缘,即6 区,采用PETD 入路则受限于同侧椎弓根,需加大尾倾角度到达责任区域,但可能造成神经损伤,难以处理位于侧隐窝内的高度移位IVD 内容物,此时应首选PEID 术式。且当突出物位于神经外侧的肩型LDH 需要考虑内侧关节成形;L4~5 节段IVD 上移。而L5~S1 节段IVD 移位的解剖特征:椎间孔狭窄,高的髂骨翼和较大的关节突关节,而椎板间隙空间大,故L5~S1 节段IVD 移位至5、6区均首选PEID 术式,必要时考虑关节面成形。
新型的全程可视化内窥镜技术应用大大拓展了PELD 术式的适应证。对于到达5 区的移位IVD,Li 等[37]结合全程可视内窥镜技术对椎弓根成形,其靶点成形位置是头端椎弓峡部外侧部分而非上关节突腹侧,术后随访结果满意。不过术式应当采用合适的保护神经装置以避免置入工作管道对神经损伤;对上移至5 区且为L4~5 节段及以上的LDH,Yu 等[38]提出一种新的技术作为PELD 术式补充,其结合全可视内窥镜技术和椎间孔切开成形,将内窥镜进至椎管内,并转至头部方向在上位椎体的后表面钻沟成形,使工作套管可以进一步沿沟向上到达5 区责任病灶,完成摘除,安全有效。Shen 等[39]则对IVD 移位到达5、6 区的LDH 患者,采取改良的PETD 术式,即运用靶向穿刺和椎间孔成形术。首先通过穿刺针靶向穿刺至移位IVD 的中心,摘除移位的椎间盘。如果穿刺通路被骨性结构阻碍,可先将穿刺针与关节突关节对接,再利用Tom 针建立到达移位IVD 的中心通道,并依次使用骨钻扩大骨通道,与椎间孔相连,完成椎间孔切开术后取出移位的IVD。再将工作套管和内窥镜移动到责任节段的椎间隙再次减压。
纤维环修复随着技术发展,PELD 术式治疗LDH 适应证扩大,在治疗脊柱方面疾病具有极大的优势,但仍面临术后LDH 复发问题,其中纤维环修复或许可作为有效手段。
LDH 复发存在一些影响因素[40],如性别、年龄、吸烟情况、BMI、创伤史、LDH 类型、关节面方向、关节突关节对称性等,还有研究认为腰骶部移行椎和屈伸片中有较大的矢状面活动范围的椎间盘也是LDH 复发危险因素[41],残余的髓核可通过纤维环破裂口复发。因此国内外学者逐渐开始重视纤维环修复与再生,包括机械修复、生物性修复。
机械修复可通过外科缝合、射频热凝术等方式修复纤维环缺口。射频热凝术一般适用于轻度纤维环撕裂,其适用范围较窄。外科缝合可借助缝合器恢复纤维环的机械完整性,但生物组织功能不能良好恢复,较为理想纤维环修复结果应是机械性和生物功能的良好恢复。目前,外科修复纤维环使用的缝合器有FAST-FIX、X-close 和EFIT。FASTFIX 操作较复杂,但缝合强度高;X-close 缝合后的患者术后复发风险显著降低,且不增加并发症风险[42]。但使用X-close 缝合会形成异物留在体内,导致其临床应用受限;国产EFIT 操作较简单、快捷、安全,但对切口或缺口周围软组织有较高要求。Li等[43]研究发现,EFIT 采用PETD 配合入路单针缝合或经PEID 配合双针缝合,随访1 年无髓核突出复发,术后获得显著改善。总之,3 种方式修复纤维环各有特点,不过缝合修复存在一定难度,且所需器械价格较高,目前还未推广使用。生物性修复领域现仍在基础实验或临床前研究阶段,但是从长远来看,具有良好的发展前景。目前较为先进的延缓或逆转IVD 退化过程的再生策略[44]包括生物分子疗法、基因疗法、细胞疗法和注射凝胶。目前已有利用植物光合作用系统来进行细胞代谢的研究[45]:通过植物类囊体获得纳米类囊体单元,并采用细胞膜伪装包封以避免免疫排斥,再通过哺乳动物的骨关节炎疾病模型验证,即经特定的光照改善软骨细胞内代谢以此延缓疾病的进展。这些技术有望进一步应用于其他退行性疾病,如LDH。随着医学、材料学、生物力学和生物学等多交叉学科深度发展,纤维环的生物性修复领域会进一步被拓展。
结语综上所述,PETD 术式适合L4~5 或以上节段LDH,也较易处理侧隐窝狭窄和椎间孔狭窄,但PETD 在处理L5~S1 节段的FLDH 的IVD内容物有时存在困难,容易发生IVD 内容物的不完全清除,这类问题仍需进一步研究,且PETD 的定位和穿刺不当会导致腰动脉和出神经根的损伤,更容易导致术后感觉障碍和血肿。另一方面,由于L5~S1 节段的椎间隙较大,PEID 处理L5~S1 节段LDH 中具有优势,但PEID 的过度拉伸可损伤硬膜囊,导致硬膜撕裂的风险较高,还会损伤椎旁肌和PLC。关于PELD 术式治疗矢状面上复杂移位型LDH,临床医师应充分考虑IVD 内容物移位位置,结合责任节段个体化选择合适的手术入路。
作者贡献声明王京 论文构思,文献整理,论文撰写和修订,制作图表。董智瑞,贺欢欣 文献整理,论文修订。赵明东 论文指导、修订和审校。
利益冲突声明所有作者均声明不存在利益冲突。
