药品、生物制品及相关样品中蔗糖含量分析方法的研究进展*
2023-11-30管艺同陆益红
管艺同,朱 渊,陆益红
江苏省食品药品监督检验研究院,南京 210019
蔗糖由一分子葡萄糖和一分子果糖的半缩醛羟基彼此缩合脱水而构成,为自然界中分布最广泛的非还原性二糖,有旋光性,但无变旋光作用。作为一种常见的辅料,其在药品和生物制品中应用广泛,不仅可以作为矫味剂或赋形剂应用于糖浆剂、颗粒剂、片剂、口服溶液剂、注射剂等剂型的生产[1],还可在生物制品中充当冷冻干燥保护剂[2]。蔗糖通过改变生物制品在冻干过程中的物理化学环境,可以减轻细胞的损伤和一些蛋白质的钝化,尽可能保持原有的生物学活性,并提高制剂稳定性[3]。因此,蔗糖在制剂制备过程中发挥着十分重要的作用。
蔗糖的含量往往对制剂的有效性、稳定性和安全性存在着一定程度的影响,例如在生物制品中,蔗糖对蛋白质的保护作用有时依赖于浓度。一般来说,在特定的浓度范围内,蔗糖的保护作用随着浓度升高而增强。然而,当达到一定浓度后,保护作用达到最大值,进一步提高蔗糖浓度则不再增加保护效果,甚至可能降低保护作用[4]。此外,蔗糖的含量还会影响制剂的渗透压,且由于不同个体耐糖量存在显著差异,过量摄入蔗糖可能对身体产生不利影响。故为使蔗糖充分发挥药用辅料的作用,有必要建立方法以准确测定其在药品和生物制品中的含量,从而指导生产工艺的优化和调整。
蔗糖含量的测定方法包括基于氧化还原反应的经典化学方法、旋光法、色谱法、近红外光谱法、毛细管电泳法等。由于蔗糖在各类制剂产品中存在的形式各有不同,且不同产品中的蔗糖含量差异较大。因此,应针对各类产品的不同特性以及蔗糖含量的水平差异,选择最合适的方法。本文列举了目前较为常用的各类蔗糖含量测定方法,并对各方法的优缺点及适用情况进行了阐述,以期为实际工作中蔗糖含量检测技术的选用提供一定参考。
1 基于氧化还原反应的经典化学方法
蔗糖本身不具有还原特性,但一分子蔗糖在酸或蔗糖酶的作用下,可以水解为一分子D-葡萄糖和一分子D-果糖,两者均为还原性糖。蔗糖的水解产物与3,5-二硝基水杨酸[5]、间苯二酚[6,7]或斐林试剂[8]等在一定条件下能够发生氧化还原反应,产生颜色或沉淀。可基于此原理,利用比色法或滴定法对蔗糖含量进行测定。
这类方法成本较低,但操作步骤繁琐,费时费力,精密度和灵敏度均不佳,且易受到多种因素的干扰,如其他还原性糖类、色素、蛋白质等的存在均可能导致测定结果不准确,因而不适合用于检测蔗糖含量较低、基质复杂的样品。
2 旋光法
蔗糖具有旋光性,可以采用旋光法测定。2020年版 《中国药典》 四部药用辅料蔗糖的质量标准[9]中,比旋度被作为性状项列出。杨烨等[10]开发了一种基于旋光法的蔗糖含量测定方法,用于定量测定b型流感嗜血杆菌结合疫苗中的蔗糖。该方法在蔗糖浓度为2~10 mg·mL-1的范围内与旋光度具有良好的线性关系(r=0.999 9),且准确性、重复性均良好。
采用旋光法测定蔗糖操作简单、成本低廉。但专属性较差,对蔗糖不具有选择性,且灵敏度低,不适用于微量蔗糖测定,在用于测定规格较小的疫苗等生物制品时存在局限性,因此目前应用较少。
3 高效液相色谱法
高效液相色谱法(high-performance liquid chromatography,HPLC)的原理是基于不同组分同时进入色谱柱后,在流动相及固定相之间的溶解度、吸附作用、渗透作用等均有一定区别,导致各个组分的移动速度产生区别,在移动一定距离后依次进入特定检测器,从而实现不同组分的分离。可根据色谱峰的保留时间对化合物进行定性,根据峰面积对化合物实现定量。HPLC 在分离和分析方面具有高度的灵活性和可调性,除了调整流动相的相关参数外,选择恰当的色谱柱和检测器同样可以优化分离效果和灵敏度,以满足特定的分析要求,这使得HPLC 适用于各种复杂样品和不同含量的蔗糖定量分析。下文将从目前蔗糖含量测定常用的检测器和色谱柱方面对HPLC 进行介绍。
3.1 检测器
HPLC 可根据待测物质的理化性质适配不同的检测器。蔗糖本身不具有生色官能团,无法直接用紫外检测器检测。在目前可采用的各类检测器中,应用最为广泛的是示差折光检测器(refractive index detector,RID)和蒸发光散射检测器(evaporative light scattering detector,ELSD)。
3.1.1 示差折光检测器 示差折光检测器是通过连续监测参比池和测量池中溶液的折射率之差来测定试样浓度的检测器。由于每种物质都具有专属的折射率,因而RID 属于通用型检测器,适用于蔗糖的检测。雒丽红等[11]采用HPLC-RID 法同时测定了乙型脑炎减毒活疫苗等4 种生物制品中的蔗糖和乳糖含量,该方法能将两种糖完全分离,特异性较好,在0.50~20.00 mg·mL-1范围内,相关系数r2均达到0.999 9 以上,蔗糖的最低检测限和定量限分别为0.01 mg·mL-1和0.10 mg·mL-1。强鹏侠等[12]采用HPLC-RID 法测定冻干b 型流感嗜血杆菌结合疫苗中的蔗糖含量,方法准确度、重现性及专属性均较好,系统适用性验证表明葡萄糖的存在对蔗糖出峰无干扰(图1)。蔗糖在2.5~40.0 mg·mL-1范围内线性关系良好(r2>0.999)。

图1 HPLC-RID 法测定冻干b 型流感嗜血杆菌结合疫苗中蔗糖含量的典型色谱图[12]
RID 对外界环境的变化十分敏感,温度、压力、浓度、流速、pH 值的变化都会引起待测物质密度变化,从而导致折射率的改变,进而影响测定结果的准确性,因此不能使用梯度洗脱,可能导致分离时间较长,不利于分离一些成分复杂的样品。同时,RID 的操作原理和结构特点使其对流动相及溶剂的纯度要求较高,并容易受到污染物的影响,故在耐用性方面存在一定不足,且相对其他检测器而言灵敏度较低。
3.1.2 蒸发光散射检测器 蒸发光散射检测器也属于通用型检测器,同样适用于没有紫外吸收的组分测定,其工作原理包括雾化、流动相蒸发和激光束检测三个过程。样品从色谱柱后流出,进入雾化器形成微小液滴,与通入的气体(通常是氮气,有时也可用空气)混匀,随后经过加热的漂移管,蒸发除去流动相,使样品组分形成气溶胶。最后利用强光或激光照射气溶胶,产生光散射,并通过光电二极管检测散射光的强度。吴国真等[13]采用HPLC-ELSD 法同时测定天麻中活性成分天麻素及风味物质果糖、葡萄糖和蔗糖的含量。该方法分析时间较短,能够实现各成分的基线分离,其中蔗糖在0.12~1.50 mg·mL-1浓度范围内线性关系良好(r2≥0.999),定量限和检测限分别为0.45 μg 和0.15 μg。陈梦等[14]采用HPLC-ELSD法同时测定微胶囊中阿拉伯糖、果糖、葡萄糖、蔗糖、麦芽糖、乳糖的含量,其中蔗糖在0.32~5.00 mg·mL-1的浓度范围内线性关系良好(r2>0.999),检出限为0.02 mg·mL-1。在方法摸索过程中发现在流动相中添加适量的氨水能够显著提高分离度并改善峰形,因此选取1%氨水和乙腈作为流动相。由于等度模式难以将色谱柱上保留的成分完全洗脱,因此实验中采用了梯度模式,实现了各成分的完全洗脱和有效分离(图2)。

图2 HPLC-ELSD 法测定微胶囊中6 种糖含量的典型色谱图[14]
相较于RID,ELSD 灵敏度更高,对流动相系统及温度变化不敏感,可以进行梯度洗脱,且不必严格控制环境温度。由于流动相及其中的挥发性成分在蒸发器内挥发气化,因此消除了前溶剂峰的干扰,可以使基线更平稳,分离时间更短,定量精度更高,不受溶剂成分影响。但蒸发光散射检测器要求组成流动相的各组分必须具有挥发性,不能使用磷酸盐等非挥发性物质。
3.1.3 电喷雾检测器 电喷雾检测器(charged aerosol detector,CAD)是一种新型的通用型检测器,可用于蔗糖含量检测。与HPLC 联用时,HPLC 的洗脱液在雾化器中雾化形成含有待测物的较小液滴,经过蒸发管干燥后与带电氮气碰撞,使得待测物质颗粒表面带上正电荷,最后通过高灵敏度的静电检测计测量待测物质的电荷量并形成电信号,该信号强度与待测物质的质量成正比。近年来,CAD 在药物分析领域的应用越来越广泛,国外药典已收载多个采用CAD 的液相色谱分析方法[15]。孙亚灵等[16]建立了测定蔗糖含量的HPLC-CAD 方法,并对色谱柱、流动相和检测器参数的优化过程进行了讨论。所建立的方法专属性强,分离效果好,受环境影响小(图3),在质量浓度为4.95~99.10 μg·mL-1的范围内线性关系良好(r >0.999)。张素红等[17]建立了利用HPLC-CAD 同时测定白茅根样品中果糖、葡萄糖和蔗糖的方法,在建立的液相色谱条件下,上述3个糖类成分分离完全,其中蔗糖进样量在5.274~31.650 μg 范围内线性良好(r=0.999 6),检测下限为5.285 μg·mL-1。

图3 HPLC-CAD 法测定蔗糖含量的系统适用性溶液(A)和空白溶剂(B)典型色谱图[16]
CAD 在原理和特征上与ELSD 有相似之处,均无需严格控制环境温度,但流动相不可使用非挥发性成分。CAD 对于高盐浓度的样品也有一定的限制,可能需要进行前处理或使用低盐流动相。与ELSD 相比,CAD 具有更高的检测灵敏度、更好的重复性和更宽的线性范围,通常可达3~4 个数量级。此外,CAD 的测定参数基本已在出厂时设定好,每次分析的条件相对固定,因此重现性较好[18]。
3.1.4 离子色谱-脉冲安培检测器 离子色谱法(ion chromatography,IC)是高效液相色谱法的一种,应用于蔗糖含量测定时一般采用脉冲安培检测器(pulsed amperometric detector,PAD),故本文将IC-PAD 法列入检测器方面进行介绍。该方法的原理是根据不同的离子态物质在离子交换柱上具有不同的迁移速率,将物质进行分离,随后离子态物质在PAD 的工作电极表面发生氧化还原反应,引起电流变化而被自动检测[19]。由于中性糖类化合物的酸离解常数在12~14 之间,在强碱淋洗液中可部分或全部解离成阴离子形式,从而在阴离子交换柱上被保留并分离[20]。阴离子态的蔗糖在脉冲安培检测器的金电极上发生氧化反应而产生电流信号,因此可以采用离子色谱法对样品中的蔗糖进行分离分析。
郭雅娟等[21]建立IC-PAD 法同时对甘露醇中的葡萄糖、甘露糖、蔗糖和果糖含量进行测定。该方法采用CarboPacPA20 分析柱(3.0mm×150mm)与CarboPac PA20 保护柱(3.0mm×30mm),以100mmol·L-1氢氧化钠溶液作为淋洗液,进行梯度洗脱。结果表明,在0.025~2.500 μg·mL-1浓度范围内,各成分峰面积均分别与质量浓度呈良好的线性关系,相关系数r 均大于0.999。
李晓东等[3]以口服轮状病毒疫苗中蔗糖组分为分析对象,分别采用旋光法、HPLC-RID 法、IC-PAD法进行测定和对比(图4)。其中HPLC-RID 法检测蔗糖的最小检出限为5 mg·L-1,而IC-PAD 法的最小检出限为6 μg·L-1,最小定量限为30 μg·L-1。上述结果表明,在灵敏度方面,IC-PAD 法是HPLC-RID法的将近1000 倍。

图4 HPLC-RID 法(A)和IC-PAD 法(B)测定疫苗制品中蔗糖含量的典型色谱图[3]
IC-PAD 法的分析时间短、专属性强、灵敏度高、样品无需衍生化。但由于流动相为强碱介质,可能造成样品中某些组分降解,因此在选择和优化分析条件时需要特别注意,以避免可能的降解影响。此外,离子色谱仪价格相对昂贵,分析条件较为苛刻,对实验室要求较高。
3.1.5 质谱检测器 质谱检测器(mass spectrometry detector,MS)具有高灵敏度和高专属性的特点。样品经过色谱分离后,首先在接口中被电离,生成的气相离子通过质量分析器按m/z 的大小顺序分离,并通过离子检测器将离子信号转化为电信号。MS常用的离子源主要为电喷雾离子源(electrospray ionization source,ESI)和大气压化学离子源(atmospheric pressure chemical ionization source,APCI)。目前在生物代谢研究中已较为广泛地利用高效液相色谱或气相色谱联用质谱检测器测定生物样品中的蔗糖,但在药品及生物制品领域仍应用较少。可将该思路迁移至药品及生物制品领域的蔗糖含量测定,以满足更高的灵敏度需求。
GEORGELIS N 等[22]采用ESI 负离子模式下的选择离子监测(selected ion monitoring,SIM),可同时快速测定植物组织中葡萄糖、果糖和蔗糖。经验证,该方法测定蔗糖的检测限为0.05 ng,定量限为0.10 ng。MIAH MK 等[23]采用ESI 负离子模式下的多重反应监测(multiple reaction monitoring,MRM)进行三重四级杆质谱分析,可用于测定脑、血浆和血液中稳定同位素修饰的[13C12]蔗糖。结果表明,蔗糖在1.0~200.0 ng·mL-1的浓度范围内线性良好(r2≥0.99),方法定量限达到柱上注射0.5 pg。
质谱检测器在灵敏度和专属性方面存在显著优势,可以在不必实现色谱峰完全分离的情况下检测待测物质,大大缩短了分析时间,也降低了液相方法的开发难度。但在联用质谱检测器时,需注意流动相中不能存在盐和表面活性剂等非挥发性的物质。此外,质谱检测器使用和维护的成本较高,对实验室环境也存在一定要求。
3.2 色谱柱
色谱柱是HPLC 分离过程的核心部件,决定着分离的效果和效率。由于蔗糖极性较高,若不经过衍生,在C18柱等普通反相色谱柱上难以获得较好的保留效果,故应用较少。根据分离原理的不同,常用于蔗糖分析的色谱柱包括氨基柱、阴离子交换柱、分子排阻色谱柱、亲水作用色谱柱等。
3.2.1 氨基柱 氨基柱全称为氨丙基键合硅胶色谱柱,既可以用于正相,也可以用于反相,还可以作为弱阴离子交换柱应用于离子交换色谱。在分析碳水化合物时,氨基柱采用的是亲水的反相分离模式,可用于分离同时含有单糖、二糖、三糖等不同聚合度的混合糖分子的样品。氨基柱的价格相对较低,但其键合相氨丙基易水解,尤其是在反相色谱条件下,所以使用过程中需注意保护。酸性或高比例水相条件会加速氨丙基水解,因此氨基柱应尽量避免在酸性或者高水相的流动相中使用,建议流动相中水相比例不超过40%。当样品显酸性时,可通过调节流动相pH 来提高氨基柱柱效和延长使用寿命。
3.2.2 阴离子交换柱 用于糖类离子色谱分析的阴离子交换柱也称糖分析柱、糖柱,常见的有戴安CarboPac PA 系列和瑞士万通的Metrosep Carb 系列。一般采用苯乙烯-二乙烯基苯共聚物为基质,金属离子对为官能团,二者通过磺酸基键合形成填料。糖分析柱的分离原理是基于配体交换反应,糖分子上每一个羟基都带有一个非常弱的负电荷,而端基异构碳上所带的羟基可被去质子化,从而带上一个很强的负电荷。糖分子上的这些负电荷与树脂表面上的金属离子正电荷之间的相互作用使糖被保留,从而达到分离目的。
3.2.3 分子排阻色谱柱 分子排阻色谱柱的固定相采用多孔凝胶,也被称为凝胶色谱柱、空间排阻色谱柱。其原理是根据凝胶孔隙大小与样品分子尺寸之间的相对关系而对待测组分进行分离,尤其适用于分离生物制品中的大分子与蔗糖。张理火等[24]建立分子排阻色谱法测定猪凝血酶中的蔗糖含量,以亲水硅胶高效体积排阻色谱柱PL aquagel-OH 20(7.5 mm×30 cm,5 μm)进行分离,采用示差折光检测器测定蔗糖含量。猪凝血酶分子尺寸较大,较蔗糖早出峰,从而实现分离,专属性较好。
3.2.4 亲水作用色谱柱 亲水作用色谱(hydrophilic-interaction chromatography,HILIC)柱类似于正相色谱柱的变体,填料为极性固定相,采用高有机相的含水流动相体系,有机相比例约占60%~95%。HILIC 在分析极性和亲水性物质方面具有极大的优势[25]。孙亚灵等[16]比较了3 种HILIC 色谱柱,最终选择分离效果最佳的Waters XBridge Amide(4.6 mm×250 mm,3.5 μm)酰胺键合的杂化硅胶色谱柱测定蔗糖及其有关物质的含量,解决了硅胶氨基柱存在的柱流失严重、方法不耐用等缺点。
总的来说,与经典化学方法和旋光法相比,HPLC 具有较好的专属性、准确度和灵敏度,也提升了检验的便捷性。HPLC 可以适配多种检测器,以满足不同的灵敏度需求。同时,通过选择不同的色谱柱或调节流动相的组成、pH 值、温度、流速等条件,可以实现对不同化合物的选择性分离,因而能够有效排除样品中其他化合物对蔗糖测定的干扰。因此,目前HPLC 在蔗糖含量测定领域中的应用最为广泛。
4 气相色谱法
由于蔗糖极性较大,沸点高达697.1℃,因此不适宜直接采用气相色谱法(gas chromatography,GC)分析,可通过衍生反应取代蔗糖的极性基团羟基以增加其挥发性,从而实现气相色谱法检测。用于碳水化合物衍生的试剂主要包括甲醚、乙酸盐、三氟乙酸酯和硅醚化试剂等。其中,三甲基硅醚衍生产物具有良好的挥发性和稳定性,非常适用于气相色谱法分析,因而应用最广[26]。衍生反应完成后,可根据待测样品中的蔗糖含量选用氢火焰离子化检测器(flame ionization detector,FID)或质谱检测器,以满足不同的灵敏度要求。FID 的电信号来源于有机物在氢火焰中燃烧产生的离子流,该信号与有机物的量成正比。目前药品和生物制品领域较少采用气相色谱法测定蔗糖含量,下文列举本方法在烟草、植物中的部分应用,可为药品和生物制品中的蔗糖含量测定提供一定参考。
张峻松等[27]建立了以三甲基氯硅烷为衍生化试剂,利用GC-FID 法定量分析烟草中葡萄糖、果糖和蔗糖含量的方法。该方法线性、重复性、加标回收率均良好。但相较而言,质谱检测器的灵敏度更高。GOMEZ-GONZALEZ S 等[28]建立GC-MS/MS 法对橄榄果实、叶和茎中的糖进行了定性定量分析。通过超声辅助将待测组分提取至二氯甲烷-甲醇(2∶1)后,利用N,O-双(三甲基硅烷基)三氟乙酰胺和三甲基氯硅烷进行衍生,最后采用质谱Full Scan模式测定。本研究用该方法测定了50 种糖类组分,其中蔗糖的检测限为0.015 μg·mL-1,定量限为0.050 μg·mL-1。
气相色谱法测定糖类的主要优点是能在相对短的分析时间内获得良好的分离度,适用于多种糖类组分的分离和基质复杂的样品。但该方法通常需要经过衍生化反应,不仅耗时较长,而且衍生化的复杂操作也可能影响测定的准确度。
5 近红外光谱法
近红外光(near infrared,NIR)是介于可见光和中红外光间的电磁波,波长通常介于780~2526nm范围内。由于物质的含量与近红外区内多个不同的波长点吸收峰呈线性关系,结合化学计量学的多元校正技术,可利用待测组分结构中含氢基团X-H(X=C、N、O)振动的合频和倍频吸收信息,对待测组分进行定性和定量分析。蔗糖结构中含有在近红外区域具有特征吸收的含氢基团,因此可利用近红外光谱法快速定量分析。近红外光谱法测定物质含量的过程一般包括以下步骤:首先收集足够数量的样品,分为校正集和验证集两组,采用可靠的分析方法获得所有样品的待测组分含量数据;接着采集校正集样品的图谱,经过图谱预处理后,利用化学计量学方法提取数据并建立预测模型;随后通过该模型获得验证集样品的预测值,与实测值比较,确定模型可行;最后进行样品分析。
郝远等[29]采用近红外光谱法结合化学计量学快速测定叶酸片中辅料蔗糖的含量。剔除异常样本后,选择样品化学信息随浓度变化显著的5901~5862 cm-1和8327~8284 cm-1为建模区间建立偏最小二乘模型,随后利用该模型预测5 个未知样品,预测值和参考值误差均小于5%,证明利用近红外光谱定量测定叶酸片中蔗糖含量的方法可行。值得注意的是,选择具有代表性的样本是建模成功的前提和关键,因此用偏最小二乘法建立定量模型前,必须选择合适的校正集和验证集。目前常用的样品集划分方法有Ranksel 法、SPXY 法、Kennard-Stone法、Randsel 法、Duplex 法等。
近红外光谱法具有快速、准确、高效、廉价等优点[30],且无破坏性,属于无损检测技术,可用于样品快速分析和原位在线分析,特别适用于含蔗糖药品及生物制品的生产控制和快速检验。但本方法前期需要收集大量样品用以建立和验证模型,且检测准确度受建模所用样品的数量及代表性影响较大。
6 毛细管电泳法
毛细管电泳(capillary electrophoresis,CE)是一种由经典电泳技术和现代微柱分离相结合的分析方法。其基本原理是以高压电场为驱动力,以毛细管为分离通道,根据样品中各组分在和分配行为上的差异而实现分离。CE 有多种分离模式,其中毛细管区带电泳法最为基础,也是糖类分析中应用最广泛的一种模式。由于蔗糖结构本身不含有共轭基团,因此无法直接采用紫外检测,目前常用的分析方法包括将毛细管电泳联用安培检测器、质谱检测器等,或采用间接紫外检测法。因安培检测器和质谱检测器前文均有提及,故此处主要介绍紫外间接检测法。
蔗糖本身不带电荷,在电泳条件下不具备迁移能力,但可利用强碱性缓冲液(pH >11)或硼酸盐缓冲液使蔗糖解离[31],使其能够在电泳条件下向阳极迁移。同时由于蔗糖无法用紫外直接定量,可将蔗糖置换为具有强紫外吸收的背景电解质溶液从而获得负峰,常见的背景电解质如2,6-吡啶二羧酸、2,6-二甲基苯酚[32]等。通常需要在背景电解质溶液中加入十六烷基三甲基溴化铵,使电渗流方向向阳极反转,缩短分析时间。吴克等[33]建立了毛细管电泳-紫外间接检测法,用于定量测定四价轮状病毒减毒活疫苗原液中的蔗糖含量。背景电解质为含0.3 mmol·L-1CTAB 的60 mmol·L-1PDC 溶液,分离电压为-12×103V,压力进样50 mbar×6 s,柱温25℃,检测波长和参比波长分别为350 nm 和275 nm。该方法专属性良好(图5),蔗糖的迁移时间约为18.0 min,在2.0~10.0 mg·mL-1范围内标准曲线r=0.999 9,检测限为0.2 mg·mL-1,定量限为1.0 mg·mL-1。
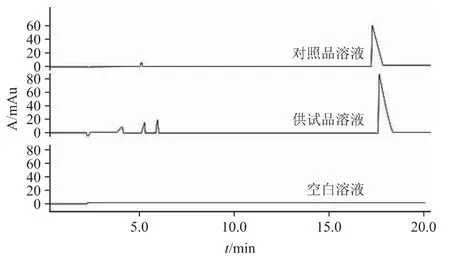
图5 CE 法测定四价轮状病毒减毒活疫苗原液中蔗糖含量的典型色谱图[33]
毛细管电泳法采用毛细管作为分离载体,相较高效液相色谱柱而言分离效能更高,且成本低廉,可以在发生吸附污染后舍弃,尤其适用于分析病毒原液等成分复杂、易污染色谱柱的样品。
7 小 结
本文对目前在药品及生物制品领域常用的各种蔗糖含量测定方法进行了归纳。综上所述,当待测样品中蔗糖含量相对较高,且不存在其他干扰物质时,可采用基于氧化还原反应的经典化学方法或旋光法测定。当待测样品中蔗糖含量相对较低或存在其他干扰物质时,可采用HPLC 法、GC 法或CE法,通过选用恰当的色谱柱和检测器以达到检测目的。其中,HPLC 法应用最为广泛,各类常用的检测器按照灵敏度由低到高排序一般为:示差折光检测器、蒸发光散射检测器、电喷雾检测器、离子色谱-脉冲安培检测器、质谱检测器,其中质谱检测器可以达到10-12级灵敏度;GC 法通常需要柱前衍生化,操作相对较为繁琐;CE 法适用于分析成分复杂、易污染色谱柱的生物制品。此外,针对大批量样品中蔗糖的快速定量分析需求,可考虑采用近红外光谱法结合化学计量学,通过建立适当模型来预测未知样品中的蔗糖含量。
