含香豆素结构的芳氧苯氧丙酸酯衍生物的设计、合成及除草活性研究
2023-11-27叶青青
叶青青,李 娜,丁 雪,雷 康
(1. 滁州城市职业学院 医学院,安徽 滁州 239000;2. 聊城大学 药学院,山东 聊城 252059)
芳氧苯氧丙酸酯 (Aryloxy phenoxy propionate, APP) 类化合物是一类重要的防除禾本科杂草的除草剂 (图1a),能够抑制植物体内乙酰辅酶A羧化酶 (Acetyl CoA carboxylase, ACCase),使植物无法正常合成脂肪酸,从而造成植物细胞中膜系统受损,最终导致植物死亡[1-3]。研究表明,APP类除草剂具有高效、低毒、对后茬作物安全等优点[4],该类除草剂在2014年的全球销售额为12.17亿美元,占除草剂总销售额的4.6 %。正因为APP类除草剂具有绿色农药的特点及良好的市场销量,对其开发已成为国外各大知名农药公司的研究热点,至今已有20多个商品化产品。然而,长期大量施用APP类除草剂使杂草ACCase中的氨基酸发生突变,导致现有的APP类除草剂不能很好的与靶标酶结合,杂草对除草剂的敏感程度降低,最终造成除草剂药效降低[5-8]。如何克服和延缓杂草对APP类除草剂的抗药性问题已经引起农药研究者的关注。目前,一个有效的解决方法就是开发结构新颖、具有更高生物活性的APP类除草剂。

图1 目标化合物CPP和CPA的设计
香豆素天然产物是含有苯并α-吡喃酮结构的一类化合物。研究发现,香豆素天然产物具有多种医用及农用生物活性[9-11],其中部分香豆素天然产物,如4-羟基香豆素[12]、补骨脂素[13]、伞形酮[14]、东莨菪内脂[15]、Wampetin[16]等,具有植物毒性,能够抑制植物生长及种子萌发 (图1b)。因此,本文通过活性亚结构拼接的方法,用香豆素结构代替APP类除草剂的芳环部分,设计合成含香豆素结构的芳氧苯氧羧酸酯类化合物CPP和CPA(图1c),研究其除草活性及构效关系,发现一种含香豆素结构的新型APP类除草剂先导结构。
1 结果与讨论
1.1 目标化合物的合成
目标化合物按照图2所示的路线合成。首先,以R取代邻羟基苯乙酮 (化合物1a~1i) 为原料,在碱性条件下,与碳酸二乙酯 (化合物2) 反应,经过关环反应得到中间体R取代4-羟基香豆素 (化合物3a~3i).中间体3a~3i与三溴化膦在0℃下反应得到中间体R取代4-溴香豆素 (化合物4a~4i)。最后,中间体4a~4i经与4-羟基苯氧羧酸 (化合物5a和5b) 进行亲核取代反应得到目标化合物CPP-1~CPP-9和CPA-1~CPA-9。所合成的18个目标化合物的结构经1HNMR,13CNMR及高分辨质谱确证。
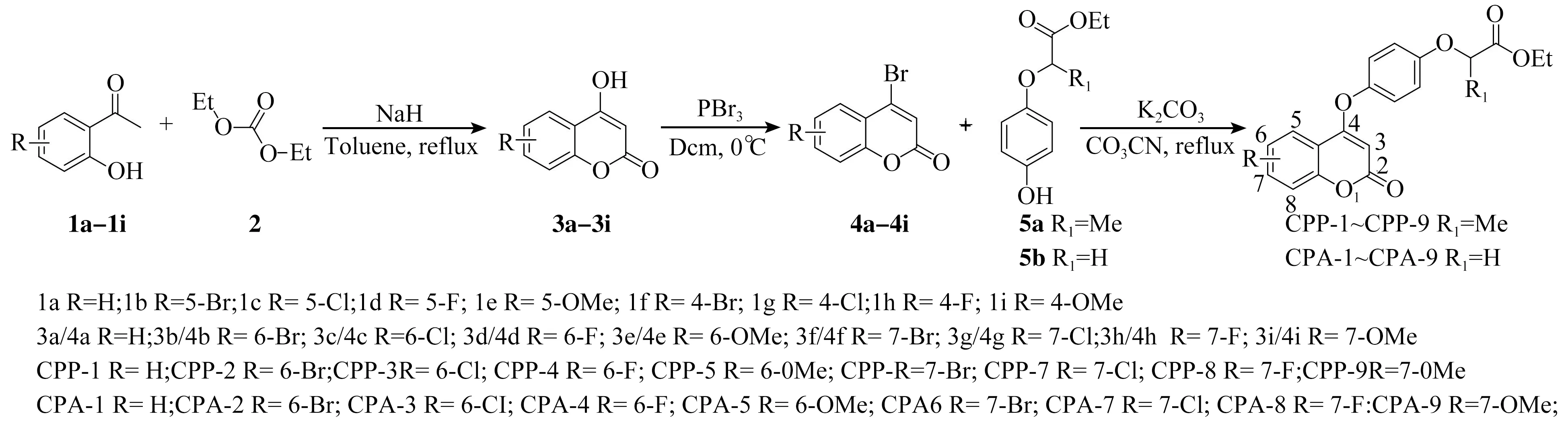
图2 目标化合物CPP-1~CPP-9和CPA-1~CPA-9的合成路线
1.2 目标化合物的除草活性研究
利用油菜平皿法和稗草小杯法对目标化合物的除草活性进行了初步测试。如表1所示,在100 μg/mL的浓度下,目标化合物对单子叶植物稗草的抑制效果优于对双子叶植物油菜的抑制效果,其中,化合物CPP-4对稗草的抑制率达到87.4%,与商品化的除草剂-喹禾灵 (Quizalofop-ethyl, QZ) 的抑制效果相当。这说明目标化合物对单子叶植物具有选择性。然而,在10 μg/mL的浓度下,大部分化合物对测试杂草的抑制效果不理想,仅化合物CPP-2,CPP-3,CPP-4对稗草的抑制率大于40%。

表1 目标化合物CPP-1~CPP-9和CPA-1~CPA-9平皿小杯法的除草活性(抑制率%)a
通过分析化合物CPP-1~CPP-9在100 μg/mL浓度下对稗草的抑制率发现,在香豆素6-位上引入取代基R,化合物CPP-2~CPP-5对稗草的抑制率高于化合物CPP-1;而在香豆素7-位上引入取代基R后,仅化合物CPP-8对稗草的抑制率高于化合物CPP-1,化合物CPP-6,CPP-7和CPP-9对稗草的抑制率低于CPP-1。这说明在香豆素6-位上引入取代基R有利于提高化合物的除草活性。通过分析化合物CPP-2~CPP-5对稗草的抑制率发现,化合物CPP-4的除草活性高于CPP-2,CPP-3和CPP-4,这说明在香豆素6-位引入氟原子比引入溴原子、氯原子和甲氧基更有利于提高化合物的除草活性。有趣的是,通过分析目标化合物CPA-1~CPA-9在100 μg/mL浓度下对稗草的抑制率发现,在香豆素6-位上引入氟原子的化合物CPA-4具有最高的除草活性,与CPP系列化合物的构效关系相似。这些分析结果说明,在香豆素6-位引入氟原子更有利于提高除草活性。另外,通过平行比较法分析CPP系列化合物和CPA系列化合物的除草活性发现,化合物CPP-1~CPP-9对稗草的抑制率均高于对应的化合物CPA-1~CPA-9,这说明当化合物的R1基团为甲基时有利于提高除草活性。因此,当R为6-氟,R1为甲基的化合物是最佳构型。这些初步的构效关系结果为今后化合物的改造提供了一些有用的信息。
随后,我们选取了化合物CPP-2,CPP-3和CPP-4进行了温室盆栽实验,其除草活性数据列于表2。在1 500 g/hm2的剂量下,化合物CPP-2,CPP-3和CPP-4经土壤处理后,对油菜、苋菜、稗草和马唐均具有一定的抑制活性,并且对稗草和马唐的抑制活性高于对油菜和苋菜的抑制活性。例如,化合物CPP-4对稗草和马唐的抑制率分别为82.3%和88.6%,而对油菜和苋菜的抑制率分别为11.2%和9.6%。这说明目标化合物对单子叶植物的抑制效果优于对双子叶植物的抑制效果,与上述小杯平皿实验结论一致。同时我们发现,在1 500 g/hm2的剂量下,化合物CPP-2,CPP-3和CPP-4经茎叶处理后的除草活性均低于经土壤处理后的除草活性。这说明目标化合物适用于土壤处理。随着化合物CPP-2,CPP-3和CPP-4使用剂量的降低,其对杂草的抑制活性显著降低。然而,商品化的除草剂-喹禾灵对单子叶植物稗草和马唐的除草活性并没有随着剂量的降低而下降,甚至在375 g/hm2的剂量下,其对稗草和马唐的抑制率仍然为100%。基于以上结果可以看出,目前合成的目标化合物的除草活性低于商品化除草剂-喹禾灵,但是,在1 500 g/hm2的剂量下,化合物CPP-4具有最高的除草活性,与商品化的除草剂-喹禾灵的除草活性相当,可以作为一个选择性的除草剂先导化合物进行进一步的优化。
2 实验部分
2.1 仪器与试剂
本实验所用试剂均为分析纯或化学纯,购于安耐吉化学试剂有限公司和TCI化学试剂公司;硅胶(200-300目) 从青岛海洋化工厂购得;Bruker 500型核磁共振仪,TMS为内标,氘代氯仿作溶剂;Ionspec 7.0T傅立叶变换离子回旋共振质谱仪,离子源为电喷雾电离源 (ESI)。
2.2 实验方法
2.2.1 中间体3的合成[17,18]。将邻羟基苯乙酮1a (270 mg, 2 mmol) 溶于60 mL的甲苯中,加入碳酸二乙酯2 (350 mg, 3 mmol),降温至0 ℃搅拌,分4批加入60%的NaH (400 mg, 10 mmol),每批间隔5分钟,加完后升温至100 ℃反应4 h,薄层层析(Thin Layer Chromatography, TLC)跟踪反应,待反应结束后,将反应体系冷却至室温,然后将反应体系加入至100 mL冰水中,收集水相,水相用乙醚洗涤2次,然后用2 M HCl酸化至pH=3,有沉淀析出,过滤,收集固体,真空干燥得到白色固体3a (220 mg, 产率68%)。其它中间体化合物3b~3i的合成方法与3a相同。
2.2.2 目标化合物CPP和CPA的合成。将4-羟基香豆素3a (162 mg, 1 mmol) 溶于10 mL的二氯甲烷中,降温至0 ℃搅拌,加入三溴化膦 (268 mg, 1 mmol),室温反应3 h,TLC跟踪反应,待反应结束后,将溶剂旋干,得到棕色固体4a。然后,将4a溶于10 mL乙腈中,依次加入碳酸钾 (207 mg, 1.5 mmol) 和4-羟基苯氧丙酸乙酯5a (210 mg, 1 mmol),反应体系升温至90 ℃反应6 h,TLC跟踪反应,待反应结束后,将溶剂旋干后,残余物经过硅胶柱层析分离(石油醚: 乙酸乙酯=10: 1, 体积比),得到白色固体CPP-1 (166 mg, 产率47%)。目标化合物CPP-2~CPP-9和CPA-1~CPA-9的合成方法与CPP-1相同。
4-((2-氧代-2H-苯并吡喃-4-基)氧)苯氧丙酸乙酯 (CPP-1): 白色固体; 产率47%;1H NMR (500 MHz, CDCl3)δ: 8.01 (dd,J=7.9, 1.4 Hz, 1H), 7.61 (ddd,J=8.6, 7.4, 1.6 Hz, 1H), 7.41-7.31 (m, 2H), 7.11~7.05 (m, 2H), 7.00~6.93 (m, 2H), 5.42 (s, 1H), 4.75 (q,J=6.8 Hz, 1H), 4.26 (q,J=7.1 Hz, 2H), 1.66 (d,J=6.8 Hz, 3H), 1.28 (t,J=7.1 Hz, 3H);13C NMR (125 MHz, CDCl3)δ: 171.79 (s), 166.64 (s), 162.63 (s), 156.02 (s), 153.68 (s), 146.41 (s), 132.78 (s), 124.08 (s), 123.07 (s), 122.24 (s), 116.86 (s), 116.77 (s), 115.44 (s), 93.39 (s), 73.27 (s), 61.47 (s), 18.53 (s), 14.17 (s); HRMS, m/z calcd. for C20H18NaO6+[M+Na]+377.099 6, found 377.100 4。
4-((2-氧代-2H-6-溴苯并吡喃-4-基)氧)苯氧丙酸乙酯 (CPP-2): 白色固体; 产率43.5%;1H NMR (500 MHz, CDCl3)δ: 8.14 (d,J=2.4 Hz, 1H), 7.70 (dd,J=8.8, 2.4 Hz, 1H), 7.24 (s, 1H), 7.10~7.04 (m, 2H), 7.01~6.94 (m, 2H), 5.43 (s, 1H), 4.75 (q,J=6.8 Hz, 1H), 4.26 (q,J=7.1 Hz, 2H), 1.66 (d,J=6.8 Hz, 3H), 1.28 (t,J=7.1 Hz, 3H);13C NMR (125 MHz, CDCl3)δ: 171.76 (s), 165.45 (s), 161.92 (s), 156.15 (s), 152.50 (s), 146.10 (s), 135.61 (s), 125.77 (s), 122.13 (s), 118.61 (s), 117.00 (s), 116.95 (s), 116.80 (s), 94.03 (s), 73.24 (s), 61.50 (s), 18.54 (s), 14.17 (s); HRMS, m/z calcd. for C20H17BrNaO6+[M+Na]+455.010 1, found 455.011 3。
4-((2-氧代-2H-6-氯苯并吡喃-4-基)氧)苯氧丙酸乙酯 (CPP-3): 白色固体; 产率51.5%;1H NMR (500 MHz, CDCl3)δ: 7.99 (d,J=2.5 Hz, 1H), 7.55 (dd,J=8.8, 2.5 Hz, 1H), 7.31 (d,J=8.8 Hz, 1H), 7.10~7.04 (m, 2H), 7.00~6.94 (m, 2H), 5.44 (s, 1H), 4.75 (q,J=6.8 Hz, 1H), 4.26 (q,J=7.1 Hz, 2H), 1.66 (d,J=6.8 Hz, 3H), 1.28 (t,J=7.1 Hz, 3H);13C NMR (125 MHz, CDCl3)δ: 171.75 (s), 165.54 (s), 161.97 (s), 156.14 (s), 152.01 (s), 146.11 (s), 132.77 (s), 129.72 (s), 122.74 (s), 122.13 (s), 118.32 (s), 116.80 (s), 116.56 (s), 94.02 (s), 73.23 (s), 61.49 (s), 18.53 (s), 14.17 (s); HRMS, m/z calcd. for C20H17ClNaO6+[M+Na]+411.060 6, found 411.061 4.
4-((2-氧代-2H-6-氟苯并吡喃-4-基)氧)苯氧丙酸乙酯 (CPP-4): 白色固体; 产率43.7%;1H NMR (500 MHz, CDCl3)δ: 7.67 (dd,J=8.2, 2.3 Hz, 1H), 7.39~7.29 (m, 2H), 7.12~7.04 (m, 2H), 7.02~6.94 (m, 2H), 5.45 (s, 1H), 4.76 (q,J=6.8 Hz, 1H), 4.26 (q,J=7.1 Hz, 2H), 1.66 (d,J=6.8 Hz, 3H), 1.29 (t,J=7.1 Hz, 3H);13C NMR (125 MHz, CDCl3)δ: 171.74 (s), 165.79 (d, J=2.5 Hz), 162.21 (s), 158.73 (d,J=244.1 Hz), 156.12 (s), 149.75 (d,J=1.5 Hz), 146.14 (s), 122.15 (s), 120.28 (d,J=24.6 Hz), 118.47 (d,J=8.3 Hz), 116.79 (s), 116.32 (d,J=8.9 Hz), 108.93 (d,J=25.6 Hz), 94.02 (s), 73.22 (s), 61.48 (s), 18.53 (s), 14.16 (s); HRMS, m/z calcd. for C20H17FNaO6+[M+Na]+395.0901, found 395.091 2。
4-((2-氧代-2H-6-甲氧基苯并吡喃-4-基)氧)苯氧丙酸乙酯 (CPP-5): 白色固体; 产率33.8%;1H NMR (500 MHz, CDCl3)δ: 7.41 (d,J=3.0 Hz, 1H), 7.29 (d,J=9.1 Hz, 1H), 7.18 (dd,J=9.1, 3.0 Hz, 1H), 7.13~7.06 (m, 2H), 7.00~6.94 (m, 2H), 5.41 (s, 1H), 4.76 (q,J=6.8 Hz, 1H), 4.26 (q,J=7.1 Hz, 2H), 3.89 (s, 3H), 1.66 (d, J=6.8 Hz, 3H), 1.29 (t,J=7.1 Hz, 3H);13C NMR (125 MHz, CDCl3)δ: 171.79 (s), 166.44 (s), 162.83 (s), 156.02 (s), 148.13 (s), 146.37 (s), 122.26 (s), 121.06 (s), 118.00 (s), 116.76 (s), 115.66 (s), 104.69 (s), 93.59 (s), 73.24 (s), 61.47 (s), 55.92 (s), 18.53 (s), 14.17 (s); HRMS, m/z calcd. for C21H20NaO7+[M+Na]+407.110 1, found 407.111 0。
4-((2-氧代-2H-7-溴苯并吡喃-4-基)氧)苯氧丙酸乙酯 (CPP-6): 白色固体; 产率61.4%;1H NMR (500 MHz, CDCl3)δ: 7.86 (d,J=8.5 Hz, 1H), 7.55 (d,J=1.8 Hz, 1H), 7.48 (dd,J=8.5, 1.8 Hz, 1H), 7.10~7.04 (m, 2H), 7.00~6.94 (m, 2H), 5.41 (s, 1H), 4.75 (q,J=6.8 Hz, 1H), 4.25 (q,J=7.1 Hz, 2H), 1.66 (d,J=6.8 Hz, 3H), 1.28 (t,J= 7.1 Hz, 3H);13C NMR (125 MHz, CDCl3)δ: 171.76 (s), 166.17 (s), 161.88 (s), 156.12 (s), 153.85 (s), 146.15 (s), 127.56 (s), 126.84 (s), 124.23 (s), 122.16 (s), 120.08 (s), 116.78 (s), 114.45 (s), 93.44 (s), 73.23 (s), 61.50 (s), 18.54 (s), 14.17 (s); HRMS, m/z calcd. for C20H17BrNaO6+[M+Na]+455.010 1, found 455.011 2.
4-((2-氧代-2H-7-氯苯并吡喃-4-基)氧)苯氧丙酸乙酯 (CPP-7): 白色固体; 产率52.3%;1H NMR (500 MHz, CDCl3)δ: 7.86 (d,J=8.5 Hz, 1H), 7.29 (d,J=1.8 Hz, 1H), 7.24 (dd,J=8.5, 1.8 Hz, 1H), 7.03~6.97 (m, 2H), 6.92~6.86 (m, 2H), 5.32 (s, 1H), 4.68 (q,J=6.8 Hz, 1H), 4.18 (q,J=7.1 Hz, 2H), 1.58 (d,J=6.8 Hz, 3H), 1.20 (t,J=7.1 Hz, 3H);13C NMR (125 MHz, CDCl3)δ: 171.74 (s), 166.09 (s), 161.95 (s), 156.10 (s), 153.91 (s), 146.15 (s), 138.78 (s), 124.72 (s), 124.15 (s), 122.16 (s), 117.08 (s), 116.77 (s), 114.05 (s), 93.22 (s), 73.21 (s), 61.48 (s), 18.53 (s), 14.17 (s); HRMS, m/z calcd. for C20H17ClNaO6+[M+Na]+411.060 6, found 411.061 6。
4-((2-氧代-2H-7-氟苯并吡喃-4-基)氧)苯氧丙酸乙酯 (CPP-8): 白色固体; 产率51.1%;1H NMR (500 MHz, CDCl3)δ: 8.00 (dd,J=8.3, 6.7 Hz, 1H), 7.08 (td,J=8.0, 1.8 Hz, 4H), 6.97 (d,J=9.0 Hz, 2H), 5.36 (s, 1H), 4.76 (q,J=6.7 Hz, 1H), 4.26 (q,J=7.1 Hz, 2H), 1.66 (d,J=6.8 Hz, 3H), 1.29 (t,J=7.1 Hz, 3H);13C NMR (125 MHz, CDCl3)δ: 171.75 (s), 166.25 (s), 165.21 (d,J=254.3 Hz), 162.30 (s), 156.08 (s), 154.88 (d,J=13.3 Hz), 146.17 (s), 125.01 (d,J=10.3 Hz), 116.75 (s), 112.16 (dd,J=23.9, 12.7 Hz), 104.28 (d,J=25.7 Hz), 92.29 (d,J=1.5 Hz), 73.21 (s), 61.47 (s), 18.52 (s), 14.16 (s); HRMS, m/z calcd. for C20H17FNaO6+[M+Na]+395.090 1, found 395.091 2.
4-((2-氧代-2H-7-甲氧基苯并吡喃-4-基)氧)苯氧丙酸乙酯 (CPP-9): 白色固体; 产率48.3%;1H NMR (500 MHz, CDCl3)δ: 7.89 (d,J=8.8 Hz, 1H), 7.09~7.05 (m, 2H), 6.98~6.93 (m, 2H), 6.90 (dd,J=8.8, 2.4 Hz, 1H), 6.83 (d,J=2.4 Hz, 1H), 5.26 (s, 1H), 4.75 (q,J=6.8 Hz, 1H), 4.31~4.19 (m, 2H), 3.90 (s, 3H), 1.65 (d,J=6.8 Hz, 3H), 1.28 (t,J=7.1 Hz, 3H);13C NMR (125 MHz, CDCl3)δ: 171.82 (s), 167.00 (s), 163.58 (s), 163.16 (s), 155.92 (s), 155.53 (s), 146.44 (s), 124.13 (s), 122.28 (s), 116.67 (s), 112.39 (s), 108.63 (s), 100.56 (s), 90.76 (s), 73.24 (s), 61.46 (s), 55.81 (s), 18.53 (s), 14.16 (s); HRMS, m/z calcd. for C21H20NaO7+[M+Na]+407.110 1, found 407.111 1。
4-((2-氧代-2H-苯并吡喃-4-基)氧)苯氧乙酸乙酯 (CPA-1): 白色固体; 产率56.2%;1H NMR (500 MHz, CDCl3)δ: 8.01 (dd,J=7.9, 1.4 Hz, 1H), 7.65~7.58 (m, 1H), 7.41~7.31 (m, 2H), 7.16~7.07 (m, 2H), 7.05~6.97 (m, 1H), 5.42 (s, 1H), 4.65 (s, 2H), 4.30 (q,J=7.1 Hz, 2H), 1.32 (t,J=7.1 Hz, 3H);13C NMR (125 MHz, CDCl3) δ: 168.55 (s), 166.62 (s), 162.59 (s), 156.25 (s), 153.67 (s), 146.59 (s), 132.80 (s), 124.10 (s), 123.06 (s), 122.31 (s), 116.86 (s), 116.37 (s), 115.41 (s), 93.41 (s), 65.92 (s), 61.54 (s), 14.19 (s); HRMS, m/z calcd. for C19H17O6+[M+H]+341.102 0, found 341.103 0。
4-((2-氧代-2H-6-溴苯并吡喃-4-基)氧)苯氧乙酸乙酯 (CPA-2): 白色固体; 产率52.8%;1H NMR (500 MHz, CDCl3)δ: 8.14 (d, J=2.4 Hz, 1H), 7.70 (dd, J=8.8, 2.4 Hz, 1H), 7.12~7.07 (m, 2H), 7.04~6.98 (m, 2H), 5.43 (s, 1H), 4.66 (s, 2H), 4.30 (q, J=7.1 Hz, 2H), 1.33 (t, J=7.1 Hz, 3H);13C NMR (125 MHz, CDCl3) δ: 168.51 (s), 165.43 (s), 161.86 (s), 156.38 (s), 152.49 (s), 146.28 (s), 135.62 (s), 125.76 (s), 122.20 (s), 118.61 (s), 94.04 (s), 65.88 (s), 61.58 (s), 14.19 (s); HRMS, m/z calcd. for C19H16BrO6+[M+H]+419.012 5, found 419.013 7。
4-((2-氧代-2H-6-氯苯并吡喃-4-基)氧)苯氧乙酸乙酯 (CPA-3): 白色固体; 产率49.4%;1H NMR (500 MHz, CDCl3)δ: 7.99 (d,J=2.5 Hz, 1H), 7.56 (dd,J=8.9, 2.5 Hz, 1H), 7.31 (d,J=8.9 Hz, 1H), 7.13~7.06 (m, 2H), 7.04~6.98 (m, 2H), 5.44 (s, 1H), 4.66 (s, 2H), 4.30 (q,J=7.1 Hz, 2H), 1.33 (t,J=7.1 Hz, 3H);13C NMR (125 MHz, CDCl3)δ: 168.53 (s), 165.55 (s), 161.99 (s), 156.37 (s), 152.01 (s), 146.29 (s), 132.81 (s), 129.74 (s), 122.74 (s), 122.20 (s), 118.34 (s), 116.42 (s), 94.04 (s), 65.88 (s), 61.59 (s), 14.19 (s); HRMS, m/z calcd. for C19H15ClNaO6+[M+Na]+397.044 9, found 397.045 7。
4-((2-氧代-2H-6-氟苯并吡喃-4-基)氧)苯氧乙酸乙酯 (CPA-4): 白色固体; 产率42.9%;1H NMR (500 MHz, CDCl3)δ: 7.70~7.63 (m, 1H), 7.33 (dd,J=6.9, 2.4 Hz, 2H), 7.13~7.07 (m, 2H), 7.05~6.98 (m, 2H), 5.45 (s, 1H), 4.66 (s, 2H), 4.30 (q,J=7.1 Hz, 2H), 1.32 (t,J=7.1 Hz, 3H);13C NMR (125 MHz, CDCl3)δ: 168.54 (s), 165.80 (d,J=2.5 Hz), 162.24 (s), 158.72 (d,J=244.4 Hz), 156.33 (s), 149.73 (d,J=1.6 Hz), 146.30 (s), 122.20 (s), 120.31 (d,J=24.6 Hz), 118.48 (d,J=8.2 Hz), 116.40 (s), 116.29 (d,J=9.0 Hz), 116.04 (d,J=14.2 Hz), 108.92 (d,J=25.5 Hz), 93.99 (s), 65.84 (s), 61.55 (s), 14.17 (s); HRMS, m/z calcd. for C19H15FNaO6+[M+Na]+381.074 5, found 381.075 1。
4-((2-氧代-2H-6-甲氧基苯并吡喃-4-基)氧)苯氧乙酸乙酯 (CPA-5): 白色固体; 产率50.3%;1H NMR (500 MHz, CDCl3)δ: 7.42 (d,J=3.0 Hz, 1H), 7.29 (t,J= 7.8 Hz, 1H), 7.19 (dd,J=9.1, 3.0 Hz, 1H), 7.14~7.09 (m, 2H), 7.04~6.98 (m, 2H), 5.41 (s, 1H), 4.66 (s, 2H), 4.30 (q,J=7.1 Hz, 2H), 3.89 (s, 3H), 1.33 (t,J=7.1 Hz, 3H);13C NMR (125 MHz, CDCl3)δ: 168.55 (s), 166.43 (s), 162.81 (s), 156.25 (s), 156.03 (s), 148.14 (s), 146.56 (s), 122.33 (s), 121.08 (s), 118.02 (s), 116.37 (s), 115.65 (s), 104.69 (s), 93.63 (s), 65.91 (s), 61.56 (s), 55.93 (s), 14.19 (s); HRMS, m/z calcd. for C20H18NaO7+[M+Na]+393.094 5, found 393.095 1。
4-((2-氧代-2H-7-溴苯并吡喃-4-基)氧)苯氧乙酸乙酯 (CPA-6): 白色固体; 产率44.7%;1H NMR (500 MHz, CDCl3)δ: 7.87 (d,J=8.5 Hz, 1H), 7.55 (d,J=1.8 Hz, 1H), 7.48 (dd,J=8.5, 1.8 Hz, 1H), 7.13~7.07 (m, 1H), 7.04~6.97 (m, 1H), 5.42 (s, 1H), 4.65 (s, 1H), 4.30 (q,J=7.1 Hz, 1H), 1.32 (t,J=7.1 Hz, 1H);13C NMR (125 MHz, CDCl3)δ: 168.52 (s), 166.15 (s), 161.86 (s), 156.35 (s), 153.85 (s), 146.34 (s), 127.57 (s), 126.86 (s), 124.22 (s), 122.23 (s), 120.09 (s), 116.40 (s), 114.43 (s), 93.47 (s), 65.89 (s), 61.58 (s), 14.19 (s); HRMS, m/z calcd. for C19H15BrNaO6+[M+Na]+440.994 4, found 440.995 0。
4-((2-氧代-2H-7-氯苯并吡喃-4-基)氧)苯氧乙酸乙酯 (CPA-7): 白色固体; 产率53.5%;1H NMR (500 MHz, CDCl3)δ: 7.94 (d,J=8.5 Hz, 1H), 7.38 (d,J=1.9 Hz, 1H), 7.33 (dd,J=8.5, 2.0 Hz, 1H), 7.12~7.07 (m, 2H), 7.04~6.97 (m, 2H), 5.40 (s, 1H), 4.66 (s, 2H), 4.30 (q,J=7.1 Hz, 2H), 1.32 (t,J=7.1 Hz, 3H);13C NMR (125 MHz, CDCl3)δ: 168.53 (s), 166.10 (s), 161.98 (s), 156.34 (s), 153.93 (s), 146.34 (s), 138.83 (s), 124.75 (s), 124.15 (s), 122.23 (s), 117.12 (s), 116.40 (s), 114.04 (s), 93.26 (s), 65.88 (s), 61.58 (s), 14.19 (s); HRMS, m/z calcd. for C19H15ClNaO6+[M+Na]+397.044 9, found 397.045 5。
4-((2-氧代-2H-7-氟苯并吡喃-4-基)氧)苯氧乙酸乙酯 (CPA-8): 白色固体; 产率57.6%;1H NMR (500 MHz, CDCl3)δ: 8.08~7.92 (m, 1H), 7.14~7.05 (m, 4H), 7.05~6.97 (m, 2H), 5.36 (s, 1H), 4.66 (s, 2H), 4.30 (q,J=7.1 Hz, 2H), 1.33 (t,J=7.1 Hz, 3H);13C NMR (125 MHz, CDCl3)δ: 168.52 (s), 166.23 (s), 164.21 (s), 162.27 (s), 156.31 (s), 154.89 (d,J=13.0 Hz), 146.35 (s), 125.01 (d,J=10.4 Hz), 122.25 (s), 116.37 (s), 112.26 (d, J=22.7 Hz), 112.05 (d,J=2.6 Hz), 104.29 (d,J=25.6 Hz), 92.32 (d,J=1.6 Hz), 65.86 (s), 61.55 (s), 14.18 (s); HRMS, m/z calcd. for C19H15FNaO6+[M+Na]+381.074 5, found 381.075 5。
4-((2-氧代-2H-7-甲氧基苯并吡喃-4-基)氧)苯氧乙酸乙酯 (CPA-9): 白色固体; 产率40.3%;1H NMR (500 MHz, CDCl3)δ: 7.89 (d,J=8.8 Hz, 1H), 7.13~7.06 (m, 1H), 7.03~6.96 (m, 1H), 6.91 (dd,J=8.8, 2.4 Hz, 1H), 6.84 (d,J=2.4 Hz, 1H), 5.27 (s, 1H), 4.65 (s, 1H), 4.30 (q,J=7.1 Hz, 1H), 3.90 (s, 1H), 1.32 (t,J=7.1 Hz, 1H);13C NMR (125 MHz, CDCl3)δ: 168.58 (s), 166.99 (s), 163.60 (s), 163.14 (s), 156.16 (s), 155.54 (s), 146.63 (s), 124.13 (s), 122.35 (s), 116.28 (s), 112.41 (s), 108.62 (s), 100.57 (s), 90.80 (s), 65.91 (s), 61.54 (s), 55.82 (s), 14.19 (s); HRMS, m/z calcd. for C20H18NaO7+[M+Na]+393.094 5, found 393.095 3。
2.3 除草活性测定[19-21]
油菜平皿法:直径6 cm的培养皿中铺好一张直径5.6 cm的滤纸,加入2 mL一定浓度的供试化合物溶液,播种浸种4~6 h的油菜种子15粒,在(28±1)℃下黑暗培养66 h后测定胚根长度。通过黑暗条件下化合物对油菜胚根的生长抑制来检测化合物的除草活性,每个实验组设置三个平行。
稗草小杯法:在50 mL的烧杯底部铺满一层大小一致的玻璃球,然后放一张与杯底大小一致的滤纸,加入配置好的待测化合物溶液,并设置一个只加蒸馏水的空白对照。播种出芽一致的稗草种子10粒,在(28±1)℃的光室内培养60 h,测定稗草幼苗地上长度。通过光照条件下化合物对稗草幼苗株高的生长抑制来检测化合物的除草活性,每个实验组设置三个平行。
土壤处理:在直径8 cm的塑料小杯中放入一定量的土,加入一定量的水,播种后覆盖一定厚度的土壤,于花房中培养,幼苗出土前以塑料覆盖。每天加一定量的清水以保持正常生长。土壤处理(出苗前),14天后调查结果,测定地上部鲜重,以鲜重抑制百分数来表示药效,每个实验组设置三个平行。
茎叶处理:在直径8 cm的塑料小杯中放入一定量的土,加入一定量的水,播种后覆盖一定厚度的土壤,于花房中培养,幼苗出土前以塑料覆盖。每天加一定量的清水以保持正常生长。当幼苗长到一定时期进行茎叶喷雾处理,21天后调查结果,测定地上部鲜重,以鲜重抑制百分数来表示药效,每个实验组设置三个平行。
3 结论
以取代邻羟基苯乙酮和碳酸二乙酯为原料,经三步反应合成了18个含香豆素结构的芳氧苯氧羧酸类化合物,其结构经1HNMR,13CNMR及高分辨质谱确证.初步的平皿小杯活性测试结果显示,该类化合物对单子叶植物具有较好的抑制活性。其中,化合物CPP-4在100 μg/mL浓度下对稗草的抑制率达到87.4%。通过构效关系研究发现,在香豆素的6-位引入取代基有利于提高化合物的除草活性,且在香豆素6-位引入氟原子比引入溴原子、氯原子或甲基更有利于提高除草活性;通过平行比较法分析了化合物CPP和CPA的除草性,发现当R1为甲基时有利于提高化合物的除草活性。这些初步的构效关系结果为今后化合物的改造提供了一些有用的信息。此外,温室盆栽活性测试结果显示,在1 500 g/hm2施药量情况下,化合物CPP-4对稗草和马唐的土壤处理呈现出很好的防除效果,抑制率达到80%以上。因此,化合物CPP-4可以作为新型芳氧苯氧羧酸酯类除草剂先导化合物进行进一步的优化。
