掺杂修饰碳糊电极对蔬菜中镉的电化学快速检测
2023-11-26罗惠莉张舸帆黄一璐龙雯琪周颖
罗惠莉,张舸帆,黄一璐,龙雯琪,周颖
(1 湖南农业大学环境与生态学院 长沙410128 2 国家环境保护重金属污染监测重点实验室 长沙410019 3 湖南国标检测科技有限公司 长沙 410005)
重金属污染已对生态环境、食品安全和人类健康构成威胁。近年来Cd 在国内谷物及米制品[1-3]、蔬菜[4-6]、茶叶[7]、水产品[8-9]等中均有检出,是农产品和食品质量安全最受关注的重金属元素之一。梁晓聪等[1]分析了陕西省2002-2018 年市售谷物中Cd 污染状况,结果显示Cd 的平均值为0.022 mg/kg,超标率为1.39%。曾婷婷等[6]对重庆蔬菜基地的辣椒中Cd 进行检测,Cd 含量为0.007~0.091 mg/kg,有3 份辣椒样品Cd 超标。邢仕歌等[8]抽测了2018-2020 年北京市售83 份蟹类样品中的Cd 含量,平均值为0.647 mg/kg。随着农产品和食品质量安全要求的提高,对重金属实时快速检测的需求迫切。
在实验室检测Cd 的常见方法有电感耦合等离子体质谱法(ICP-MS)[4,10]和原子吸收光谱法(AAS)[11-12]。近年来电化学检测技术的发展,使其在重金属快速检测中应用增多,主要仍集中在水样检测[13-14],而食品、农产品中Cd 的电化学检测较少。碳糊电极(CPE)因制作简单,背景电流低、电极表面容易更新等特点[15]而具有较好的应用价值。如Ogunlesi等[16]以玻碳电极(GCE)为工作电极,采用线性扫描阳极溶出伏安法(LSASV)检测玉米叶和小米叶中的Cd。样品经65%的HNO3和70%的HClO4消化处理,检出量为0.00~5.74 mg/kg,部分超过联合国粮食及农业组织规定限值(2 mg/kg)。近来,纳米金属及其氧化物因表面积大、吸附容量高而受到关注并应用于电极修饰[13,17-18]。如Ashrafi等[17]采用锑纳米粒子/多壁碳纳米管修饰的CPE 对小麦粉中Cd 进行检测,检测限为0.65 μg/L。
植物和食品样品比水样品成分复杂,往往需通过酸消解后转为待测液。也有通过预处理提取重金属后再检测。Silva等[19]用7 mol/L 硝酸溶液和超声波提取巧克力中的Cd、Pb 和Cu,采用方波阳极溶出伏安法(SWASV)-薄型凝胶膜修饰玻碳电极,同时测定Cd、Pb 和Cu 的检测限达到0.089,0.059,0.018 μg/g。Wang等[20]采用稀酸萃取,ASVGCE 快速现场测定小龙虾中Cd,检出限为0.005 mg/kg。蔬菜样品不经消解,直接进行重金属电化学测定的研究[21]很少,如:Ion等[21]在测定卷心菜中Pb(DPV 法)时,直接将卷心菜切块,加入0.01 mol/L 磷酸盐缓冲液后制成汁,使用表面氨基化剥落石墨纳米板铋修饰电极(CO-NH2-xGnP/GCE),在铋膜沉积预浓缩下测定Pb。
本研究选择3 种常见的含水率高的蔬菜——黄瓜、西红柿、小白菜为试验材料,参考Silva等[19]和Ion等[21]的前处理方式,将蔬菜样匀浆后用0.1 mol/L 硝酸稀释并超声提取。采用纳米氧化铝/氧化铋掺杂修饰的碳糊电极(CPE),经方波阳极溶出伏安法(SWASV)检测其中的Cd。比较不同蔬菜基质对Cd 电化学检测的基质效应,确定适宜检测的基质稀释比。本研究结果对开发蔬菜中重金属快速检测技术,简化检测流程,推动自动化检测设备研发有积极的意义。
1 材料与方法
1.1 试验材料与试剂
1.1.1 试剂 Cd 标准溶液(1 000 mg/L,标准物质);氯化亚锡(SnCl2)、铁氰化钾(K3[Fe(CN)6])、醋酸、硝酸,均为分析纯。石墨粉(微米级),石蜡油(化学纯);氧化铝,氧化铋(纳米级)。
1.1.2 试验材料 试验用的蔬菜均购自周边市场。其中黄瓜基质的电导率为0.43 ms/cm,pH 值为6.32;西红柿基质的电导率为2.73 ms/cm,pH值为4.31;小白菜基质的电导率为1.39 ms/cm,pH值为6.48。
1.2 试验仪器
电化学工作站(CHI830D),上海辰华仪器公司,参比电极为甘汞电极,对电极为铂电极,工作电极为CPE 电极;电导率仪(DDSJ-308A),上海精密仪器有限公司;pH 计(PHS-3C),上海精密仪器有限公司;ICP-MS(NexlON 1000),美国珀金埃尔默股份有限公司。
1.3 电化学检测方法
于电解池中加入0.1 mol/L 醋酸-醋酸钠缓冲溶液,SnCl2溶液和待测液。选用SWASV 法,工作电压-1.4 V 持续120 s,然后施加正向方波扫描电势:方波振幅:25 mV;步进电势:5 mV;方波频率:25 Hz,由-1.4 V 扫描至0 V。由溶出峰电流值(Ip)对Cd 浓度进行定量分析。
1.4 CPE 电极掺杂修饰及优化
CPE 电极及修饰:石墨粉与液体石蜡(质量比3∶1)混合,研磨均匀装填压实,表面打磨光滑。采用掺杂法修饰时,在石墨粉中掺入10%~30%的修饰剂。
以氧化铝、氧化铋为修饰剂分别对CPE 进行修饰,参考Svancara等[22]的研究,将掺加比例控制在10%~30%。通过比较对Cd 检测响应值,确定适宜的掺加比。比较以氧化铝、氧化铋、氧化铝/氧化铋作为修饰剂的检测差异,以确定对Cd 检测最优的掺杂修饰电极。
1.5 样品处理与检测
蔬菜样匀浆后超声破壁并脱气,密封冷藏。检测前基质样品经1% HNO3稀释后超声。根据1.3节检测条件和1.4 节确定的修饰CPE 检测其中的Cd,确定样品检测的适宜稀释比和检测操作条件。
1.6 基质效应与干扰分析
结合XRF 分析,考察基质中含量较高金属元素的离子,如K+,Ca2+,Mg2+,Fe3+,Fe2+和Zn2+等对Cd电化学检测干扰,明确主要干扰金属离子。
1.7 电化学检测的准确性验证
对添加Cd 的蔬菜样品分别通过SWASV 法与ICP/MS 检测,比较2 种方法的检测结果,分析SWASV 法检测的准确性。
ICP/MS 检测的样品,参考Xu等[23]的样品前处理,蔬菜样经浓HNO3∶HClO4=4∶1 湿法消解。
2 结果与分析
2.1 掺杂修饰及优化
2.1.1 单一掺杂修饰 以氧化铝、氧化铋为修饰剂,分别替代石墨粉的质量比(即掺加比)为10%,20%和30%。用修饰的CPE 检测10 μg/L Cd,比较2 种修饰剂的差异,初步确定适宜的掺加比。
结果表明,掺加20%氧化铝时,对Cd 的检测响应最大,Ip为2.311 μA;相比未修饰CPE 检测的Ip值增加了62.98%。氧化铝掺加比从10%增加到20%,Ip值增加了18.42%;而由20%增加到30%,Ip值反而下降了17.94%。掺加20%氧化铋时修饰效果也好于其它比例。但氧化铋掺加比由20%提高至30%,Ip值差异不大。
根据以上试验结果,初步确定修饰剂适宜的掺加比为20%。
2.1.2 掺杂修饰优化 在2.1.1 节试验基础上,以氧化铝为主修饰剂,氧化铋掺加比取1%,5%,8%,总掺加比为20%,进行氧化铝/氧化铋混合修饰。图1 为20%氧化铝、20%氧化铋、15%氧化铝/5%氧化铋作修饰剂,检测10 μg/L Cd 的溶出伏安图。
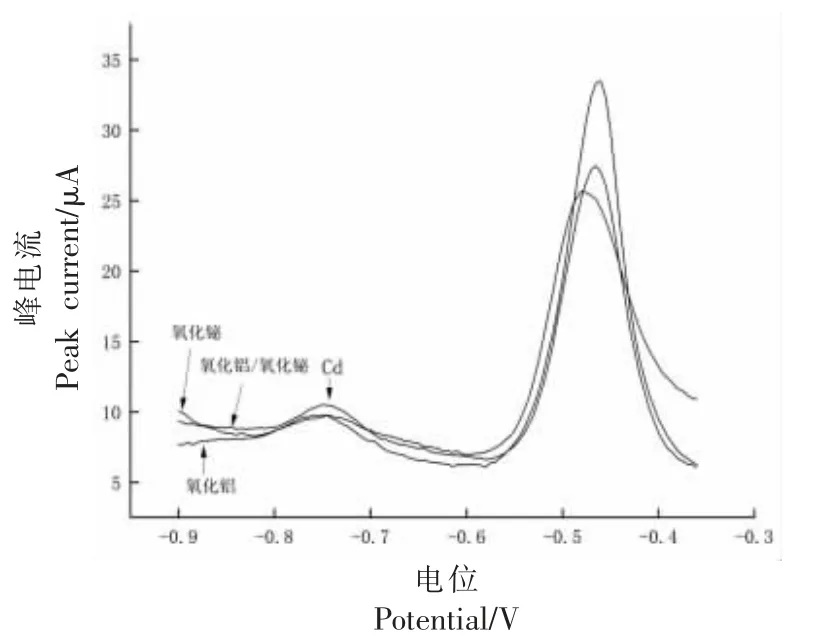
图1 修饰剂对Cd 检测响应的影响Fig.1 Effects of modifier on Cd detection response

图2 Cd 的检测标准曲线和溶出伏安图Fig.2 Standard curve and voltammogram of Cd
以20%氧化铝修饰电极为比较基础,15%氧化铝/5%氧化铋修饰电极对10 μg/L Cd 的峰电流值为2.559 μA,好于其它掺加比(2.227 和2.249 μA);也好于单独掺加氧化铝或氧化铋;且Cd 的溶出峰峰形得到改善。因此后续试验采用15%氧化铝/5%氧化铋混合修饰电极(记为DMCPE)。
用金属氧化物修饰电极,能扩大CPE 的比表面积,富集待测离子[24];同时促进电子转移,增强离子溶出响应[25]。但掺加超过一定量,即修饰剂浓度过高,会使得电极的欧姆电阻率和背景电流增加[26],从而影响沉积物剥离,导致溶出峰电流值下降。氧化铋修饰相比氧化铝对Cd 检测的响应稍差,但掺加氧化铋后利于Sn 的沉积和溶出[27],从而通过Cd-Sn 共沉淀影响Cd 的溶出响应(见图1)。这与Zheng等[25]的研究一致。
2.2 蔬菜基质对Cd 的检测影响
2.2.1 确定蔬菜基质的稀释比 分析基质对Cd电化学检测的影响,Cd2+质量浓度为30 μg/L,分别在静置和搅拌(转速为80 r/min)时对Cd 检测,以得到稳定的检测条件。黄瓜、西红柿、小白菜各基质稀释比(待测液体积/基质体积)见表2。
静置检测条件下,黄瓜基质稀释倍数为30,西红柿基质稀释倍数为100,小白菜基质稀释倍数为300 时,相比对应空白(不加基质)的Cd 溶出峰电流值分别降低6.55%,3.23%,9.52%。增加基质添加量,Cd 峰电流值进一步降低。
采取低速搅拌,黄瓜稀释倍数仍取30,此时Cd 峰电流降低9.23%。西红柿稀释倍数100 降为60,Cd 峰电流降低9.93%。小白菜稀释倍数可采用100,Cd 峰电流降低7.68%。表明低速搅拌时比静置时检测响应稍高,最主要的是小白菜样品稀释比降低了,有利于提高检测准确性。
比较3 种蔬菜基质对Cd 检测的干扰影响(由大到小):小白菜>西红柿>黄瓜。这与基质的电导率排序一致,表明基质中离子(尤其是金属阳离子)对Cd 检测有干扰。
2.2.2 主要干扰离子分析 根据表1 中主要金属元素含量,考察含量较高的K+,Ca2+,Mg2+,Fe3+,Fe2+和Zn2+的检测干扰。以小白菜中各元素含量为基数值,稀释60 倍(取整数值)后,以DMCPE 分析其对30 μg/L Cd 的检测影响。结果发现主要是Zn的干扰,1.5 mg/L 的Zn2+使Cd 的Ip值下降了16.07%。
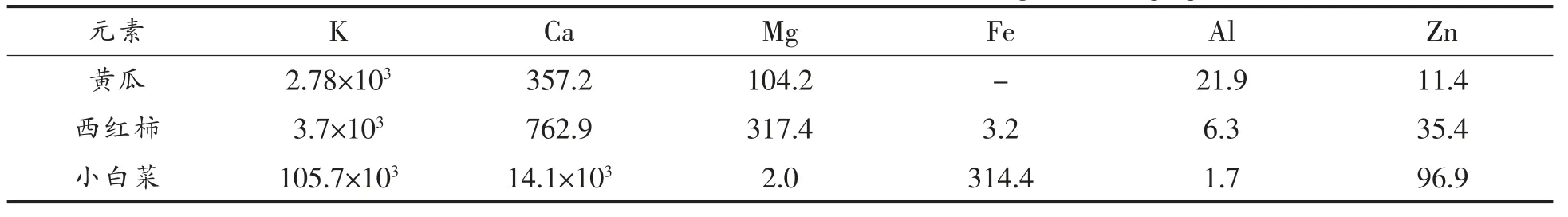
表1 蔬菜中主要金属元素含量(mg/kg)Table 1 Contents of main elements in the three vegetables(mg/kg)
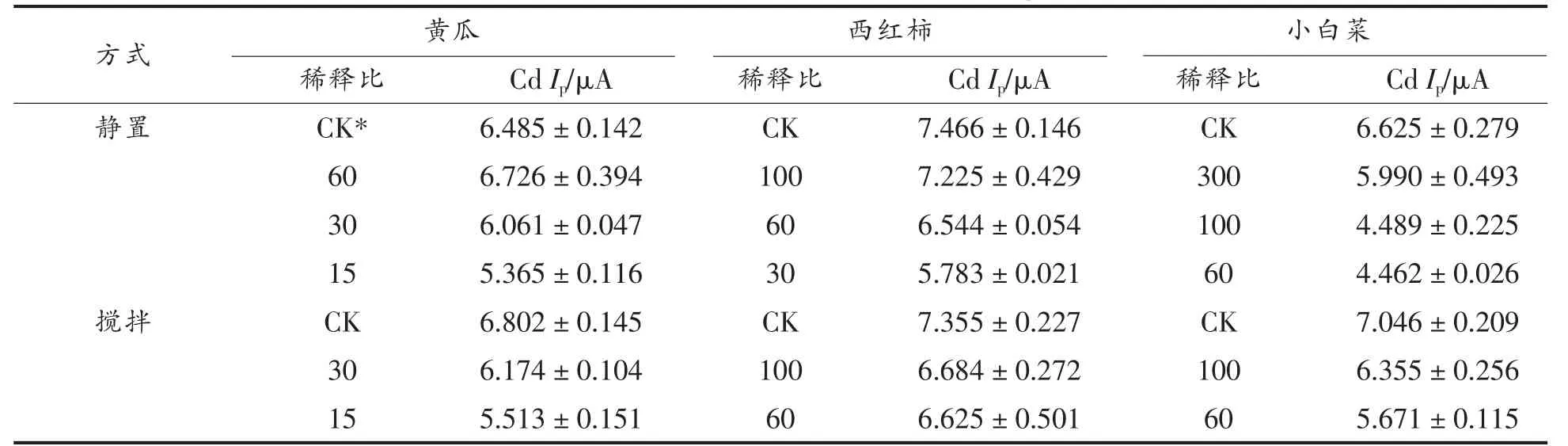
表2 蔬菜中Cd 检测的稀释比Table 2 Dilution ratio for Cd detection in vegetables
在前期试验中,以西红柿中较高含量金属进行的干扰分析也表明,Zn 对Cd 检测干扰最大。以未修饰CPE 检测100 μg/L Cd 时,0.8 mg/L 的Zn2+使Cd 的Ip值下降了34.87%;8 mg/L Mg2+使Cd 的Ip值下降了20.03%;而K+,Ca2+的干扰影响小。
由于小白菜中Mg 含量不高,以西红柿中Mg含量为基础,同前期试验(稀释40 倍,测100 μg/L Cd),发现采用DMCPE 检测,Mg2+造成Cd 的Ip值只降低了9.02%。
试验结果表明,蔬菜中高含量的Zn、Mg 对Cd的电化学检测有干扰;采用DMCPE 可降低这些干扰离子的影响。
Yukird等[28]测定废水中Cd(II)和Zhao等[29]测定土壤中Cd(II)时,均发现Zn(II)会产生干扰。相比重金属Cd,Zn 易于被植物吸收,尤其是白菜类的蔬菜易富集Zn,因此采用电化学方法检测蔬菜中Cd 时,要考虑高浓度Zn 的干扰和消除,这值得进一步研究。但少有文献报道分析Mg 的干扰影响。
2.3 Cd 检测方法
2.3.1 检测标准曲线 以15%氧化铝/5%氧化铋修饰的CPE 为工作电极,方波振幅25 mV;步进电势5 mV;方波频率25 Hz;工作电压-1.4 V;沉积时间120 s,SnCl2质量浓度为3.5 mg/L,低速搅拌。建立Cd 的检测标准曲线。其线性范围为0.2~70 μg/L。线性回归方程及相关系数为:Ip=0.1774C+0.3646(Ip:μA,C:μg/L);R=0.9983,检测限为0.2 μg/L。
2.3.2 添加回收试验 根据2.2.1 节试验结果,在蔬菜样品中添加0.1 mg/kg 和1 mg/kg 的Cd,按照1.5 节进行样品前处理,黄瓜、西红柿、小白菜基质稀释比分别取30,60,100。按照2.3.1 节检测条件进行检测,添加回收率、相对标准偏差见表3。另外取蔬菜样品,添加0.1 mg/kg 的Cd,按上述稀释比和SWASV 法检测,同时按照1.7 节样品处理后经ICP-MS 检测,2 种检测方法结果比较见表3。

表3 SWASV 法测Cd 的添加回收率及与ICP-MS 检测比较Table 3 Recovery rate of Cd detection by SWASV and comparison with ICP-MS
对3 种蔬菜样品两个浓度的添加试验,添加回收率在87.45%~101.14%。表明在上述样品处理和检测条件下能有效进行该3 种高含水蔬菜中Cd 的电化学检测。
SWASV 法对Cd 检测可达到ICP/MS 检测的87.25%~108.25%。总体来看,利用本文建立的DMCPE-SWASV 法对蔬菜中Cd 进行检测是满足检测要求的。
3 结论
1)氧化铝和氧化铋修饰CPE 均提高了Cd的检测响应。采用15%氧化铝/5%氧化铋修饰电极DMCPE 对Cd 检测线性范围为0.2~70 μg/L,线性相关系数r=0.9983,方法检测限为0.2 μg/L。
2)蔬菜样经过匀浆-HNO3稀释-超声提取的前处理,黄瓜基质稀释比为30,西红柿稀释比为60,小白菜稀释比为100 时,采用DMCPE-SWASV法检测Cd 的添加回收率为87.45%~101.14%。
3)3 种蔬菜基质对Cd 检测的影响为:小白菜>西红柿>黄瓜。与基质的电导率排序一致。蔬菜中高含量的Zn、Mg 对Cd 的电化学检测有干扰,其中Zn2+对Cd2+检测干扰最大,其次是Mg2+。采用DMCPE 测Cd 时,离子造成的干扰小于采用未修饰CPE 时。
4)SWASV 法对Cd 检测值可达到ICP/MS 检测结果的87.25%~108.25%。采用本文建立的DMCPE-SWASV 法对高含水蔬菜中Cd 进行检测可实现准确的快速检测。
由于Zn、Mg 是蔬菜易吸收的微量元素,基质中这些离子,尤其是Zn,对重金属电化学检测的干扰影响还需要进一步研究。
