L-白雀木醇通过激活Wnt/β-catenin信号通路促进骨折愈合
2023-11-24白立曦谢万科徐之超杜俊凯
白立曦,许 静,段 鹏,谢万科,徐之超,杜俊凯
(西安交通大学第一附属医院急诊中心,西安 710061;*通讯作者,E-mail:68631784@qq.com)
骨折是临床中最常见的创伤之一,虽然手术治疗后大多数骨折患者都能正常愈合,然而,仍有5%~10%的患者会出现骨折不愈合或延迟愈合的现象[1]。如何有效加速骨折愈合是骨科重点研究领域,服用促进骨折愈合的药物具有重要作用。L-白雀木醇(L-quebrachitol,L-Q)是一种存在于多种植物中具有光学活性的肌醇甲氧基类似物。L-白雀木醇具有多种生物活性,包括抗氧化、抗炎、抗糖尿病、抗癌等活性[2]。其异构体D-松醇对破骨细胞生成具有抑制活性,但对成骨细胞生成没有任何影响[3]。最近有学者报道,L-白雀木醇促进小鼠胚胎成骨细胞前体细胞MC3T3-E1的增殖、分化和矿化[4]。然而,尚不清楚L-白雀木醇在体内是否可促进骨折愈合。骨折愈合过程中的骨再生类似于胚胎发生过程,参与这一过程的有骨膜骨化和软骨内骨化两个方面,后者的作用更为重要[5]。在软骨内骨化过程中,损伤组织周围的间充质细胞分化为软骨细胞,形成软骨桥,然后被编织骨再生替代并最终转变为板层骨[6]。多种生长因子和信号通路参与骨折愈合过程,其中,Wnt/β-catenin信号通路扮演重要角色,参与骨折愈合中软骨细胞的增殖和分化、软骨内骨化、骨痂改建等各个阶段的调节。Wnt/β-catenin信号通路的激活通过上调Runt相关转录因子-2(Runt-related transcription factor 2, Runx2)的表达促进成骨分化[7]。Wnt/β-catenin信号通路的抑制会延迟软骨内骨化和骨折愈合[8]。本研究通过观察L-白雀木醇对胫骨骨折大鼠模型的治疗作用及其对Wnt/β-catenin信号通路的影响,旨在探讨L-白雀木醇治疗骨折愈合的作用和机制,为骨折的临床治疗提供候选天然药物。
1 材料与方法
1.1 实验材料
L-白雀木醇(HY-N2375)购自美国MedChemExpress。二甲基亚砜(DMSO,SC05064)购自北京凯诗源生物科技有限公司。番红O-固绿染色试剂盒(G1371)购自北京索莱宝科技有限公司。TRIzol(R0016)、RIPA裂解缓冲液(P0013B)、BCA蛋白浓度测定试剂盒(P0010)、超敏ECL化学发光试剂盒(P0018S)购自碧云天生物技术研究所Transcriptor First Strand cDNA Synthesis Kit(4379012001)购自瑞士Roche。SYBR Green Master Mix(Q111)购自南京诺唯赞生物科技股份有限公司。Wnt-3a(ab81614)、Wnt-5a(ab235966)、β-catenin(ab223075)、GSK-3β(ab32391)和GAPDH(ab9485)、HRP标记的二抗(ab6721)购自英国Abcam。
1.2 实验仪器
ABX Pentra X-120血细胞分析仪购自法国HORIBA公司。7020全自动生化分析仪购自日本日立公司。μCT-40 Micro-CT系统购自瑞士Scanco Medical公司。7500实时荧光定量PCR仪购自美国ABI公司。
1.3 实验动物
SPF级Sprague-Dawley(SD)雄性大鼠(6~7周,250~280 g)和雌性大鼠(6~7周,180~120 g)购自西安交通大学实验动物中心,生产许可证:SCXK(陕)2020-001。大鼠饲养于25 ℃、55%相对湿度的环境中,光照调节设置为12 h光照/黑暗交替,大鼠自由饮水和进食。本研究已获得西安交通大学第一附属医院动物医学伦理审查委员会批准(批件号:2022动伦审科字第(216)号)。
1.4 L-白雀木醇安全性评价
大鼠预适应饲养1周后,将40只大鼠随机分为对照组和白雀木醇组(L-Q组),每组20只,雌雄各半。对照组大鼠腹腔注射2 ml的1%二甲基亚砜(DMSO),L-Q组大鼠腹腔注射2 ml剂量为30 mg/(kg·d)的L-白雀木醇,共给药4周。给药期间观察大鼠外观和行为有无异常,给药4周后测定大鼠体质量、摄食量。末次给药24 h后,腹腔注射3%的戊巴比妥钠麻醉大鼠,腹主动脉取血,使用X-120血细胞分析仪检测大鼠的血液学指标,包括白细胞计数(WBC)、红细胞计数(RBC)、血红蛋白(HGB)、血小板计数(PLT)和淋巴细胞计数(LYM)。使用7020全自动生化分析仪检测血清生化指标,包括丙氨酸氨基转移酶(ALT)、谷氨酸氨基转移酶(AST)、尿素氮(BUN)、肌酐(CRE)和血糖(GLU)。分离大鼠心脏、肝脏和肾脏,计算脏器系数(脏器质量/体质量×100%),并进行HE染色观察脏器形态。
1.5 骨折大鼠模型的建立和分组处理
参考文献[17]方法建立胫骨骨折模型。腹腔注射3%的戊巴比妥钠麻醉大鼠。右后肢剃毛,在胫骨中上1/3交界处进行15 mm的纵向皮肤切口,切开皮肤、皮下组织和筋膜,暴露胫骨,将克氏针自胫骨下端逆行向上打入胫骨上端,用手术钳在胫骨中上1/3处切断胫骨,然后缝合伤口。40只大鼠共有36只建模成功,4只死亡。将36只建模成功的大鼠随机分为3组:模型组、10 mg/(kg·d)L-白雀木醇组(10L-Q组)和30 mg/(kg·d)L-白雀木醇组(30L-Q组),每组12只。10L-Q组和30L-Q组大鼠分别腹腔注射2 ml的10 mg/(kg·d)和30 mg/(kg·d)的L-白雀木醇,模型组大鼠腹腔注射2 ml的1% DMSO,各组大鼠均给药3周。
1.6 X线检查和Mirco-CT分析大鼠胫骨骨折愈合情况
各组大鼠治疗3周后,首先进行X线片检查大鼠胫骨骨折愈合情况。然后解剖并取出胫骨髓内钉,使用μCT-40 Micro-CT系统扫描骨痂组织。
1.7 番红O-固绿染色评价骨折愈合情况
分离大鼠胫骨,4%多聚甲醛固定72 h,在4 ℃下用10% DETA脱钙4周,然后固定在70%乙醇中。再使用75%~100%乙醇脱水,二甲苯透明,石蜡包埋后切成4 μm厚的切片。根据试剂盒说明对切片进行番红O-固绿染色。
1.8 qRT-PCR检测骨痂组织中成骨相关基因和Wnt/β-catenin信号通路相关基因转录
使用TRIzol试剂提取大鼠骨痂组织的总RNA。使用Transcriptor First Strand cDNA Synthesis Kit将RNA(50 μg)反转录为cDNA。使用SYBR Green Master Mix在7500实时荧光定量PCR仪上进行qRT-PCR分析。PCR程序如下:95 ℃ 5 min,95 ℃ 20 s,60 ℃ 30 s,72 ℃ 20 s,40次循环。GAPDH作为内参基因,通过2-ΔΔCt方法计算mRNA相对表达量。基因特异引物见表1。

表1 引物序列
1.9 Western blot检测骨痂组织中Wnt/β-catenin信号通路相关蛋白表达
使用RIPA裂解缓冲液提取大鼠骨痂组织中的蛋白质并使用BCA法测定其含量,取25 μg蛋白质采用10% SDS-PAGE电泳分离,然后转移到硝酸纤维素膜上,并在4 ℃下与Wnt-3a(1∶2 000稀释)、Wnt-5a(1∶2 000稀释)、β-catenin(1∶2 000稀释)、GSK-3β(1∶2 000稀释)和GAPDH(1∶1 000稀释)一抗孵育过夜。然后将膜与1∶2 000稀释的HRP标记的二抗(1∶2 000稀释)室温孵育2 h,并用ECL试剂盒显影。用ImageJ对蛋白质条带密度进行定量分析。GAPDH作为内参。
1.10 统计学方法

2 结果
2.1 L-白雀木醇的安全性评价
对照组和L-Q组大鼠在给药4周期间均无明显外观和行为异常。在给药4周期间内,对照组和L-Q组大鼠的体质量和摄食量均无显著差异(P>0.05,见表2)。给药4周后,对照组和L-Q组大鼠的血液学指标(WBC、RBC、HGB、PLT和LYM)和血清生化指标(ALT、AST、BUN、CRE、GLU)水平均无显著差异(P>0.05),两组大鼠的心脏、肝脏和肾脏脏器系数均无显著差异(P>0.05,见表3~5)。L-Q组大鼠心脏、肝脏和肾脏细胞形态正常、排列规则,无明显炎性细胞浸润,未见明显脏器组织损伤(见图1)。
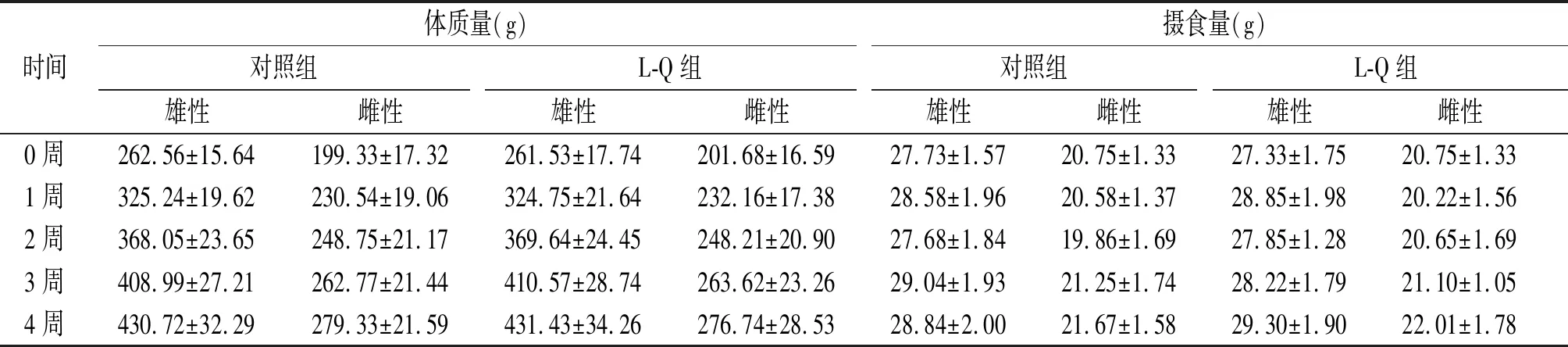
表2 对照组和L-Q组大鼠给药4周期间内的体质量和摄食量
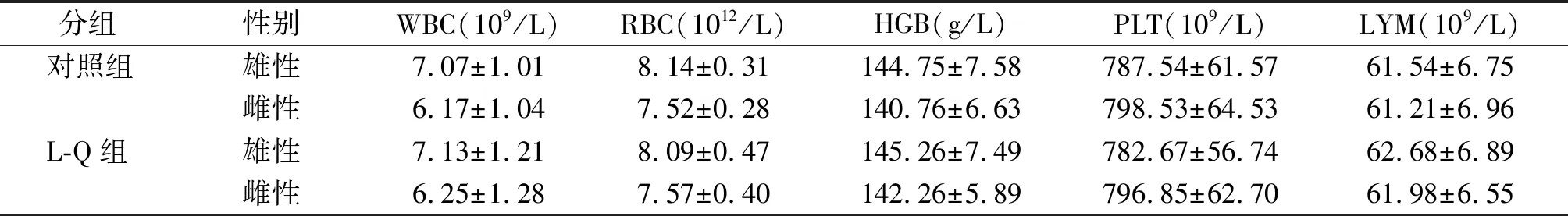
表3 对照组和L-Q组大鼠给药4周后的血液学指标水平

表4 对照组和L-Q组大鼠给药4周后的血清生化指标水平

表5 对照组和L-Q组大鼠给药4周后的心脏、肝脏和肾脏脏器系数
2.2 L-白雀木醇促进胫骨骨折大鼠骨折愈合
X线检查和Mirco-CT分析结果显示,给药3周后,模型组大鼠骨折线明显,骨痂开始形成,但密度较低;10L-Q组大鼠骨痂致密,骨折线模糊,骨痂跨越骨折端,出现骨性愈合;30L-Q组大鼠骨折线基本消失,骨折愈合情况最佳(见图2)。骨痂组织番红O-固绿染色显示,模型组大鼠骨折端存在较多纤维组织和软骨细胞,骨痂内可见新生骨小梁和成骨分化;10L-Q组大鼠软骨细胞减少,骨痂内新生骨小梁明显增多,成骨分化过程明显;30L-Q组大鼠可见软骨细胞逐渐被编织骨替代,骨痂跨越骨折端,骨性愈合良好(见图3)。
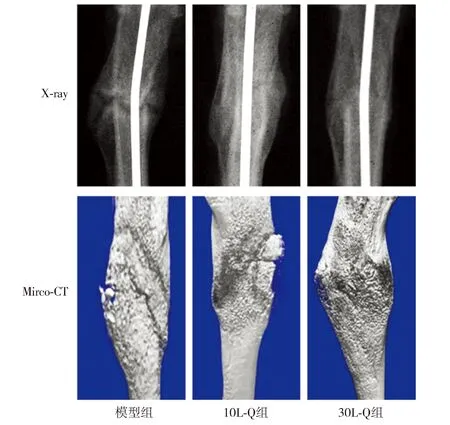
图2 各组大鼠建模3周后的X线检查和Mirco-CT分析
2.3 L-白雀木醇对胫骨骨折大鼠骨痂组织中成骨相关基因表达的影响
与模型组相比,10L-Q组和30L-Q组大鼠骨痂组织中OCN、OPN、Runx2、ALP和BMP-2的mRNA水平均升高(P<0.05,见图4)。
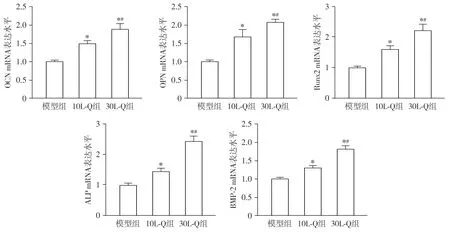
与模型组比较,*P<0.05;与10L-Q组比较,#P<0.05
2.4 L-白雀木醇对胫骨骨折大鼠骨痂组织Wnt/β-catenin信号通路的影响
与模型组相比,10L-Q组和30L-Q组大鼠骨痂组织中Wnt-3a、Wnt-5a和β-catenin的mRNA水平均升高(P<0.05),GSK-3β的mRNA水平降低(P<0.05,见图5)。
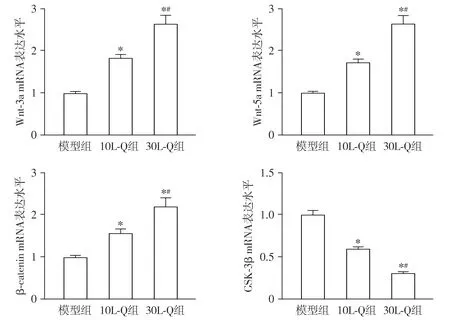
与模型组比较,*P<0.05;与10L-Q组比较,#P<0.05
与模型组相比,10L-Q组和30L-Q组大鼠骨痂组织中Wnt-3a、Wnt-5a和β-catenin蛋白水平均升高(P<0.05),GSK-3β蛋白水平降低(P<0.05,见图6)。
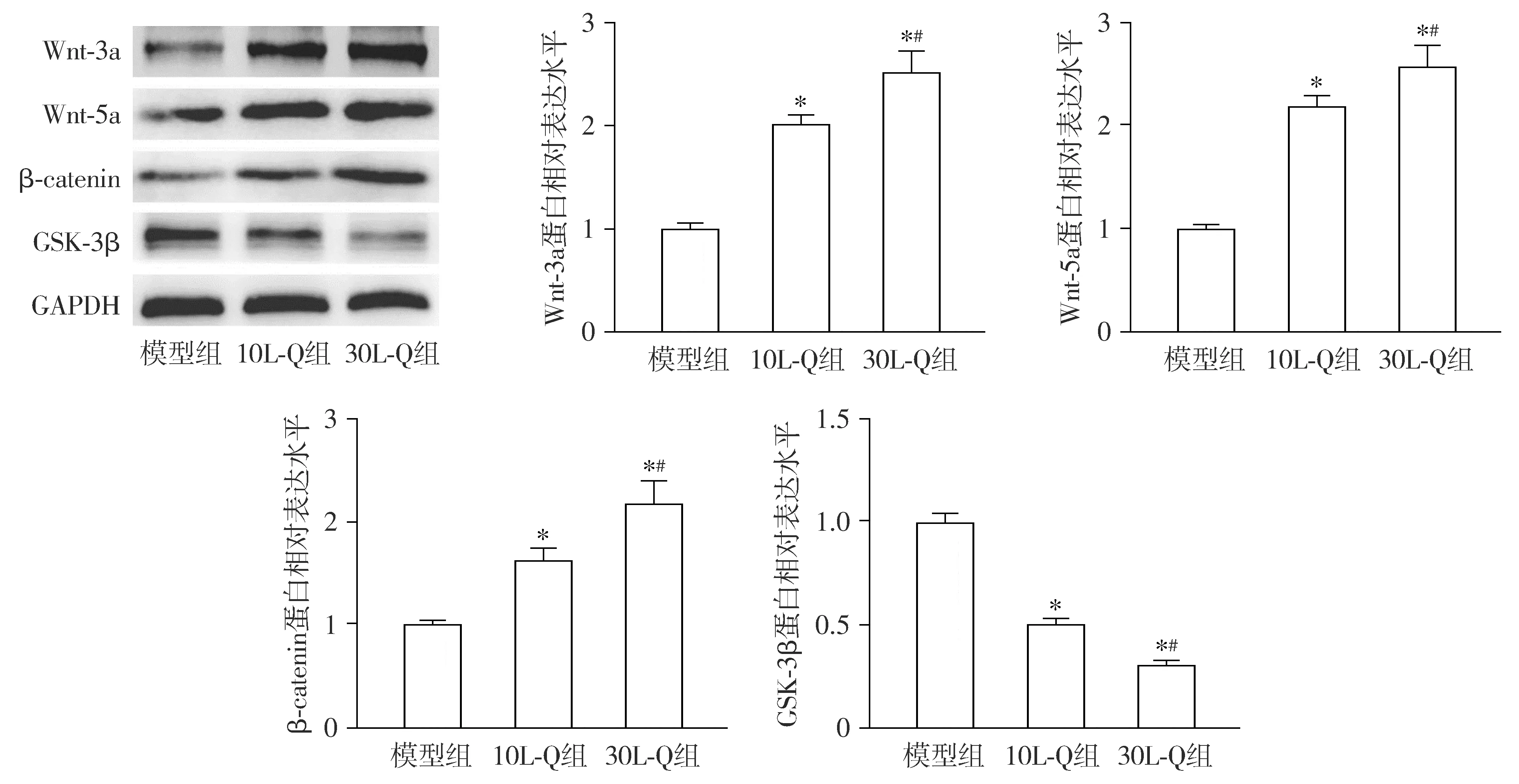
与模型组比较,*P<0.05;与10L-Q组比较,#P<0.05
3 讨论
目前,尚无治疗骨折不愈合或延迟愈合的特效药,因此,急需要开发相关药物[1]。许多植物类化合物能促进成骨细胞诱导的骨形成,包括糖苷、黄酮类、萜类、香豆素、酚类、酚酸等。L-白雀木醇是从如沙棘等多种植物中分离得到的肌醇甲醚衍生物[9-11]。文献报道,L-白雀木醇具有抗氧化、抗炎、抗糖尿病等多种生物活性[2],并且其异构体D-松醇可抑制核因子-κB受体活化因子配体(receptor activator of nuclear factor κB ligand,RANKL)诱导的破骨细胞分化,防止体内卵巢切除术引起的骨质流失[3]。另外,L-白雀木醇可促进小鼠胚胎成骨细胞前体细胞的增殖、分化和矿化[4]。基于上述文献报道,本研究推测L-白雀木醇可能有助于骨折愈合,因此开展了本项研究。
曾奇兵等[12]报道,L-白雀木醇的异构体D-松醇对大鼠的最大无毒性作用剂量为雄性30.88 mg/(kg·d)和雌雄33.58 mg/(kg·d)。王梦等[13]应用30 mg/(kg·d)的D-松醇治疗2型糖尿病大鼠,发现其可提高大鼠对葡萄糖的耐受能力,缓解胰岛素抵抗。基于上述文献,本研究首先考察了30 mg/(kg·d)的L-白雀木醇连续灌胃4周的安全性,结果表明30 mg/(kg·d)的L-白雀木醇给药未影响大鼠的外观和行为、体质量和摄食量、血液学指标、血清生化指标,且未对大鼠心脏、肝脏和肾脏造成损伤,上述结果说明L-白雀木醇具有良好的安全性。
本研究分别使用10 mg/(kg·d)和30 mg/(kg·d)的L-白雀木醇治疗骨折大鼠3周,X线检查、Mirco-CT分析和骨痂组织番红O-固绿染色结果显示,L-白雀木醇以剂量依赖性方式促进胫骨骨折大鼠骨折愈合,主要表现为L-白雀木醇促进了软骨内骨化过程,加速了软骨向编织骨的转化,缩短了骨痂跨越骨折端的时间。包括OCN、OPN、Runx2、ALP和BMP-2在内的多种基因调节成骨细胞的增殖和分化,从而参与骨形成的调控[14]。据报道,BMP-2通过调节Runx2诱导成骨细胞分化,Runx2的激活通过增加ALP活性和OCN、OPN等骨基质蛋白的合成进一步调节成骨细胞分化[15,16]。Yodthong等[4]报道,L-白雀木醇可促进MC3T3-E1细胞的增殖、分化和矿化,同时增加ALP、I型胶原、OCN、OPN、BMP-2和Runx2的表达,下调RANKL的表达。本研究显示,L-白雀木醇剂量依赖性地上调了胫骨骨折大鼠骨痂组织中OCN、OPN、Runx2、ALP和BMP-2的mRNA水平,这些结果充分说明L-白雀木醇具有促进成骨分化和骨形成的作用。
Wnt/β-catenin信号通路通过调节成骨细胞的增殖、分化和矿化在骨形成中发挥关键作用。当细胞外的Wnt配体与卷曲受体及其辅助受体LRP5和LRP6结合时,Wnt/β-catenin信号通路被激活,促进了转位到细胞核中β-catenin的释放,从而激活靶基因的表达[17,18]。Wnt/β-catenin信号通路通过激活BMP信号通路协同控制成骨细胞的分化和骨形成[19]。已有报道称,Wnt/-catenin信号通路可以诱导成骨细胞分化基因如ALP和OPN的表达[20],Wnt/β-catenin信号通路失活会抑制成骨细胞分化[21]。Yodthong等[4]研究也显示,L-白雀木醇可促进MC3T3-E1细胞Wnt/β-catenin信号通路相关基因的表达。本研究显示,L-白雀木醇剂量依赖性地上调了胫骨骨折大鼠骨痂组织中Wnt-3a、Wnt-5a和β-catenin的蛋白表达水平,降低了GSK-3β的蛋白表达水平,从而激活了Wnt/β-catenin信号通路。因此,Wnt/β-catenin信号通路的激活可能介导L-白雀木醇对骨折愈合的促进作用。
综上所述,本研究首次表明L-白雀木醇可促进胫骨骨折大鼠骨折愈合,其机制可能与Wnt/β-catenin信号通路的激活有关。L-白雀木醇可能是治疗骨折愈合的潜在天然药物,具有较高的研究价值。
