靶向IL-6药物不良反应的信号挖掘:基于FAERS数据库的真实世界研究
2023-11-18卞叶萍徐剑吴玲邓晓静
卞叶萍,徐剑,吴玲,邓晓静
(南京医科大学附属老年医院 重症医学科,江苏 南京 210024)
白细胞介素-6(Interleukin-6, IL-6)[1]是一种由机体内多种细胞产生的功能广泛的细胞因子,通过与细胞表面I型细胞因子受体复合物及可溶形式的IL-6受体结合发出信号,发挥广泛的作用。IL-6的表达失调刺激多种自身免疫性和慢性炎性疾病的发生和发展。近年来,IL-6细胞因子家族的成员开始成为治疗感染、炎症、自身免疫和癌症的药物靶标。药物类别包括针对特定细胞因子或细胞因子受体的单克隆抗体和重组蛋白形式。靶向IL-6已成为免疫介导的炎症性疾病的主要治疗策略,可通过抗IL-6Rα抗体或直接抑制IL-6细胞因子来干扰IL-6通路的特异性受体[2]。截止到2022年底,已经在美国食品药品监督管理局(Food and Drug Administration,FDA)上市的有4种靶向IL-6药物:托珠单抗[3-4](Tocilizumab)、司妥昔单抗(Siltuximab)[5]、萨瑞鲁单抗(Sarilumab)[6]、萨特利珠单抗(Satralizumab)[7]。临床应用从以关节病变为主的自身免疫性疾病逐渐延伸到其他疾病,特别是随着新型冠状病毒感染的暴发,研究发现病毒感染导致机体过度炎症反应从而大大增加病死率[8],而靶向IL-6药物可以通过调控炎症反应从而改善预后[9]。但是因药物较新,上市及应用经验有限,国内对其不良反应的报道较少,在临床使用过程中仍需密切监测其安全性。美国FDA不良事件报告系统(FDA adverse event reporting system,FAERS)数据库是一个免费公开的自发报告系统,用于评估药物上市后的安全性,其中全球上报的药物不良事件(adverse drug event,ADE)的病例报告是来自于真实世界的数据,是临床用药参考的重要指引。因此本研究拟基于FAERS数据库的靶向IL-6药物的ADE进行信号挖掘及数据分析,为以后国内此类药物的临床安全使用提供参考。
1 资料与方法
1.1 资料来源与筛选
为兼顾4种靶向IL-6药物的上市使用时间,限定研究时间区间为2010年第1季度到2022年第4季度。从FAERS数据库下载此时间段的ASCⅡ数据包,将数据导入到SAS9.4软件中。将目标药物选定为“ACTEMRA”“ATLIZUMAB”“TOCILIZUMAB”“ROACTEMRA”“SILTUXIMAB”“SYLVANT”“SARILUMAB”“KEVZARA”“SAR153191”“SATRALIZUMAB”“ENSPRYNG”,并进行数据清理,删除重复数据和存疑数据后得到本研究的原始研究数据。
1.2 方法
1.2.1 数据整理及标准化 本研究选用国际医学用语词典(Medical Dictionary for Regular Activities,MedDRA 25.1)的系统器官分类(system organ class, SOC)及首选术语(preferred term, PT)对ADE进行标准化阐述和分类,以标准化的SOC和PT为研究对象。
1.2.2 信号强度计算及分析 目前国内外最广泛使用的ADE的数据挖掘方法主要是比例失衡法,常用的主要有报告比值比(reporting odds ratio,ROR)法、贝叶斯可信区间递进神经网络(Bayesian confidence propagation neural network,BCPNN)法、比例报告比值法、综合标准法等。其中ROR法源于荷兰药物警戒中心Lareb实验室,具有偏倚较少、灵敏度较高等特点,因此应用广泛[10]。BCPNN法将贝叶斯逻辑学和神经网络结构结合起来,提供了可描述各属性子集间因果关系的模型,具有比较理想的特异度和灵敏度,是目前国内外应用比较成熟的信号检测方法[11]。通过公式计算出ROR值和BCPNN值,该数值越大,信号强度就越强,表明目标药物与目标ADE之间的统计学关联越强。为保证研究的准确性,本研究同时使用ROR和BCPNN两种方法进行信号分析,两者结合可以减少偏倚,以上两种计算方法均生成1个信号最终确认为产生1个风险信号。
2 结 果
2.1 靶向IL-6药物不良事件上报基本情况
FAERS数据库中2010年第1季度至2022年第4季度以4种靶向IL-6药物为首要怀疑药物的ADE共55 068例。4种靶向IL-6药物ADE的性别、年龄、报告者、报告国家及报告年份等基本信息见表1。结果提示FAERS数据库中存在报告信息填写不完善的表现,表现为较多未知数据;FAERS数据库中报告靶向IL-6药物使用以托珠单抗使用为主,报告涉及的患者中女性居多,年龄集中于45~65岁,上报事件来源以美国及欧洲国家为主,报告年份在药物上市后呈逐年递增的趋势。
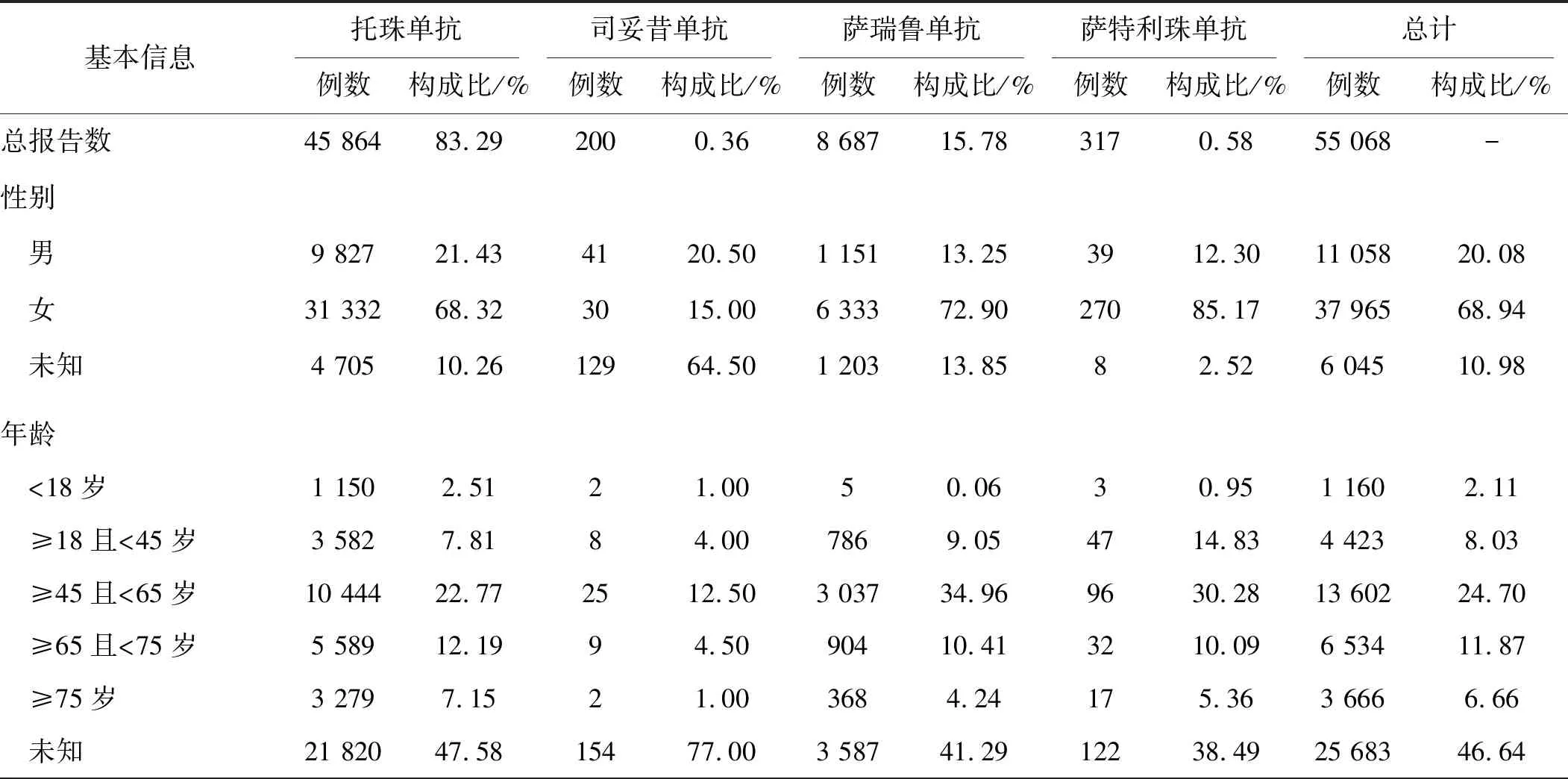
表1 靶向IL-6药物ADE报告的基本信息
2.2 靶向IL-6药物ADE累及的SOC分析
本研究挖掘得到总的靶向IL-6药物ADE信号846个。对4种靶向IL-6药物挖掘得到ADE信号数分别为:托珠单抗850个,司妥昔单抗15个,萨瑞鲁单抗190个,萨特利珠单抗30个。使用MedDRA 25.1对ADE信号进行SOC分类,结果显示,4种靶向IL-6药物中有3种IL-6受体拮抗剂(托珠单抗、萨瑞鲁单抗、萨特利珠单抗),ADE信号共累及27个SOC,其中含有信号个数最多的3个SOC分别为感染及侵染类疾病、各类检查及各种肌肉骨骼及结缔组织疾病;而唯一一个IL-6拮抗剂(司妥昔单抗)似乎显示出较少的ADE信号,累及的SOC也较少,结果详见表2及图1。
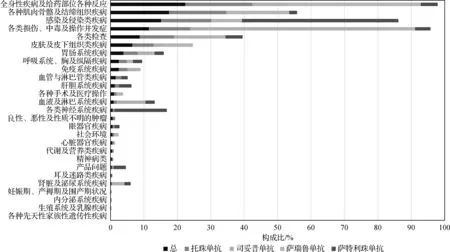
图1 靶向IL-6药物累及的SOC的ADE构成比
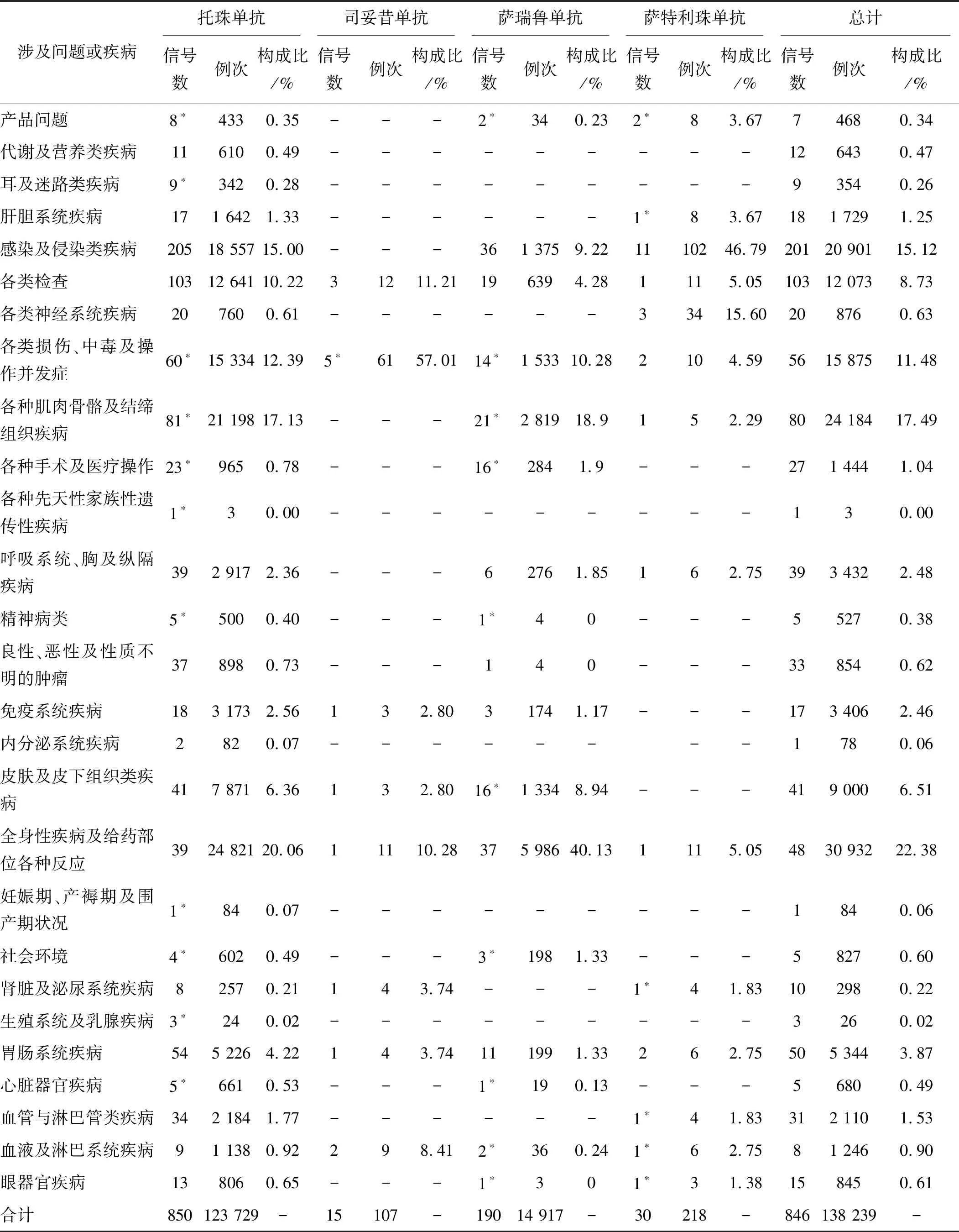
表2 靶向IL-6药物累及的SOC信号数及ADE构成比
将筛选出的ADE信号与说明书对照,除去可能与目标药物本身关系不大的社会问题、各类损伤、中毒及操作并发症、各种手术及医疗操作及各种先天性家族性遗传性疾病等,结果发现有一些SCO的信号是说明书中尚未提及的,如:(1) 产品问题表现出有较多信号数;(2) 托珠单抗显示较强信号数的耳及迷路类疾病,也显示出较多心脏器官疾病信号;(3) 托珠单抗和萨瑞鲁单抗显示出较多的各种肌肉骨骼及结缔组织疾病信号;(4) 托珠单抗和萨瑞鲁单抗出现精神病类信号;(5) 萨特利珠单抗及萨瑞鲁单抗显示出眼器官疾病信号。
2.3 靶向IL-6药物ADE信号分析
对上述挖掘出的风险ADE的进行排序筛选出报告例数前20位以及信号强度前20位的ADE进行进一步分析(因篇幅限制,此部分结果未以图表形式展示)。结果发现所有靶向IL-6药物的ADE信号分析提示报告例数以及信号强度排名靠前的与说明书基本一致,以感染及侵染类疾病为主,另外各种肌肉骨骼及结缔组织疾病有较高的报告例数以及信号强度。针对托珠单抗的挖掘发现,发现说明书中尚未提及可能需要引起关注的ADE有脱发以及治疗效果下降。司妥昔单抗的各种检查的PT显示出较多例数及较强信号强度,说明书尚未提及如C反应蛋白升高、腹水等,另外细胞因子释放综合征、盗汗等在说明书中也尚未提及。萨瑞鲁单抗ADE与说明书一致,以感染及侵染类疾病为主,局部注射部位并发症比较明显,各种肌肉及骨骼系统疾病ADE增加,但其中值得注意是眼溃疡及视网膜炎信号强度较高,另外适应障碍伴抑郁情绪虽然报告例数不多也有较高信号强度,这些在说明书中尚未强调。对于萨特利珠单抗的挖掘发现肾脏及泌尿系统疾病如肾盂肾炎、尿路感染、肾脏感染、膀胱炎及肾功能损害等,即使除去感染性因素,也显示出可能对肾功能有潜在影响,且视神经炎及视力减退等眼器官疾病尚未在说明书中提及,此外深静脉血栓的报告也需要引起关注。
3 讨 论
随着医学研究的不断深入,生物制剂类药物不断上市走入临床,给许多复杂的难治性疾病带来了新的希望。但是作为一种特殊类型的药物,由于其临床使用时间较短,且临床研究尚未完全深入,导致不良事件可能未完全显现,尤其是靶向IL-6药物这种针对体内炎症信号通路、可能影响广泛的药物,潜在的不良反应可能较多[12]。因此本研究针对FDA已经上市的4种靶向IL-6药物进行深度挖掘分析,为进一步的临床应用提供参考。
本研究收集了FAERS数据库中4种靶向IL-6药物的ADE进行真实世界研究,发现女性患者ADE的报告数量多于男性患者,并且年龄主要集中于45~65岁,提示中老年女性患者使用靶向IL-6药物可能需要留意ADE的发生。ADE上报数量逐年上升,且近3年明显增加,在分析原因的时候考虑可能是由于新冠疫情在全球的暴发,过度的全身炎症反应导致病死率增加,而靶向IL-6药物在临床使用过程中显示出较好的治疗作用,因此近3年随着适应证的扩增药物使用量也逐年上升,从而ADE的上报也增加[13]。另外,从基本信息来看,FAERS数据库中较多ADE存在信息填写不完整以及错误的情况,导致出现未知数据的量较大,影响分析结果。这点也为国内药物不良事件上报工作提供了一些经验,如何更好地优化上报系统,给用户提供较为简洁明了、不易混淆的框架数据填写系统是不容忽视的问题。
进一步分析靶向IL-6药物ADE累及的SOC可以为临床合理用药提供参考,说明书中提及的ADE累及的系统疾病在本研究中均有检出信号,提示本研究数据的可靠性。4种靶向IL-6药物中有3种IL-6受体拮抗剂(托珠单抗、萨瑞鲁单抗、萨特利珠单抗),它们涉及的ADE信号共累及27个SOC,其中含有信号个数最多SOC为“感染及侵染类疾病”,这与说明书基本也一致;而4种靶向IL-6药物中唯一一个IL-6拮抗剂(司妥昔单抗)似乎显示出较少的ADE信号,累及的SOC也较少。在挖掘出的所有SOC信号中,除去明显的混杂因素不做进一步讨论,我们将筛选出的ADE信号与FDA提供的4种药物的最新版说明书对照,发现有一些SOC的信号是说明书中尚未提及的,在以后的临床使用过程中可能需要重视和关注。具体有:(1) 产品问题,从各药物分析结果看似乎为共性问题,涉及的ADE有针头问题、针管问题、产品温度偏移、设备故障及给药装置问题等,反映了临床使用操作过程存在的一些问题,应当引起重视。(2) 托珠单抗显示较强信号数的耳及迷路类疾病,具体PT包括耳痛、耳瘙痒、耳聋、鼓膜穿孔、产生过多耵聍等,这部分在说明书中尚未提及,需要警惕;另外也显示出较多心脏器官疾病信号,具体PT如心包炎、心脏毒性、无症状性心肌梗死、冠状动脉瘤等,在说明书注意事项中虽然有心血管风险的警示,但未提及具体的心血管风险的ADE有哪些,本研究结果可能可以作为临床用药参考的补充信息;针对托珠单抗的ADE排名及信号强度靠前的PT与说明书对照,发现说明书中尚未提及可能需要引起关注的ADE有脱发以及治疗效果下降;另外托珠单抗的说明书中强调还没有数据表明托珠单抗会产生药物依赖,但是本研究的信号挖掘显示有ADE为治疗效果下降,这间接说明可能会有药物依赖的倾向。(3) 托珠单抗和萨瑞鲁单抗显示出较多的各种肌肉骨骼及结缔组织疾病信号,且涉及的ADE的PT较多,但这些ADE似乎可能与目标药物的适应证的临床症状有较多交叉,难以鉴别是目标药物导致的ADE还是疾病本身临床表现。(4) 托珠单抗和萨瑞鲁单抗出现精神病类信号,具体ADE有预想性焦虑、睡眠障碍、适应障碍伴抑郁情绪等,虽然排名不靠前但对患者的心理影响大,如进一步发展甚至可能导致自杀等严重的不良事件,需要引起警惕。(5) 萨特利珠单抗及萨瑞鲁单抗检出眼器官疾病信号,具体ADE为视力减退及眼溃疡等,虽然信号数及报告例数很少,但这部分在这两种药物的说明书中未提及,仍需引起警惕。(6) 司妥昔单抗因上报的ADE较少,可能与其适应证窄应用数量少有关,风险ADE信号大部分与说明书一致,其中各种检查信号强度及报告例数较多,而说明书中这部分主要重点描述了肝脏功能检查指标异常以及白细胞减少、血小板减少,未提及C反应蛋白升高、腹水等,另外细胞因子释放综合征、盗汗等在说明书中尚未提及[14]。(7) 对萨特利珠单抗的挖掘发现肾脏及泌尿系统疾病,如肾盂肾炎、尿路感染、肾脏感染、膀胱炎及肾功能损害等,即使除去感染性因素,也显示出可能对肾功能有潜在影响,此外深静脉血栓的报告也需要引起关注。
本研究存在一定的局限性:(1) FAERS数据库的上报数据存在填报信息不完善如少报、漏报以及报告不完整的情况,所以可能导致挖掘出的信号存在低估可能性,出现信息偏倚;(2) 从报告的基本信息可以看出,报告来源以美国为首,欧美国家占大多数,种族偏倚可能较大;(3) 本研究采用的ROR法和BCPNN法只能从统计学上反映出目标药物与ADE的关联程度,并不能说明使用目标药物与ADE的因果关系,也不能说明ADE发生率的高低;(4) 本研究尚未对于风险ADE出现的原因和机制进一步深入探讨,后续需要更多证据级别更高的研究对本研究相关结论加以证实。
本研究通过对FARES数据库的挖掘分析,研究了真实世界中临床使用靶向IL-6药物过程中发生的各系统ADE信号。结果提示,除说明书提示的常见不良反应外,在临床应用时应对靶向IL-6药物引起的发生率高且信号强的ADE给予重点关注。在使用靶向IL-6药物应做好用药评估,使用中应密切监测上述指标以及原发疾病进展,如发生ADE或疾病进展,应及时进行干预,保障患者的用药安全。
