阳离子对乳化沥青稳定性影响的分子模拟
2023-11-17陈宏宇王叶飞
袁 燕,陈宏宇,王叶飞,徐 松,薛 斌
(福州大学 土木工程学院,福建 福州 350108)
乳化沥青是沥青在熔融状态下通过机械剪切作用,将沥青分散成细小的微粒状态,再与乳化剂稳定结合在水中,从而形成的一种特殊状态的沥青[1].根据乳化剂分子的不同,可将其分为阴离子型乳化沥青、阳离子型乳化沥青以及非离子型乳化沥青.其中,阴离子型乳化沥青由于来源广和成本低而广受欢迎,但在其使用及存放过程中的稳定性受到多种因素影响.
近年来,由于计算机水平的高速发展,分子动力学模拟(MD)已经成为研究沥青机理的重要方法.Li等[2]提出了沥青的十二组分模型,以此提高了沥青分子模型的适用性.范维玉等[3]根据乳化沥青水包油的特性,通过分子模拟软件构造出“沥青-乳化剂-水-乳化剂-沥青”的双层界面模型.
乳化剂用水是影响乳化沥青稳定性的重要因素之一,一般要求是中性水,但实际工程上,乳化剂用水可能会遇到含有Ca2+/Mg2+的偏硬水.徐静等[4]提出使用硬水(水溶液中含有Ca2+/Mg2+)会导致沥青微粒聚集,降低阴离子乳化沥青的贮存稳定性.对此现象,尚无文献从纳观层面进行分析和解释.
本文通过分子动力学,建立了不含盐及含盐乳化沥青体系模型,并在水中加入金属阳离子(Ca2+/Mg2+)代替硬水,对十二烷基硫酸钠(SDS)阴离子乳化沥青的稳定性进行研究,探讨了金属阳离子对阴离子乳化沥青储存稳定性的影响机理.
1 模型的建立、验证与计算
1.1 沥青分子模型构建
沥青是一种化学成分和组分都十分复杂的聚合物材料,想要准确了解其化学性质是非常困难的.随着国内外学者的不断研究[5],提出了每种组分多种分子以提高沥青模型的适用性.本文采用十二组分模型[2],以此来构建基质沥青模型.
通过Materials studio(MS)软件将沥青的十二组分按相应的比例随机组合至3.74 nm×3.74 nm×3.74 nm 尺寸的晶胞内,并通过Forcite 模块中Geometry Optimization 进行结构优化,保证能量收敛次数充分.在Compass Ⅱ力场下,先后通过NPT 系综和NVT 系综能量弛豫,使沥青模型达到平衡状态(见图1).

图1 基质沥青平衡模型Fig.1 Base asphalt balance model
1.2 沥青模型的验证
对平衡后的沥青模型进行分析验证,包括密度、玻璃化转变温度Tg和内聚能密度,并与试验数据进行对比验证.沥青分子模型的基本性质见表1.由表1可见,沥青模型经过分子动力学的充分弛豫后,模型的属性与参数与其他学者的试验结果[6-8]相一致,这说明沥青的模型构建、电荷分配以及力场参数合理.

表1 沥青分子模型的基本性质Table 1 basic properties of asphalt molecular model
1.3 乳化剂沥青模型
目前,主流乳化沥青分子模型有2 种,分别为乳化沥青分子模型[3]与乳化沥青残留物模型[9].本文用乳化沥青分子模型进行研究分析.
通常,在无盐体系中,无需加入任何离子,即可保证体系的电中性.而在无盐体系中加入Ca2+/Mg2+则可以形成含Ca2+/Mg2+的乳化沥青分子体系,方法是在水盒子中随机加入16 个Ca2+/Mg2+和32 个Cl-,既满足高盐度环境的需要,又满足体系电中性需求.
以含Ca2+的乳化沥青分子模型为代表,建立了由2 个沥青相(见图1)、2 个SDS 乳化剂分子单层以及11 个含Ca2+的水层组成的乳化沥青分子模型(见图2),在该模型的3 个空间方向上都设置具有周期性的边界条件.先对模型进行几何优化,以避免分子重叠的可能性;随后再进行NVT 系综以及NPT 系综的充分弛豫;最后再以1 fs 步长进行时长为1 ns 的NVT 系综弛豫,以此来记录轨迹信息,并用于数据分析.
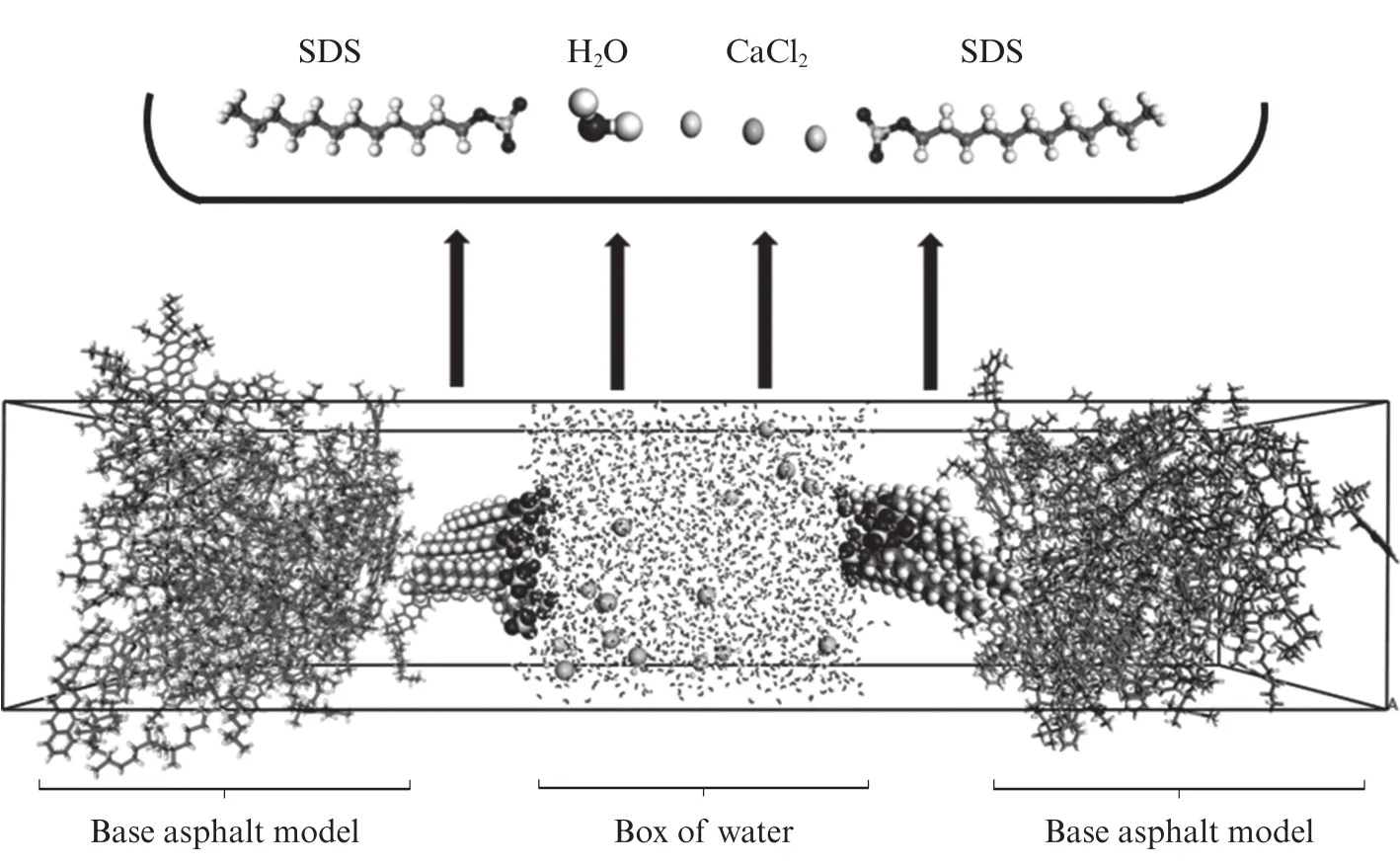
图2 含Ca2+的乳化沥青分子模型Fig.2 Molecular model of emulsified asphalt with Ca2+
2 结果与讨论
2.1 界面整体形貌分布
SDS 乳化沥青模型在不同水环境下的平衡结构见图3.由图3 可见,乳化剂的头基分子与水分子相结合,而尾部的烷烃链与沥青相相结合,这种构型与乳化沥青试验研究和其他MD 模拟中报道的构型相似[10];无盐的乳化沥青体系中Na+游离于SDS 乳化剂的磺酸头基附近,与阴离子乳化剂形成稳定的双电层保护膜结构;含有金属阳离子盐的体系中Ca2+和Mg2+会取代部分Na+与乳化剂的头基分子进行结合吸附.

图3 SDS 乳化沥青模型在不同水环境下的平衡结构图Fig.3 Equilibrium structure of SDS emulsified asphalt in different water environments
2.2 乳化剂分子膜厚度
通过乳化沥青的相对浓度分布,可以确定乳化剂膜的厚度.若乳化剂分子膜越厚,说明乳化沥青的稳定性就越强[10].SDS 乳化沥青在不同水环境下的相对浓度分布见图4.由图4 可见,无盐的SDS 乳化沥青体系与添加Ca2+/Mg2+的SDS 乳化沥青体系的界面厚度分别为2.087、1.943、1.799 nm,即在不同水环境下SDS 乳化沥青界面膜厚度从大到小依次为无盐体系、含Ca2+体系和含Mg2+体系.因此,相较于添加Ca2+与Mg2+体系,无盐体系下的乳化沥青的界面膜更加稳定.
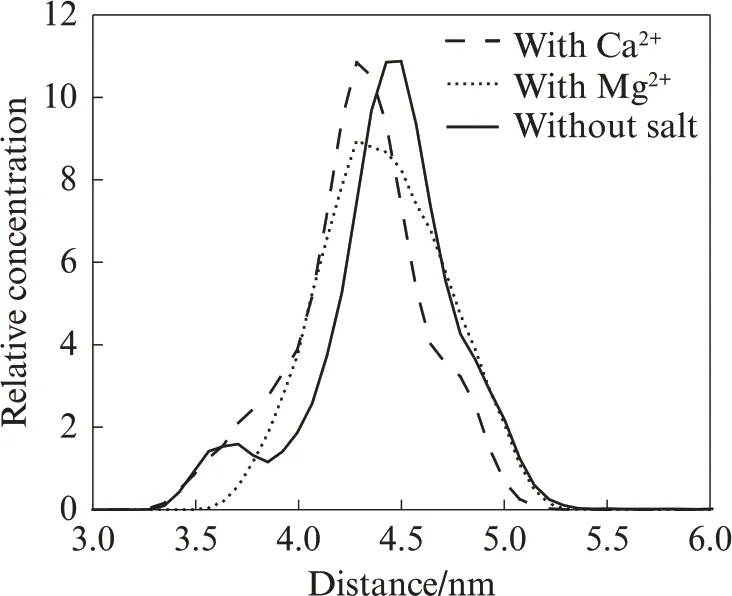
图4 SDS 乳化沥青在不同水环境下的相对浓度分布Fig.4 Relative concentration distribution of SDS emulsified asphalt in different water environments
2.3 乳化剂分子倾角
为了更清楚地了解乳化剂分子在油-水界面之间的倾角问题,对亲水头基上S 原子和亲油烷烃链上最后1 个C 原子之间的倾角进行分析.将磺酸头基上S 原子与烷烃尾部C 原子之间的倾角记为θ.SDS 分子中S 原子与C 原子之间的倾角示意图见图5.由图5可得θ的计算式为:

图5 SDS 分子中S 原子与C 原子之间的倾角示意图Fig.5 Sketch diagram of inclination angle between S atom and C atom of SDS molecule
式中:lz为乳化剂分子投影到Z轴上的长度;l为磺酸头基中S 原子到烷烃尾链上C 原子之间的距离.
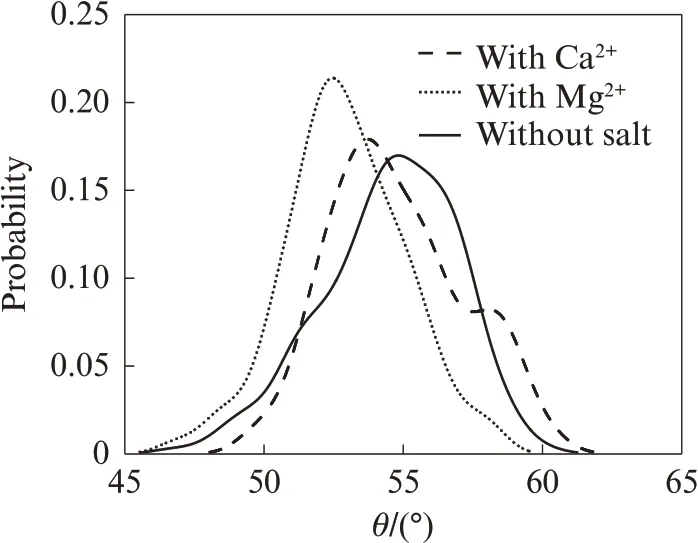
图6 SDS 乳化剂分子相对于Z 轴方向倾角的概率分布图Fig.6 Probability distribution of inclination angle of SDS emulsifier molecule relative to Z-axis
2.4 界面相互作用能
不同物质之间相互作用的强弱可以通过界面之间的相互作用能来衡量,而相互作用能通过结合能来体现.结合能由整个体系的总能量减去单个组分的能量所得.若结合能为负值,说明沥青相、水相、乳化剂分子三者之间的相互作用力主要是引力;反之,三者之间的相互作用力主要为斥力.结合能越大,引力(斥力)就越强烈.
沥青与水之间的结合能是由乳化剂分子与水之间的相互作用E1、沥青与水之间的相互作用能E2以及乳化剂分子与沥青的相互作用能E3共同决定.在“沥青-乳化剂-水-乳化剂-沥青”体系中,E1、E2、E3的计算式为:
式中:Etotal为体系的总能量;Easphaltene、EH2O、Eemulsifier分别为沥青分子、水分子和表面活性剂分子的能量;EH2O+emulsifier为水与乳化剂分子的能量;EH2O+asphaltene为水与沥青分子的能量;Easphaltene+emulsifier为沥青与乳化剂分子的能量.
由式(2)~(4)可得到“沥青-乳化剂-水-乳化剂-沥青”体系中水界面与沥青界面的相互作用能ΔE为:
不同盐离子的“沥青-乳化剂-水-乳化剂-沥青”体系的相互作用能包括Etotal、范德华能Evdw、静电能Eelc和非键相互作用能Enon,结果见表2.由表2可知,无盐体系、含Ca2+体系及含Mg2+体系沥青与水分子的相互作用能分别为-730.07、-535.51、-324.26 kJ/mol,可见Ca2+和Mg2+的加入会降低阴离子乳化沥青中沥青与水之间的结合能;3 种体系的Etotal与Enon均相等,说明在沥青乳化过程中,并没有产生相应的化学键,而是依靠分子间的作用力;相较于无盐体系,含Ca2+和Mg2+体系的乳化沥青静电作用力从-102.63 kJ/mol 分别上升至300.12、349.53 kJ/mol,说明随着金属阳离子的加入,沥青与水之间的静电相互作用由相互吸引变至相互排斥.这主要是因为金属阳离子的加入,破坏了阴离子乳化沥青的双电层结构,增大了沥青微粒与水分子之间的斥力,加强了沥青微粒之间结合的可能性,从而降低了乳化沥青的稳定性.
2.5 金属阳离子对乳化剂分子的影响
表面活性剂头基附近水分子以及金属阳离子附近水分子的分布情况可以根据径向分布函数g(r)来分析,以此来解释在金属阳离子影响下表面活性剂分子与水分子之间相互作用结合的强弱问题.g(r)表征的是在一定距离r下1 个原子找到另1 个原子的概率问题,其计算式为:
式中:ρ为体系密度;N为体系中原子的数目.
表面活性剂头基(以氧原子表示)、金属阳离子与水分子(以氧原子表示)的径向分布函数见图7.由图7(a)可见:含Ca2+和Mg2+的乳化沥青体系的最强峰均位于r=0.245 nm,这表明表面活性剂头基部位与水分子之间最有可能性的距离为0.245 nm;含Mg2+体系的径向分布函数曲线的第1 峰要高于含Ca2+体系,表明相较于含Ca2+乳化沥青体系,含Mg2+体系下的表面活性剂分子与水分子结合的能力更强.由图7(b)可见:相较于含Ca2+体系,Mg2+与水分子之间的距离更近,并且与水的结合数量更多,这与已报道的Ca2+/Mg2+的水化结果一致[11].这主要是因为Mg2+的离子半径(0.065 nm)比Ca2+的离子半径(0.099 nm)更小[11].离子半径越小,电场能力越强,极化能力越大,与水分子的吸引力越大.
综上,相较于Ca2+,Mg2+的极化能力更强,不仅与水分子的吸引力更大,而且与头基中氧原子的结合能力也更强.Mg2+与乳化剂头基分子相结合,会带动周围所吸引的水分子,因此在含Mg2+水溶液中,乳化剂头基周围的水分子数量要大于含Ca2+水溶液中的.此外,较强极化能力的阳离子会吸引头基分子,使头基聚集在一起,而并非均匀分布在沥青界面上,从而降低了乳化沥青界面膜的稳定性.
3 结论
(1)从平衡状态下的界面形貌来看,乳化剂分子的头基会和水分子结合,烷烃链会和沥青相结合,无盐乳化沥青体系界面膜最厚,其次是含Ca2+/Mg2+乳化沥青体系;相较于无盐乳化沥青体系,含Ca2+/Mg2+的乳化剂分子倾角相对较小,表明金属阳离子的加入会降低乳化剂分子与沥青分子之间的吸附能力.
(2)从沥青相、水相、乳化剂分子三者的相互作用能来看,无盐乳化沥青体系,其水油之间相互作用能总是大于含盐乳化沥青体系水油之间相互作用能.
(3)从乳化剂分子对水分子的亲水能力来看,Mg2+的极化能力更强,与水分子结合能力更大.强极化能力的阳离子更易与乳化剂头基分子相结合,使头基分子聚合,降低界面稳定性.
(4)硬水(水溶液中加入Ca2+/ Mg2+代替)配制乳化沥青,会对阴离子乳化沥青的稳定性造成负面影响.
