肉豆蔻化学成分及抗炎活性研究
2023-11-15肖雯雯万仁山张红林曾天艳白梦微李大山邵立东
肖雯雯,万仁山,张红林,曾天艳,白梦微,李大山,邵立东
(云南中医药大学,云南 昆明 650500)
肉豆蔻为肉豆蔻科(Myristicaceae) 肉豆蔻属(Myristica)植物肉豆蔻(Myristica fragrans Houtt.)的干燥种仁,又名豆蔻、玉果、肉果等,为肉豆蔻科乔本植物,主要分布于巴西、马来西亚、印度、印度尼西亚及西印度群岛等热带地区,我国台湾、广西、海南、广东、云南等地亦有引种栽培[1]。肉豆蔻为传统中药材,历版《中国药典》均有记载,其性温,味辛,归脾、胃、大肠经,具有温中行气、涩肠止泻等功效,用于治疗脾胃虚寒,久泻不止,脘腹胀痛,食少呕吐等症[2]。化学成分研究表明,肉豆蔻主要含有挥发油、苯丙素类、木脂素类、二芳基烷烃类、黄酮类等多种化学成分[3-10]。现代药理活性研究表明,肉豆蔻具有抗炎镇痛[11-13]、抗氧化[4,13]、抗菌[14]、抗肿瘤[8]、降血糖[6,15]等多方面药理活性。为深入开展对肉豆蔻化学成分的分离鉴定、药理活性筛选研究,以期为肉豆蔻的进一步研究和开发利用提供科学依据。本实验对肉豆蔻的石油醚与乙酸乙酯部位进行化学成分研究,从中分离得到15 个化合物,分别鉴定为化合物1:2-(4-烯丙基-2,6-二甲氧基苯氧基)-1-(4-羟基-3-甲氧基苯基)丙烷[2-(4-allyl-2,6-dimethoxyphenoxy)-1-(4-hydroxy-3-methoxyphenyl)propane]、化合物2:肉豆蔻异木脂素(iso-lignan)、化合物3:4-(2-(4-烯丙基-2,6-二甲氧基苯氧基)-1-羟丙基)-2,6-二甲氧基苯酚[4-(2-(4-allyl-2,6-dimethoxyphenoxy)-1-hydroxypropyl)-2,6-dimethoxyphenol]、化合物4:(E)-4-(1-羟基-2-(2-甲氧基-4-(丙烯基)苯氧基)丙基)-2-甲氧基苯酚[(E)-4-(1-hydroxy-2-(2-methoxy-4-(propenyl)phenoxy)propyl)-2-methoxyphenol]、化合物5:(-)-miliusfragrin、化合物6:去氢二异丁香酚(dehydrodiisoeugenol)、化合物7:反式-2,3-二氢-7-甲氧基-2-(3,4-二甲氧基苯基)-3-甲基-5-(1-(E)-丙烯基)苯并呋喃 [trans-2,3-dihydro-7-methoxy-2-(3,4-dimethoxyphenyl)-3-methyl-5-(1-(E)-propenyl)benzofuran]、化合物8:(-)-eusiderin A、化合物9:acetyl oleiferin C、化合物10:补骨脂酚(psoralen)、化合物11:3-(4-羟基-3-甲氧苯基)丙烷-1,2-二醇[3-(4-hydroxy-3-methoxyphenyl)propane-1,2-diol]、化合物12:1-(3,4-二甲氧基苯基)丙烷-2-酮[1-(3,4-dimethoxyphenyl)propan-2-one]、化合物13:broussochalcone B、化合物14:bavachinin、化合物15:malabaricone C。化合物5,8~14 为首次从该属植物中分离得到。通过LPS 诱导RAW 264.7 巨噬细胞NO 释放抗炎模型,对所得化合物进行体外抗炎活性研究,结果表明,化合物13 和15 对LPS 诱导的RAW 264.7 细胞NO 释放有较强抑制活性,其IC50分别为8.57 ± 0.11 和(12.01 ± 1.27)μmol·L-1。化合物1 和7 显示一定抑制活性,其IC50分别为34.48 ± 3.05 和(42.76 ± 1.53)μmol·L-1。
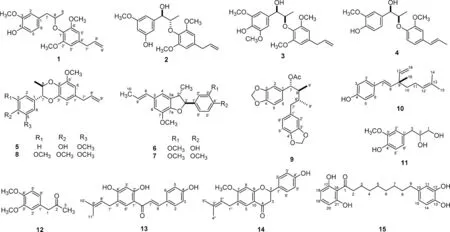
图1 化合物1~15 的结构
1 材料与方法
1.1 仪器与材料 Bruker AVANCE-III(500、600 MHz)型核磁共振波谱仪(德国Bruker 公司);Agilent 6540 Q-TO 型质谱仪(美国Agilent 公司);RPC18半制备色谱柱(10 mm × 250 mm,5 μm,美国Agilent 公司);色谱硅胶(200~300 目,青岛海洋化工厂);GF254 薄层色谱硅胶(青岛海洋化工厂);LH-20 羟丙基葡聚糖凝胶(Sephadex LH-20,美国Pharmacia 公司);反相中压和常压材料(ODS,德国Merck 公司);薄层色谱显色剂(10% 硫酸乙醇溶液);石油醚、二氯甲烷、氯仿、乙酸乙酯、丙酮、甲醇等试剂为重蒸的工业或化学纯溶剂;色谱甲醇(上海星可高纯溶剂有限公司)。
药材样品采购于昆明市螺蛳湾药材市场,经云南中医药大学董发武副教授鉴定为肉豆蔻(Myristica fragrans Houtt.)的种仁,凭证标本(YNYZ20190503)现存于云南中医药大学中药学院科研实验室。
1.2 提取与分离 粉碎过后的肉豆蔻种仁20 kg,先用水蒸气蒸馏法提取挥发油大约150 mL,剩余的药渣用70%的乙醇浸泡提取2 次,每次48 h,将两次的提取液进行合并,减压回收至无醇味,剩余的水相分别使用石油醚、乙酸乙酯、正丁醇进行萃取。分别合并3 部位的萃取液,减压浓缩后分别得到石油醚部位萃取物790 g,乙酸乙酯部位萃取物240 g,正丁醇部位萃取物220 g。
将石油醚部位萃取物(790 g) 过中压反相,以(70%、80%、95%和100%)甲醇-水梯度洗脱,得到9 个流分段(Fr.1~Fr.9)。Fr.3(48.6 g)经硅胶柱色谱,以石油醚-乙酸乙酯(100 ∶1~1 ∶1)梯度洗脱,得到6 个流分段(Fr.3.1~Fr.3.6)。Fr.3.6(690.3 mg)经反复的制备薄层、半制备液相得到化合物1(8.3 mg)、2(9.7 mg)、3(6.1 mg)、4(6.9 mg)。Fr.4(56 g)经硅胶柱色谱,以石油醚-乙酸乙酯(100 ∶1~1 ∶1)梯度洗脱,得到6 个流分段(Fr.4.1~Fr.4.6)。Fr.4.4(2.8 g)经Sephadex LH-20 色谱,氯仿-甲醇(3 ∶2),反复制备薄层,得到化合物5(9 mg)。Fr.5(20.2 g)经硅胶柱色谱,以石油醚-二氯甲烷-乙酸乙酯(30 ∶1 ∶1~1 ∶1 ∶1)梯度洗脱,得到7 个流分段(Fr.5.1 ~ Fr.5.7)。Fr.5.4(861.6 mg)经Sephadex LH-20 凝胶色谱,氯仿-甲醇(3 ∶2),制备薄层得到化合物6 (18.2 mg)、7(10.6 mg)。Fr.5.6(1.8 g)经Sephadex LH-20 凝胶色谱,氯仿-甲醇(3 ∶2)、制备薄层得到化合物8(5.7 mg)。Fr.6(52.2 g)经硅胶柱色谱,以石油醚-乙酸乙酯(40 ∶1~1 ∶1)梯度洗脱,得到7 个流分段(Fr.6.1~Fr.6.7)。Fr.6.4(2 g)经Sephadex LH-20 色谱、硅胶柱色谱、反复制备薄层得到化合物9(8 mg)、10(27.7 mg)。
将乙酸乙酯部位(240 g)过中压反相,以(20%~100%)甲醇-水梯度洗脱,得到12 个流分段(Fr.1~Fr.12)。Fr.2(2.2 g)经Sephadex LH-20 凝胶色谱,氯仿-甲醇(3:2),得到6 个流分段(Fr.2.1~Fr.2.6)。Fr.2.1(161.6 mg)经硅胶柱色谱,以石油醚-二氯甲烷-丙酮(2 ∶1 ∶1) 为洗脱剂得到化合物11 (37.3 mg)。Fr.4(10.8 g)经Sephadex LH-20 色谱,氯仿-甲醇(3 ∶2),得到3 个流分段(Fr.4.1~Fr.4.3)。Fr.4.1(2.4 g)经反相柱色谱、Sephadex LH-20 凝胶色谱,氯仿-甲醇(3 ∶2)、硅胶柱色谱得到化合物12(10.1 mg)。Fr.10(19 g)经硅胶柱色谱,以石油醚-二氯甲烷-乙酸乙酯(50 ∶1 ∶1~1 ∶1 ∶1) 梯度洗脱,得到7 个流分段(Fr.10.1~Fr.10.7)。Fr.10.6(552.5 mg)经Sephadex LH-20凝胶色谱,氯仿-甲醇(3 ∶2)、制备薄层得到化合物13(10.1 mg)、14(10 mg)。Fr.10.7(3.2 g)经Sephadex LH-20 凝胶色谱,氯仿-甲醇(3 ∶2)、制备薄层得到化合物15(85 mg)。
1.3 结构鉴定
化合物1:黄色油状物,ESI-MS m/z:381.1672[M+Na]+,分子式为C21H26O5。1H-NMR(CDCl3,500 MHz)δ:6.81(1H,d,J=8.0 Hz,H-5),6.76(1H,d,J=1.7 Hz,H-2),6.69 (1H,dd,J=8.0 Hz,1.7 Hz,H-6),6.40(2H,s,H-3’,H-5’),5.93~6.01 (1H,m,H-8’),5.47(1H,s,4-OH),5.08~5.13 (2H,m,H-9’),4.29~4.35(1H,m,H-8),3.86(3H,s,3-OCH3),3.79(6H,s,2’-OCH3,6’-OCH3),3.34 (2H,d,J=6.7 Hz,H-7’),3.12(1H,dd,J=13.5,5.1 Hz,H-7b),2.72 (1H,dd,J=13.5 Hz,8.3 Hz,H-7a),1.19 (3H,d,J =6.2 Hz,H-9);13C NMR(CDCl3,125 MHz)δ:153.6(C-2’,C-6’),146.1(C-3),143.8 (C-4),137.3 (C-8’),135.5 (C-1’),134.3(C-1),131.0(C-4’),122.1(C-6),116.0(C-9’),113.9(C-5),112.2(C-2),105.5(C-3’,C-5’),80.2(C-8),56.0(OCH3),55.9(OCH3),42.9(C-7),40.6(C-7’),19.6(C-9)。以上波谱数据与文献报道基本一致[16],故鉴定化合物1 为2-(4-烯丙基-2,6-二甲氧基苯氧基)-1-(4-羟基-3-甲氧基苯基)丙烷。
化合物2:无色油状物,ESI-MS m/z:397.1622[M+Na]+,分子式为C21H26O6。1H-NMR(CDCl3,500 MHz)δ:6.88 (1H,s,H-4),6.84 (2H,s,H-2,H-6),6.44 (2H,s,H-3’,H-5’),5.97 (1H,m,H-8’),5.60(1H,s,5-OH),5.09-5.14(2H,m,H-9’),4.94(1H,s,7-OH),4.61(1H,d,J=8.6 Hz,H-7),3.92(1H,dq,J=8.5 Hz,6.3 Hz,H-8),3.87(3H,s,3-OCH3),3.86(6H,s,2’-OCH3,6’-OCH3),3.35(2H,d,J=6.7 Hz,H-7’),1.18(3H,d,J=6.3 Hz,H-9);13C NMR(CDCl3,125 MHz)δ:152.8(C-2’,C-6’),146.6(C-3),145.4(C-5),137.2(C-8’),136.0(C-4’),135.4(C-1),132.9(C-1’),120.8(C-6),116.3(C-9’),114.1(C-4),109.6(C-2),105.6(C-3’,C-5’),86.8(C-7),79.2(C-8),56.1 (2’-OCH3,6’-OCH3),56.1 (3-OCH3),40.7(C-7’),17.7(C-9)。以上波谱数据与文献报道基本一致[17],故鉴定化合物2 为肉豆蔻异木脂素。
化合物3:无色油状物,ESI-MS m/z:427.1723[M+Na]+,分子式为C22H28O7。1H-NMR(CDCl3,500 MHz)δ:6.55(2H,s,H-2,H-6),6.46(2H,s,H-3’,H-5’),5.94~6.02 (1H,m,H-8’),5.43 (1H,s,7-OH),5.11~5.15 (2H,m,H-9’),4.78 (1H,d,J=2.7 Hz,H-7),4.31 (1H,dq,J=2.9 Hz,6.4 Hz,H-8),3.87(12H,s,OCH3× 4),3.37(2H,d,J=6.7 Hz,H-7’),1.11(3H,d,J=6.4 Hz,H-9);13C NMR(CDCl3,125 MHz)δ:153.7(C-2’,C-6’),147.0(C-3,C-5),137.2(C-8’),136.3(C-1’),133.7(C-1),133.2(C-4),131.3(C-4’),116.4(C-9’),105.7(C-3’,C-5’),102.9(C-2,C-6),82.5(C-7),73.2(C-8),56.5(OCH3× 2),56.3(OCH3×2),40.7(C-7’),12.9(C-9)。以上波谱数据与文献报道基本一致[16],故鉴定化合物3 为4-(2-(4-烯丙基-2,6-二甲氧基苯氧基)-1-羟丙基)-2,6-二甲氧基苯酚。
化合物4:黄色油状物,ESI-MS m/z:367.1519[M+Na]+,分子式为C20H24O5。1H-NMR(CDCl3,500 MHz)δ:6.74~6.98(6H,m,Ar-H),6.36(1H,dd,J=15.7 Hz,1.5 Hz,H-7’),6.12 ~6.19 (1H,m,H-8’),5.57(1H,s,7-OH),4.82 (1H,d,J =2.9 Hz,H-7),4.33(1H,dq,J=3.1 Hz,6.4 Hz,H-8),3.89 (6H,s,OCH3×2),3.53 (1H,s,4-OH),1.88 (3H,dd,J =6.6 Hz,1.6 Hz,H-9’),1.17(3H,d,J=6.4 Hz,H-9);13C NMR(CDCl3,125 MHz)δ:151.7(C-6’),146.8(C-3),145.8(C-1’),144.9(C-4),133.9(C-4’),132.0(C-1),130.6(C-7’),125.2(C-8’),120.1(C-6),119.3(C-3’),119.2(C-2’),114.1(C-5),109.5(C-5’),109.0(C-2),82.7(C-7),73.7(C-8),56.1(OCH3),56.0(OCH3),18.5(C-9’),13.5(C-9)。以上波谱数据与文献报道基本一致[18],故鉴定化合物4 为(E)-4-(1-羟基-2-(2-甲氧基-4-(丙烯基)苯氧基)丙基)-2-甲氧基苯酚。
化合物5:无色油状物,ESI-MS m/z:343.1550[M +H]+,分子式为C20H22O5。1H-NMR(CDCl3,500 MHz)δ:6.94(1H,d,J=8.0 Hz,H-3),6.87(1H,dd,J =8.9,0.8 Hz,H-2),6.85 (1H,s,H-6),6.47 (1H,d,J=1.3 Hz,H-2’),6.37(1H,d,J=1.5 Hz,H-6’),5.95(1H,ddt,J =16.8 Hz,10.0 Hz,6.8Hz,H-8’),5.69(1H,s,4-OH),5.05-5.11(2H,m,H-9’),4.57(1H,d,J=7.9 Hz,H-7),4.06-4.12(1H,m,H-8),3.91(3H,s,5’-OCH3),3.89(3H,s,3’-OCH3),3.29(2H,d,J =6.7 Hz,H-7’),1.24(3H,d,J=6.4 Hz,H-9);13C NMR(CDCl3,125 MHz)δ:148.7(C-5’),147.0(C-5),146.4(C-4),144.6(C-3’),137.5(C-8’),132.5(C-1’),131.5(C-4’),129.1(C-1),121.2(C-2),115.9(C-9’),114.6(C-3),109.8(C-6),109.6(C-2’),104.7(C-6’),81.0(C-7),74.4(C-8),56.3(3-OCH3),56.2(5-OCH3),40.2(C-7’),17.4(C-9)。以上波谱数据与文献报道基本一致[19],故鉴定化合物5 为(-)-miliusfragrin。
化合物6:白色固体,ESI-MS m/z:349.1410 [M+Na]+,分子式为C20H22O4。1H-NMR(CDCl3,500 MHz)δ:6.98 (1H,s,H-2’),6.90 (2H,s,H-5 ’,H-6’),6.79(1H,s,H-4),6.77 (1H,s,H-6),6.37 (1H,dd,J =15.7,1.5 Hz,H-8),6.08 ~6.15 (1H,m,H-9),5.67(1H,s,4’-OH),5.10 (1H,d,J =9.5 Hz,H-2),3.90(3H,s,OCH3),3.88(3H,s,OCH3),3.42 ~3.48(1H,m,H-3),1.87(3H,dd,J=6.6,1.5 Hz,10-CH3),1.38(3H,d,J =6.8 Hz,3-CH3);13C NMR (CDCl3,125 MHz)δ:146.8(C-3’),146.6(C-7a),145.9(C-4’),144.2(C-7),133.4(C-3a),132.3(C-5),132.2(C-1’),131.0(C-8),123.6(C-9),120.1(C-6’),114.2(C-5’),113.4(C-4),109.2(C-6),109.0(C-2’),93.9(C-2),56.1(OCH3),56.0(OCH3),45.7(C-3),18.5(10-CH3),17.6(3-CH3)。以上波谱数据与文献报道基本一致[20],故鉴定化合物6 为去氢二异丁香酚。
化合物7:黄色油状物,ESI-MS m/z:363.1567[M+Na]+,分子式为C21H24O4。1H-NMR(CDCl3,500 MHz)δ:6.98(1H,d,J=1.8 Hz,H-2’),6.95(1H,dd,J=8.2,1.9 Hz,H-6’),6.84(1H,d,J=8.2 Hz,H-5’),6.79(1H,s,H-6),6.77(1H,s,H-4),6.36(1H,dd,J =15.7,1.3 Hz,H-8),6.07~6.15(1H,m,H-9),5.12(1H,d,J=9.7 Hz,H-2),3.88(3H,s,OCH3),3.87(3H,s,OCH3),3.85 (3H,s,OCH3),3.43-3.50 (1H,m,H-3),1.87(3H,d,J=5.7 Hz,10-CH3),1.38(3H,d,J=6.8 Hz,3-CH3);13C NMR (CDCl3,125 MHz)δ:149.2 (C-3’,C-4’),146.7(C-7a),144.3(C-7),133.4(C-3a),132.7(C-1’),132.3(C-5),131.0(C-8),123.7(C-9),119.4(C-6’),113.4(C-6),110.8(C-5’),109.6(C-4),109.3(C-2’),93.8(C-2),56.0(OCH3× 3),45.7(C-3),18.5(10-CH3),17.6(3-CH3)。以上波谱数据与文献报道基本一致[21],故鉴定化合物7 为反式-2,3-二氢-7-甲氧基-2-(3,4-二甲氧基苯基)-3-甲基-5-(1-(E)-丙烯基)苯并呋喃。
化合物8:无色油状物,ESI-MS m/z:409.1623[M+Na]+,分子式为C22H26O6。1H-NMR(CDCl3,600 MHz)δ:6.57(2H,s,H-2,H-6),6.49(1H,d,J=1.1 Hz,H-2’),6.38(1H,d,J=1.3 Hz,H-6’),5.91~5.98(1H,m,H-8’),5.05~5.11 (2H,m,H-9’),4.56 (1H,d,J=7.9 Hz,H-7),4.07 ~4.12 (1H,m,H-8),3.89(3H,s,OCH3),3.88(6H,s,2’-OCH3,6’-OCH3),3.86(3H,s,OCH3),3.30(2H,d,J =6.7 Hz,H-7’),1.26(3H,d,J =6.4 Hz,H-9);13C NMR(CDCl3,150 MHz)δ:153.6(C-3,C-5),148.7(C-5’),144.4(C-3’),138.4(C-4),137.4(C-8’),132.6(C-1,C-1’),131.3(C-4’),116.0(C-9’),109.7(C-2’),104.7(C-6’),104.4(C-2,C-6),81.1 (C-7),74.2 (C-8),61.0 (OCH3× 2),56.3(OCH3× 2),40.2(C-7’),17.5(C-9)。以上波谱数据与文献报道基本一致[22],故鉴定化合物8 为(-)-eusiderin A。
化合物9:无色油状物,ESI-MS m/z:385.1656[M+H]+,分子式为C22H24O6。1H-NMR(CDCl3,500 MHz)δ:6.44-6.73(6H,m,Ar-H),5.95(2H,s,-OCH2O-),5.92(2H,s,-OCH2O-),5.51(1H,d,J=9.7 Hz,H-7),2.39(2H,dd,J=7.7,3.5 Hz,H-7’),2.00(3H,s,OAc),1.89~1.93 (1H,m,H-8),1.51-1.57 (2H,m,H-8’),0.92(3H,d,J=6.8 Hz,H-9),0.78(3H,d,J=6.8 Hz,H-9’);13C NMR(CDCl3,125 MHz)δ:170.5(C=O),147.8(C-3),147.6(C-3’),147.3(C-4),145.7(C-4’),134.7(C-1’),133.7(C-1),121.9(C-6’),121.4(C-6),109.4(C-5’),108.1(C-5,C-2’),107.7(C-2),101.2(-OCH2O-),100.9(-OCH2O-),79.4(C-7),41.5(C-7’),39.9 (C-8),34.8 (C-8’),21.4(OCH3),14.0(C-9’),9.9(C-9)。以上波谱数据与文献报道基本一致[23],故鉴定化合物9 为acetyl oleiferin C。
化合物10:无色油状物,ESI-MS m/z:255.1747[M -H]-,分子式为C18H24O。1H-NMR(CDCl3,500 MHz)δ:7.27 (2H,d,J=8.6 Hz,H-2,H-6),6.79(2H,d,J=8.5 Hz,H-3,H-5),6.28 (1H,d,J=16.2 Hz,H-7),6.08 (1H,d,J =16.2 Hz,H-8),5.91 (1H,dd,J =17.5,10.7 Hz,H-17),5.12~5.15(1H,m,H-12),5.02~5.07(2H,m,H-18),4.95(1H,s,4-OH),1.98(2H,dd,J =16.4,7.5 Hz,H-11),1.70 (3H,s,15-CH3),1.62(3H,s,14-CH3),1.50~1.54(2H,m,H-10),1.22(3H,s,16-CH3);13C NMR (CDCl3,125 MHz)δ:154.8 (C-4),146.1(C-17),136.0(C-8),131.4(C-13),131.1(C-1),127.5(C-2,C-6),126.6(C-7),125.0(C-12),115.5(C-3,C-5),112.0(C-18),42.7(C-9),41.4(C-10),25.8(15-CH3),23.5(16-CH3),23.4(C-11),17.8(14-CH3)。以上波谱数据与文献报道基本一致[24],故鉴定化合物10 为补骨脂酚。
化合物11:无色油状物,ESI-MS m/z:197.0809[M-H]-,分子式为C10H14O4。1H-NMR((CD3)2CO,600 MHz)δ:7.33 (1H,s,4’-OH),6.86 (1H,d,J=1.8 Hz,H-2’),6.72(1H,d,J=8.0 Hz,H-5’),6.67(1H,dd,J=8.0,1.9 Hz,H-6’),3.81(3H,s,OCH3),3.75~3.79(1H,m,H-2),3.48~3.50(1H,m,H-1b),3.39~3.43(1H,m,H-1a),2.72(1H,dd,J=13.7,5.6 Hz,H-3b),2.60(1H,dd,J =13.7,7.3 Hz,H-3a);13C NMR((CD3)2CO,150 MHz)δ:148.1(C-3’),145.7(C-4’),131.4(C-1’),122.7(C-6’),115.5(C-5’),113.9(C-2’),74.1(C-2),66.5(C-1),56.2(3-OCH3),40.4(C-3)。以上波谱数据与文献报道基本一致[25],故鉴定化合物11 为3-(4-羟基-3-甲氧苯基)丙烷-1,2-二醇。
化合物12:黄色油状物,ESI-MS m/z:195.1009[M +H]+,分子式为C11H14O3。1H-NMR(CDCl3,500 MHz)δ:6.83(1H,d,J=8.1 Hz,H-5’),6.75(1H,dd,J=8.1,1.7 Hz,H-6’),6.70(1H,d,J=1.7 Hz,H-2’),3.86(6H,s,OCH3),3.62(2H,s,H-1),2.14(3H,s,3-CH3);13C NMR(CDCl3,125 MHz)δ:206.9(C-2),149.3(C-3’),148.3(C-4’),126.9(C-1’),121.7(C-2’),112.6(C-5),111.6(C-6’),56.0(OCH3),56.0(OCH3),50.7(C-1),29.2(C-3)。以上波谱数据与文献报道基本一致[26],故鉴定化合物12 为1-(3,4-二甲氧基苯基)丙烷-2-酮。
化合物13:黄色固体,ESI-MS m/z:325.1434 [M+H]+,分子式为C20H20O4。1H-NMR((CD3)2CO,500 MHz)δ:13.50 (1H,s,2’-OH),7.95 (1H,s,H-6’),7.82(1H,d,J=15.4 Hz,H-8),7.73(1H,d,J=15.4 Hz,H-7),7.70(2H,d,J=8.6 Hz,H-2,H-6),6.93(2H,d,J=8.6 Hz,H-3,H-5),6.41 (1H,s,H-3’),5.34(1H,dddt,J=8.5,5.6,2.8,1.3 Hz,H-8’),3.30(2H,d,J=7.1 Hz,H-7’),1.73(3H,s,H-11’),1.72(3H,s,H-10’);13C NMR((CD3)2CO,125 MHz)δ:191.8(C =O),165.0(C-4’),162.5(C-2’),160.1(C-4),143.9(C-8),131.5(C-9’),131.3(C-6’),130.7(C-2,C-6),126.7(C-1),123.0(C-8’),120.4(C-5’),117.5(C-7),115.9 (C-3,C-5),113.4(C-1’),102.6 (C-3’),27.9(C-7’),24.9(C-10’),17.0(C-11’)。以上波谱数据与文献报道基本一致[27],故鉴定化合物13 为broussochalcone B。
化合物14:黄色油状物,ESI-MS m/z:361.1407[M+Na]+,分子式为C21H22O4。1H-NMR(CDCl3,500 MHz)δ:7.68(1H,s,H-5),7.34(2H,d,J=8.5 Hz,H-2’,H-6’),6.90(2H,d,J=8.6 Hz,H-3’,H-5’),6.44(1H,s,H-8),5.88 (1H,s,4’-OH),5.38 (1H,dd,J=13.4,2.8 Hz,H-2),5.27(1H,t,J=8.0 Hz,H-2”),3.84(3H,s,7-OCH3),3.24 (2H,d,J=7.3 Hz,H-1”),3.04(1H,dd,J=16.9,13.4 Hz,H-3b),2.78 (1H,dd,J=16.9,2.9 Hz,H-3a),1.73(3H,s,H-4”),1.69(3H,s,H-5”);13C NMR(CDCl3,125 MHz)δ:191.6(C-4),164.4(C-7),162.6(C-9),156.5(C-4’),133.2(C-3”),131.0(C-1’),128.1(C-2’,C-6’),127.2(C-5),125.1(C-6),121.8(C-2”),115.8(C-3’,C-5’),114.0(C-10),99.0(C-8),79.9(C-2),55.9(7-OCH3),44.2(C-3),27.9(C-1”),26.0(C-4”),17.9(C-5”)。以上波谱数据与文献报道基本一致[28],故鉴定化合物14 为bavachinin。
化合物15:黄绿色油状物,ESI-MS m/z:359.1852[M+H]+,分子式为C21H26O5。1H-NMR(CD3OD,500 MHz)δ:7.20(1H,t,J=8.2 Hz,H-19),6.67(1H,d,J=8.0 Hz,H-14),6.61(1H,d,J=1.4 Hz,H-11),6.49(1H,dd,J=8.0,1.5 Hz,H-15),6.35(2H,d,J=8.2 Hz,H-18,H-20),3.12(2H,t,J=7.4 Hz,H-2),2.45(2H,t,J=7.6 Hz,H-9),1.65~1.71 (2H,m,CH2-3),1.54~1.59(2H,m,CH2-8),1.29~1.38(8H,m,CH2-4,5,6,7);13C NMR(CD3OD,125 MHz)δ:209.7(C-1),163.4(C-17,C-21),146.0(C-12),144.0(C-13),136.8(C-19),135.8(C-10),120.6(C-15),116.5(C-11),116.2(C-14),111.4(C-16),108.3(C-18,C-20),45.7(C-2),36.3(C-9),32.9(C-8),30.6(C-5,C-6),30.5(C-4),30.3(C-7),25.8(C-3)。以上波谱数据与文献报道基本一致[29],故鉴定化合物15 为malabaricone C。
1.4 抗炎活性实验 采用MTT 法检测化合物对细胞活力影响,将RAW 264.7 细胞按密度为4 × 104/孔接种于96 孔板,37 ℃培养箱中培养24 h,加入含不同浓度的化合物继续培养24 h。设置正常对照组和空白对照组,每孔加入20 μL MTT(5 mg/mL),继续培养3.5 h 后,吸去板内培养液,每孔加入150 μL DMSO,避光振荡10 min 使其混匀,多功能读扳机490 nm 处测量吸光度值[30]。
采用Griess 法进行体外抑制一氧化氮作用筛选,取生长状态良好的RAW 264.7 细胞,按密度为4 ×104/孔接种于96 孔板,37 ℃培养箱中培养24 h,设置对照组、模型组和给药组并继续培养24 h。收集上清后加入Griess 试剂,多功能读扳机540 nm 处测量吸光度值[31]。
活性筛选结果见表1。
表1 分离化合物对LPS 诱导的RAW 264.7 细胞NO 生成抑制活性(±s,n=3)

表1 分离化合物对LPS 诱导的RAW 264.7 细胞NO 生成抑制活性(±s,n=3)
注:a 化合物2~6、8~12、14 未显示抑制活性;b 单位为μg/mL
化合物a IC50 /(μmol·L-1) CC50 / (μmol·L-1)石油醚部位萃取物b 61.08±5.76 >100乙酸乙酯部位萃取物b 22.53±2.84 >100挥发油b >100 >100 34.48±3.05 >100 7 42.76±1.53 >100 13 8.57±0.11 69.633±12.03 15 12.01±1.27 25.53±3.47 L-NMMAb 11.18±0.46 >100 1
1.5 数据处理 数据利用SPSS 24.0 统计软件进行数据处理及统计分析,实验数据采用均数± 标准差(±s) 表示,组间比较采用单因素方差分析(ANOVA)统计,统计结果P<0.05,P<0.01,P<0.001 为差异有统计学意义。
2 结果与讨论
本研究综合运用硅胶柱色谱、薄层制备、中压及常压反相ODS 柱色谱、Sephadex LH-20 凝胶柱色谱、半制备HPLC 等多种分离纯化技术,结合核磁共振、质谱等波谱鉴定技术对肉豆蔻的化学成分进行研究,从中分离鉴定了15 个化合物。化合物1~9 为木脂素类化合物,化合物1~4 为8-O-4’型木脂素,化合物6~7 为苯并呋喃型木脂素,是肉豆蔻中的主要成分类型;化合物5 和8 为二氧六环型木脂素,首次从该属植物中报道;化合物9 为二苄基丁烷型木脂素,首次从该属植物中分离得到;化合物10 为异戊二烯基酚萜类化合物,首次从该属植物中分离得到;化合物11~12 为简单苯丙素,首次从该属植物中分离得到;化合物13~14 为黄酮类化合物,首次从该属植物中分离得到;化合物15 为二芳基烷烃类化合物。该研究结果进一步揭示肉豆蔻的化学成分,为活性研究提供了物质基础。
抗炎活性结果表明,化合物13 和15 对LPS 诱导的RAW 264.7 细胞NO 释放有较强抑制活性,其IC50分别为(8.57 ± 0.11)和(12.01 ± 1.27)μmol·L-1。化合物1 和7 显示一定抑制活性,其IC50分别为(34.48 ±3.05)和(42.76 ± 1.53)μmol·L-1。以上结果丰富了肉豆蔻的抗炎活性,为进一步开发利用肉豆蔻的药用价值和开展后续研究提供了参考。
