高效液相色谱法测定双唑泰凝胶中抑菌剂羟苯乙酯
2023-11-09张红梅王晓丹崔玉玲
张红梅,王晓丹,崔玉玲
(济南市食品药品检验检测中心,济南 250014)
双唑泰主要成分有抗厌氧菌和抗滴虫的高效杀菌剂甲硝唑、广谱抗真菌药克霉唑、广谱外用杀菌消毒药乙酸氯己定,主要用于治疗细菌性、霉菌性、滴虫性及混合感染性阴道炎等,药物各组分既保持各单味药抑杀细菌、真菌、滴虫的作用,又有协同治疗作用,对妇科生殖道感染有良好的治疗效果,偶见皮疹、阴道烧灼感、瘙痒或其它黏膜刺激症状等不良反应[1-2]。其凝胶剂属生物黏附制剂,为水溶性凝胶,在阴道内滞留性好,药物作用时间长,能充分促进药物吸收,提高生物利用度,且给药方便,无刺激,无异物感[3-5]。目前《中华人民共和国药典》(以下简称《中国药典》)2020年版二部中收录的双唑泰剂型只有双唑泰栓剂[6],处方中无抑菌剂,而双唑泰凝胶剂是通过国家药品监督管理局注册并批准的双唑泰的一种新剂型,其说明书明确表明辅料中含有抑菌剂羟苯乙酯。
羟苯酯类是一种常用的广谱型抑菌剂,抑菌剂也叫作防腐剂,是指抑制微生物生长的化学物质,主要作用在于抑制微生物的繁殖增长,防止因微生物污染而影响药品质量。羟苯乙酯的化学名为4-对羟基苯甲酸乙酯,俗称尼泊金乙酯,具有抑菌效果好、毒性低、作用迅速、无臭无味等优点[7-8],不仅广泛用于食品及化妆品的抑菌[9-14],在药物液体制剂及半固体制剂中也得到广泛应用[15-17]。凝胶剂中常含大量的水,在使用过程中易受微生物污染,导致安全性问题,故需加入一定量的抑菌剂,以保证其在储存和使用过程中的安全性。
抑菌剂本身是一种化学物质,不同抑菌剂的抑菌机理不同,但普遍具有一定的毒性,使用过程中对人体都有一定的毒副作用。世界卫生组织(WTO)规定判断食品添加剂安全性的常用指标为日允许摄入量(ADI),即每天摄入均不会造成急性与慢性中毒的量和最大使用量,即GB 2760—2014《食品安全国家标准 食品添加剂使用标准》中所规定的添加剂最大使用量[18]。欧洲药品管理局(EMA)和人用药品注册技术要求国际协调会(ICH)建议在药品质量标准中应建立抑菌剂的定性和限量检查[8],《中国药典》2020 年版要求成品制剂中的抑菌剂有效浓度应低于对人体有害的浓度;EMA 建议以文献和/或实验数据为依据说明抑菌剂及用量的安全性,除非抑菌剂是常见的并且通常以相同浓度和相同给药途径使用[8]。所以为确保药物制剂使用时的安全性,必须合理控制抑菌剂的种类及用量,保证药品制剂中使用的抑菌剂都应该为其最低有效量[19]。
作为一种复方抗菌药物,双唑泰凝胶需要控制辅料中抑菌剂羟苯乙酯的用量,以保证用药的安全性和有效性。目前尚未见对双唑泰凝胶中抑菌剂羟苯乙酯进行控制的相关报道。笔者在参考文献[20]~[23]的基础上建立了高相液相色谱法测定双唑泰凝胶中抑菌剂羟苯乙酯的含量分析方法,并进行相关方法学验证,为双唑泰凝胶质量标准改进与提高提供一定参考。
1 实验部分
1.1 主要仪器与试剂
液相色谱仪:LC-20AT 型,配二极管阵列检测器,日本岛津公司。
电子天平:MS105DU 型,感量为0.01 mg,瑞士梅特勒-托利多公司。
恒温数控超声波清洗器:KQ-600GDV型,昆山市超声仪器有限公司。
微量高速离心机:CF16RN型,日本日立工机有限公司。
超纯水机:Milli-Q2882 型,美国密理博公司。
甲醇、乙腈、庚烷磺酸钠:色谱纯,国药集团化学试剂有限公司。
三乙胺:色谱纯,天津市科密欧化学试剂有限公司。
羟苯乙酯对照品:质量分数为100.0%,批号为100847-202105,中国食品药品检定研究院。
双唑泰凝胶样品:规格为5 g,批号为22601031,22601201,22601273,山东明仁福瑞达制药股份有限公司。
其它试剂均为分析纯。
1.2 溶液配制
稀释溶剂:甲醇-水-三乙胺,体积比为70∶30∶0.3,含庚烷磺酸钠10 mmol/L,用磷酸调pH值至4.0。
羟苯乙酯对照品储备液:512.8 μg/mL,精密称取羟苯乙酯对照品0.025 64 g,置于50 mL 容量瓶中,加入甲醇溶解并稀释定容至标线,摇匀。
羟苯乙酯系列标准工作溶液:精密量取羟苯乙酯对照品储备液5.0 mL,置于50 mL容量瓶中,用上述稀释溶剂稀释并定容至标线,摇匀,得到质量浓度为51.28 μg/mL羟苯乙酯标注中间溶液。分别精密吸取羟苯乙酯标注中间溶液1.0、5.0 mL,置于2 只100 mL 容量瓶中;再另分别精密吸取1.0、2.0 mL,置于2 只10 mL 容量瓶中。以上4 份溶液均用上述稀释溶剂稀释并定容至标线,摇匀,配制成羟苯乙酯的质量浓度分别为0.512 8、2.564、5.128、10.256、51.28 μg/mL的系列标准工作溶液,用0.45 μm 的滤膜过滤,取续滤液测定。
双唑泰凝胶样品溶液:精密称取双唑泰凝胶样品约0.5 g,置于100 mL 容量瓶中,加入上述稀释溶剂约70 mL,振摇,使分散均匀,再恒温超声30 min,然后以10 000 r/min 转速离心10 min,吸取上清液,用0.45 μm 的滤膜过滤,取续滤液测定。
1.3 仪器工作条件
色谱柱:Agilent Zorbax SB C8柱(250 mm × 4.6 mm,5 μm,美国安捷伦科技有限公司);流动相:甲醇-水-三乙胺(体积比为70∶30∶0.3),含庚烷磺酸钠10 mmol/L,用磷酸调pH 至4.0,流量为1.0 mL/min;检测器:二极管阵列检测器;检测波长:256 nm;柱温:30 ℃;进样体积:20 μL。
2 结果与讨论
2.1 实验条件优化
2.1.1 色谱条件
参考《中国药典》2020 版四部羟苯乙酯含量测定的色谱条件[24]及文献[20-23],色谱柱采用C18柱(250 mm×4.6 mm,5 μm)。分别选择流动相为甲醇-1%(体积分数,下同)乙酸溶液、甲醇-1%三乙胺、乙腈-1%乙酸溶液、乙腈-1%三乙胺,通过调节有机相与无机相的比例,有机相体积分数在30%~80%内改变,流动相的pH 在2.5~4.0 内改变,分离效果均不理想。试验发现,有机相比例过高则羟苯乙酯色谱峰与乙酸氯己定色谱峰不能分离;有机相比例过低则克霉唑色谱峰保留时间过长,色谱峰展宽严重。参考《中国药典》2020 版二部双唑泰栓测定的色谱条件:色谱柱采用Agilent Zorbax SB C8柱(250 mm×4.6 mm,5 μm),流动相为甲醇-水-三乙胺(体积比为70∶30∶0.3)(含庚烷磺酸钠10 mmol/L,用磷酸调pH值至4.0);羟苯乙酯色谱峰与相邻色谱峰分离度均大于1.5,拖尾因子小于1.2,且样品中所有产生色谱响应的成分均在10 min内出峰,故直接采用双唑泰栓测定的色谱条件。
2.1.2 检测波长
通过高效液相色谱在线紫外扫描,紫外光谱图如图1所示。由图1可以看出,羟苯乙酯在201、256 nm处有较强吸收,201 nm处的吸收易受溶剂影响,故选择检测波长为256 nm。
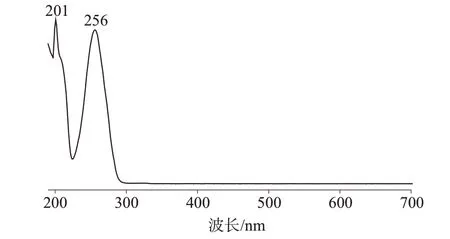
图1 羟苯乙酯紫外光谱图
2.1.3 提取溶剂
参考《中国药典》二部双唑泰栓质量标准,采用甲醇-水(体积比为70∶30,下同)溶液提取双唑泰凝胶样品,超声后溶液呈白色乳浊液,过滤后进行液相色谱分析,羟苯乙酯的提取回收率为99.1%,而以流动相甲醇-水-三乙胺(体积比为70∶30∶0.3)溶液为提取溶剂时的提取回收率为100.9%,二者无明显差异,表明以甲醇-水溶液为提取溶剂,双唑泰凝胶中羟苯乙酯基本提取完全,但色谱图中未出现乙酸氯己定的色谱峰。改变甲醇比例,分别采用100%甲醇、80%甲醇溶液、60%甲醇溶液、40%甲醇溶液、20%甲醇溶液进行超声提取,经液相色谱分析,结果均与70%甲醇溶液的提取情况一致,且经20%、40%与100%甲醇提取的样品溶液含有更多的杂质。而采用流动相作提取溶剂,超声后溶液几乎澄清,液相色谱图出现4 个完全分离的色谱峰,故选择色谱流动相作为提取溶剂。
2.1.4 超声时间
取双唑泰凝胶样品5份,按1.2方法制备样品溶液,于室温下超声处理,超声频率为40 kHz,分别选择超声时间为10、20、30、40、50 min,然后按1.3色谱条件测定。结果表明,超声30 min 后,羟苯乙酯含量测定值比较稳定,故选择超声时间为30 min。
2.1.5 离心转速与离心时间
取双唑泰凝胶样品适量,按1.2方法制备样品溶液,于室温下超声处理,超声频率为40 kHz,超声时间为30 min,分别设置离心转速为3 000、5 000、10 000 r/min,离心时间为10、20、30、40 min,按1.3色谱条件测定。结果表明,样品溶液经不同转速、不同离心时间处理后,羟苯乙酯含量测定值无明显差异。当转速为10 000 r/min、离心时间为10 min,转速为5 000 r/min、离心时间为20 min,转速为3 000 r/min、离心时间为30 min 时,样品上清液均较易过滤,可根据实验室条件自行选择,该试验采用转速为10 000 r/min、离心时间为10 min。
2.2 系统适用性试验
在1.3 色谱条件下,分别测定空白溶液、羟苯乙酯对照品溶液、双唑泰凝胶样品溶液,色谱图如图2所示。理论板数按羟苯乙酯峰计算不低于5 000,羟苯乙酯色谱峰与相邻峰分离度均大于1.5,拖尾因子小于1.2,系统适用性试验结果均符合相关要求。

图2 高效液相色谱图
2.3 线性方程与检出限
取羟苯乙酯系列标准工作溶液,按1.3色谱条件进行测定,以溶液质量浓度(x,mg/mL)为横坐标,以对应的色谱峰面积(y)为纵坐标,绘制标准曲线,采用线性回归法计算线性方程和相关系数。
对最低质量浓度的羟苯乙酯标准溶液进行逐级稀释并检测,以3倍的信噪比作为方法检出限。
羟苯乙酯的质量浓度线性范围、线性方程、相关系数、检出限列于表1。由表1 可知,羟苯乙酯的质量浓度在0.512 8~51.28 μg/mL 范围内与色谱峰面积线性关系良好,线性相关系数为0.999 9,方法检出限为0.08 μg/mL。
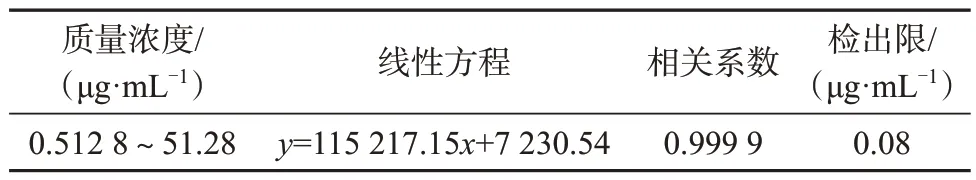
表1 羟苯乙酯的质量浓度线性范围、线性方程、相关系数及检出限
2.4 精密度试验
按1.2 方法制备6 份双唑泰凝胶样品溶液,按1.3色谱条件测定,按照标准曲线法计算羟苯乙酯的含量,再按照样品取样量和稀释倍数反推计算,得出样品中羟苯乙酯的质量分数,结果列于表2。由表2可知,测定结果的相对标准偏差为0.3%,表明该方法具有良好的精密度。
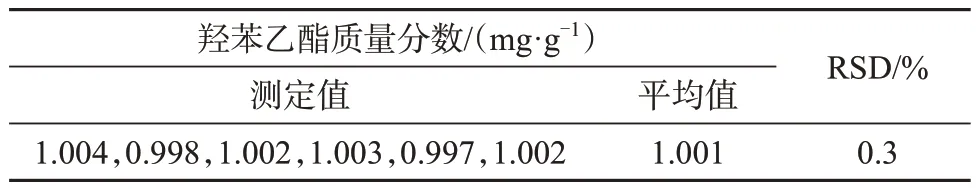
表2 精密度试验结果
2.5 稳定性试验
配制双唑泰凝胶样品溶液,在配制完成后第0、2、4、6、8、12、24 h分别进样,按1.3色谱条件测定,计算羟苯乙酯含量。结果显示,放置不同时间后样品中羟苯乙酯含量的相对标准偏差为0.7%,表明双唑泰凝胶样品溶液在室温放置24 h稳定性良好。
2.6 加标回收试验
精密称取双唑泰凝胶样品9 份,各约0.25 g,分别置于100 mL容量瓶中,按照羟苯乙酯标示含量的80%、100%、120%三个浓度水平,分别向9份样品中加入质量浓度为51.28 μg/mL的羟苯乙酯标准溶液3.0、5.0、7.0 mL,每个浓度水平样品按1.2 方法平行制备3 份,分别进样测定,取色谱峰面积平均值,计算羟苯乙酯含量及加标回收率,结果列于表3。由表3 可知,不同浓度水平的样品加标回收率为99.80%~102.20%,平均回收率为100.9%,表明该方法准确度较高。
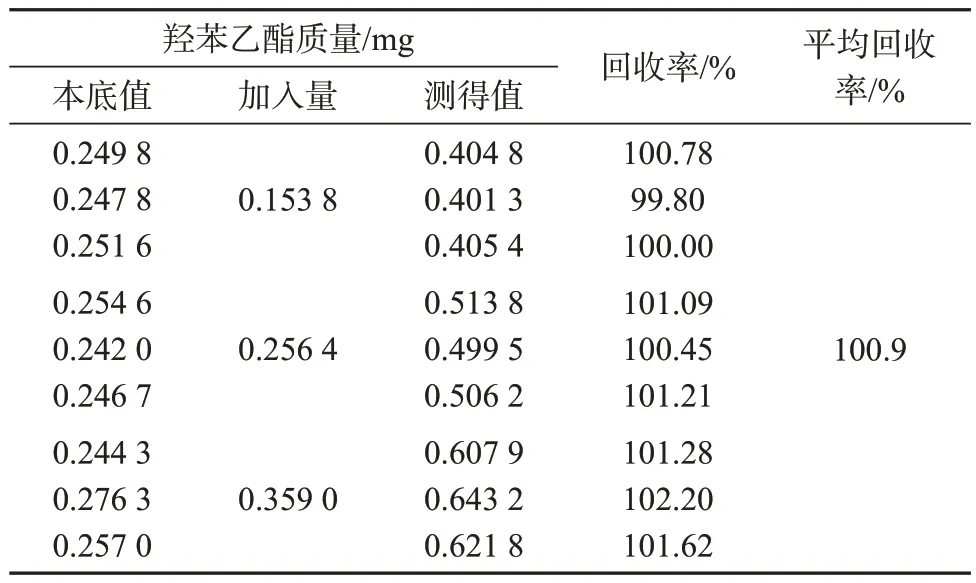
表3 加标回收试验结果
3 结语
建立了高效液相色谱法测定双唑泰凝胶中羟苯乙酯含量的质量分析方法,该方法操作相对简便、灵敏度较高、专属性与重现性好,结果准确可靠,可作为控制双唑泰凝胶中羟苯乙酯限度的检测方法,为双唑泰凝胶制剂的标准提高、改进提供参考依据,为双唑泰凝胶使用的安全性提供进一步的保证。
目前,美国食品药品管理局(FDA)对抑菌剂的使用上限已有明确的要求,但国际标准化组织(ISO)及相关标准未对筛选最低有效浓度有明确的方案,只有抑菌效力测定方法[25];《中国药典》2020 年版四部中对注射剂和糖浆剂中的抑菌剂种类与限度进行了明确规定,而对其它制剂如凝胶剂、乳膏剂等只规定根据需要可加入抑菌剂,但抑菌效力应符合抑菌效力检查法的规定[24],而对于双唑泰凝胶这种复合抗菌凝胶剂,理化测定法只能测出抑菌剂的加入量,至于是否需要添加抑菌剂、添加抑菌剂的量、生产企业是否过量添加都需要进一步结合抑菌效力试验进行验证[24,26-27]。
试验过程中发现双唑泰凝胶采用可压缩的塑料瓶进行包装,通过挤压方式挤出内容物,但很难将内容物全部挤出,多次试验发现每支大约能挤出3.5 g左右,仅占总量的70%,这样势必降低药物实际有效性,影响疗效。作为一种常用妇科外用非处方药,为保证双唑泰凝胶使用的安全性,建议相关药品标准增加抑菌剂的检查;为保证其有效性,建议生产企业结合实际使用情况合理加大内容物的装量,或者进一步改换包装如采用推进式包装等。
