肺间质疾病患者疲劳症状的临床特征及影响因素分析
2023-11-07罗成张宁彭艳茹李舒郭亚丽王玉光
罗成,张宁,彭艳茹,李舒,郭亚丽,王玉光
随着对肺间质疾病(interstitial lung disease,ILD)研究的不断深入,国内外学者发现ILD 患者除咳嗽和呼吸困难外,疲劳症状也较为突出[1-2]。流行病学调查显示,普通人群疲劳发生率为5%~20%[3],虽然ILD 患者疲劳尚未引起重视,但已有研究报道90%的结节病患者出现疲劳,其中48%的患者呈极度疲劳状态[2]。除结节病外,其他ILD 中疲劳发生率也远高于正常人群,特发性肺纤维化(idiopathic pulmonary fibrosis,IPF)患者中高达95%的患者出现疲劳[4],87% 的过敏性肺炎(hypersensitivity pneumonitis,HP)患者出现疲劳[5]。虽然疲劳不危及生命,但在系统性硬化症相关性间质病(interstitial lung disease associated with systemic sclerosis,SSc-ILD)患者中疲劳是常见的致残症状,与生活质量下降有关[6]。许多治疗ILD 的药物也会导致疲劳发生,疲劳是糖皮质激素的一种已知的常见不良反应,可能会导致或加重结节病患者的疲劳[7],其他ILD患者应用激素可能也会加重疲劳。疲劳是吡非尼酮的不良反应之一,在吡非尼酮治疗特发性肺纤维化的3 期临床试验中,有21%的患者出现疲劳[8]。目前国内尚缺乏针对ILD相关疲劳的研究。本研究通过疲劳评定量表(fatigue assessment scale,FAS)对ILD患者疲劳的临床特征及相关影响因素进行初步探究,以期引起临床重视及为后续研究提供参考。
1 对象与方法
1.1 研究对象 选取2021年11月—2023年1月就诊于首都医科大学附属北京中医医院呼吸科门诊或住院的ILD患者。所有患者经临床-影像-病理多学科讨论在我院或外院明确诊断为ILD。IPF 符合2018 年及2022 年美国胸科学会(American Thoracic Society,ATS)/欧洲呼吸学会(European Respiratory Society,ERS)/拉丁美洲胸科协会(the Latin American Thoracic Association,ALAT)/日本呼吸学会(the Japanese Respiratory Society,JRS)制定的IPF 诊断标准;结缔组织病相关性ILD(connective tissue diseases-interstitial lung disease,CTD-ILD)患者满足2018 年中国结缔组织相关间质性肺疾病诊断和治疗专家共识;其他ILD:具有自身免疫特征的间质性肺炎(interstitial pneumonia with autoimmune features,IPAF)诊断基于ATS和ERS制定的分类诊断标准;特发性间质性肺炎(idiopathic interstitial pneumonia,IIP)诊断符合2013 年国际IIP 指南和2018 年特发性肺纤维化诊断专家共识解读中关于IIP 的分类诊断标准;HP 符合2020 年ATS/JRS/ALAT制定的成人HP诊断的国际循证指南;结节病满足2019 年中国肺结节病诊断和治疗专家共识。纳入标准:(1)年龄≥18岁。(2)意识清楚,具有一定的交流能力。排除标准:(1)合并癌症、慢性疲劳综合征、维持性血液透析等因其他疾病所致疲劳的患者。(2)因各种原因出现长期卧床或影响躯体功能的患者。(3)合并严重的心、肝、肾、血液系统疾病者。(4)临床资料不全者。共纳入238 例,年龄33~91 岁,平均(64.93±10.63)岁,BMI为24.14(22.04,26.30)kg/m2,病程为60(36,96)个月。所有患者均签署知情同意书,自愿参加本研究,本研究经由首都医科大学附属北京中医医院伦理委员会审批通过(伦理批号2022BL02-060-01)。
1.2 资料收集 采用自主设计的一般资料问卷进行调查,主要包括性别、年龄、婚姻状况、体质量指数(BMI)、职业、文化程度、吸烟和饮酒情况。
1.3 肺功能检测 根据成人常规肺功能测定规范中国专家共识的测定标准对所有患者进行肺功能测定,使用JAEGER肺功能仪器,检测用力肺活量占预计值的百分比(FVC%pred)、第1 秒用力呼气量占预计值的百分比(FEV1%pred)、第1 秒末用力呼气量占用力肺活量的百分比(FEV1/FVCpred),重复测量3次,测量结果差异不超过5%或FVC差值不超过150 mL,取3 次中的最大值;一氧化碳弥散量占预计值的百分比(DLCO%pred),重复测量2次,测定结果差异≤10%,取2次平均值。
1.4 临床症状评估和疲劳症状评估 (1)疲劳症状评估。采用FAS 评估患者躯体和精神的疲劳情况。FAS 由10 个条目组成,每个条目为1~5分,总得分≥22分为疲劳,总得分≥34分为严重疲劳。(2)呼吸困难程度评估。采用英国医学研究委员会呼吸问卷改良版(mMRC)评估患者的呼吸困难程度,分级0~4 级,等级越高说明呼吸困难程度越重。(3)合并症评估。采用Charlson 合并症指数对患者合并症进行赋值,评估合并症的严重程度,得分越高,合并症越严重(≤2分为轻度;3~4 分为中度;≥5 分为重度)。(4)心理及睡眠情况评估。采用医院焦虑抑郁量表(HADS)对患者焦虑和抑郁程度进行评分,分别为HADS-A和HADS-D,得分标准:0~7分为正常;8~10 分为轻度抑郁/焦虑;11~14 分为中度抑郁/焦虑;≥15 分为严重抑郁/焦虑。采用匹兹堡睡眠质量指数(pittsburgh sleep quality index,PSQI)评估患者的睡眠质量,总得分≤7 分为睡眠正常;总得分>7分为睡眠障碍。
1.5 统计学方法 采用SPSS 22.0软件进行数据分析。正态分布或近似正态分布的计量资料以表示,2组间比较采用独立样本t检验,多组间比较采用单因素方差分析,组间多重比较采用Bonferroni法,相关性分析采用Pearson相关性检验;非正态分布的计量资料以M(P25,P75)表示,相关性分析采用Spearman相关性检验;计数资料采用例(%)表示。采用多元线性逐步回归分析ILD患者疲劳的影响因素,进入值为0.05,删除值为0.10,P<0.05为差异有统计学意义。
2 结果
2.1 不同临床特征ILD 患者疲劳情况分析 238例患者FAS 得分为(26.03±9.53)分,精神疲劳(12.25±5.14)分,躯体疲劳(13.79±4.97)分。159例(66.81%)出现疲劳,其中60 例(37.74%)为严重疲劳。不同mMRC 分级的ILD 患者FAS 得分差异有统计学意义:mMRC 0 级和1 级ILD 患者的FAS 得分低于mMRC 2—4级的患者,mMRC 2级ILD患者的FAS得分低于mMRC 4 级患者(P<0.01);不同病程、年龄、性别、婚姻、工作情况、教育程度、吸烟、饮酒情况、ILD类型、Charlson合并症指数患者FAS得分差异均无统计学意义,见表1。
Tab.1 Comparison of FAS scores between ILD patients with different clinical characteristics表1 不同临床特征ILD患者FAS得分比较(分,)

Tab.1 Comparison of FAS scores between ILD patients with different clinical characteristics表1 不同临床特征ILD患者FAS得分比较(分,)
**P<0.01;a与mMRC 0级比较,b与mMRC 1级比较,c与mMRC 2级比较,P<0.05。
变量病程n t或F 1.735年龄≥60个月<60个月<60岁≥60岁1.367性别0.978婚姻情况男女已婚1.746工作情况0.528教育程度2.090吸烟0.008饮酒0.597 ILD类型0.079 Charlson合并症指数0.936 mMRC分级丧偶/离异体力劳动非体力劳动小学及以下初中高中本科及以上从不已戒正在从不已戒正在IPF CTD-ILD IIP其他轻度中度重度0级1级2级3级4级128 110 71 167 109 129 211 27 77 161 26 73 77 62 164 60 14 183 47 8 65 76 46 51 191 43 4 51 74 56 32 25 FAS得分27.02±9.60 24.88±9.36 24.83±8.33 26.54±9.98 25.38±9.89 26.59±9.22 25.65±9.58 29.04±8.73 26.51±9.73 25.81±9.46 29.69±10.15 25.59±10.13 26.57±9.66 24.35±8.02 25.98±9.45 26.15±9.77 26.14±10.17 26.23±9.55 25.85±9.57 22.50±9.50 25.57±10.43 26.04±8.22 26.15±9.38 26.51±10.51 25.54±9.09 28.19±11.43 26.25±6.34 19.04±6.09 22.43±7.84 28.89±7.83ab 32.31±8.74ab 36.52±7.98abc 33.890**
2.2 肺功能和心理睡眠情况 患者肺功能FVC%pred 为(79.53±21.76)% ,FEV1%pred 为(79.43±20.21)%,FEV1/FVCpred 为(81.42±9.43)%,DLCO%pred 为(55.89±17.35)%。HADS-A 为4.0(2.0,7.0)分,HADS-D 为4.0(2.0,9.0)分,PSQI 为(9.45±4.78)分。
2.3 FAS 得分与临床特征相关性分析 238 例ILD患者的FAS 得分与年龄、病程、HADS-A、HADS-D、PSQI 呈正相关(r分别为0.176、0.125、0.502、0.591和0.570,P<0.05),与DLCO%pred 呈负相关(r=-0.136,P<0.05),与BMI、FVC%pred、FEV1%pred、FEV1/FVCpred 无相关性(r分别为-0.109、-0.070、-0.028、-0.072,P>0.05)。
2.4 ILD患者疲劳影响因素的分析 以FAS得分为因变量,mMRC分级、年龄、病程、DLCO%pred、PSQI、HADS-A和HADS-D为自变量建立多元线性逐步回归模型,结果表明HADS-D、mMRC 分级、PSQI 和病程是FAS得分的影响因素(P<0.05),见表2。
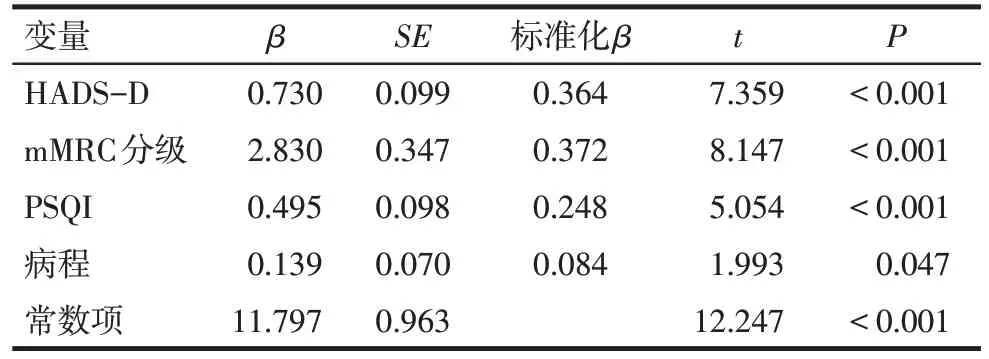
Tab.2 Multiple linear stepwise regression analysis of factors affecting the score of FAS in ILD patients表2 多元线性逐步回归分析ILD患者FAS得分的影响因素
3 讨论
疲劳是许多慢性疾病患者的普遍症状,也是ILD 患者的常见症状之一[1-2],严重影响患者的生活质量,但关于ILD 疲劳的管理和病因研究仍有限。最近的一项研究表明,仅有11%的疲劳能通过具体的诊断进行解释,其他疲劳主要是通过非诊断因素进行解释,如动力减弱、身体功能受限、活动水平减少和睡眠质量差等[9]。近年来,如何评估疲劳和其影响因素是研究热点,但由于我国ILD 患者疲劳的相关研究相对较少,研究工具的选取尚无统一标准,同时由于疲劳的主观性和复杂性,限制了对其影响因素的深入探究。结节病是ILD中疲劳症状较为突出的疾病,且国外结节病发病率较高。荷兰的一项重点针对结节病患者疲劳的研究在综合多个疲劳问卷后制定出FAS量表用于评估结节病患者的疲劳情况[10]。后在多个研究中[11-12]应用于IPF、结节病等多种ILD 疾病,是目前评估ILD 疲劳的潜在工具。本研究采用中文版FAS量表对ILD患者疲劳及影响因素进行初步探究,结果与欧洲IPF 登记中心测得的疲劳发生率相近[1],238 例患者中37.74%的患者为重度疲劳,稍低于结节病患者[2]。本研究发现,大部分患者对疲劳症状不重视,因其过于主观且难以描述,在就诊时常不会将其当做疾病的主要症状,且医护人员更加关注呼吸困难、咳嗽及其他便于测量的临床指标从而忽视疲劳症状。本研究通过多元逐步回归分析发现ILD 患者疲劳的影响因素包括病程、mMRC 分级、PSQI 和HADS-D。可见病程、呼吸困难、睡眠和抑郁对ILD患者有重要影响。
本研究显示,ILD 患者病程越长,疲劳越严重。这与心律失常患者及类风湿性关节炎患者疲劳影响因素相同[13-14]。随着医疗技术的进步,慢性疾病患者生存时间进一步延长,病程也进一步延长,患者机体各项机能下降,心肺功能减退,长期忍受疾病所带来的痛苦和困扰,同时医疗费用支出会加重患者的经济负担和心理压力,亦会导致疲劳程度的加重[15]。
在慢性阻塞性肺疾病和哮喘中,严重呼吸困难的患者疲劳发生率显著增高[15-16],这与本研究结果相似,提示呼吸困难是疲劳的重要影响因素。疲劳与呼吸困难密切相关,常相互影响,其可能原因为外周感觉感受器监测到呼吸困难后将信号传至中枢神经系统,机体为维持稳态而做出保护性反应,通过调节神经内分泌系统,使机体维持在低代谢的疲劳状态[17]。Troy等[18]认为ILD患者呼吸困难会导致机体缺氧,从而加重患者的疲劳程度。可见,临床中需重点关注患者的呼吸困难程度,采取相应措施改善呼吸困难,如吸氧、减少日常活动以改善ILD患者的疲劳程度,最终改善ILD患者的生活质量。
本研究发现,PSQI 越高,ILD 患者疲劳得分越高,与潘瑞丽等[19]的研究相似,其认为ILD患者的日间功能紊乱和睡眠时长会影响疲劳,睡眠时间不足、常感到困倦、做事精力不充沛的患者,疲劳程度越高。与健康人群比较,ILD 患者睡眠障碍的情况更为常见[20]。ILD 患者的睡眠结构经常被打乱,快速眼动睡眠时间减少,睡眠碎片化和夜间缺氧增加[21-22]。Mermigkis等[23]发现ILD患者夜间血氧饱和度和疲劳之间存在相关性。Agarwal 等[24]认为睡眠障碍是导致ILD患者疲劳的重要因素。其他还可能改变睡眠结构的ILD相关因素包括咳嗽以及皮质类固醇等药物使用[21]。此外,ILD 患者呼吸睡眠暂停的发生率高达88%,即使排除肥胖或上呼吸道病变引起的呼吸睡眠暂停,仍有68%的ILD 患者出现呼吸睡眠暂停[21-22]。在诊治过程中,要采用各种可行性措施改善ILD 患者的睡眠状况,保障夜间睡眠的质量,从而使疲劳症状改善,提高患者的生活质量。
情绪对疲劳的影响不容忽视,慢性病患者由于躯体症状、社会问题等的影响,罹患心理疾病的风险升高[25]。ILD 目前尚无逆转疾病进展的方法,病情反复、严重低氧血症、药物治疗昂贵等特点易造成患者无法脱离吸氧,丧失劳动和社交能力,给患者造成极大的心理负担,影响生活质量[26]。焦虑和抑郁作为常见的心理问题,在ILD 中更为普遍[9,27]。ILD 患者抑郁和焦虑中的发病率为23%~57%和27%~60%[28-29],焦虑抑郁等不良情绪与疲劳常互相影响。本研究中HADS-A 和HADS-D 与FAS 得分呈正相关,多元线性逐步回归结果提示ILD 患者抑郁程度越高,疲劳症状越严重,与相关研究[15-16]一致。因此,医护人员需要加强对ILD 患者心理状况的评估及筛查,早期干预,做好患者宣教工作,使患者家属参与其中,全方面改善患者心理状态,缓解疲劳。
综上,ILD 患者疲劳症状发生率较高且疲劳程度较重,影响因素包括疾病病程、呼吸困难、抑郁和睡眠障碍,医护工作者在疾病管理时应重点关注。本研究尚存在一定的局限性:研究对象均来自同一医院,无法避免病例选择偏倚,结论的适用性局限。本研究未纳入药物治疗、日常活动等其他可能影响疲劳的因素,后续可进一步探究ILD 疲劳与其影响因素间的因果关系。
