急性前循环大血管闭塞性脑梗死血管内治疗预后模型的构建与评估*
2023-11-06陈竞引卢亚凤李王文张丽娜刘兴华
陈竞引,卢亚凤,李王文,张丽娜,周 杰,李 莉,郭 靖,刘 进,杨 丹,刘兴华,刘 勇△
(1.锦州医科大学研究生学院,辽宁锦州 121001;2.重庆大学附属三峡医院神经内科,重庆 404000;3.重庆大学附属三峡医院放射科,重庆 404000)
急性前循环大血管闭塞性脑梗死血管内治疗较标准内科治疗能够改善患者临床预后,但并不是所有血管成功再通患者都能够获得良好的临床预后[1-3]。研究证实临床预后主要与核心梗死大小、侧支循环、时间窗相关[4-6]。核心梗死大小、侧支循环临床上最常用的评价工具分别是 ASPECTS 评分、ASITN/SIR 侧支循环分级系统[7-8]。结合各大研究和临床实践发现单一应用 ASPECTS 评分、ASITN/SIR侧支循环分级、时间窗对临床预后预测的准确性有限[9-10]。目前集合三大关键影响因素与血管内治疗预后的预测研究暂无报道。本研究旨在通过对行血管内治疗的急性前循环大血管闭塞患者的影像学及临床资料进行回顾性分析,构建一种基于术前ASPECTS 评分、ASITN/SIR 侧支循环分级和时间窗对急性前循环大血管闭塞性脑梗死血管内治疗预后的预测模型,期望应用此预测模型为临床选择急性前循环大血管闭塞的患者行血管内治疗提供决策依据,以做到个体化、精准化治疗,从而提升急性前循环大血管闭塞性脑梗死的临床疗效。
1 资料与方法
1.1 一般资料
纳入2020年4月至2022年1月在重庆大学附属三峡医院就诊的急性前循环大血管闭塞性脑梗死患者150例。纳入标准:(1)年龄18~85岁;(2)发病到股动脉穿刺时间在6 h以内;或者发病到股动脉穿刺时间为6~24 h,基于RAPID分析符合DAWN研究[11]的入组标准;(3)颈总动脉、颈内动脉、大脑中动脉M1、M2、M3段闭塞。排除标准:(1)病前mRS评分>2分;(2)存在严重心功能障碍、肺功能障碍、肝功能障碍、肾功能障碍;(3)合并脑动脉以外的动脉急性闭塞;(4)PT-INR>1.7,血小板<100×109/L;(5)近3个月服用过改善凝血功能的相关药物;(6)合并妊娠。剔除标准:(1)行血管内治疗前向血流为改良脑梗死溶栓血流分级(modifiedTreatment in Cerebral Ischemia grade,mTICI)0~2a级;(2)血管内治疗术后行去骨板减压术或颅内血肿清除术。前瞻性选取2022年2-6月本院收治的69例急性前循环大血管闭塞性脑梗死患者进行模型验证。本研究由本院伦理委员会审核通过且患者均知情同意。
1.2 方法
1.2.1侧支循环评估
患者取仰卧位,常规消毒铺巾后,以右侧腹股沟韧带下1 cm股动脉搏动明显处为穿刺点,局部麻醉,采用Seldinger技术穿刺右侧股动脉成功后,置入8F动脉鞘,全身肝素化,在0.035导丝引导下应用5F pigtail、单弯导管行脑血管造影,确认闭塞的责任血管,并行侧支循环评估。侧支循环评估使用基于DSA的ASITN/SIR侧支循环分级,0级:缺血部位无侧支血流;1级:缺血部位周边有缓慢的侧支血流,但缺乏持续的血流灌注;2级:缺血部位周边有快速的侧支血流,但缺乏持续的血流灌注,仅有部分血流灌注到缺血部位;3级:缺血部位静脉晚期可见缓慢完整的侧支血流;4级:缺血部位存在快速而完整的侧支血流。
1.2.2血管内治疗
脑血管造影确认存在前循环大血管闭塞,行全身麻醉,采用Solumbra、SWIM、SAVE、ADAPT等技术行血管内治疗。以大脑中动脉M1段闭塞SWIM技术为例,应用8F导引导管、5F Navien中间导管、Rebar18、Solitaire支架、微导丝及50 mL注射器,将导引导管置于目标动脉近端的颈内动脉颈升段,微导管、微导丝在中间导管辅助下超选至大脑中动脉闭塞段远端,中间导管送至大脑中动脉闭塞段的近端,经微导管造影确认在血管腔内后经微导管引入Solitaire支架至闭塞段并予以释放。经中间导管造影明确闭塞血管是否恢复前将血流及血栓位于支架有效段,在闭塞血管恢复前将血流支架静置5 min后回撤支架取栓,回撤支架同时将中间导管送至大脑前动脉远端,将支架连同血栓一起回收入中间导管内,同时回撤中间导管、微导管、支架系统,并经中间导管及导引导管持续负压抽吸,尽可能保持血栓的完整性,前向血流达到mTICI 2b~3级为成功灌注,如果1次取栓不成功可连续取栓3次,可依据术中情况应用支架置入、球囊扩张等措施。
1.2.3核心梗死评估
核心梗死评估使用基于NCCT的ASPECTS评分方法:在NCCT图像中选取大脑中动脉供血区两个层面的10个区域,(1)尾状核及其以下层面划分为M1、M2、M3、尾状核C、豆状核L、内囊IC、岛叶Ⅰ共计7个区域;(2)核团以上层面:包括M4、M5和M6共计3个区域。基于NCCT的ASPECTS评分正常为10分,脑梗死病灶每累及1个区域出现低密度影则减去1分。
1.2.4资料收集
收集入组患者的临床资料,包括性别、年龄、脑血管危险因素、病前mRS评分、TOAST分型、入院时美国国立卫生研究院卒中量表(the National Institutes of Health Stroke Scale,NIHSS)评分、入院时ASPECTS评分、基于DSA的ASITN/SIR侧支循环分级、闭塞血管、溶栓情况、取栓次数、术中mTICI分级、从发病到股动脉穿刺的时间、从股动脉穿刺到血管再通的时间、欧洲急性卒中合作组(European Cooperative Acute Stroke Study,ECASS)分型、术后90 d mRS评分等影像和临床资料。
1.2.5临床预后评估
采用mRS评分对预后进行评估,术后90 d mRS评分认定为急性前循环大血管闭塞性脑梗死血管内治疗的预后。术后90 d mRS评分0~2分组为良好预后组,3~6分组为不良预后组[9]。
1.2.6时间窗的确定
发病时间为症状出现的时间点,患者意识丧失的中风以最后一次见到患者正常的时间为时间点;从发病时间到股动脉穿刺的时间确定为时间窗,以分钟为单位。
1.3 统计学处理
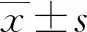
2 结 果
2.1 临床资料比较
150例患者术后90 d mRS评分0~2分的67例(44.67%)为良好预后组,3~6分的83例(55.33%)为不良预后组。良好预后组与不良预后组的年龄、糖尿病、高脂血症、高血压、饮酒、吸烟、病前mRS评分、TOAST分型、闭塞血管、是否溶栓、取栓次数、股动脉穿刺到血管再通时间、ECASS分型比较,差异无统计学意义(P>0.05);不良预后组的性别、NIHSS评分、ASPECTS评分、基于DSA的ASITN/SIR侧支循环分级、术中mTICI分级、从发病到股动脉穿刺的时间与良好预后组比较,差异有统计学意义(P<0.05),见表1。
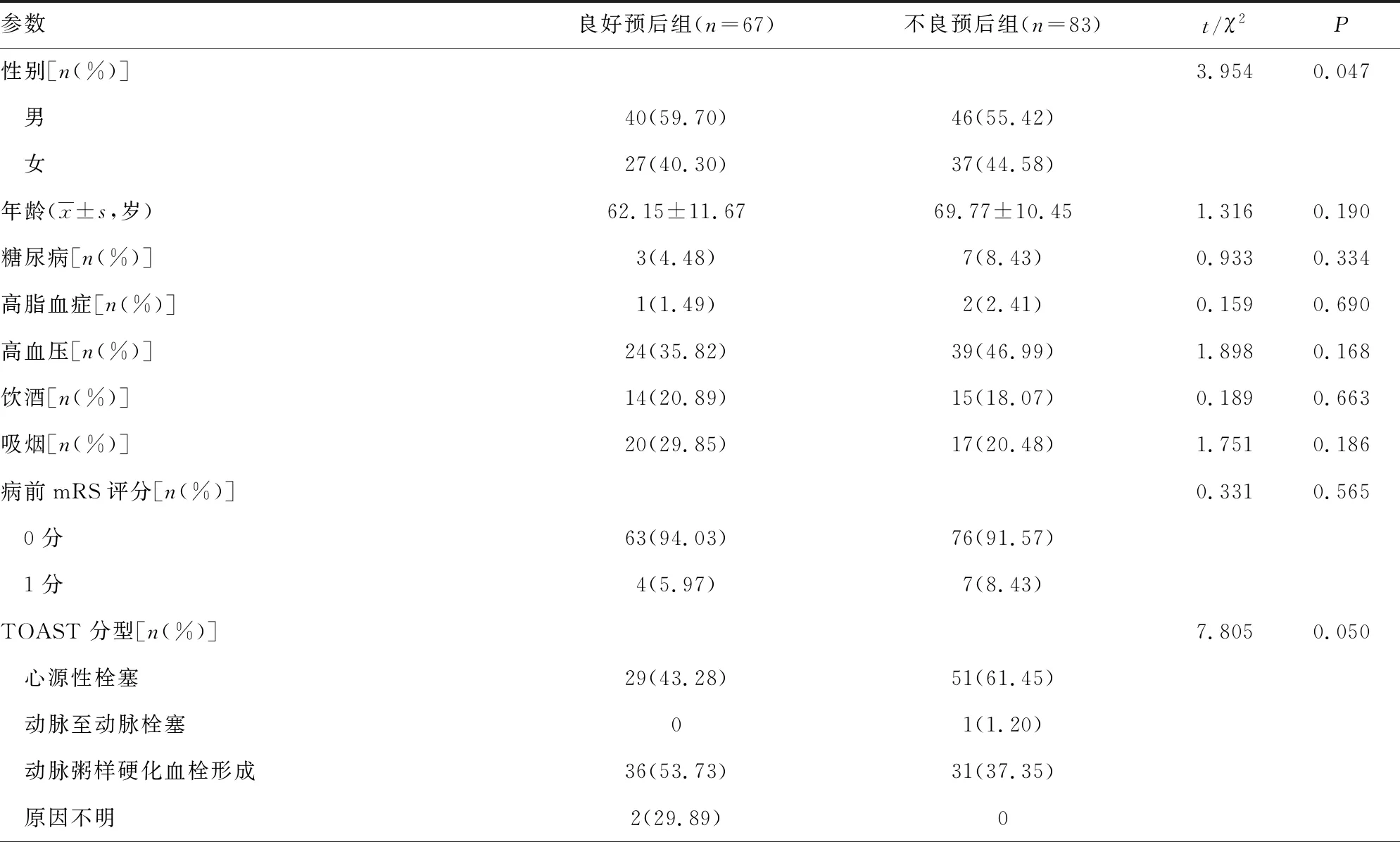
表1 临床资料比较
2.2 影响患者血管内治疗术后 90 d预后的多因素logistic回归分析
以患者血管内治疗术后 90 d是否(是=0,否=1)良好分作为因变量,将上述表中差异有统计学意义的参数纳入多因素logistic回归分析,分类变量赋值[性别(男=1,女=0)、基于DSA的ASITN/SIR侧支循环分级(0~2级=1,3~4级=0)、术中mTICI分级(2b级=1,3级=0)],连续性变量以原值录入。多因素logistic回归分析结果显示,NIHSS评分、基于DSA的ASITN/SIR侧支循环分级、从发病到股动脉穿刺的时间是血管内治疗术后 90 d预后不良的独立影响因素,ASPECTS 评分是保护因素(P<0.05),见表2。
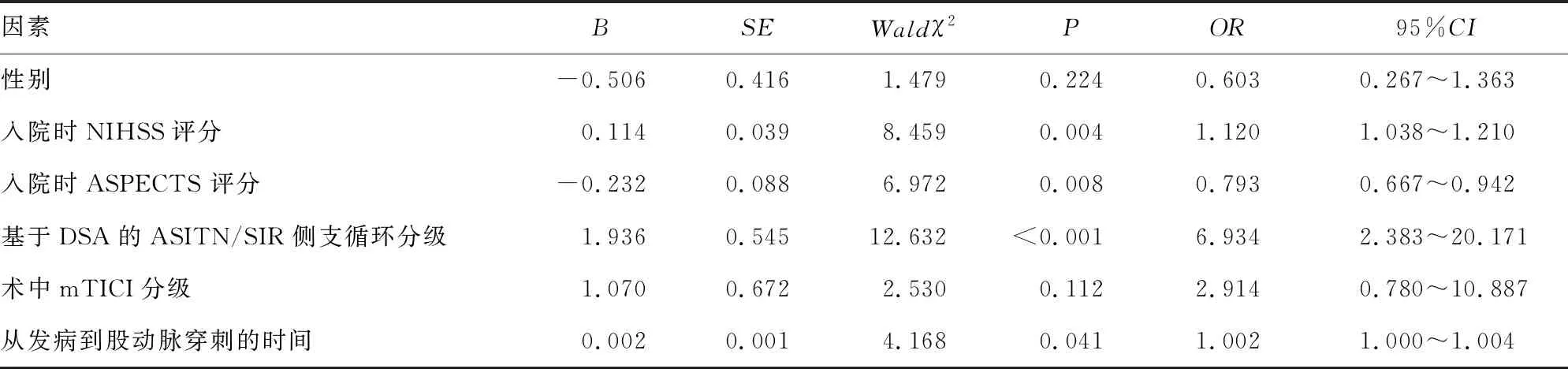
表2 影响患者血管内治疗术后 90 d预后的多因素logistic回归分析
2.3 入院时NIHSS评分、入院时ASPECTS 评分、基于DSA的ASITN/SIR侧支循环分级、从发病到股动脉穿刺的时间与预测模型对患者血管内治疗术后 90 d预后的评估比较
将上述4种指标再次纳入多因素logistic回归分析并构建 Logit(P)模型, Logit(P)=-1.967+0.114×入院时NIHSS评分-0.232×入院时ASPECTS评分+1.936×基于DSA的ASITN/SIR侧支循环分级+0.002×从发病到股动脉穿刺的时间。结果显示,入院时ASPECTS 评分、基于DSA的ASITN/SIR侧支循环分级的特异度较高,但灵敏度较低;从发病到股动脉穿刺的时间特异度较高,但灵敏度较低;而与其他单独评估指标相比,预测模型其特异度与灵敏度相对较好,AUC为0.849(95%CI:0.782~0.917),截断值为0.622,灵敏度为90.4%,特异度为68.7%,见表3和图1。
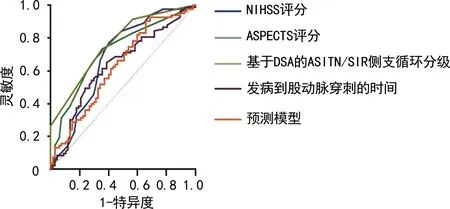
图1 各指标与预测模型评估患者血管内治疗术后90 d预后的ROC曲线比较
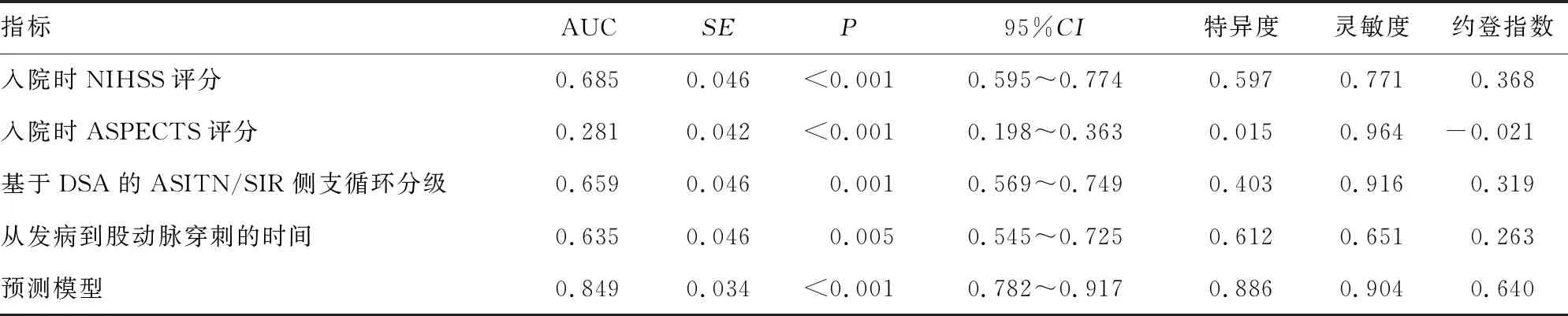
表3 各影响因素与预测模型对患者血管内治疗术后 90 d预后的评估比较
2.4 模型检验
以0.622为预测模型的临界值,前瞻性选取2022年2-6月本院收治69例急性前循环大血管闭塞性脑梗死患者进行模型验证,结果显示,模型预测血管内治疗术后90 d预后不良的灵敏度为90.32%,特异度为89.47%,准确度为89.86%,见表4。
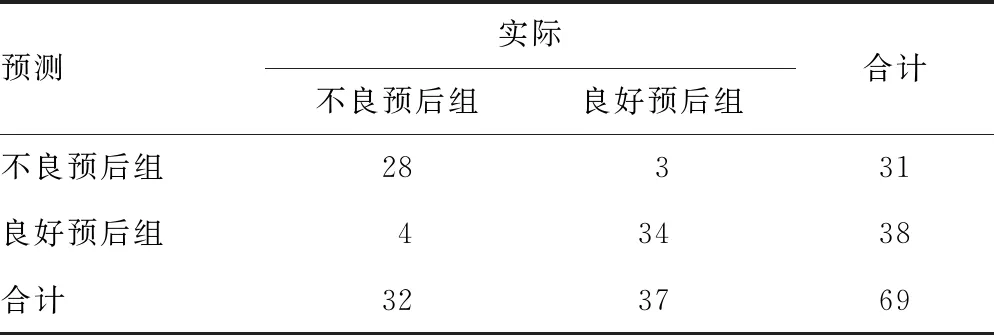
表4 预测模型效果验证结果(n)
3 讨 论
血管内治疗是当前临床治疗急性前循环大血管闭塞性脑梗死的重要手段,目前血管内治疗得到国内外指南最高级别的推荐[10-12]。血管内治疗再通率高达 80%以上,但高再通率不意味着高获益率。一项荟萃分析显示,机械取栓不良预后率为 54%,且约20%的患者在大血管闭塞取栓治疗后90 d内死亡[13]。我国的数据与之相似,前循环大血管闭塞机械取栓不良预后率为 56.4%[14]。因此,术前筛选合适的患者进行血管内治疗对改善急性前循环大血管闭塞性脑梗死患者的预后至关重要。本研究旨在探讨影响急性前循环大血管闭塞性脑梗死患者血管内治疗术后90 d预后的独立影响因素,构建评估患者病情及预后的预测模型。
本研究发现,患者血管内治疗术后 90 d不良预后率55.33%,与上述相关研究结果相近,提示前循环大血管闭塞机械取栓不良预后率较高。本研究多因素logistic回归分析结果显示,NIHSS评分、基于DSA的ASITN/SIR侧支循环分级、从发病到股动脉穿刺的时间是血管内治疗术后 90 d预后不良的独立影响因素。NIHSS评分可评估脑卒中神经功能损伤程度,是影响脑卒中预后的一个重要因素[15]。还有研究[16]发现,NIHSS评分是急性前循环大血管闭塞性脑梗死患者血管内治疗预后不良的一个独立危险因素。多项研究均使用NIHSS评分作为卒中预后的预测因子或标准[17]。目前基于 DSA的ASITN/SIR侧支循环分级作为判断的金标准,且具备血管内治疗条件的卒中中心均能在血管内治疗前完成评估。LENG等[21]的系统评价显示好的侧支循环能明显增加血管内治疗患者血管开通率,并且与良好功能预后及较低的症状性颅内出血率、死亡率相关。本研究也发现ASPECTS评分是预后的保护因素(P<0.05)。ASPECTS是评估核心梗死大小的最常用工具,适合各卒中中心,评分越低提示梗死核心或面积越大。研究[18]发现,患者入院前ASPECTS评分低与脑卒中血管内治疗后不良神经功能密切相关,并且还与血管内治疗的死亡率增加有关。ETIS 结果表明ASPECTS 评分≥6 分的患者良好预后率更高,同时也发现 ASPECTS 评分<5分的患者,无论有无再灌注,获得良好预后的比例都很低[19]。另一项研究发现ASPECTS评分>2分的血管内治疗患者即可获得良好的功能预后[20]。以上均提示高ASPECTS 评分是患者血管内治疗术后 90 d预后的保护因素。从发病到股动脉穿刺时间即时间窗,时间窗对于急性前循环大血管闭塞性脑梗死血管内治疗的患者预后至关重要,“时间就是大脑”已经成为共识。2015 年美国缺血性脑卒中指南推荐血管内治疗时间窗规定在6 h以内,时间越短预后越好;研究[21]显示时间窗超过7.3 h取栓获益消失;由于随着发病时间到股动脉穿刺时间的延长,颅内压持续升高,患者卒中造成的脑组织损伤越重,因此预后不佳。
本研究最后将上述4 种指标再次纳入多因素 logistic回归分析并建立预测模型,结果显示,与各单一的指标相比,预测模型评估患者血管内治疗术后 90 d预后的特异度与灵敏度相对较好,且AUC为0.835(95%CI:0.764~0.905),均高于单一指标,取得截断值为0.622,灵敏度为0.904,特异度为0.687;对模型进行验证发现,模型验证准确度为89.86%,该模型具有较好的区分能力,且具有一定的临床实用性,当Logit(P)模型大于0.622时,提示该患者术后 90 d预后不良,应积极采取干预,改善患者预后。但本研究为回顾性单中心研究,样本量较少,代表性可能不足,仍需扩大样本量进一步验证该模型价值。针对临床预后的评估标准,本研究只讨论了以mRS评分为界定标准,后续可以以NIHSS评分、日常生活能力评分表(ADL)评分的变化程度来定义预后情况。
综上所述,NIHSS评分、基于DSA的ASITN/SIR侧支循环分级、从发病到股动脉穿刺的时间是血管内治疗术后 90 d预后不良的独立影响因素,ASPECTS 评分是保护因素;相较于单一指标,基于上述指标所构建的预测预后模型诊断效能更佳。
