超高效液相色谱-串联质谱法同时测定牙膏中三七皂苷和人参皂苷
2023-11-01夏泽敏聂明霞陈彦君梁文耀李鑫宇谭建华席绍峰
税 钿 夏泽敏 聂明霞 廖 娜 陈彦君 梁文耀 李鑫宇 谭建华 席绍峰
(广州质量监督检测研究院,国家化妆品质量监督检验中心(广州),广州 511447)
三七为五加科多年生草本植物,是我国传统名贵中药材,具有活血化瘀,消肿止痛等功效。三七提取物作为中国特色植物原料,被广泛用于功效型牙膏,对口腔溃疡、牙菌斑、牙龈炎和牙龈出血等有显著的疗效[1,2]。但部分产品虚假宣称,实则不含所标示的三七提取物,也达不到所宣称的功效,甚至一些不法厂家通过添加违禁药物来达到所宣称的消肿、抗炎等功效。这些情况不仅影响行业秩序,更严重损害消费者的权益和健康。三七的有效成分为三七总皂苷,其中三七皂苷R1是三七总皂苷的特征化合物,人参皂苷Rb1和人参皂苷Rg1是总皂苷中含量最多的两种成分[3~5]。通过检测三七皂苷几种特征物质的含量可表征是否含有三七提取物,为牙膏功效宣称提供技术支撑。另外考虑到人参提取物液被应用在功效型牙膏中,其特征组分与三七较为相似,主要为人参皂苷Rb1、人参皂苷Rg1和人参皂苷Re[3]。为提高方法的适用范围,本方法拟建立三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1及人参皂苷Re等四种组分的分析方法。
通过国内外相关标准和文献资料检索,近年来在三七和人参提取物有效成分的检测方面,检测方法主要有薄层扫描法[4,6]、高效液相色谱法[7~12]、液相色谱-串联质谱法[13~15]等。而针对牙膏产品,主要有薄层色谱法[4]和高效液相色谱法[7~9]。现有标准中,《功效型牙膏(QB/T 2966-2014)》附录中规定了液相色谱紫外检测法测定牙膏中人参皂苷Rg1、人参皂苷Rb1及三七皂苷R1三种组分的检测方法,但该方法前处理较复杂,耗费时间长;由于几种皂苷均为四环三萜类结构,结构相似,方法的色谱分离时间长,严重影响检测效率;人参皂苷类化合物在紫外区的吸收较弱,容易受到样品基质的干扰。此外,当采用液相色谱法对牙膏中四种皂苷类物质进行测定时,三七皂苷Rg1、人参皂苷Re在色谱柱上分离度差,目前有文献报道使用二维柱切换高效液相色谱法[9]来对四种皂苷进行分析,但三七皂苷Rg1、人参皂苷Re的分离度仍不理想。而且,牙膏中提取物添加量一般比较低,液相色谱法难以满足检测要求。鉴于液相色谱-质谱联用法具有很好的分辨率和灵敏度,本方法拟采用高效液相色谱-串联质谱法测定牙膏中三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1及人参皂苷Re,为广大日化行业的检测机构和企业用户提供一种快捷简便、准确高效的测定方法。
1 实验部分
1.1 仪器与试剂
岛津超高效液相色谱仪-SCIEX AB 5500+三重四极杆质谱仪(美国赛默飞公司);Milli-Q超纯水器(美国Millipore公司);IKA MS3 digital涡旋振荡器(德国IKA公司);SK8200H超声波清洗器(上海科导超声仪器有限公司);BS 224S电子天平(德国赛多利斯公司)。
三七皂苷R1(CAS号80418-24-2)、人参皂苷Rg1(CAS号22427-39-0 )、人参皂苷Rb1(CAS号41753-43-9)及人参皂苷Re(CAS号52286-59-6),纯度均大于98%,美国Stanford Chemicals公司;甲醇,色谱纯,德国Merck公司;乙腈,色谱纯,德国Merck公司;甲酸,分析纯,上海安谱科学仪器有限公司;醋酸铵,分析纯,广州化学试剂厂;石英砂,分析纯,广州化学试剂厂,超纯水,电阻率为18.2 MΩ·cm。
甲醇水溶液(90%,体积分数):准确移取900 mL甲醇置于适量水中,再加水稀释至1000mL,混匀。
醋酸铵水溶液(10mmol/L,含0.1%甲酸):准确称取0.7708 g醋酸铵,于烧杯中用1L纯水溶解,准确量取1mL甲酸至烧杯中,混匀。
1.2 标准溶液的配制
分别准确称取三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1及人参皂苷Re的标准品10mg (精确至0.1mg)于10mL容量瓶中,用甲醇定容至刻度,配制成质量浓度约为1000mg/L的标准储备液。使用时,稀释至所需要的质量浓度的标准工作溶液。
1.3 样品处理
将牙膏试样挤出约20mm后,准确称取试样0.5g(精确到0.001g)于10mL具塞比色管中,加入约0.5g石英砂,混匀,再准确加入90%甲醇水10mL,涡旋混匀后超声提取20min,放置冷却后经0.22μm滤膜过滤后待测。
1.4 仪器条件
色谱条件:色谱柱:Phenomenex Kintext C18(3×100mm,2.6μm);流动相:A:10mmol/L醋酸铵水溶液(含0.1%甲酸),B:乙腈;梯度洗脱程序(0~3min,80% A;3~8min,80%~30% A;8~8.1min,30%~10% A;8.1~11min,10% A;11~11.1min,10%~80% A;11.1~14min,80%A);流速:0.3mL/min;柱温:30℃;进样体积:5μL。
质谱条件:离子源为电喷雾离子源,负离子模式;喷雾电压:4500KV;干燥气压力:50psi;气帘气压力:20psi;碰撞气压力:9psi;离子源温度:450℃;扫描模式:多反应监测(MRM)模式(223.0)。四种皂苷的母离子、子离子、碰撞能量见表1。

表1 四种皂苷的质谱参数
2 结果与讨论
2.1 提取方式及溶解的选择
根据三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1、人参皂苷Re的结构以及理化性质,对提取溶剂和提取方法进行考察,筛选合理的提取方法。通过查询资料可知,三七皂苷R1、人参皂苷Rb1、人参皂苷Rg1、人参皂苷Re的Log p值在2.5~4之间,具有一定的脂溶性,在有机溶剂中溶解性较好。同时,考虑到牙膏产品在水中分散效果较好,本方法采用有机溶剂-水体系作为提取溶剂。考察了不同比例的甲醇水溶液(50%,70%,90%,100%)对牙膏样品中三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1、人参皂苷Re的提取效果。随着有机相比例增加,样液变澄清,样液变得容易经滤膜过滤,当有机相比例超过90%,样品容易成团,不易分散。对实际样品添加浓度100μg/kg的人参皂苷Re、三七皂苷R1和浓度为200μg/kg的人参皂苷Rb1、人参皂苷Rg1,并对样液进行测定。结果显示,在甲醇水溶剂体系中,不同比例有机溶剂对人参皂苷Re、三七皂苷R1和人参皂苷Rg1的提取率相似,但人参皂苷Rb1的提取率随甲醇比例增加而有所提高。因此选择90%甲醇水作为三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1、人参皂苷Re的提取溶剂。另外,为了提高牙膏在提取溶剂中的分散效果,本方法选择加入适量石英砂对牙膏试样进行辅助分散。
2.2 色谱柱的选择
考察了Waters ACQUITY HSS C18(2.1×100mm,1.8μm)、Waters ACQUITY BEH C18(2.1×100mm,2.7μm)、Agilent Poroshell 120 SB C18(2.1×100mm,2.7μm)、Phenomenex Kintext C18(3×100mm,2.6μm)等不同品牌的C18色谱柱对三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1、人参皂苷Re等四种组分和样品基质的分离效果。结果显示,在优化的流动相条件下,各C18色谱柱上四种组分的峰型都尖锐对称,虽然四种组分保留时间比较接近,但不影响质谱分析结果,且C18色谱柱通用性好。综合考虑,本方法采用C18色谱柱作为分离色谱柱。
2.3 流动相的选择
比较了甲醇-0.1%甲酸水、乙腈-0.1%甲酸水、乙腈-0.2%甲酸水和乙腈-10mM醋酸铵水溶液(0.1%甲酸)几种流动相体系对目标物保留时间和峰型的影响。结果表明当乙腈作为有机相时,化合物峰型更对称,且随着甲酸浓度增加,化合物响应有所增强,在乙腈-10mM醋酸铵水溶液(0.1%甲酸)作为流动相时,醋酸铵大大提高了化合物离子化效率,四种皂苷的响应最高。比较5、10、15、20mM的添加0.1%甲酸的醋酸铵溶液作为水相的分析结果发现,随着醋酸铵浓度的增加,四种化合物的响应都增加,增加到10mM后,信号增加不明显,且盐浓度过高可能会析出后磨损液相柱塞杆或在质谱离子源口结晶。因此,选用乙腈-10mM醋酸铵水溶液(0.1%甲酸)作为流动相。

图1 四种皂苷混合标准溶液的总离子色谱图(50ng/mL)
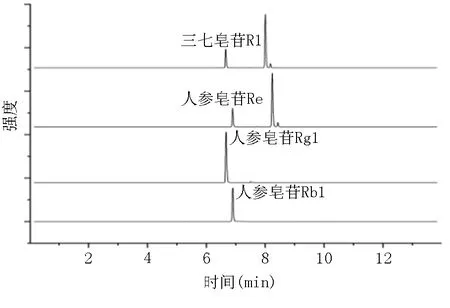
图2 阳性样品总离子色谱图
2.4 质谱参数的选择
比较了正负两种电离模式下四种皂苷的响应强度。在正离子模式下,出现[M+H]+、[M+Na]+、[M+NH4]+准分子离子峰,负离子模式下有[M-H]-、[M+CH3COO-]-准分子离子峰。当选择[M+CH3COO-]-峰作为母离子时,化合物信号响应强度最高。
四种皂苷的分子结构都含相同的皂苷苷元和不同的糖基,通过对[M+CH3COO-]-峰产生的离子碎片进行分析发现,在质谱裂解过程中有相似的规律。通过调节碰撞能,四种准分子离子首先断裂失去甲酸根,形成[M-H]-的子离子,人参皂苷Rb1和人参皂苷Rg1再进一步失去1个葡萄糖基,分别形成m/z为945.5和637.5的特征离子;人参皂苷Re失去一个葡萄糖基和鼠李糖基,形成m/z为637.5的特征离子;三七皂苷R1则失去一个葡萄糖基和阿拉伯糖基形成m/z也为637.7的特征离子。从而确定4种皂苷的质谱参数(见表1)。
2.5 离子源温度的选择
比较450℃、500℃、550℃、600℃ 4个离子源温度对皂苷信号响应强度的影响。实验结果显示,随着温度升高,四种化合物的响应均成下降趋势,当温度超过500℃时,响应下降更为明显。离子源温度过低,会降低气化和雾化效率,因此,本方法选择450℃作为离子源温度。
2.6 线性方程和检出限
在1.4仪器条件下对系列标准工作溶液进行测定。以各目标物质量浓度(x)为横坐标,对应峰面积(y)为纵坐标,分别绘制标准工作曲线。对阴性样品添加适量4种皂苷混合标准溶液,按照试样前处理方法和仪器条件进行测定,以信噪比S/N≥3确定方法检出限,以信噪比S/N≥10确定方法定量限。线性范围、线性方程、相关系数、检出限和定量限见表2。

表2 四种目标物的线性方程、线性范围、相关系数、方法检出限和定量限
由表2可知,人参皂苷Rb1、人参皂苷Rg1、人参皂苷Re和三七皂苷R1的质量浓度在各自范围内与相应色谱峰面积呈良好的线性关系,人参皂苷Rb1和人参皂苷Rg1的方法检出限为0.04μg/g,方法定量限为0.10μg/g;人参皂苷Re和三七皂苷R1的方法检出限为0.02μg/g,方法定量限为0.05μg/g。
2.7 精密度试验及加标回收试验
选用二氧化硅基质、碳酸钙基质和磷酸氢钙基质3种空白牙膏样品为加标基质,按1.3方法进行处理,分别加入低、中、高3个加标水平的皂苷标准溶液(其中人参皂苷Rb1和人参皂苷Rg1添加0.1μg/g、10μg/g、100μg/g三个浓度水平,人参皂苷Re和三七皂苷R1添加0.05μg/g、10μg/g、100μg/g三个浓度水平),在1.4仪器条件下平行测定6次,测定结果见表3。由表3可知,三七皂苷R1的平均回收率在90.0%~102.1%之间,相对标准偏差(RSD,n=6)在1.42%~5.84%之间;人参皂苷Rg1的平均回收率在92.0%~102.0%,相对标准偏差(RSD,n=6)在1.69%~5.61%之间;人参皂苷Rb1的平均回收率在90.3%~97.7%之间,相对标准偏差(RSD,n=6)在2.26%~5.10%之间;人参皂苷Re的平均回收率在89.0%~101.7%之间,相对标准偏差(RSD,n=6)在1.90%~5.87%之间。结果表明,本方法具有良好的准确度和精密度,满足分析要求。
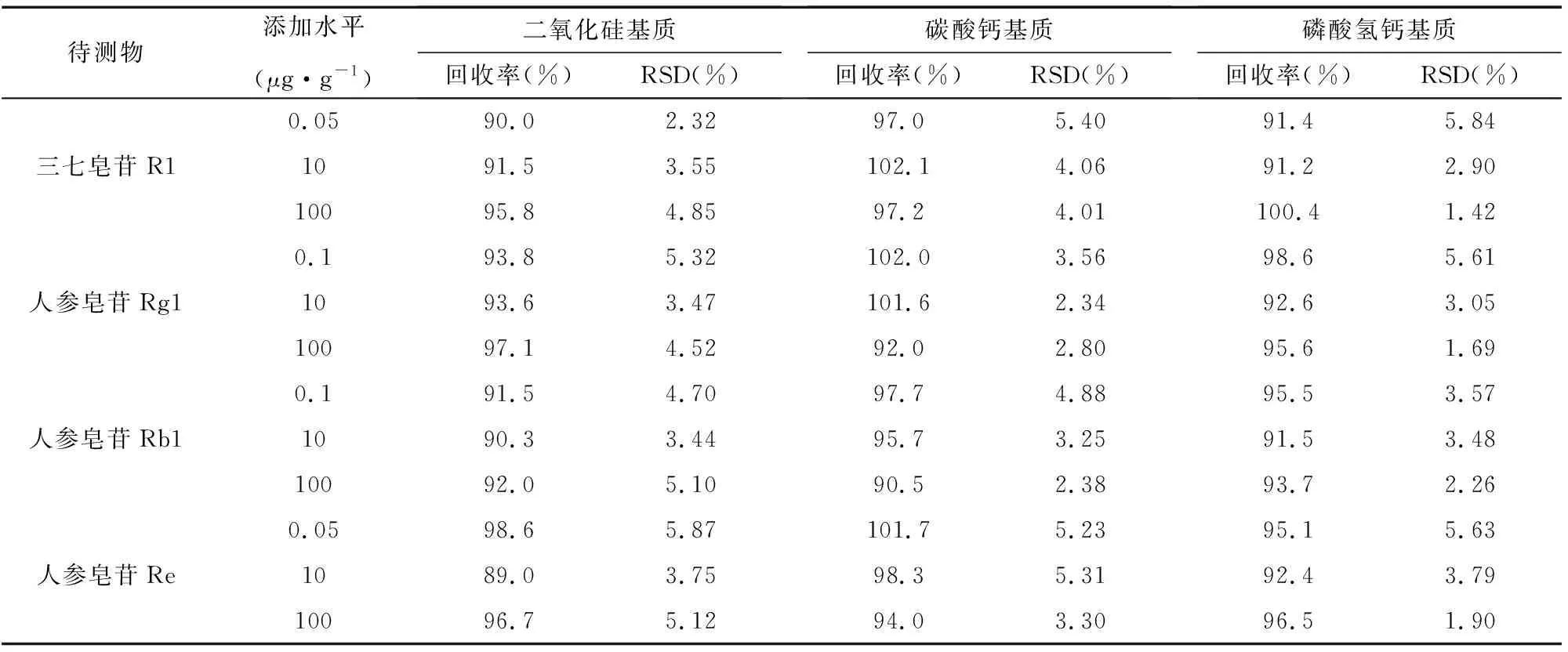
表3 精密度试验和加标回收试验结果
2.8 实际样品的分析
采用本方法对市售的40批次牙膏样品(其中16批次二氧化硅基质牙膏,13批次碳酸钙基质牙膏,11批次磷酸氢钙基质牙膏)进行四种皂苷的测定。结果显示,有4支牙膏4种皂苷均有检出,另外有1支牙膏检出人参皂苷Rb1和人参皂苷Rg1。人参皂苷Rb1的检出量为0.24~318.74μg/g,人参皂苷Rg1添加量为0.18~698.92μg/g,人参皂苷Re添加量为0.71~50.89μg/g,三七皂苷R1添加量为0.05~92.11μg/g。所有阳性样品在成分表中均标示添加了三七提取物或者粉末,但同时存在有产品标示添加了三七提取物但未检出相关成分的情况。
3 结论
本研究采用高效液相色谱-串联质谱技术建立了牙膏中三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1及人参皂苷Re的检测方法。对提取条件、色谱条件和质谱条件等进行了优化,并将该方法应用于不同基质牙膏的检测。结果表明,该方法能对三七皂苷R1、人参皂苷Rg1、人参皂苷Rb1及人参皂苷Re进行准确测定,且方法精密度好,满足相关检测需求,可为牙膏产品的质量监控提供有力的技术支撑。
