CO与H2气氛下赤铁矿还原动力学及矿相转化机理研究
2023-10-19李新玉王若枫张洪浩李艳军
李新玉 袁 帅,3 高 鹏 王若枫 张洪浩 李艳军
(1.东北大学资源与土木工程学院,辽宁 沈阳 110819;2.难采选铁矿资源高效开发利用技术国家地方联合工程研究中心,辽宁 沈阳 110819;3.矿物加工科学与技术国家重点实验室,北京 100192)
近年来,国民经济的持续快速发展促进了我国钢铁行业的迅猛发展,并由此带动了我国对铁矿石的需求量大幅增加[1]。从我国铁矿资源的利用情况来看,优质铁矿资源正面临日益短缺的局面,而占铁矿石资源总量18%以上的赤铁矿资源由于禀赋差,利用难度比较大[2]。研究表明[3-5],矿相转化是难选赤铁矿资源高效利用的有效手段之一。
许多学者对赤铁矿矿相转化工艺和机制进行了研究[6-9],谢朝明[10]对高磷鲕状赤铁矿进行热力学分析,结果表明,在固定碳氧化还原体系,当反应温度T<646.85 ℃,赤铁矿还原后产物主要为Fe3O4;当反应温度T处于646.85~694.85 ℃,还原产物主要为FeO;当反应温度T>694.85 ℃且CO 浓度>59.1%时,铁氧化物可以完全转变成金属铁。由此可知,赤铁矿的矿相转化过程是一个多步反应。由于试验采用的原矿来源、矿相转化设备、试验方法的不同,得到的反应活化能也相差很大。韩文杰等[11]针对海南石碌铁矿在氢气气氛下进行了还原动力学研究,得到反应活化能为75.99 kJ/mol。CHEN 等[12]对氢气气氛下赤铁矿还原为多孔磁铁矿过程进行探究,得到反应平均活化能为79.1~86.1 kJ/mol。除此之外,许多研究人员对赤铁矿转化为磁铁矿的成核机理以及新生磁铁矿的形貌进行了研究。余建文等[13]对赤铁矿还原过程中磁铁矿的形成及生长规律进行探究,研究表明磁铁矿的生长分为诱导期和生长期两个时期,且矿相转化温度和时间对磁铁矿生成过程影响显著。
不同气氛对于铁矿物还原效果有着显著的影响,目前气体还原铁氧化物的研究主要集中在焙烧过程的影响因素研究、热力学研究以及焙烧产品的特性分析,但缺少对还原过程系统的动力学分析及不同气氛的动力学对比研究。通过动力学分析可明确矿相转化过程不同阶段控制因素及确定最概然机理函数。因此,本文从动力学角度,对CO 和H2气氛下铁矿物不同还原效果进行了对比,以赤铁矿纯矿物为研究对象,开展CO 和H2的矿相转化过程等温动力学研究,计算反应动力学参数并确定最概然机理函数,对比不同气氛反应过程中矿相转化产品的微观形貌演化规律,为赤铁矿在H2和CO 气氛下矿相转化过程的调控提供理论支撑。
1 试验原料及方法
1.1 试验原料
经破碎、磨矿、摇床后获得满足试验要求的高品位赤铁矿纯矿物,其粒度分析、化学成分分析及矿物组成分析结果分别见图1、表1 及图2所示。

图1 赤铁矿样品的激光粒度分析结果Fig.1 Laser particle size analysis results of hematite sample

图2 赤铁矿样品的XRD 图谱Fig.2 XRD pattern of hematite sample
由图1、表1 及图2 可知:试验样品主要由赤铁矿和石英组成,颗粒粒度以100 μm 为主;样品中TFe品位为67.40%,FeO 含量为0.35%,赤铁矿纯度达96.29%;主要杂质成分为SiO2和Al2O3,有害元素P和S 的含量较低。
1.2 试验方法
试验主要通过测算矿相转化产品中FeO 含量随时间变化来推算矿相转化过程的还原度,对CO 和H2气氛下赤铁矿反应过程进行动力学试验研究,计算动力学反应参数并确定最概然机理函数。
图3 为本研究所用矿相转化系统示意,试验装置由卧式炉、控制系统和供气系统三部分构成。试验所用矿相转化气体为CO 和H2,保护性气体为N2,纯度均为99.99%。试验过程为:在室温下称取20 g 赤铁矿样品,放入卧式管式炉中,先以500 mL/min 的气体流量通入5 min 氮气,排净石英管内的空气,待管式炉以15 ℃/min 的升温速率升高到指定温度(460、500、540、580 和620 ℃)后,按照矿相转化气体体积浓度为30%的比例,分别通入指定的CO/H2,始终保持气体总流量为500 mL/min,开始计时。达到预定矿相转化时间后关闭CO/H2气体通道,继续通入5 min 氮气排净CO/H2。最后将矿相转化样品冷却至室温,制样以便于分析检测,并用化学滴定法测定其FeO 含量。

图3 矿相转化系统示意Fig.3 Diagram of mineral phase transformation system
对于总质量为20.0 g 的纯赤铁矿样品,其纯度为96.29%,则赤铁矿的质量为19.26 g,杂质石英等的质量为0.74 g。随着反应的进行,根据质量守恒定律,得到转化率的计算公式如下:
式中,α为反应进行的程度,即Fe2O3的转化率;wFeO为FeO 含量,%。
对反应转化率α与矿相转化时间t的拟合曲线进行求导,从而获得反应速率v。等温条件下,均相或非均相化学反应的动力学方程可以用式(2)表示:
式中,v为反应速率,min-1;f(α)为反应机理函数;k(T)为反应速率常数;T为热力学温度,K。通过对式(2)排列积分可得:
式中,G(α)是f(α)的积分形式。由式(3)可知,G(α)与矿相转化时间t是线性关系,线性相关度最高的G(α)对应的f(α)即为最佳机理函数,反应速率常数k(T)即为最佳机理函数对应的回归直线方程斜率。反应速率常数与指前因子和活化能之间的关系可以通过如式(4)所示的阿伦尼乌斯方程表示。
通过变换可得出k(T)的表达式:
式中,A为指前因子,min-1;E为反应的表观活化能,J/mol;R为理想气体常数,8.314 J·mol-1·K。
2 试验结果与讨论
2.1 转化率和反应速率
CO 和H2气氛下,在温度为460、500、540、580 和620 ℃下分别开展动力学试验,结合wFeO和式(1)可得不同温度下转化率曲线,结果如图4所示。

图4 不同矿相转化温度下的转化率曲线Fig.4 Curves of conversion rate at different mineral phase transformation temperatures
由图4 可知,在CO 和H2气氛下,赤铁矿反应过程有着相似的趋势。同一矿相转化温度条件下,随着反应时间的延长,转化率逐渐增大。矿相转化前期,转化率随时间迅速增加,反应后期,转化率增长逐渐趋于平缓,且矿相转化温度越高,转化率趋近于1 所需时间越短。在矿相转化温度为620 ℃时,CO 气氛下20 min 反应完全,而H2气氛下14 min 即反应完全,说明相比于CO 气氛,赤铁矿在H2气氛中完全转化所需时间更短。
通过对转化率曲线求导,得到不同温度下反应速率曲线,如图5所示。

图5 不同矿相转化温度下的反应速率曲线Fig.5 Curves of reaction rates at different mineral phase transformation temperatures
由图5 可知,当矿相转化温度相同时,反应速率随着矿相转化时间的增加而迅速增加,在达到反应速率的峰值后逐渐降低。在CO 气氛下,温度为460 ℃时,反应速率在5 min 达到峰值0.052 8 min-1,温度为620 ℃时,反应速率在2 min 达到峰值0.082 7 min-1;而在H2气氛下,温度为460 ℃时,反应速率在8 min 达到峰值0.046 5 min-1,温度为620 ℃时,反应速率在3 min 达到峰值0.115 8 min-1。这表明提高矿相转化温度可以缩短反应速率达到峰值的时间,同时可以提高反应速率的峰值,且H2气氛的矿相转化效果要优于CO 气氛的矿相转化效果。结果表明,在一定温度范围内提高温度,可以提高赤铁矿矿相转化的反应速率,缩短反应时间。
2.2 动力学模型的确定
迄今为止,众多学者建立了许多不同的机理函数用于描述化学反应,可概括为随机成核模型、收缩核模型、扩散模型、幂函数法则和化学反应控制模型五大类。采用积分法将赤铁矿矿相转化动力学数据进行线性回归分析,得到CO、H2气氛中不同矿相转化温度下拟合效果均较好的最概然机理函数分别为收缩核模型R2和R3,其积分形式分别为G(α)=1-(1-α)1/2、G(α)=1-(1-α)1/3。将不同试验条件下的转化率分别代入收缩核模型R2、R3机理函数的积分形式G(α),然后对矿相转化时间t进行线性回归分析,结果如图6所示,各回归曲线的斜率即为不同温度下的反应速率常数K(T),如表2 和表3所示。

表2 CO 气氛下的机理函数和反应速率常数Table 2 Mechanism functions and reaction rate constants in CO atmosphere

表3 H2 气氛下的机理函数和反应速率常数Table 3 Mechanism functions and reaction rate constants in H2 atmosphere
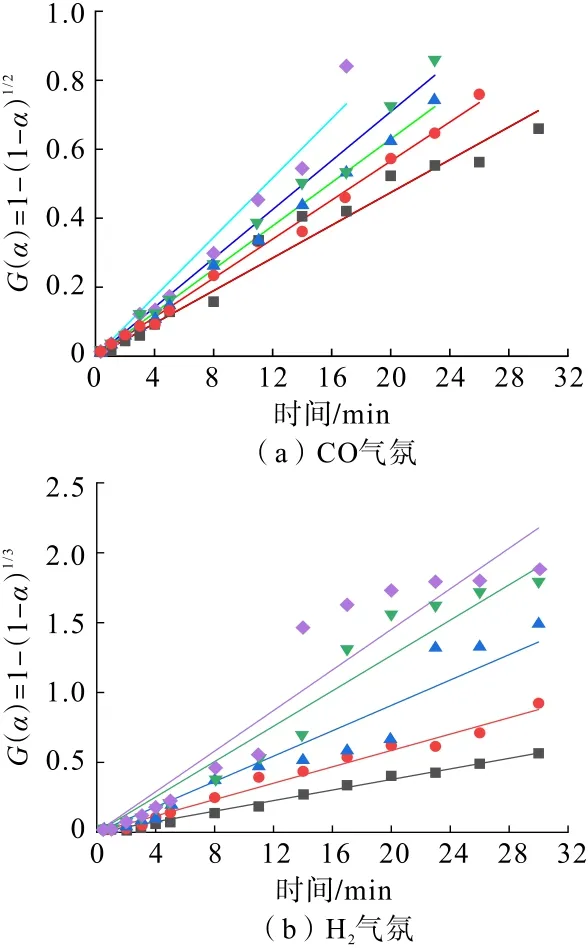
图6 G(α)随时间变化的线性回归曲线Fig.6 Linear fitting of G(α)versus time
将不同试验条件下的反应速率常数k代入式(4),并对函数lnk和1/T进行回归计算和线性拟合,结果如图7所示。

图7 lnk 和1/T 的线性拟合结果Fig.7 Linear fitting results of lnk versus 1/T
由图7 可知,lnk与1/T两者之间具有良好的线性相关性,在CO 和H2气氛下,相关系数分别高达0.977 1、0.989 3。根据回归直线的斜率和截距计算可得,CO 气氛下,赤铁矿矿相转化反应的活化能E为8.35 kJ/mol,指前因子A为0.21 min-1;H2气氛下,赤铁矿矿相转化反应的活化能E为20.73 kJ/mol,指前因子A为4.37 min-1。
2.3 矿物物相转化分析
采用X 射线衍射仪,在反应温度540 ℃的条件下考察反应时间对CO 和H2矿相转化产物的影响规律,结果如图8所示。
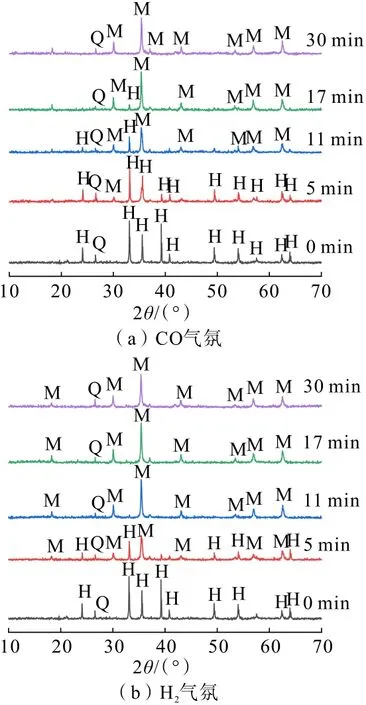
图8 不同反应时间下矿相转化产品的XRD 图谱Fig.8 XRD patterns of product at different reaction time in mineral phase transformation
由图8 可知,540 ℃时,在CO 气氛下,随着矿相转化时间的延长,赤铁矿的衍射峰逐渐减弱,磁铁矿的衍射峰逐渐增强,直至17 min 以后,赤铁矿的衍射峰完全消失,30 min 时,只有石英和磁铁矿的衍射峰,说明赤铁矿已经基本转化为磁铁矿;在H2气氛下,赤铁矿与H2反应生成磁铁矿,矿相转化时间为11 min 时,赤铁矿的衍射峰就已经完全消失了,样品中仅剩下磁铁矿和石英的衍射峰,且无过还原产物(FeO)衍射峰的出现,说明赤铁矿已经基本转化为磁铁矿。相比于CO,H2气氛下赤铁矿矿相转化所需要的时间更短,效果更好。
2.4 微观结构演变规律分析
为了进一步探究赤铁矿在矿相转化过程中微观结构的变化,通过SEM 对矿相转化温度为540 ℃、CO/H2气体体积浓度均为30%的矿相转化产物进行微观形貌分析,结果如图9~图12所示。

图9 矿相转化前样品的SEM 图Fig.9 SEM image of the sample before mineral phase transformation

图10 8 min 时矿相转化产物微观形貌变化Fig.10 Microscopic morphological changes of mineral phase transformation products at 8 min
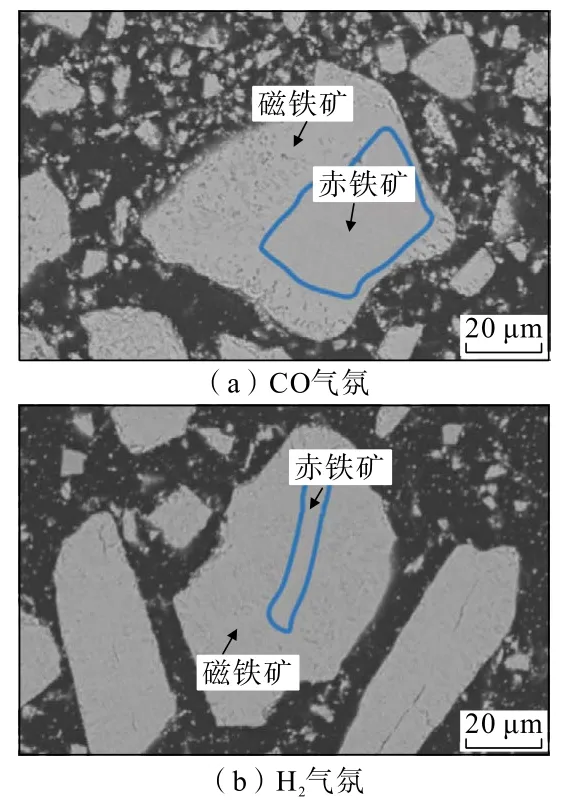
图11 14 min 时矿相转化产物微观形貌变化Fig.11 Microscopic morphological changes of mineral phase transformation products at 14 min

图12 30 min 时矿相转化产物微观形貌变化Fig.12 Microscopic morphological changes of mineral phase transformation products at 30 min
分析可知,在反应开始之前,赤铁矿样品的表面比较致密和光滑,颗粒比较完整,没有明显裂纹,反应开始之后,矿相转化的产物形貌差异明显。反应初期,磁铁矿优先在赤铁矿颗粒边缘处生成,颗粒边缘变得疏松多孔。新生磁铁矿结构疏松多孔,在颗粒边缘生成的裂纹有利于气体进入颗粒内部进一步发生反应,将赤铁矿转化为磁铁矿。随着反应的进行,赤铁矿内核逐渐缩小,磁铁矿外壳不断变厚,直至最终完全转变为磁铁矿。跟CO 气氛下的颗粒相比,相同矿相转化时间下,H2气氛下赤铁矿矿相转化过程中磁铁矿外壳更厚,反应速率更快,矿相转化程度更高,同时也佐证了前述H2气氛比CO 气氛矿相转化效果更好的结论。
3 结论
(1)在CO、H2气氛中,不同矿相转化温度下赤铁矿转化率随时间呈现出相同的变化趋势,即转化率先迅速增加后趋于稳定;同一时间内转化率α随温度升高而增加,说明升温有助于缩短化学反应完全所需时间。同时,与CO 相比,H2矿相转化的效率更高,效果更好。
(2)赤铁矿矿相转化过程中,在CO 气氛下,反应动力学的最佳机理函数为收缩核模型,积分形式为G(α)=1-(1-α)1/2,反应活化能E为8.35 kJ/mol,指前因子A为0.21 min-1;在H2气氛下,反应动力学的最佳机理函数为收缩核模型,积分形式为G(α)=1-(1- α)1/3,反应活化能E为20.73 kJ/mol,指前因子A为4.37 min-1。
(3)赤铁矿的矿相转化过程是由外向内进行的,赤铁矿原矿结构致密无裂纹,随着矿相转化时间的延长,赤铁矿不断转化成磁铁矿,颗粒外部逐渐变得疏松多孔,气体沿着裂纹进入颗粒内部,增大了气体与颗粒的接触面积,从而提高赤铁矿的转化效率。
