制药企业压缩空气系统及压缩空气质量控制方法的探讨
2023-10-14许建明麦志雄梁云飞
许建明 麦志雄 梁云飞
制药企业压缩空气系统及压缩空气质量控制方法的探讨
许建明1麦志雄2梁云飞2
(1.广西梧州中恒集团股份有限公司,广西 梧州 543000;2.广西梧州制药(集团)股份有限公司,广西 梧州 543000)
文章简要阐述了压缩空气的定义以及特点,详细介绍了制药企业压缩空气系统的质量要求、系统构成以及运行原理。在药品的生产当中,由于压缩空气会与药品直接或间接接触,与药品直接接触的压缩空气的品质则直接影响了产品质量的好坏,因此文章对《药品生产质量管理规范》(GMP)要求下的制药企业压缩空气质量控制方法进行了进一步的探讨,并对其包括含油量、露点、悬浮粒子和浮游菌等方面的质量控制方法进行了实施,确保经过严格净化措施后出来的压缩空气质量得到可靠的保证,证明压缩空气质量符合GMP要求。
压缩空气系统;质量控制方法;GMP
引言
压缩空气是一种动力源,被广泛应用于工业活动中。在制药企业,压缩空气特指进入洁净室或者与清洁的产品容器或物料相互接触的空气,主要用于灌装机、蒸汽灭菌设备、洗瓶机、制粒机和包装机等,可为相关设备提供动力源,或用于日常的干燥、吹扫、自动控制和物流运输等。由于在药品的生产过程中,特别是无菌产品的生产,压缩空气直接或间接与产品进行接触,有可能影响到产品的质量,所以为了保证压缩空气的质量,必须对压缩空气系统采取严格的净化控制措施和进行检测项目的控制。对压缩空气系统所产生的压缩空气进行质量控制,用以证明系统符合《药品生产质量管理规范》(GMP)和生产工艺要求,使制药企业生产出质量合格的产品。
1 制药企业用压缩空气系统
制药企业用压缩空气系统是生产压缩空气主要设备的统称,生产出的压缩空气按用途可以分为工艺用气和仪表用气两类,工艺用气一般会与工艺产品有接触,有可能会影响到产品的质量,属于直接影响系统,需要重点关注,而仪表用气主要是给设备提供动力,属于间接影响系统[1]。
1.1 压缩空气定义及特点
压缩空气,即空气经过机械压缩后形成的气体,由于空气被压缩,体积变小,使得其内部压强增大。当外部的机械外力撤销后,压缩空气恢复到原来的体积,对外就会产生强大的压力能。
压缩空气具有以下特点:(1)压缩空气是一种透明气体,无有害性能,无起火危险,输送方便;(2)是仅次于电力以外的第二大动力能源,是具有多重用途的工艺气源,可应用于化工、医药、汽车制造、轻工、机械等部门行业;(3)可进行仪表、阀门的控制,还用于加工中心、机床、列车制动阀的控制;(4)可用于金属表面喷砂、喷漆等。
1.2 制药用压缩空气质量要求
根据GMP的要求,制药企业所用的压缩空气系统应采用无油无水压缩空气系统,压缩空气经过无油空气压缩机压缩后,经冷凝器冷却、分子筛除水、管道过滤器过滤掉尘埃粒子后,就可以得到干燥、洁净的压缩空气。
而与药物直接接触的压缩空气,则应设置净化装置,干燥设备的出风口应该有放置空气倒灌的装置,经过净化处理的空气应该符合规定的空气洁净度要求。制药企业生产的压缩空气根据产品质量和工艺的要求,可以参考ISO 8573的相关要求进行质量控制,如压缩空气的露点应≤-20℃,含油量应≤0.01 mg/m3,悬浮粒子应符合相应级别洁净区尘埃粒子相关规定,压缩空气的微生物也应该符合药品生产工艺的要求。
另外,无菌生产工艺使用的压缩空气,需要在使用点经过0.22 μm孔径的终端气体过滤器过滤掉可能存在的微生物和微粒,气体过滤器为疏水性过滤器,可方便用纯蒸汽进行在线蒸汽灭菌。而最终灭菌产品使用的压缩空气,则建议经过除菌过滤器后再使用,由于风险较低,可六个月到一年更换一次过滤器,也不必对过滤器进行灭菌。
1.3 制药用压缩空气系统运行流程及结构
制药用压缩空气系统通常由无油空气压缩机、储气罐、油水分离器、干燥机和过滤器组成[2],其流程如图1所示。

图1 压缩空气系统运行流程图
1.3.1 无油空气压缩机
无油空气压缩机是产生压缩空气的主要设备,其工作循环可以分为吸气、压缩和排气三个过程,随着螺旋形转子的旋转,每对相互啮合的齿相继完成相同的工作循环,被密封在齿间容积中的气体随着齿移动所占据的体积也随之减少,导致压力升高,从而实现气体的压缩过程,当齿间容积与排气孔口连通后,即开始排气过程。
1.3.2 储气罐
压缩空气储气罐的作用是用来储存压缩空气,也起到减少流脉动的作用。当压缩空气气体瞬时消耗之后,可以从罐体内进行补偿,从而避免压缩空气的频繁波动,此外,罐体还具有排水和排污的作用。
1.3.3 油水分离器
油水分离器的作用是分离压缩空气中的水分和油,一般由外壳、分离器、滤芯和排污部件组成,当含有大量油和水固体杂质的压缩空气进入分离器后,沿其内壁旋而下,所产生的离心作用,使油水从汽流中析出并沿壁向下流到油水分离器底部,然后再由滤芯进行精过滤。
1.3.4 冷冻式干燥机
冷冻式压缩空气干燥机的原理是利用冷却后的空气,降低空气温度,将湿空气中的水分通过冷凝后从空气中析出,从而得到较干燥的空气。
压缩空气首先进入冷冻式干燥机的预冷器,与来自吸干机的干燥压缩空气进行热交换,使干燥压缩空气温度升高,同时降低了进入蒸发器的压缩空气温度,除去一部分水分,使其降至常温。此后,压缩空气再进入蒸发器进行热交换,使压缩空气冷却至10℃左右,此时,压缩空气中的大部分水分及部分杂质被凝结,水分经自动排水器排除,干燥后的压缩空气就会进入吸干机,进一步除去水分,使露点温度符合要求。
1.3.5 过滤器
压缩空气过滤器是结合除油、除臭、除尘为一体的精密过滤器,用于冷冻式干燥机之后,可以确保空气中不含油分。
1.4 压缩空气污染物及来源
压缩空气并不是一种没有问题的动力源,压缩空气的污染,会导致实际生产过程中产生各种各样的问题。一般来说,压缩空气系统主要有十种污染物,分别为水蒸气、微生物、尘埃、油蒸汽、水雾、凝结水、液态油、油雾、铁锈和管道剥落物。而这十种污染物,通常来自大气、空气压缩机、储气罐和管路。
2 压缩空气质量控制方法
由于制药企业生产的药品会直接或间接地接触压缩空气,因此需要采取相应的措施除去压缩空气附带的污染物,并通过相应的质量控制方法对压缩空气系统产出的压缩空气进行检测,从而判定压缩空气是否符合相关质量要求。对于非直接接触药物的压缩空气,一般只进行压力测量,对于直接接触药物的压缩空气,还需要对其进行含油量、露点、悬浮粒子和微生物等方面的测试[3]。以下将对这几个质量控制方法进行探讨。
2.1 检测仪器与材料
德尔格压缩空气检测仪、LighthouseAC100H浮游菌检测仪、浮游菌采样仪、胰酪大豆胨琼脂培养基、90 mm玻璃培养皿、恒温培养箱。
2.2 质量控制方法
2.2.1 含油量测试
由于制药企业用压缩空气有可能会直接或间接与药物接触,基于GMP中需要有效防止污染和交叉污染的重要规定,特别是无菌制剂车间,防止压缩空气中的油污染到生产过程中的药品,就尤为重要。所以对压缩空气的含油量进行检测,可以对压缩空气质量进行控制,也确保了药品生产的质量。
常规含油量的测试通常采用显色反应的方法,其原理为一定量的空气通过吸附了浓硫酸的载体后,油份和浓硫酸反应后会显黑色。
在药品生产中,可选取药液浓配和稀配中的液体压送、洗瓶机吹瓶、物料的密闭输送这三个有可能直接或间接与药物进行接触的使用点进行检测,测试步骤如下:
(1)把油检测盒安装在适配器上,将适配器插入检测仪;
(2)打开使用点的压缩空气进行检测,锁定4 L/min的空气流量,用计时器进行计时,测量5 min,测试完成后,取出油检测盒;
(3)撕开检测盒保护膜,观察检测盒油斑,并与对照油斑进行比较,一般该测试连续进行三次。
2.2.1.1 判定标准
压缩空气的含油量应不大于0.1 mg/m³。
2.2.1.2 测试结果
实验人员根据操作步骤对浓配、稀配、吹瓶、物料输送这四个使用点各进行了三次含油量测试,其含油量均比0.1 mg/m³的对照小,说明压缩空气系统经过除油措施后,能够产出洁净的压缩空气,也证明了通过该质量控制的手段,能够定性地检测出压缩空气中油分,防止含油压缩空气与药物接触,污染药品而滋生细菌。
2.2.2 露点测试
压缩空气露点的检测,实质是空气中含水量的检测,露点的标准取决于药品对水分的敏感程度、空气与产品接触的量。对于以水为主要溶剂的注射液而言,空气中含水量多少对产品本身没有什么风险,但考虑到水分对气体传输管道的腐蚀性,还有含水会加速细菌的生长繁殖速度,以及让某些药品吸潮变质,对压缩空气进行露点的质量控制,就尤为重要了。露点与水分含量的关系见表1。

表1 露点与水分含量对照表
采用德尔格压缩空气质量检测仪,对压缩空气进行露点检测,测试步骤如下:(1)把水分检测管安装在适配器上,将适配器插入检测仪;(2)打开使用点的压缩空气进行检测,锁定4 L/min的空气流量,用计时器进行计时,测量5 min,测试完成后,取出水分检测管,并读取水分含量数据。
2.2.2.1 判定标准
水分含量应小于1.07 g/m³,即露点温度应小于-20℃。
2.2.2.2 测试结果
实验人员根据操作步骤对浓配、稀配、吹瓶、物料输送这四个压缩空气使用点各进行了三次水分测试,其露点均小于-20℃,符合医药行业压缩空气相关要求,防止压缩空气中的水分在生产过程带来微生物,影响药品的质量。
2.2.3 浮游菌测试
浮游菌测试也是压缩空气质量控制中一项重要测试项目,通过测试,可以考察压缩空气细菌污染情况,其测试步骤如下:(1)将各用气点的压缩空气出口分别连接至减压阀(减压阀设定压力为0.1 MPa),并将减压阀与不锈钢装置连接;(2)排放压缩空气5 min,然后将不锈钢装置整体罩住浮游菌采样仪;(3)开启浮游菌采样仪,采样量为1 m³,高流速气流撞击在培养皿表面,采样结束后,将采集的培养皿置于恒温培养箱培养72 h,并观察结果。
2.2.3.1 判定标准
一般应根据产品风险来确定压缩空气的微生物限度,压缩空气浮游菌测试的判定标准,可以参考GMP附录里无菌药品浮游菌的标准,详见表2。

表2 压缩空气浮游菌测试标准
2.2.3.2 测试结果
压缩空气浮游菌测试结果如表3所示。

表3 压缩空气浮游菌测试结果
由表3检测结果可以看出,压缩空气所在区域浮游菌的测试结果均为小于1 cfu/m³,说明经过压缩空气净化系统过滤后出来的压缩空气,能够完全符合医药行业微生物要求,甚至能够达到A级洁净区浮游菌的标准,把控制浮游菌作为测试压缩空气的质量控制方法,可以监测压缩空气微生物水平,降低药品生产过程中受到污染的风险。
2.2.4 悬浮粒子测试
悬浮粒子来自于交通运输、工业活动、建筑工地和森林燃烧等众多污染源,是指不超过10微米的颗粒物,包括释放的烟尘、车尘、化学颗粒、有机和无机的有害物质等。由于压缩空气由气体压缩而成,所以对悬浮粒子进行控制就很有必要,对压缩空气的悬浮粒子进行检测,可以依照以下步骤进行:(1)将各用气点的压缩空气出口分别连接至减压阀(减压阀设定压力为0.1 MPa);(2)排放压缩空气5 min,然后将减压阀与悬浮粒子采样仪连接;(3)开启悬浮粒子采样仪,采样时间为10 min,采样结束后记录结果。
2.2.4.1 判定标准
压缩空气悬浮粒子测试的判定标准,可以参考GMP附录里无菌药品悬浮粒子静态的标准,详见表4。

表4 压缩空气悬浮粒子测试标准
2.2.4.2 测试结果
压缩空气悬浮粒子测试结果如表5所示。
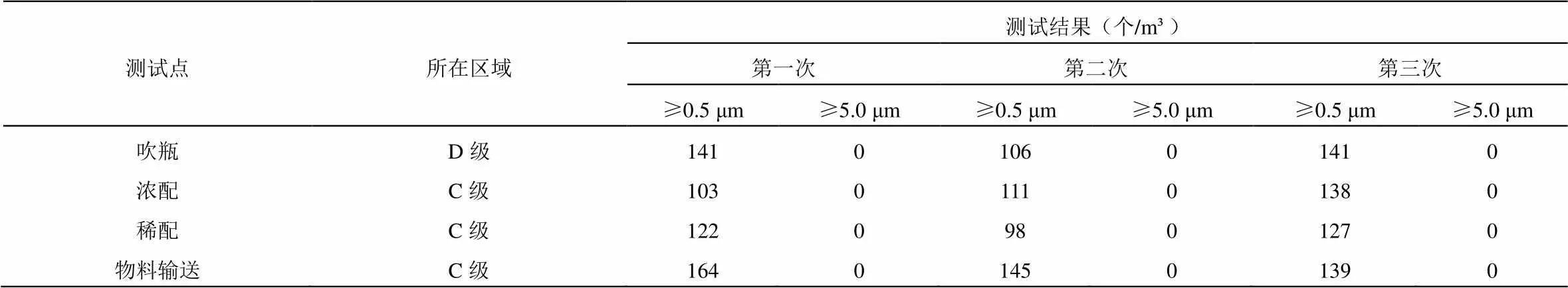
表5 压缩空气悬浮粒子测试结果
由表5的压缩空气悬浮粒子检测数据可以看出,压缩空气所在区域测试点的悬浮粒子测试结果均符合相应级别的要求,甚至能达到A级洁净区级别悬浮粒子的要求,该质量控制方法能有效监测压缩空气系统性能,保障药品生产质量安全。
3 结束语
制药行业的洁净压缩空气制备系统,一般以空气压缩机、干燥及过滤净化设备为核心,并结合各种辅助设备共同组成,在实际运行中,则以药品剂型对压缩空气的要求为导向来采取合适的工艺流程,所以流程并非一成不变的,需要根据药品生产实际情况灵活配置,还需要重点考虑生产规模、药品剂型对压缩空气的要求,从而提高压缩空气净化工艺流程的可行性。根据GMP要求,制药企业还需要定期对压缩空气系统进行验证,而压缩空气作为药品生产过程中一种关键的介质,需要对其质量进行控制,除了含油量、露点、悬浮粒子和浮游菌外,希望更多工艺技术人员能够开发出更多质量控制手段来提高质量标准,保证压缩空气正常运行,给药品生产质量提供更多支持。
[1] 国家食品药品监督管理局药品认证管理中心. 药品GMP指南: 无菌药品[M]. 北京: 中国医药科技出版社,2011.
[2] 陈琦. 制药行业压缩空气的净化系统及验证[J]. 机电信息,2014(32): 18-23.
[3] 鱼宝生,全新利,尚功双. 制剂用压缩空气系统的设计与验证[J]. 医药工程设计杂志,2001,22(2): 19-25.
Discussion on Compressed Air System and Compressed Air Quality Control Methods in Pharmaceutical Enterprises
This paper briefly expounds the definition and characteristics of compressed air, and introduces the quality requirements, system composition and operation principle of compressed air system in pharmaceutical enterprises in detail. In the production of drugs, the quality of compressed air in direct or indirect contact with drugs directly affects the quality of products. Therefore, this paper further discusses the quality control methods of compressed air in pharmaceutical enterprises under GMP requirements, and implements the quality control methods including oil content, dew point, suspended particles and planktonic bacteria to ensure that the quality of compressed air produced after strict purification measures is reliably guaranteed, proving that the quality of compressed air meets the requirements of GMP.
compressed air system; quality control methods; GMP
TH41
A
1008-1151(2023)09-0046-04
2023-03-13
梧州市科技计划项目(202102015)。
许建明,女,广西梧州中恒集团股份有限公司工程师,研究方向为质量管理。
麦志雄,男,广西梧州制药(集团)股份有限公司高级工程师,研究方向为中药、民族药质量标准建立和质量风险管理。
