质子交换膜燃料电池中氧还原反应抗毒性电催化剂研究进展
2023-10-14张启赵红荣峻峰
张启,赵红,荣峻峰
(中国石化石油化工科学研究院有限公司,北京 100083)
质子交换膜燃料电池(PEMFC)是通过电化学反应直接将燃料氢气和氧化剂的化学能转变为电能的装置,因其具有能量密度高、启动快、能量转化效率高、污染小等优点,被认为是最有可能大规模替代现有能源技术的新型能源技术之一。
在质子交换膜燃料电池中,目前还有许多问题亟待解决,其中问题最多的就是阴极催化剂。阴极发生的是氧还原反应(oxygen reduction reaction,ORR),而催化氧还原性能最好的依然是铂系贵金属催化剂,但是Pt 催化氧还原反应对于氧气的纯度要求比较高,某些少量的杂质会导致Pt 催化剂中毒,从而降低催化剂的活性,影响PEMFC 的性能。现在绝大多数PEMFC 阴极所使用的原料气均为空气,而空气中或多或少会包含有容易导致Pt催化剂中毒的物质,如SO2、NO2等。PEMFC 长期在这种环境下运行会对其寿命和性能产生极大影响。因此在保持催化剂活性、稳定性的基础上,提高催化剂的抗毒性成为推动PEMFC 规模化应用的关键问题之一。目前,研究人员关于阳极侧中毒问题的关注较高,研究较久,但关于阴极侧中毒问题在实际应用中才得到研究人员的关注。本文针对阴极侧抗毒性催化剂进行了系统性梳理,以推进阴极侧抗毒性催化剂的进程,加快PEMFC 的大规模应用。
1 质子交换膜燃料电池及催化剂中毒机理
1.1 质子交换膜燃料电池工作原理
质子交换膜燃料电池是一种利用氢气与氧气的电化学反应产生电能的装置,通过氧化还原过程中的电子得失,使电子不断通过外电路由阳极运动到阴极,使整个反应过程达到物质的平衡与电荷的平衡,而外部用电器可以获得燃料电池所提供的电能[1]。
质子交换膜燃料电池的具体工作原理如图1所示,氢气传输到阳极,在阳极催化剂的作用下发生氧化反应,生成H+和电子,H+经质子交换膜传输到阴极,电子通过外电路迁移到阴极,此过程称为氢气氧化反应(hydrogen oxidation reaction,HOR);在阴极,传递到阴极催化剂表面的氧气得电子被还原,与H+反应生成水,此过程称为氧气还原反应(oxygen reduction reaction,ORR)。其电极反应可表示为式(1)、式(2)[2]。
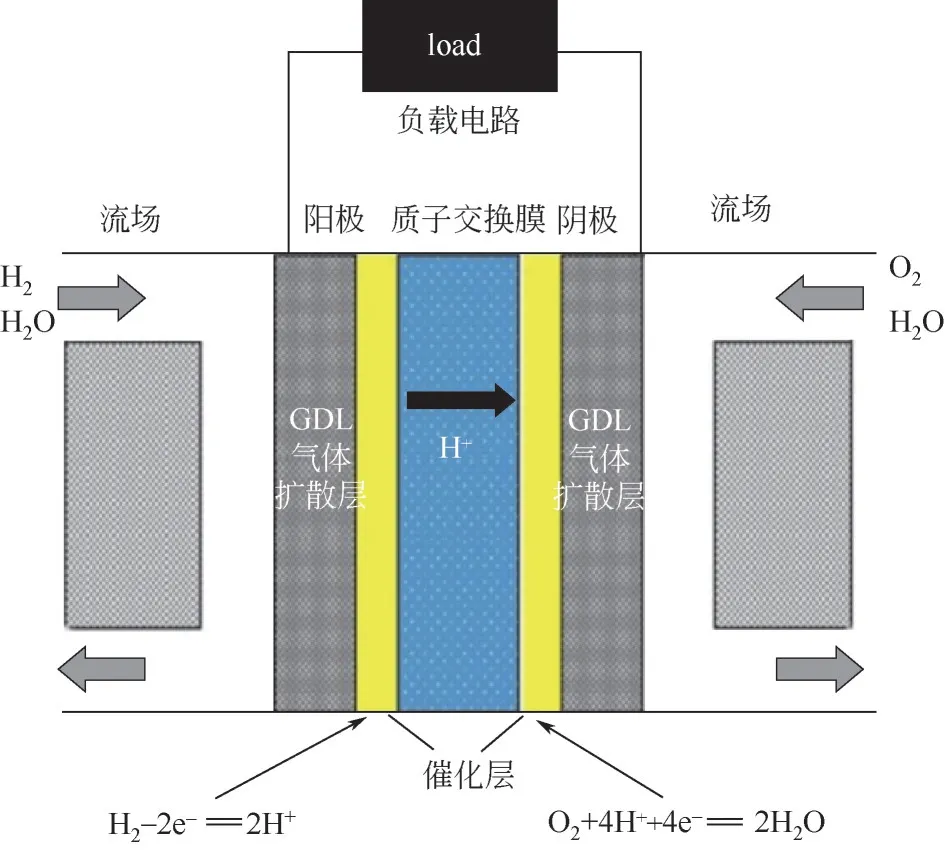
图1 质子交换膜燃料电池工作原理
质子交换膜燃料电池中总的化学反应方程式可表示为式(3)。
与此同时,氢原子在阳极失去的电子在外电路连接下形成了电子流,流经负载并对负载做功,然后再到达阴极供氧化剂消耗。以上整个过程就表示了由简单的氢氧燃烧放热反应转化成高能量利用率的放电过程[3-4]。
燃料电池的阳极氧化反应较为简单,是一个快速动力学过程;但是阴极氧还原反应涉及多电子的得失,动力学过程极其缓慢,其反应速率相比阳极慢了6 个数量级以上[5]。因此,阴极氧还原反应的速率是影响燃料电池性能的关键因素,开发高效、耐用的阴极催化剂就成为制约燃料电池规模化应用的关键。
1.2 阴极氧还原反应易中毒问题
在PEMFC 中的阴极侧还有很多问题制约着它的发展,比如:阴极水淹问题以及“负差效应”、渗透效应、成本高、耐久性差、催化剂容易中毒等[6],其中多数问题已得到研究者关注并取得了许多进展,而阴极催化剂易中毒问题随着PEMFC 的实际应用正在逐渐显现。
目前PEMFC 催化剂中毒问题在阴阳两电极都会发生。出于成本及实用性的考虑,PEMFC 阳极侧所采用的燃料气通常是通过重整等途径制备的富氢气体,而重整气中大多会存在一定的杂质,如CO、CO2、NH3以及H2S 等[7]。同样,PEMFC 阴极侧所用的氧气也并非高纯氧气,而采用的是空气,空气中存在污染物,比如汽车尾气排放的SOx、NOx等,尤其在交通繁忙的公路环境中,SOx浓度可能达到42mg/m3及以上。这些污染物大多都能在Pt 表面形成强烈的吸附并成键,从而使Pt 催化剂中毒失活,进而造成ORR 发生困难。SO2、CO可以强键合力的形式吸附在Pt表面,占据Pt的活性位点[8-11]。当燃料气体中CO 的体积分数高于0.001%时,可导致电池性能显著降低。与CO 相比,SO2对Pt催化剂的失活作用更明显,毒化后的催化剂可恢复性也很小[12-13]。目前,阳极催化剂的抗毒性问题已经得到了研究者的关注,但阴极催化剂由于活性和稳定性等问题尚未完全解决,因此阴极易中毒问题在最近才进入研究人员的视野当中。
Misz等[14]总结了有关重要空气污染物对PEMFC影响,其中二氧化硫(SO2)、氮氧化物(NOx)、氨(NH3)和有机化合物被选为本研究的重点研究对象。他们在不同浓度与不同污染物的条件下,对电池进行恒电压测试,监测电流变化情况,结果如表1 和图2 所示。研究发现,污染物SO2、NO2、NO、NH3均会导致燃料电池输出电流下降,且浓度越高,降幅越大。魏子栋团队[15]也发现,极少量的有毒物质会导致性能的急剧下降。

表1 污染物浓度对电流的影响[14]

图2 在电池温度为70℃和电池电位为0.7V时,电流随毒化物浓度的变化曲线[14]
由此可见,想要实现质子交换膜燃料电池的大规模应用,并且与传统内燃机之间形成较大的竞争力,依然还有很多的“卡脖子”技术需要一一攻克。在燃料电池车实际运行时,其稳定性的下降除了常见的铂溶解、团聚及碳腐蚀等造成的铂流失之外,毒化物的影响也不可忽视,只是在目前,由于催化剂自身稳定性带来的燃料电池性能下降仍占主导,随着催化剂性能的进一步提升以及燃料电池车更长时间的运行,催化剂的毒化问题将逐渐凸显。
1.3 阴极氧还原反应中毒机理
1.3.1 SO2中毒
关于Pt的SO2中毒机理现尚未完全明确,有研究人员认为,当电极保持在指定的电位时,硫通过式(4)、式(5)被吸附到Pt 位点上,并占据一个或两个铂位点,从而导致其失活[16-18]。
也有研究人员认为,一些被吸附的硫具有桥的几何形状,每个二氧化硫通过S和O原子占据两个Pt位点,其吸附后如结构式(6)所示[19]。
在研究了溶液中SO2在Pt电极上的吸附后,发现硫的最终氧化状态在很大程度上取决于电化学槽内的电极电位[17-18,20-29]。在低电位(0.05~0.4V)下,铂上吸附的硫物种转化为零价硫。在高电位(0.8~1.4V)下,零价硫和铂上吸附的硫在酸性电解质中通过一个六电子过程被氧化为水溶性硫酸盐(SO42-),并从Pt 表面氧化解离下来,如式(7)、式(8)所示[30-31]。至于中间电位(0.4~0.8V)、氧化状态以及Pt电极上SO2吸附硫种的化学特性仍存在争议,许多研究人员认为,吸附硫物种以零价硫的形式存在[17,20,32],但有人认为硫以铂硫化物(-2价态)的形式存在[21,24,33],也有人提出在高硫覆盖层存在硫双分子层[17-18,22]。无论硫以何种状态存在,其都会造成Pt不可逆的中毒。
1.3.2 CO中毒
对多晶铂在25℃下的研究表明,CO 中毒是由于其在催化剂表面的强吸附,阻断了O2吸附和电还原的表面活性位点。在这种情况下,O2还原电流将产生于CO 层上存在的表面空位。通过动力学分析表明,CO 中毒效应是通过自由铂位点攻击机制发生的,主要涉及两种吸附的CO[34-37]:线性吸附通过5σ 和2π*轨道与Pt 5d 表面态重叠,如式(9)所示;通过桥型吸附,其中σ键可能涉及两个相邻的Pt位点,如式(10)所示。
2 PEMFC中ORR抗毒性催化剂
目前针对质子交换膜燃料电池中阴极侧抑制SOx、CO 等的中毒问题主要提出了4 种解决办法:增设空气过滤器、臭氧处理、电化学恢复及开发新的催化剂材料[38]。
想要从根本上解决催化剂中毒的问题,就需要开发出具备抗中毒性的PEMFC 催化剂。目前研究者们对于新型催化剂主要集中于三大领域的研发:铂基改性催化剂、非贵金属催化剂和无金属的碳基催化剂。
2.1 铂基改性催化剂
铂基改性催化剂是以贵金属铂作为活性金属,由于铂的特殊电子结构,对ORR 有着良好的催化活性,如图3所示,所以一直以来就被人们视为理想的PEMFC 电催化剂[39]。目前较为有效的改性策略主要有以下几方面:①抑制毒化物与铂之间的电子作用;②增强溢出效应;③锚定金属原子等。

图3 氧还原活性作为氧结合能函数的趋势[39]
Liu 等[40-41]通过水热合成法成功制备了一种耐SO2的Pt-MoO3/C催化剂。通过对比SO2中毒前后线性扫描曲线可知,在0.3V(vs.Ag/AgCl)下,在含有0.1mmol/L 亚硫酸钠的0.5mol/L 硫酸溶液中经过120s 毒化后,Johnson Matthey(JM) Pt/C 催化剂电流衰减达到了22.51%,而Pt-MoO3/C 仅衰减10.53%。毒化后在-0.2~1.0V(vs.Ag/AgCl)电压范围经过50 圈CV 扫描,Pt-MoO3/C 催化剂活性基本恢复到初始水平,而JM Pt/C活性恢复程度较小。CV扫描可使催化剂活性恢复是因为吸附在电催化剂表面的SO2被氧化,从而使得占据的活性位点被释放。其电化学测试结果如图4所示。

图4 催化剂中毒前后催化性能图[40]
结果表明,Pt-MoO3/C 催化剂不仅具有较高的催化活性,而且具有较好的抗SO2中毒性能和较好的毒性恢复性能。导致Pt-MoO3/C催化剂具有抗毒性的原因是MoO3的存在削弱了S—Pt键合强度,降低了SO2在Pt-MoO3/C上的吸附能,从而减弱了SO2对Pt-MoO3/C 电子结构的影响,使催化剂在吸附SO2后保持原有的电子结构。
Xia 等[42]利用密度泛函理论(DFT)研究了双金属PtMo催化剂的电子结构与SO2耐受性能之间的关系,并分别计算了SO2及解离中间物种S和SO3在Pt(111)和PtMo(111)表面的吸附构型。表2 表示了S和SO3在Pt(111)和PtMo(111)上的吸附能和距离。与纯Pt 催化剂相比,Mo 的引入一方面减弱了SO2与PtMo 催化剂之间的相互作用;另一方面,Mo 原子抑制了吸附的SOx向Pt的电子转移。因此,PtMo催化剂的原始电子结构和Pt 原子活性保持不变,从而Mo改性Pt催化剂具有耐受SO2及其中间体(如S和SO3)的能力。

表2 S和SO3在Pt(111)和PtMo(111)上的吸附能和距离[42]
Xu等[43]通过在Pt/C 催化剂中引入了高达6%的非晶态氧化铈来提高催化剂的抗毒性,其TEM 图如图5(a)、(b)所示。当CeO2质量分数为2%和4%时,催化剂表面氢吸附/解吸活性位点的损失可以忽略不计,几乎不影响催化剂的性能。并且2%的CeO2对SO2氧化有较好的促进作用,如图5(c)所示,2%的CeO2使SO2氧化的峰值电位降低了50mV,而较高含量的CeO2对SO2氧化有抑制作用。这是由于适量纳米尺寸的CeO2有利于O2的传输,为SO2氧化提供了恰当的氧气,而当CeO2含量过高时,所提供的氧气超过最优值,影响SO2氧化过程。

图5 催化剂的TEM和循环伏安曲线[43]
Prithi 等[44]采用硬模板法成功制备了介孔铂粒子,结果表明,铂的介孔结构具有比微孔结构更好的活性,其ECSA 提高20%,半波电位正移88mV。进一步研究了介孔铂电催化剂对SO2的耐受性,如图6 所示,经SO2毒化120s 后,介孔铂(meso-Pt)的总硫覆盖率为其ECSA 的38%,而铂黑(Pt-B)的总硫覆盖率为其ECSA的58%。
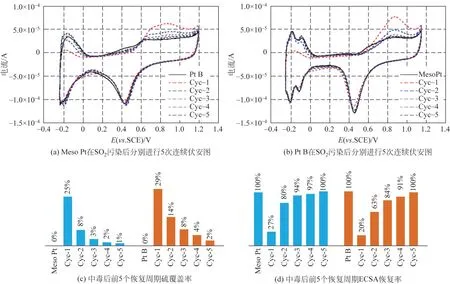
图6 催化剂在毒化后进行5次连续循环伏安性能[44]
研究发现,介孔Pt 的多面体结构具有许多缺陷位点,且具有缺陷和台阶等低配位点的铂表面比平阶的更能促进氧在这些配位点上的解离吸附,从而使硫的氧化速度更快。Kahng 等[45]也提出了高浓度的原子尺度表面缺陷的存在提高了氧以更高速率去除硫的能力,这是因为表面缺陷部位被有效阻塞或缺陷部位上的硫迁移增强。
Awad 等[46]研究了多晶Pt(poly-Pt)电极和纳米Pt修饰玻碳(nano-Pt/GC)电极在硫中毒下的氧还原反应电催化活性的再生行为。研究发现,在0.06~1.56V(vs.RHE)电压下进行的长期恢复可以完全回收两个电极,而在0.06~1.06V(vs.RHE)下进行的短期恢复只能在纳米Pt/GC电极上得到一定程度的恢复。他们在多晶Pt 电极上观察到有强结合的氢吸附在Pt(100)面上,而在纳米Pt/GC电极上没有显示。这反映了纳米Pt/GC电极在其他两个低折射率面的相对富集,即Pt(110)和Pt(111)面。而正因为纳米Pt/GC电极Pt(100)面的比例较低,所以能在纳米Pt/GC电极上观察到较强的回收率,其Pt(100)面与其他低折射率晶体面相比,具有更大的硫吸附热。
Jayaraj 等[47]指出,石墨烯(作为催化剂载体)上的铂(Pt/G)比普通催化剂上的铂(Vulcan XC碳载体)表现出更好的SO2耐受性。如图7 所示,PEM 燃料电池暴露在含有2.86mg/m3二氧化硫的气流中约3h 后,Pt/C 催化剂失去了88%的起始电流密度,而Pt/G 催化剂在相同条件下电流密度仅有31%的减少。

图7 在0.6V下Vulcan碳上的铂(Pt/C-MEA)和石墨烯上的铂(Pt/G-MEA)暴露于SO2的电流[47]
Xu 等[48]研究了WOx改性Pt 金属催化剂(WOx-Pt/C) 在SOx中毒条件下的催化活性,并表明WOx-Pt/C 催化剂是一种有前景用于含硫杂质的催化剂。经过电化学测试和计算,发现在一定毒化物浓度,WOx-Pt/C 催化剂在经过毒化后的硫覆盖率小于商业催化剂Pt/C,其计算结果见表3。他们发现硫覆盖率下降的原因在于SOx氧化性能提高,而SOx氧化性能的提高归因于WOx诱导效应:①Pt纳米颗粒与WOx的协同效应,即WOx亲水表面产生—OH 基团;②WOx发生氢气溢出效应,如图8所示;③W(V)/W(VI)的氧化还原耦联促进了WOx与Pt纳米颗粒的电子相互作用。

表3 Pt/C与质量分数5% WOx-Pt/C在经过一定浓度毒化物毒化后的SOx初始覆盖率和损失程度[48]
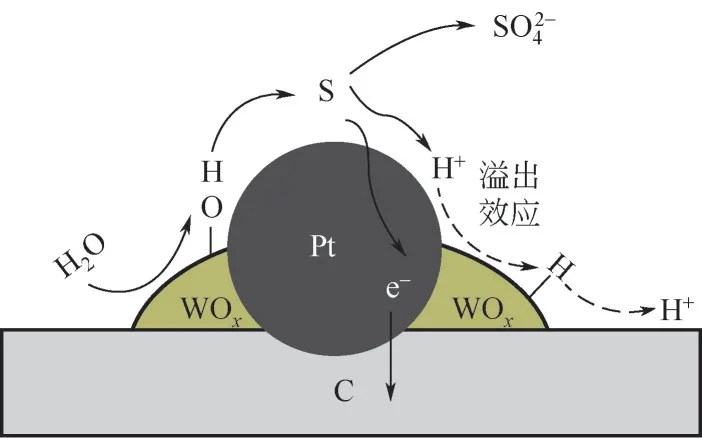
图8 WOx促进碳载Pt催化剂上SOx氧化的机理[48]
Garsany 等[49-50]研究了Pt3Co/Vulcan Carbon 和Pt/Vulcan Carbon 在燃料电池ORR 中抗SO2中毒的性能。研究发现在相同的Pt负载量下,Pt3Co/VC电极上的ORR性能受硫的毒害程度大于Pt/VC电极。而两种电催化剂的ORR 性能损失都伴随着过氧化氢的生成。Pt3Co/VC 电极的硫覆盖率明显高于Pt/VC电极,这是由于其较低的Pt 电化学表面积或较低的表面氧覆盖率,但是对于硫覆盖率相似的电极,Pt3Co/VC显示出比Pt/VC更优的ORR活性。这是由于Pt3Co中的Co配体削弱了Pt—OH和Pt—S键,从而推动—OH吸附到更高的电位,而SO2氧化为SO3/SO4则发生在较低的电位。这使得OH 吸附和硫氧化过程在Pt3Co/VC上在相似的电位发生,所以每个CV循环Pt3Co/VC比在Pt/VC上去除更多的硫。这一结果也证实了被SO2毒化后的Pt3Co/VC 阴极MEAs可以在空气中循环到约0.9V来恢复,而恢复Pt/VC的MEAs需要更高的电位。
叶菁等[51-52]通过微波辅助乙二醇还原法制备了Pt/TiO2/C 复合催化剂,通过电化学测试发现,SO2中毒后所有催化剂的ORR 活性都有所下降,但是Pt/10TiO2/C 催化剂仍然具有最好的ORR 活性。随着TiO2的加入,动力学电流密度的下降率明显降低,其中Pt/10TiO2/C催化剂的活性衰减最小,仅为44.4%,而Pt/C 催化剂的活性衰减为67.8%,Pt/10TiO2/C 中毒后的半波电位下降53mV,远低于Pt/C 的71mV,结果如图9(a)、(b)所示。说明Pt/10TiO2/C对SO2的耐受性较Pt/C有较大提高。

图9 催化剂毒化前后性能图和抗毒化作用原理[51]
研究表明,Pt/TiO2/C 能够提高SO2耐受性是由于TiO2加速了SO2的电氧化。研究者认为,Pt 和TiO2之间的电子相互作用以及羟基的溢出效应不仅可以提高ORR活性,还可以缓解SO2中毒。前者可通过电子相互作用削弱Pt—S键,后者羟基可通过溢出效应转移到Pt 表面,使得Pt—OH 增加,同时羟基基团作为含氧物种参与了含硫物质的氧化过程,对促进SO2的氧化脱除具有积极作用,其作用机理如图9(c)所示。
与此同时,他们还对Pt/TiO2/C进行了抗NOx毒性测试,发现NOx对Pt/C和Pt/TiO2/C的毒化程度都非常严重。通过电化学测试发现,Pt/TiO2/C并不能促进NOx的脱除,且NOx毒化后ORR活性衰减程度与Pt/C相比没有明显差别,结果如图9(d)所示,说明Pt/C-TiO2在抗NOx毒化上作用不明显。
2.2 非贵金属催化剂
由于铂存储量匮乏且价格昂贵,所以在大量的商业化开发当中,铂基催化剂的成本将会成为阻碍其发展的一大关键因素。开发具备同样催化活性、廉价且高效的非贵金属催化剂成为目前研究热点。
Deng等[53]制备了一种包裹在豆荚状碳纳米管内的铁纳米催化剂(Pod-Fe),其TEM 结果如图10(a)、(b)所示,研究表明,金属Fe 被完全包裹在CNTs内,这可以防止Fe长时间暴露在空气中被氧化。同时也可以很好地避免金属颗粒与酸性介质、空气污染物等直接接触,然而这种保护并不会妨碍其催化剂的活性与稳定性。通过在空气中加入28.60mg/m3SO2,考察恒电流下催化剂的耐久性,其测试结果如图10(c)所示,发现Pod-Fe 在800min内保持电压稳定,而20% Pt/C 在1h 内电压下降40%左右。

图10 催化剂的电镜图像和稳定性测试结果[53]
Reshetenko 等[54]以硝酸铁和4-氨基安替吡啉(AAPyr)为前体合成了非贵金属催化剂Fe/N/C,非贵金属氧还原催化剂的耐毒性可能是由于含铁活性中心与SO2的相互作用较弱或缺乏相互作用所致。他们使用DFT计算了在Fe-N4、Fe-N2C2和N掺杂石墨烯催化(氮掺杂石墨烯是从石墨烯薄片上去除一个C 原子,空位被一个氮原子填充;Fe-N4和Fe-N2C2是分别去除两个相邻的C 原子,内部边缘分别被4N 或2N 取代,使Fe-N4和Fe-N2C2结构进一步配位到Fe 原子上)位点与氧和污染物的结合能。根据Sabatier 原理,氧还原活性强烈依赖于氧与催化剂的相互作用。利用带有PBE的DFT,计算出氧分子在Fe-N4、Fe-N2C2和N掺杂石墨烯位点上的吸附能(表4) 分别为-1.01eV、-2.34eV 和-0.15eV,SO2的吸附能耗分别为-0.81eV、-1.63eV和-0.17eV,SO2与O2的吸附能比较表明,SO2与Fe-N4和Fe-N2C2的相互作用比与O2更弱。因此,SO2不会被含铁中心强烈吸附,不影响氧还原性能。

表4 Fe-N4、Fe-N2C2和N掺杂石墨烯对O2、NO、NO2、CO和SO2的吸附能[54]
在PEMFC 中,不仅SOx会导致催化剂中毒失活,CO也有同样的毒性,研究者们早已关注到CO对于催化剂中毒的影响,并在此领域已经做了大量的工作。目前,研究人员主要针对M-N-C(M 为非贵金属)的结构进行重点研究。
Xiang 等[55]提出了加入非贵金属的碳化共价有机聚合物作为氧还原反应催化剂的替代物。他们由各种含氮金属-有机配合物(如金属-卟啉配合物)合成了一类二维共价有机聚合物(COP),加入金属后命名为COP-P-M (M=Fe, Co, Mn;P=卟啉环),再进行碳化,将COP-P-M 转化为金属结合的C-COP,并命名为C-COP-P-M, M = Fe, Co, Mn,其结构如图11 所示。除了耐久性和活性测试,他们还研究了C-COP-P-Fe、C-COP-P-Mn 和C-COP-P-Co 的CO 中毒耐受性,结果表明,在向O2流引入体积分数10% CO的情况下,上述催化剂的电流损失仅为约15%,而同样条件下Pt/C的电流损失约为75%。
Zhang等[56]通过DFT计算模拟了各种Fe-N的活性位点,如图12所示,研究了CO在Fe/N/C催化剂4个不同活性位点上的吸附和氧化,包括Fe-N4类卟啉碳纳米管(T-FeN4)、Fe-N3 类吡啶碳纳米管(T-FeN3)、Fe-N4 类卟啉石墨烯(G-FeN4) 和Fe-N2 纳米带(R-FeN2)。他们发现CO 的吸附和氧化具有结构选择性,CO 在T-FeN4 和G-FeN4 上的吸附比O2的吸附更有利,且CO 在T-FeN4 和GFeN4 上的氧化作用更强,表明这两种构型可能都被CO吸附所毒害。而T-FeN3和R-FeN2更容易吸附O2,CO 容易被O2氧化,说明T-FeN3 和R-FeN2具有较好的耐CO性能。

图12 T-FeN4、T-FeN3、G-FeN4和R-FeN2上吸附的CO和O2的优化结构[56]
He 等[57]也通过实验验证了氮自掺杂石墨烯基非贵金属催化剂在ORR 中抗中毒性的应用。他们发现,一旦将一氧化碳注入电解液中,Pt/C电极就会迅速中毒。然而在相同的测试条件下,Fe-N-石墨烯只检测到微小的变化。
随后有研究人员将Co 加入N-C 结构,并探究其抗毒性。Liu等[58]对Co-N-C碳纳米管进行了热活化,以增强氧还原反应的性能,制备出了高活性催化剂,即CO-N/CNT-900-1-1,然后将其暴露于含CO 的空气中作为毒物,并与商业Pt/C 催化剂的行为进行比较。结果表明,商业Pt/C在中毒条件下运行800s 后损失了56%的初始电流,而Co-N/CNT-900-1-1表现出显著的一氧化碳耐受性,电流损失的量级仅为5%。
Zhang 等[59]通过电化学测试和漫反射红外傅里叶变换(DRIFT)光谱研究对比了Fe-N-C 和氮掺杂碳(CNx)对于CO 的抗毒性,发现Fe-N-C 的CO耐受性优于商业Pt/C,但低于CNx型材料,测试结果如图13 所示。通过DFT 计算结果表明,所有CNx位点均表现出弱CO 吸附和强O2吸附,CO 在Fe-N-C 位的结合能与Pt(111)处的结合能相似,但CO 在Fe-N-C 位的结合能弱于O2,以上结果表明Fe-N-C和CNx催化剂都具有一定的CO耐受性。在之前的报道当中也有研究人员对于CNx的抗毒性进行过研究。

图13 CNx和FeNC在经过CO毒化前后的极化曲线[59]
2.3 非金属碳基催化剂
除了铂基贵金属催化剂和非贵金属催化剂外,也有少量研究以杂原子掺杂的碳材料直接作为ORR 催化剂,由于其无金属存在,通常具有良好的抗毒性。
Von Deak 等[60]对铂基催化剂和CNx氧还原催化剂进行了H2S 中毒处理,研究了中毒前后CNx氧还原活性的变化。通过电化学测试发现,硫处理明显降低了铂催化剂上ORR 的活性,证明了硫中毒处理的有效性,而H2S 处理后的CNx催化剂活性不仅没有降低,反而得到了提高,测试结果如图14 所示。但是由于活性金属的缺失,其电化学性能较差。
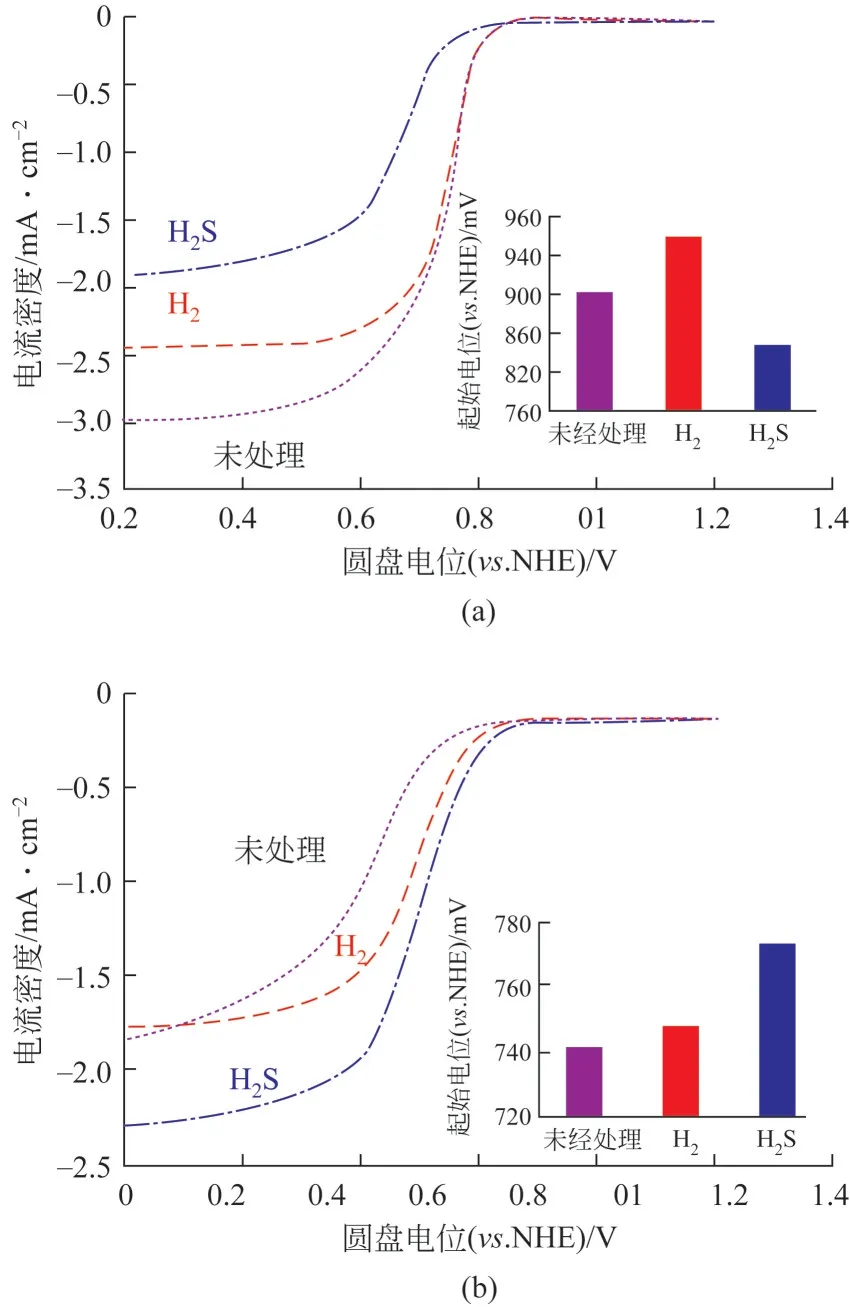
图14 H2S处理对Pt/Vulcan碳催化剂和CNx催化剂氧还原活性的影响[60]
Chen 等[61]对氮掺杂碳纳米笼电催化剂NCNC700/900(700 和900 分别为生长温度和退火温度)进行了类似的CO 抗中毒实验,结果表明,当暴露于体积分数10% CO 时,Pt/C 会在3000s 内损失80%的初始电流,但NCNC700/900 在相同条件下对这种中毒不敏感。并且在100h 的长期稳定性试验中,该电催化剂的电流仅下降10%,明显优于Pt/C 的40%。Qu 等[62]对氮掺杂石墨烯(N-石墨烯)电极进行了类似的测试,结果表明,在中毒条件下运行800s后,Pt/C下降到初始电流的20%,而在4000s内,N-石墨烯的电流没有下降。
Li 等[63]研究了磷掺杂对于催化剂抗毒性的影响,他们将氧化石墨烯与1-丁基-3-甲基咪唑六氟磷酸盐的均匀混合物在氩气气氛下进行热退火,成功制备了大表面积(496.67m2/g)和较高磷掺杂水平(原子百分比1.16%)的无金属掺杂磷石墨烯纳米片(P-TRG)。研究结果表明,P 原子进入到碳骨架中并被部分氧化,为氧还原反应创造了新的活性位点。在P-TRG 中,部分氧化的P 与C 共价成键,并以四面体形式存在,如C3PO、C2PO2和CPO3,如图15(a)所示。由于P 的部分氧化,原子电荷会在P掺杂的石墨烯上重新分布,电负性最高的O原子会先使P原子极化,然后以极化的P原子为桥梁从碳原子中抽离电子,在P原子附近的碳原子上形成正电荷。因此,带正电的碳原子就成为有利于O2吸附的活性位点,削弱O—O键,并从阳极吸引电子,与N掺杂的碳一样,通过高效的四电子路径促进O2还原为OH-。随后进行了CO中毒试验,测试结果如图15(b)所示,当在电解液中加入相同流量的CO 时,由于CO 中毒,Pt/C 电极上的ORR电流减弱了约82.5%。相反,在P-TRG 电极上,ORR 电流只有轻微的衰减,这是由于O2的分压降低导致O2在电解质中的溶解度降低,这表明PTRG催化剂本质上对CO不敏感。P-TRG催化剂对CO的耐受性优于商业Pt/C。
魏子栋团队[64]发现在氮掺杂石墨烯中引入磷原子可以提高结构稳定性和抗中毒性能,如图16 所示。通过热解聚二氨基吡啶(PDAP)和肌醇六磷酸的混合物,制备了一系列P、N 共掺杂碳材料(PNC)。PNC 在SO2-3(50mmol/L NaHSO3)、NO2-(50mmol/L NaNO2)和HPO2-4(50mmol/L Na2HPO4)存在下的ORR 活性均稳定,而商业Pt/C 在相同条件下严重中毒。本实验还表明,在Fe-N-C 中加入磷也能提高其抗中毒性能。研究表明,氮碳中的磷掺杂促进了碳原子向氮的电子转移,从而形成氧键碳原子,同时通过促进氮掺杂在边缘产生更多的活性位点,从而建立起较强的结构稳定性,防止了活性位点的损失。同时,磷的掺杂会使碳骨架产生大量缺陷,有利于氮的掺杂,并在热解过程中形成磷和氮共掺杂结构。而这种氮和磷共掺杂的碳网络正是实现抗中毒的关键,因为氮和磷共掺杂在碳骨架中会引起碳原子上的电子密度重分布,而单杂原子掺杂碳结构对抗中毒效果无明显影响。
3 结语
经过研究者们不断地努力,ORR 电催化剂的抗毒性研究已经取得了很大的进展。归纳起来,主要集中在三大领域:①铂基改性贵金属催化剂;②非贵金属催化剂;③无金属碳基催化剂。铂系贵金属改性催化剂主要通过抑制毒化物与铂之间的电子作用、增强溢出效应、锚定金属原子等方式来增强催化剂的抗毒性。非贵金属催化剂在抗中毒上也有较好的表现,然而其活性和稳定性还有待进一步提高。无金属的碳基催化剂由于不存在易被毒化的金属,因此具有优异的抗毒性,是抗毒性催化剂研发的重要方向之一,但其相关研究还处于起步阶段,催化剂性能仍有很大提升空间。在未来一段时间内,实际应用过程中仍将以铂基贵金属催化剂改性为主,目前的研究主要集中于如何降低毒化物的去除电位,即提升催化剂中毒后的恢复能力。如何精准调控Pt 的电子状态,以抑制Pt 与毒化物之间的电子相互作用,从而减缓催化剂在毒化物存在时的性能下降是解决问题的根本。
在PEMFC飞速发展的这十几年,关于CO会导致催化剂中毒的事实早已经被研究者们关注,并且在此领域做了大量的研究,其毒化机理和抗毒性催化剂已经较为成熟。近几年来,SOx被发现对于ORR电催化剂也具有不可逆转的负面影响。目前,关于抗SOx电催化剂的报道还比较少,不过有许多研究者也开始慢慢关注SOx的毒化机理研究,并开始进行抗SOx电催化剂的研究。由于NOx对于阴极侧中毒效应比SOx小,在SOx还没完全攻克的当下,针对NOx的抗毒性催化剂就更是少之又少,尽管也有人对NOx进行抗中毒催化剂开发与设计,但其抗毒性结果并不理想。这对中毒机理的充分认识和有效的抗中毒电催化剂的设计原则提出了更高的要求。PEMFC 电催化剂的抗中毒性策略也被赋予高度期望。基于对抗毒性机理的深入认识,开发兼具高活性、高稳定性和良好抗毒性的催化剂是未来的研究方向。
