Ti电絮凝去除饮用水中砷的效能与机理
2023-10-12曹玉敏吕建波宋晓鹏张欣桐王春泉
曹玉敏,吕建波,宋晓鹏,张 鹏,张欣桐,王春泉
(1.烟台大学土木工程学院,山东 烟台 264005;2.烟台市环境监控中心,山东 烟台 264003;3.烟台市标准计量检验检测中心,山东 烟台 264003)
砷是人们关注的一类重要饮用水污染物,据报导全世界有数百万人受到地下水砷污染的影响[1]。长期摄入砷会导致癌症、疼痛性皮肤损伤、心血管和生殖问题,并可能对儿童的智商产生不利影响。因为这些致病性危害,在《生活饮用水卫生标准》[2]中砷的标准限值从原来的0.05 mg·L-1降低到0.01 mg·L-1。在水资源匮乏、卫生条件有限的地区,受砷污染地下水的有效处理显得更为重要。迄今为止,各种技术已被报道用来去除水中的砷,包括化学混凝、吸附、生物法和离子交换等[3-6]。然而,这些方法存在耗时、去除效率低、化学试剂额外消耗、运行成本高以及二次污染物大量产生等缺点。目前,电絮凝(Electrocoagulation,EC)作为一种新兴技术,因其能够在不投加化学试剂的情况下快速高效去除水中的砷而受到越来越多的关注。
EC通常使用铝、铁作为阳极[7],但用于饮用水处理时,铝电絮凝经常会导致出水中的铝含量过高,可能引起老年痴呆症;而铁电絮凝不仅会引发色度问题,溶解的铁可能还会刺激细菌滋生[8]。钛作为一种新兴的极板材料,正在受到越来越广泛的关注。钛电絮凝已被研究用于去除水中的腐殖酸、高氯酸盐、硝酸盐和溴酸盐等[9-11]。CHEN等[9]使用钛代替铁和铝作为新的牺牲阳极,将EC工艺与超滤相结合,不仅能够有效地去除水中的腐殖酸,而且可以进行钛基污泥的回收。WANG等[10]使用钛阳极-铁阴极进行EC实验,利用阳极溶解产生的多价钛物种来还原高氯酸盐和硝酸盐,在6~8 h的反应时间内,初始浓度分别为200 mg·L-1和1000 mg·L-1的高氯酸盐和硝酸盐,被还原到最终浓度分别低于20 μg·L-1和200 μg·L-1。ZHONG等[11]利用双室电解池,在电化学诱导钛阳极点状腐蚀的作用下产生活性的钛离子,如Ti2+和Ti3+,这些多价的Ti物种能够有效地将BrO3-还原成Br-。目前,国内外关于钛电絮凝除砷的研究仍然较少。此前,KUMAR等[12]对铁、铝、钛的除As(Ⅲ、Ⅴ)效能进行对比,结果表明钛极板不如铁和铝极板的除砷性能好。但相较于铝和铁,钛不会给人体健康带来负面影响,而且产生的污泥还可以用来回收TiO2以作为颜料、催化剂等[13-14],具有很大的开发潜力。然而关于钛电絮凝去除水中砷的效能、机理以及钛极板在目标溶液中的电化学性能尚不清晰,因此本研究对钛电絮凝去除水中砷的效能和机理进行初步探索,以期为钛电絮凝除砷技术的应用提供技术支持。
1 材料与方法
1.1 实验试剂
砷酸钠、氯化钠、硝酸钠、无水硫酸钠、盐酸和氢氧化钠均为分析纯,硝酸为优级纯,均购自于国药集团化学试剂有限公司;磷酸氢二铵为色谱纯,购自阿拉丁化学试剂网。
1.2 实验仪器
Seven compact型pH计(上海梅特勒-托利多国际贸易有限公司);SX813型电导率测量仪(上海三信仪表厂);ZETASIZER Nano series型Zeta 电位仪(英国Malvern公司);7800型电感耦合等离子体质谱仪(美国Agilen公司);CHI 760E型辰华电化学工作站(上海辰华仪器有限公司);Nicolet IS10型傅氏转换红外线光谱(FTIR)分析仪(美国Thermo Fisher Scientific公司);Escalab 250Xi型X射线光电子能谱(XPS)微探针(美国Thermo Fisher Scientific公司);高效液相色谱-电感耦合等离子体质谱联用(HPLC-ICP-MS)仪(美国Agilen公司);PRP-X100型阴离子色谱柱(美国 Hamilton公司);WGZ-200S型浊度计(上海昕瑞仪器仪表有限公司)。
1.3 实验装置
静态实验(单因素实验和响应面实验)装置包含1 L圆柱形反应器(内径12 cm,高度14.8 cm)、钛板电极(各元素含量:钛99.29%,铁0.30%,碳0.10%,氮0.05%,氢0.01%,氧0.25%;尺寸:长×宽×厚=23 cm×9 cm×0.2 cm)、直流稳压电源、磁力搅拌器、转子及导线,如图1(a)。连续流实验装置包含EC反应器(长×宽×高: 20 cm×10 cm×15 cm,有效容积为2.3 L),钛板电极、直流稳压电源、导线、蠕动泵、调节池及滤柱(内径4.4 cm,高度153 cm),如图1(b)。
1.4 实验方法
1.4.1 含砷水的配制 实验所用含砷水由砷酸钠和去离子水进行配制,其浓度约为200 μg·L-1,无特别说明时添加NaCl作为背景电解质,其浓度为0.01 mol·L-1,溶液的电导率约为1000 μS·cm-1。
1.4.2 EC除砷静态实验 采用盐酸和氢氧化钠溶液调节反应溶液的初始pH,随后测定溶液的电导率。极板的浸没深度为9.5 cm,每块极板的有效浸没面积为85.5 cm2,每次实验前用砂纸打磨电极以去除其表面金属氧化物,并用纯水进行清洗,然后擦拭干净以备使用。初步的动力学实验表明,反应30 min时可以达到去除平衡,因此每次实验运行时间定为30 min,期间间隔一定时间进行取样。取样后,立即用0.22 μm的滤膜过滤,并用体积分数为2%的硝酸酸化,测定总砷浓度,同时测定每个取样点溶液的pH和Zeta电位。
实验运行结束,将絮体过滤并称量其湿重,用于确定污泥产量。测定阳极在反应前后的重量差,记为阳板损失。实验所需能耗(E)的计算公式为
(1)
式中:U为电压,V;I为电流,A(恒定电流);t为反应时间,s;V为反应溶液体积,L。
电流效率(Current efficiency,CE)是EC过程中一个非常重要的性能指标,CE表示阳极溶解的实际量与按照法拉第定律所计算的理论溶解量的比值[15],表征电流利用率的大小,其计算公式为
(2)
式中:m为阳极损失量,g;Z为电极反应中转移电子数,对于钛,Z=4;F为法拉第常数,96 485 C·mol-1;M为钛的相对原子质量,47.867;I为电流,A;t为反应时间,s。
1.4.3 电极材料腐蚀性能的表征 电化学测试(极化曲线)采用辰华电化学工作站和三电极体系进行,其中铂片作为辅助电极,饱和甘汞电极作为参比电极。将工作电极(钛板:10 mm×10 mm×2 mm)与铜丝焊接,并用树脂进行封装,其有效工作面积为1 cm2。工作电极首先用砂纸进行打磨,然后在无水乙醇中超声5 min以除去表面杂质,最后用超纯水进行冲洗,擦拭干净即刻使用。将工作电极浸入电解液中600 s后首先进行开路电位的测试,测试时间300 s,极化曲线的扫描范围在开路电位± 0.5 V的范围内由负向正扫描,扫描速率固定在5 mV·s-1。通过极化曲线可以获得极板材料在特定腐蚀体系中的自腐蚀电位(Ecorr)和腐蚀电流(Icorr)。Ecorr负值越大,腐蚀倾向越大;Icorr值越大,腐蚀速率越快。
1.4.4 EC除砷机理分析实验 该实验采用两块钛极板在15 A·m-2的电流密度下去除5 mg·L-1的砷,反应时间30 min,用HPLC-ICP-MS测定反应过程中溶液内As(Ⅲ)和As(Ⅴ)的浓度变化,色谱条件为:流动相为0.05 mol·L-1(NH4)2HPO4溶液(HNO3调整溶液pH值为5.6)和水,体积配比为 80∶20,进样量为50 μL。收集上述反应后的絮体,经过滤、冲洗、冷冻干燥和研磨后用于FTIR和XPS表征,将不添加砷时所制备的絮体作为FTIR表征的对照组。
1.4.5 电絮凝-吸附过滤连续流实验 采用单极并联的方式将8块钛极板进行连接,极板间距为1 cm,浸没深度为12.3 cm,电流密度2.66 A·m-2,水力停留时间为1 h;吸附滤料高度80 cm,接触时间30 min。从EC出水开始计时,EC出水30 min后开始取样测试,EC出水和过滤出水间隔75 min,按照设定的取样点对反应后出水进行取样,并测定出水的总砷浓度、pH以及浊度。
2 结果与讨论
2.1 单因素试验
2.1.1 极板间距的影响 极板间距会影响溶液的传质效果和电能的消耗,选用电流密度15 A·m-2,在极板间距分别为0.4、0.9、1.8、2.7 cm的条件下进行实验,探究不同极板间距对污染物去除以及其他指标的影响。
如图2所示,在4个极板间距条件下均可实现95 %以上的总砷去除率,其中,极板间距为0.9 cm时,总砷去除率达到最大。同时,当极板间距从0.4 cm增大至2.7 cm,由于维持恒定电流的电压增大,相应的能耗也在增大;但与此不同的是,极板间距为0.9 cm时的阳极损失最小。由于过小的极板间距不利于溶液的充分混合以及絮体的形成与扩散,而较大的极板间距虽然有利于溶液的充分混合和减少浓差极化,但同时也造成了能耗的增大[16]。因此为保证极板间溶液的充分混合,考虑处理效果及成本,后续实验均在0.9 cm的极板间距下进行。
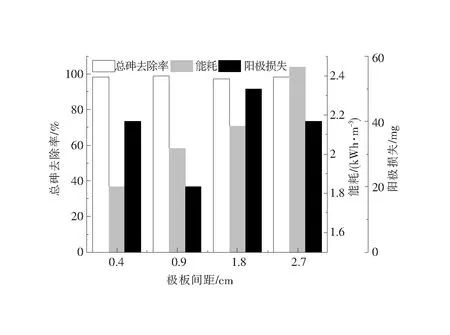
图2 不同极板间距对EC反应的影响
2.1.2 电流密度的影响 图3(a)显示了不同电流密度条件下总砷去除率随时间的变化,结果表明,总砷的去除主要集中在前10 min内,且电流密度越大,总砷的去除速率越快,但处理20 min后,不同电流密度下的去除效果几乎没有差别。这可能是因为在较高的电流密度条件下,单位时间内阳极溶解的钛较多,能够更快地形成絮体用于除砷,但反应一定时间后,溶液中剩余的砷浓度已经很低,因而难以进一步去除。随着反应进行,低电流密度条件下絮体逐渐增多,因此最终的去除效果与高电流密度相差不大。图3(b)中可以看出,电流密度越大,阳极损失、能耗以及污泥产量则越大,所需要的处理成本也越大。综合考虑去除效果、阳极损失、能耗以及污泥产量,采用15 A·m-2的电流密度较为合适。
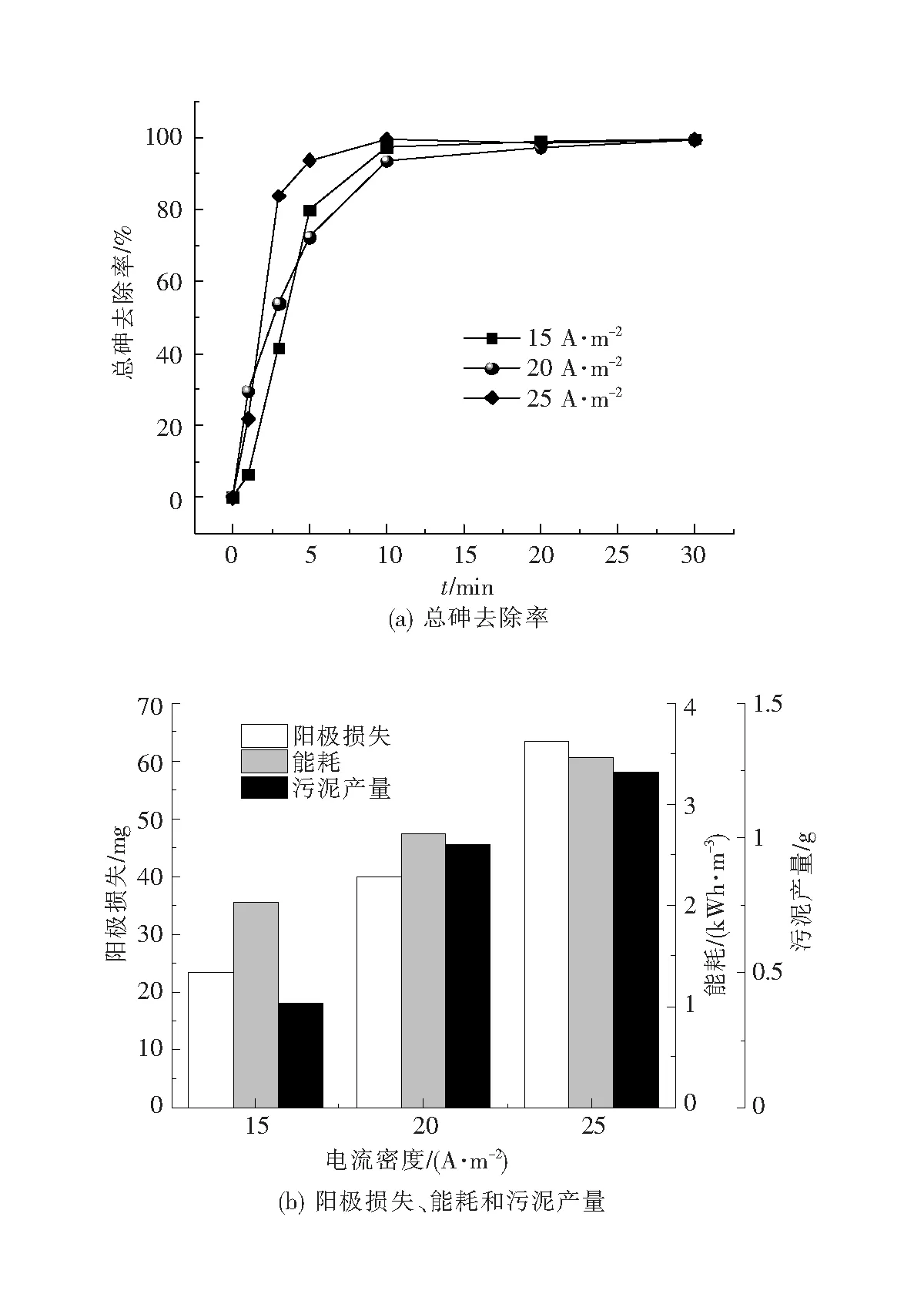
图3 不同电流密度对EC除砷的影响
2.1.3 初始pH的影响 pH值的大小直接影响EC反应和砷的形态分布。不同初始pH(3.9、6.9、9.9)对总砷去除效果的影响如图4。图4(a)是总砷去除率在不同初始pH条件下随时间的变化,酸性和中性条件下总砷的去除速率明显快于碱性条件,且最终去除率也高于碱性条件。在pH 为3.9和6.9时,10 min去除达到平衡,而pH为 9.9时,30 min才能达到平衡。不同pH值对去除效能的差异主要与EC生成的钛活性物种和砷的形态分布有关。如图4(b),在最佳电化学参数条件下,无砷和有砷时EC絮体的零电荷点pH(pHPZC)分别为4.4和4.3,因此,在pH 3.9的酸性条件下,钛絮体(主要为钛氧化物)由于羟基质子化导致其所带电荷为正。且从图4(c)中可以看出,在pH 3.9时EC絮体所带的电荷为正,而在本实验所考察的pH(3.9~9.9)范围内,As(Ⅴ)主要以带负电荷的H2AsO4-、HAsO42-的形式存在[7],所以EC产物会与带负电荷的砷物种之间产生静电引力(式(3)),因此在酸性条件下总砷的去除速率较快。有报道称[13]钛阳极在中性及酸性条件下的腐蚀电位更低,所以在中性及酸性条件下会有利于阳极的溶解,从而产生更多的絮体,进而促使五价砷能够被更好地去除。另外,在碱性条件下所产生的胶体所带电荷为负,可能会与带负电荷的H2AsO4-、HAsO42-之间产生静电排斥进而导致总砷的去除速率相对较慢。如图4(d),在初始pH为酸性和中性的条件下,溶液的pH值呈现上升趋势,是因为在阴极附近发生了电解水的析氢反应[17],如式(4)。
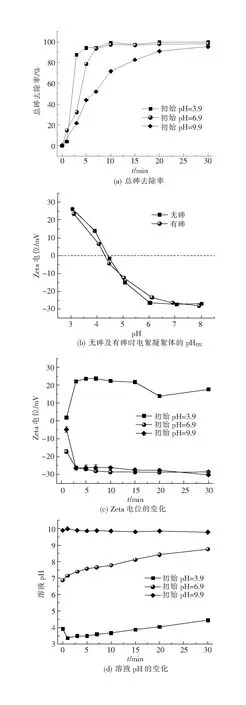
图4 不同初始pH对EC除砷的影响
(3)
2H2O+2e-→H2↑+2OH-。
(4)
2.1.4 不同阴离子的影响 选择NaCl、NaNO3和Na2SO4作为背景电解质,以探究不同阴离子对钛电絮凝除砷的影响,如图5(a),Cl-存在的情况下,实验结果最有利,相比之下,NO3-和SO42-都在一定程度上抑制砷的去除:NO3-存在的情况下,30 min后总砷去除率仅为53.9%,而SO42-存在的情况下,总砷去除率仅为8%~15%。

图5 不同阴离子对EC除砷的影响
图5(b)显示出不同阴离子存在情况下EC产物外观的差异,Cl-存在时,产物以絮体的形式存在,清晰可见且比较松散,这与此前EL-GHENYMY等[13]报道的氯化物等腐蚀性离子可以穿透钝化氧化膜导致阳极的高溶解率的结果一致。当NO3-存在时,产物为胶体,不易聚集与沉降;而共存阴离子为SO42-时,溶液中并无明显的可见物,这与图5(c)中的结果是一致的。图5(c)为钛极板在三种电解质溶液中的极化曲线,钛极板在NaCl溶液中的腐蚀电位(Ecorr)明显小于其在NaNO3和Na2SO4溶液中的Ecorr,分别为:NaCl -608 mV、NaNO3-586.6 mV、Na2SO4-541.45 mV,说明在NaCl溶液中钛阳极更容易发生腐蚀反应,溶解产生钛的絮体,这也就解释了为什么NaCl溶液中所产生的絮体会多于NaNO3和Na2SO4溶液。由图5(d)可见,在三种不同阴离子条件下,反应过程中的电压都是逐渐升高的,加入SO42-的溶液,其电导率虽然高于另外两者(Na2SO41872 μS·cm-1, NaCl 1108 μS·cm-1, NaNO31071 μS·cm-1),但反应过程中电压升高较快;加入Cl-和NO3-后溶液的电导率差异不大,但反应过程中NO3-存在的溶液中电压升高的速度大于Cl-存在的溶液,而电压越高使得反应过程中所需的能耗就越高,不利于EC技术的实际应用。考虑到Cl-是各种水体中广泛存在的阴离子类型,因此后续实验进一步考察不同Cl-浓度对钛电絮凝除砷效能的影响。
2.1.5 Cl-浓度的影响 在EC过程中,阳极表面形成的钝化膜会极大地破坏EC工艺的性能。这种钝化膜限制了腐蚀速率,降低了阳极界面处的电荷转移效率,增大了能耗,会给EC处理技术带来相关问题[18]。但是,氯化物等腐蚀性离子可能穿透钝化膜,使得阳极的溶解率增大[13]。为此,本研究考察了Cl-浓度对钛电絮凝除砷的影响。
设置 4个Cl-浓度梯度:0.005 mol·L-1、0.01 mol·L-1、0.05 mol·L-1和0.25 mol·L-1。图6(a)显示了总砷去除率在不同Cl-浓度条件下随时间变化的曲线,随着Cl-浓度的增大,反应的速率总体呈加快趋势,这是因为Cl-对极板的腐蚀,致使表面层下的金属得以暴露从而参与反应[13]。在Cl-浓度为0.005 mol·L-1时,约需15 min达到饮用水限值要求(10 μg·L-1)[2],在Cl-浓度为0.01~0.25 mol·L-1时,约需10 min即可达到饮用水限值要求。图6(b)为钛极板在不同Cl-浓度中的极化曲线,根据塔菲尔曲线外推法可求得不同Cl-浓度所对应的腐蚀电流(Icorr),分别为:0.005 mol·L-10.43 μA·cm-2、0.01 mol·L-10.59 μA·cm-2、0.05 mol·L-10.76 μA·cm-2、0.25 mol·L-11.10 μA·cm-2,由此可见,随着Cl-浓度的增大,钛极板在溶液中的Icorr不断增大,极板的腐蚀速度加快,这与图6(c)中的结果是一致的。如图6(c),随着Cl-浓度增大,钛阳极的电流效率也在增大,当Cl-浓度增大到0.25 mol·L-1时,电流效率超过100%,促进了钛阳极的溶解,由此也证实了Cl-对钛极板的腐蚀。溶液中的Cl-浓度越大,溶液的电导率就越大,从而反应过程中的电压上升相对缓慢,且降低电压能够降低能耗,但是考虑到投加氯化钠的成本以及不显著的能耗降低,并且天然水体的Cl-浓度一般小于0.01 mol·L-1,因此后续实验都选择在0.01 mol·L-1的Cl-浓度条件下进行。

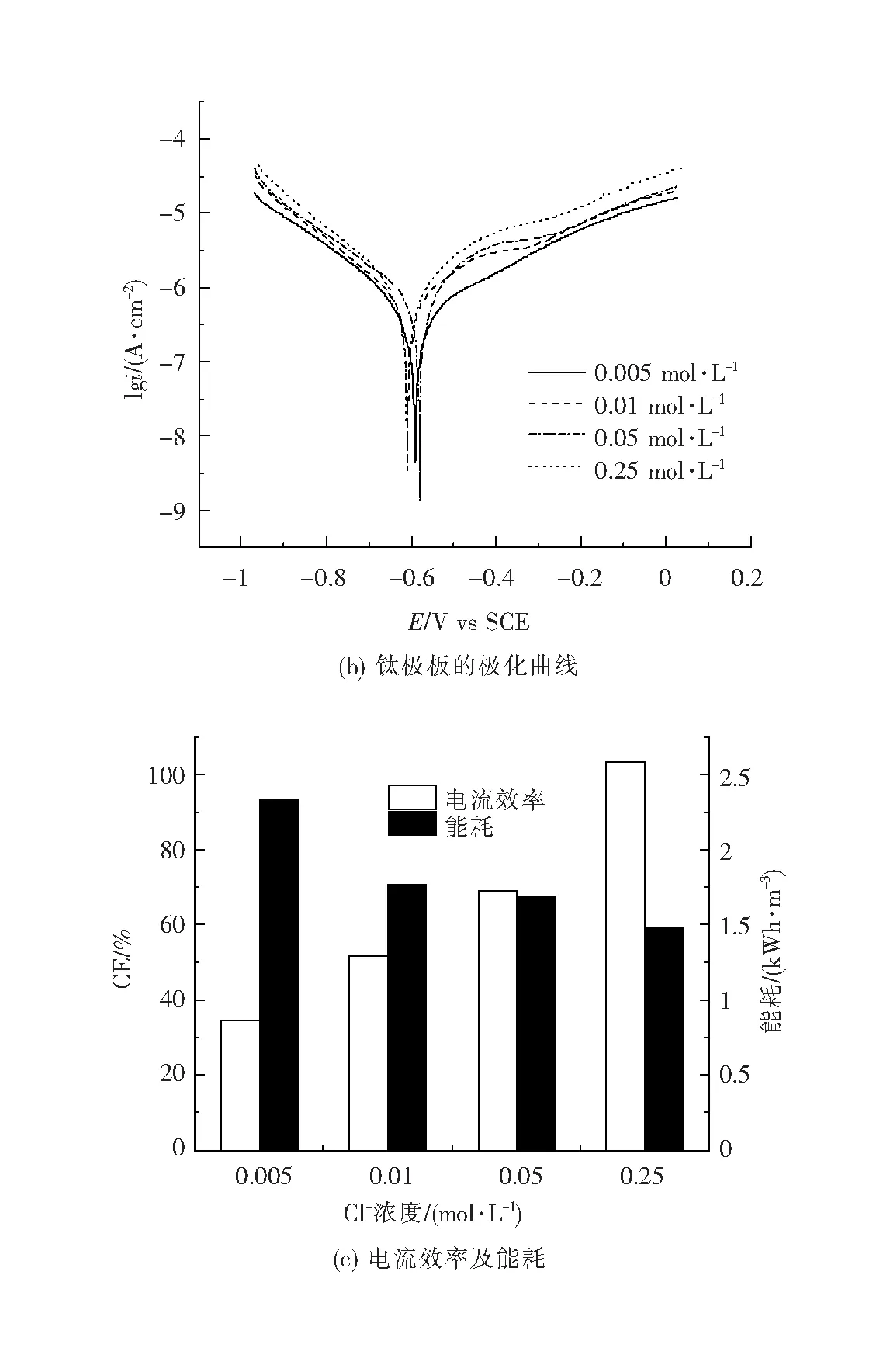
图6 不同Cl-浓度对EC除砷的影响
2.2 实验参数的响应面分析
2.2.1 模型的建立及显著性检验 在单因素实验基础上,采用0.01 mol·L-1的NaCl作为背景电解质,以反应30 min后的总砷去除率(Y)为响应值,以极板间距(X1)、电流密度(X2)和初始pH(X3)为考察因素,Box-Behnken实验因素与水平见表1,实验结果与分析见表2。
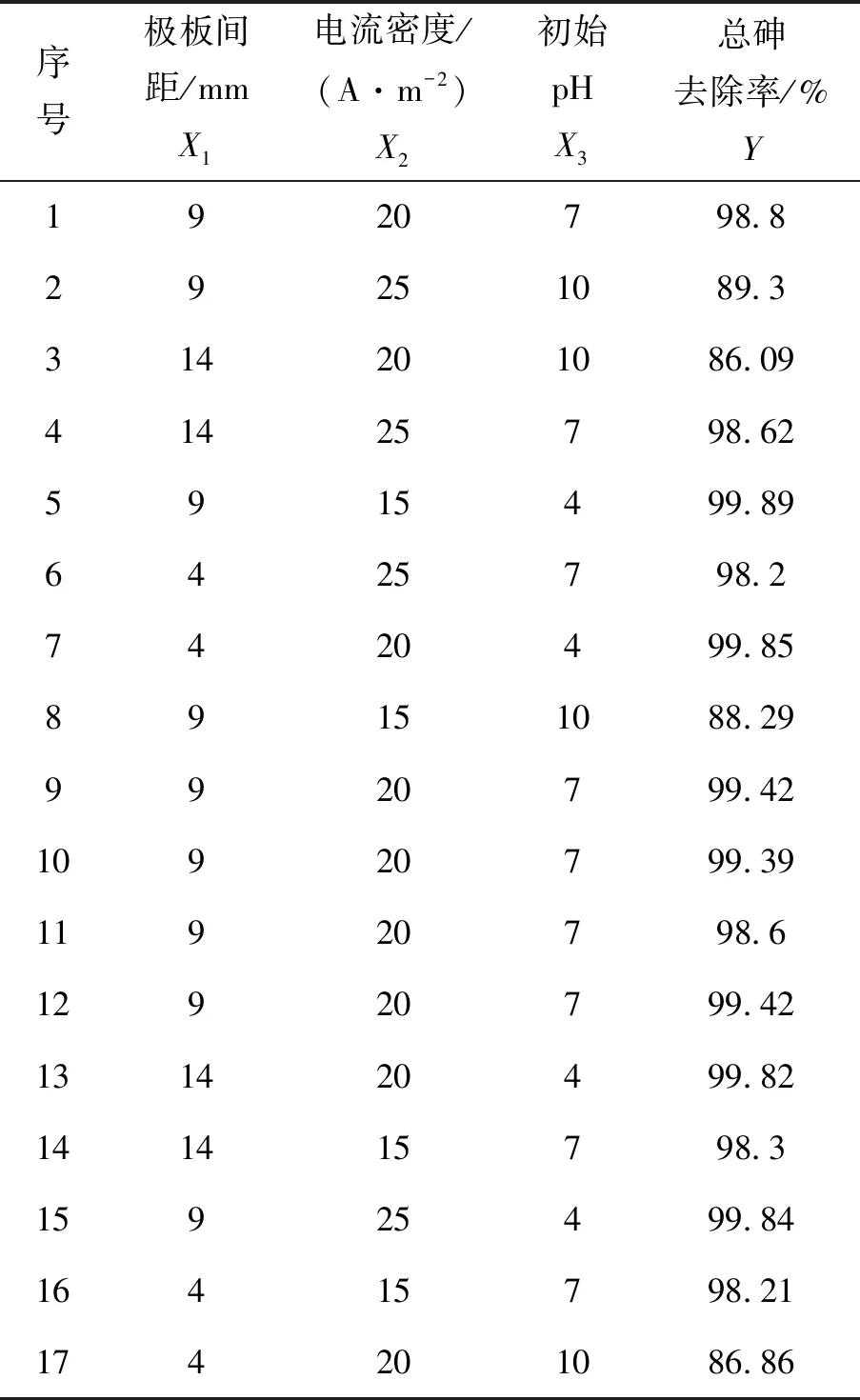
表2 总砷去除条件优化Box-Behnken实验结果与分析
运用Design Expert V10.0.7软件对表2中总砷去除率进行拟合,二次多项式模型的拟合效果要好于其他模型,所得回归方程为
Y=99.13-0.036X1+0.16X2-6.11X3+
0.082X1X2-0.18X1X3+0.26X2X3-
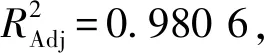
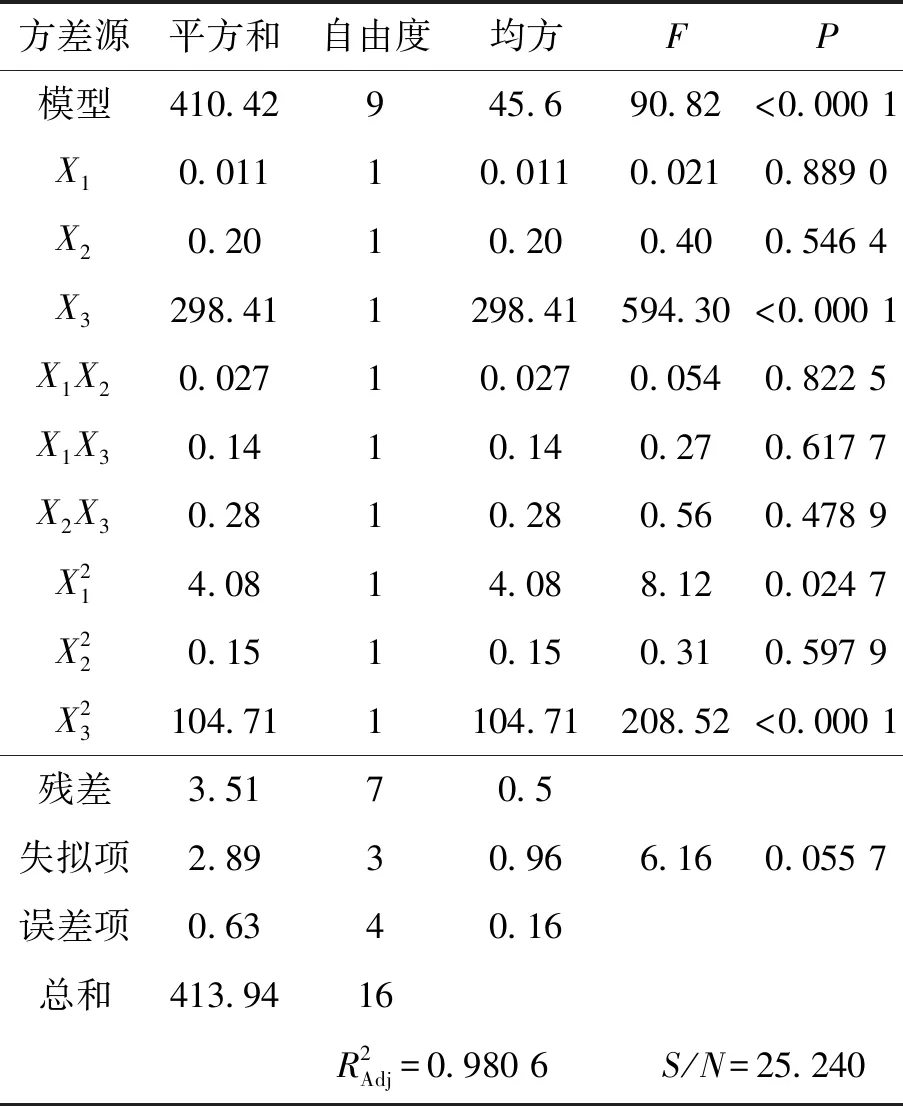
表3 响应面实验结果方差分析
2.2.2 响应面分析 极板间距、电流密度和初始pH交互作用对总砷去除率影响的响应面曲线及等高线如图7。由图7(a)可知,当固定初始pH时,随着极板间距的增大,总砷去除率呈现先升高后降低的趋势,但随着电流密度的增大,总砷去除率呈现略微的先降低后升高的趋势,极板间距在7~10 mm内较适合,电流密度在15~16 A·m-2范围内较合适。由图7(b)可知,当固定电流密度时,随着初始pH和极板间距的增大,总砷去除率都是呈现先升高后降低的趋势,初始pH在4~7和极板间距在7~10 mm的范围内效果较好。由图7(c)可知,当固定极板间距时,随着初始pH的增大,总砷去除率呈现先增加后降低的趋势,但随着电流密度的增大,总砷去除率呈现略微的先降低后升高的趋势,初始pH在4~7范围内较适合,电流密度在15~16 A·m-2范围内较合适。

图7 各因素交互作用对总砷去除率影响的响应面和等高线
利用Design Expert 10.0.7软件对所得的回归方程进行逐步回归,确定最佳工艺参数为极板间距9.4 mm、电流密度15.5 A·m-2、初始pH 6.4,此时总砷去除率预测值可达100%。为了便于实际操作和实验条件的限制,将最佳工艺参数修订为极板间距9 mm、电流密度15 A·m-2、初始pH 6.4,在此条件下,总砷去除率为99.98%,与模型预测值(100%)较一致,验证了模型的可靠性。
2.3 机理分析
为进一步探究钛电絮凝除砷的机制,将钛电絮凝除砷的絮体(初始pH 6.8)进行FTIR和XPS分析,结果见图8。由FTIR分析结果可知(图8(a)),有无砷条件下的絮体都在3738 cm-1、3381 cm-1和1633 cm-1处具有特征峰,其中3738 cm-1处的特征峰属于Ti-OH基团[19],絮体主要为Ti(OH)4,而3381 cm-1和1633 cm-1处的特征峰分别为羟基官能团的伸缩振动和对称弯曲振动[20]。对比表明,有砷条件下的红外光谱显示出802 cm-1处的特征峰,此为As—O弹性吸收谱带[21],说明砷被吸附到EC所产生的絮体中。
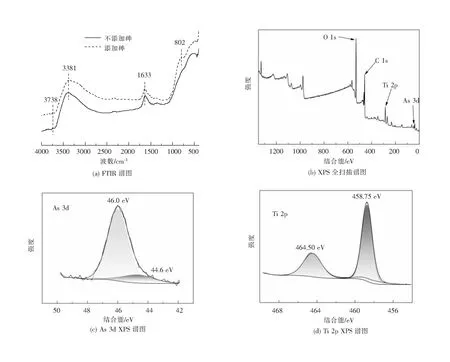
图8 絮体的FTIR和XPS谱图
由XPS结果(图8(b)、(c)和(d))可见,全扫描谱图中有As 3d的峰,进一步说明砷被吸附到EC所产生的絮体中。此外,As 3d谱图中两个峰的结合能为46.0 eV、44.6 eV,分别对应As(Ⅴ)和As(Ⅲ)[22-23],Ti 2p谱图中两个峰的结合能为464.50 eV和458.75 eV,表明钛的价态是Ti(Ⅳ)[24],生成的絮体主要为Ti(Ⅳ)氧化物。
为进一步探讨反应所产生的絮体中As(Ⅲ)的来源,使用HPLC-ICP-MS来分析钛电絮凝除砷过程中溶液里砷元素的形态变化,结果如图9。由图9可见,使用砷酸钠配制的原水样中发现少量As(Ⅲ)的存在,且在反应过程中,As(Ⅲ)的浓度随时间不断减少(峰面积代表浓度大小),说明溶液中原本就存在的As(Ⅲ)在EC过程中被去除,从液相转移到固相,进入絮体内,从而使得XPS的分析结果中有As(Ⅲ)的存在。
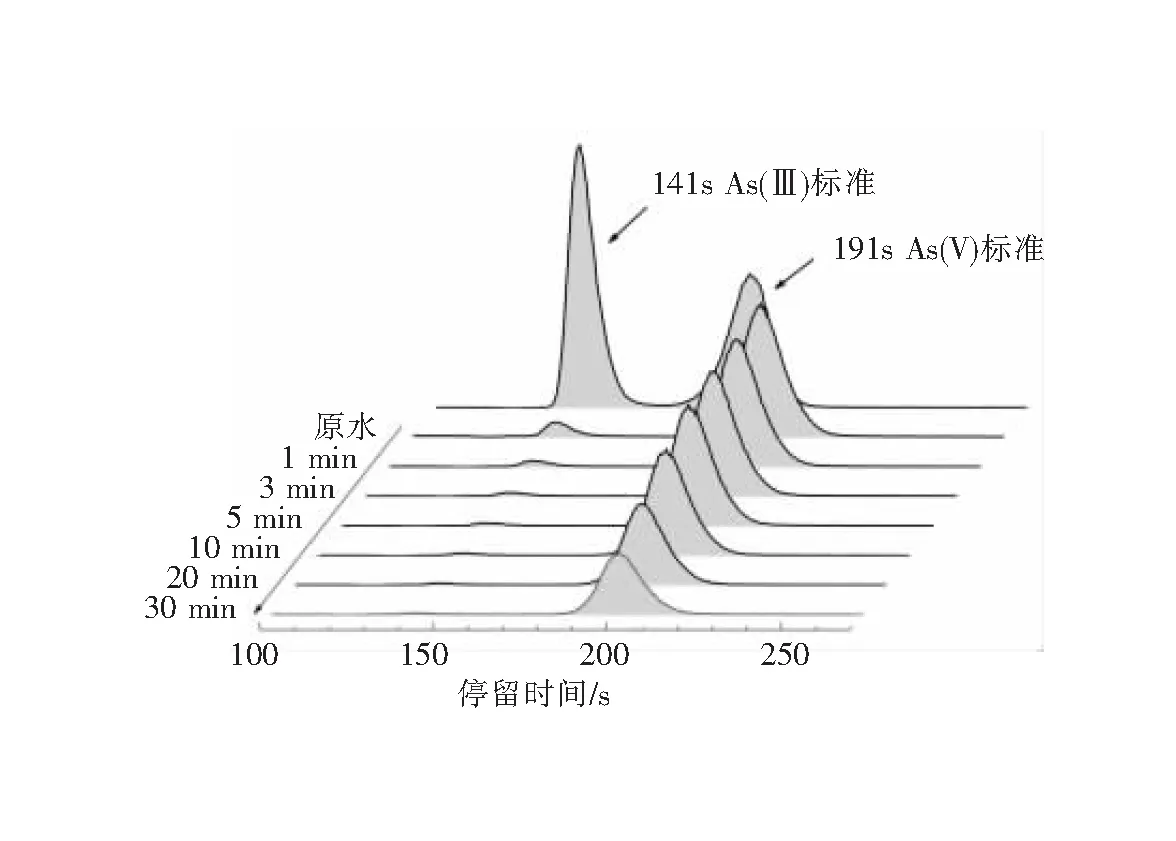
图9 反应过程溶液中As(III)和As(V)的浓度变化
2.4 连续流性能初探
基于饮用水处理的多级屏障理念,为保障出水砷浓度、浊度和pH值等指标满足《生活饮用水卫生标准》[2]要求,考虑到吸附滤料良好的除浊除砷性能,因此进一步采用在EC装置后加吸附过滤装置,考察电絮凝-直接吸附过滤工艺的除浊除砷效果。
如图10(a),EC出水总砷的质量浓度在34.4~49.4 μg·L-1之间,去除率在75.4%~82.9%之间。经吸附过滤之后总砷的质量浓度进一步削减,最终出水总砷的质量浓度在1.5~2.0 μg·L-1之间,满足《生活饮用水卫生标准》限值要求(<10 μg·L-1),经吸附过滤后的去除率达到99%以上,且在整个处理过程中,出水总砷质量浓度比较稳定。从图10(b)中可以看出,经EC处理后水样的浊度不到10 NTU,但是过滤能够进一步降低出水浊度,并且满足《生活饮用水卫生标准》(1 NTU)。此外,过滤能够进一步降低出水pH至中性,如图10(c)。因此,采用电絮凝-吸附过滤工艺,在总砷浓度、浊度以及pH上都能达到《生活饮用水卫生标准》中的要求。
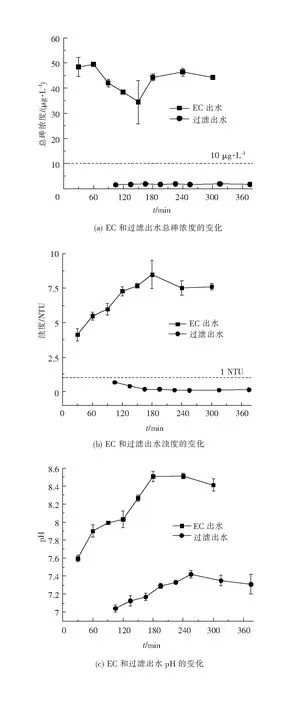
图10 连续流电絮凝-吸附过滤工艺的性能
3 结 论
(1)采用钛电絮凝对模拟含砷饮用水进行处理,单因素实验结果表明,钛电絮凝对砷具有良好的去除效果。对于实验所选取的四个极板间距,均可实现95%以上的总砷去除率;电流密度越大,总砷的去除速率越快,但最终的去除效果几乎没有差别;初始pH对钛电絮凝除砷的速率影响较大,但反应30 min后的总砷去除率接近;不同阴离子对总砷去除的影响较大,总砷去除率顺序为:Cl-> NO3-> SO42-;Cl-浓度对总砷去除率的影响不大,但是Cl-浓度越高,能耗越低。
(2)在单因素实验的基础上,应用响应面法进一步分析了极板间距、电流密度和初始pH对于总砷的去除率之间的相互作用关系,二次多项式模型的拟合效果要好于其他模型,并优化获得钛电絮凝除砷的技术参数取值范围:极板间距7~10 mm、初始pH 4~7以及电流密度15~16 A·m-2。
(3)5h的连续流电絮凝-吸附过滤工艺表明,该工艺能够保证出水总砷浓度、浊度以及pH满足《生活饮用水卫生标准》中的相关要求,且处理性能优良,后续尚需进行长时间的运行研究,考察其性能及稳定性。
