一种水溶性佐剂CS-GTA-ML对H7N9亚型禽流感灭活疫苗免疫效果评价
2023-09-25尹文竹许泽玉邓碧华周明旭王海燕张金秋
尹文竹,许泽玉,邓碧华,马 芳,周明旭,王海燕,卢 宇,*,张金秋,*
(1.江苏省农业科学院 动物免疫工程研究所 国家兽用生物制品工程技术研究中心,江苏 南京 210014;2.江苏省食品质量安全重点实验室-省部共建国家重点实验室培育基地,江苏 南京 210014;3.南京农业大学 动物医学院,江苏 南京 210095)
目前,疫苗提高了预防传染性疾病的能力,降低了患病风险。然而,对于一些免疫原性较差的灭活疫苗而言,佐剂是其中必不可缺的关键成份[1]。水性佐剂,即传统的铝盐佐剂,主要诱导体液免疫应答,不能有效地刺激细胞免疫,同时会引起注射部位局部出现肿胀、红斑、硬块等不良反应。
壳聚糖(chitosan,CS)是一种来源广泛、价格低廉、具有良好生物相容性、可降解性和安全无毒等特点的阳离子型天然高分子聚合物,目前被广泛应用在畜禽饲料及疫苗佐剂。徐怀英等[6]利用其高度黏着性及长链结构,通过戊二醛乳化交联新城疫病毒,制备成口服型新城疫微球疫苗,对强毒株有较强的保护性,且能同时促进体液免疫和细胞免疫。但天然的CS在生理pH值下无法溶解,难以发挥其生物学活性。因此,解决CS在纯水中的溶解性问题,是提高其生物利用度的关键环节。其中CS结构中2-位氨基和3,6-位羟基是进行化学修饰的重要位点。据文献报道,通过双亲性、季磷化[9-10]、季胺化、烷基化、羧基化等化学修饰对其电荷、结构、亲疏水能力等进行改造,从而解决CS的溶解性问题。
递送类载体佐剂配伍疫苗后通过细胞膜运输到细胞内,通过溶酶体逃逸,最终将抗原释放于细胞质才能发挥作用,其中溶酶体逃逸是的提高疫苗效力的关键步骤。溶酶体(lysosomes)为单层膜包被的囊状结构,一般为真核细胞中的一种细胞器,其内部pH值4.5~5.5。吗啉环(morpholine)具有弱碱性(pKa = 8.36)作为一种溶酶体靶向定位基团,在荧光探针领域被广泛报道。此外,吗啉环具有双亲性,更易透过细胞膜进入细胞内。当含吗啉环疫苗进入溶酶体后,能在它的酸性微环境中质子化,使得溶酶体膜破裂,破坏了溶酶体结构,引发抗原在溶酶体逃逸,大量的抗原被精准地递送给CD4 T细胞,引起强烈的免疫反应。
本试验首先利用壳聚糖链2-位氨基与环氧丙基三甲基氯化铵(GTA)发生加成开环反应,制备水溶性CS季铵盐CS-GTA中间体,然后再与4-(2-氯乙基)吗啉(ML)进行N-烷基化反应引入具有溶酶体靶向的吗啉环基团,制备了CS-GTA-ML聚合物。由于CS-GTA-ML的电正性,能与带负电荷的抗原通过静电作用包裹抗原,同时利用CS对细胞的黏附性和吗啉环的溶酶体靶向性,实现抗原提呈和溶酶体逃逸,从而起到免疫增强效应和抗原递送功能。
1 材料与方法
1.1 实验动物及细胞4~6周龄ICR雌性小鼠购自扬州大学比较医学中心。小鼠饲养于独立的笼具中,自由采食与饮水,饲料过程中严格按照免疫程序进行免疫。SPF鸡胚购自济南鑫盛达生物工程有限公司。动物房定期消毒,室内温度为(25±1)℃,湿度为(50±10)%。1%红细胞(RBCs)由SPF鸡采血分离得到。
1.2 主要试剂CS(MW=20 W)、1 mol/L PBS缓冲液均购自Sigma-Aldrich试剂公司。环氧丙基三甲基氯化铵(C6H14ClNO,)、4-(2-氯乙基)吗啉(C6H12ClNO)、氢氧化钠(NaOH,AR级)、乙醇(EtOH,AR级)等试剂均购自国药集团化学试剂有限公司(Sinopharm Chemical Reagent Co.)。DMEM培养基、RPMI1640培养基、胎牛血清均购自赛默飞世尔生物化学制品(北京)有限公司产品。CCK-8试剂盒购自上海百赛生物技术股份有限公司。4%多聚甲醛、红细胞裂解液、FITC anti-mouse CD3抗体、APC anti-mouse CD4抗体和PE anti-mouse CD8a抗体均购自上海生物科技股份有限公司。超纯水由实验室Millipore Milli-Q纯水仪制备。小鼠细胞因子IL-2、IL-4、IL-6及IFN-γ 的ELISA试剂盒均购自上海酶免生物技术有限公司。
1.3 CS-GTA-ML的制备方法CS-GTA-ML的合成路线如图1所示。

图1 CS-GTA-ML的合成路线图
1.3.1CS-GTA的制备 参照文献[20]方法,取5 g CS、10 g GTA于250 mL圆底烧瓶中,加入70 mL去离子水,80℃搅拌反应8 h,反应至溶液澄清时停止反应。将反应液在85℃、35 r/min条件下旋转蒸发。产物不完全蒸干,加入适量95%乙醇洗涤浸泡30 min后取出析出的固体物质。粗产品通过抽滤,滤渣继续用适量95%乙醇搅拌洗涤。搅拌3 h后,再次抽滤,滤渣利用红外灯干燥,得到白色固体纯品CS-GTA(9.2 g)。
1.3.2CS-GTA-ML的制备 取2 g CS-GTA、2 g ML和1 g NaOH加入到100 mL圆底烧瓶中,加入30 mL去离子水,80℃搅拌反应12 h后停止反应。待温度降至室温后,加入适量95%乙醇洗涤浸泡30 min后取出析出的粗产品。采用相同的纯化方式得到白色纯品CS-ML-ML(2.5 g)。
1.4 体外细胞毒性检测采集ICR小鼠脾脏且去除RBCs后,分离悬浮单一的脾细胞并细胞计数,加入96孔细胞板中保持 2×106个/孔,然后在37℃、5% CO2条件下孵育24 h;弃去培养基后加入100 μL含不同质量浓度CS-GTA-ML的培养基继续孵育24 h;再次弃去培养基后,用PBS缓冲液洗涤1次;最后加入90 μL纯DMEM培养基和10 μL的CCK-8试剂继续孵育1 h,使用酶标仪(Bio-Rad,CA,USA)检测D450 nm值。按照以下公式进行计算:

1.5 体外溶血试验检测采集SPF鸡的新鲜血样,1 000 r/min离心10 min收集RBCs。用PBS溶液洗涤3次,然后配制成1%的RBCs悬液,备用。将0.3 mL的 1% RBCs悬液分别加入到1.2 mL不同质量浓度(0.005~10 g/L)的CS-GTA-ML溶液中。以1% RBCs悬液分别加入超纯水和PBS作为阳性对照和阴性对照。所有样品利用涡旋振荡仪快速振荡30 s后在室温下放置2 h。4℃、1 500 r/min离心10 min,使用酶标仪在D450 nm激发光下测定上清溶液的D值,并观察541 nm处的最大D值。其溶血率(HR)由如下式计算:
1.6 HE组织染色试验20只4~6周龄ICR雌性小鼠随机分为试验组和对照组,每组10只。试验组腹腔注射200 μL CS-GTA-ML(1 g/L),对照组注射相同剂量的PBS缓冲液。7 d内观察小鼠临床反应并记录其体质量变化。注射后7 d,将小鼠安乐处死,分别取其心脏、肝脏、脾脏、肺脏、肾脏及注射部位皮肤组织,利用4%多聚甲醛进行固定,之后进行脱水、石蜡包埋、切片、染色,最后通过显微镜进行观察。
1.7 小鼠体内免疫评价试验48只4~6周龄ICR雌性小鼠随机分为6组,每组8只。按表1进行背部皮下免疫,在接种后14,28,42 d采血并分离血清,用于血凝抑制效价检测。所有动物试验均符合江苏省农业科学院实验伦理要求。

表1 H7N9亚型禽流感灭活疫苗的小鼠免疫试验分组 μL
1.8 SPF鸡体内免疫评价60只6周龄SPF鸡随机分为6组,每组10只。按表2进行颈部皮下免疫,在接种后14,28 d采血并分离血清,用于血凝抑制效价检测。所有动物试验均符合江苏省农业科学院实验伦理要求。

表2 H7N9亚型禽流感灭活疫苗的SPF鸡免疫试验分组 μL
1.9 脾CD4+、CD8a+T淋巴细胞的流式分析随机每组抽取3只免疫后28 d的小鼠,安乐处死后取出脾脏并分离脾细胞,细胞计数后调整为2×106个/150 μL的单分散脾细胞悬液,分别加入FITC anti-mouse CD3抗体、APC anti-mouse CD4抗体和PE anti-mouse CD8a抗体,4℃避光共孵育30 min,PBS洗涤2次后,通过BD AccuriTMC6 Plus流式细胞仪进行检测。

2 结果
2.1 CS-GTA-ML的结构表征CS主链上引入吗啉环和季铵盐后得到CS-GTA-ML,CS-GTA-ML能被核磁共振氢谱(1H NMR)和傅里叶红外光谱(FT-IR)所表征。
如图2A所示,CS、CS-GTA和CS-GTA-ML在D2O中的1H NMR中,δ 1.97×10-6(绿色区域)为CS去乙酰化残留甲基质子峰;和CS相比,CS-GTA和CS-GTA-ML分别在约3.21×10-6处观察到一个非常强的峰值,表明季铵侧链中的甲基基团存在;在红色区域δ 2.494×10-6,4.381×10-6,3.413×10-6处的峰可以归属为H-a、H-b和H-c。和CS-GTA相比,CS-GTA-ML在蓝色区域内出现一个新峰,表明吗啉环被修饰在CS的主链上。利用峰宽半定量估算出GTA嫁接率约为53%,ML的嫁接率约为15%。
同样利用FI-IR(图2B)可以观察到,CS被GTA修饰后,在约1 478 cm-1处出现N-CH3的C-H不对称弯曲振吸收峰(绿色区域)。一般来说,甲基的C-H不对称弯曲振动吸收峰约为1 430 cm-1。由于季铵盐阳离子强的吸电子效应,使得其向高波数方向移动。ML被修饰到CS-GTA分子中后,出现1个1 127 cm-1的新峰[23]。与ML的红外谱图相比,可以认为它来自于ML环C-N伸缩振动吸收峰。这些数据进一步证实了CS-GTA-ML的结构。

图2 CS、CS-GTA和CS-GTA-ML的1H NMR图(溶剂为D2O)(A)、FI-IR图(B)和Zeta电位图(C)
从图2C中可以看出,随着CS主链上GTA、ML的嫁接,中间体CS-GTA和目标佐剂CS-GTA-ML仍带正电荷分别为38.1,15.4 mV。配伍带负电荷的H7N9亚型禽流感灭活抗原后,仍保持着12.5 mV的电正性。
此外,从表3中可以发现CS-GTA-ML在不同pH值下的水溶液中均可以溶解,在pH=5.5的酸性Tris缓冲液中最大溶解度为82.4 g/L;在pH=7.2的生理缓冲液(PBS)中最大溶解度为67.2 g/L;在pH=8.9的碱性Tris缓冲液中的最大溶解度为78.6 g/L。

表3 CS-GTA-ML在不同pH值下水溶液中的溶解度
2.2 CS-GTA-ML的生物相容性评价利用小鼠原代脾细胞为模式细胞器,配置不同质量浓度的CS-GTA-ML进行体外安全性评价。如图3所示,当质量浓度低于50 mg/L时,CS-GTA-ML对脾细胞有增殖效果;当质量浓度达到200 mg/L时,其细胞存活率仍高达92%;当质量浓度高达2 000 mg/L时,脾细胞仍有73%左右的存活率。
从图4的直观图中可以看出,随着CS-GTA-ML质量浓度的提高,EP管中上清液呈无色透明状,RBCs沉积在管底、仍无破裂。从光谱图中也可以看出D值随着CS-GTA-ML质量浓度的增加无明显变化。当质量浓度高达10 g/L时,通过公式计算发现HR仅0.5%左右,几乎没有溶血现象。
随后,对皮下注射后7 d小鼠连续观察其生活和精神状态,试验组(CS-GTA-ML)小鼠饮食、睡眠及精神状态正常,小鼠被毛柔顺,注射部位未出现红肿、发炎、脱毛等反应。进一步对小鼠的重要器官和注射部位皮肤进行病理切片分析(图5),心脏、肝脏、脾脏、肺脏等脏器均无病变和损伤,其注射部位皮肤也未出现炎症反应等。
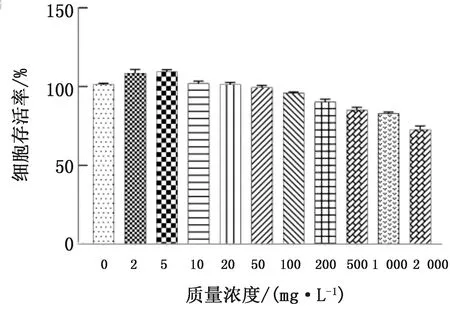
图3 不同质量浓度的CS-GTA-ML对原代脾细胞存活率

图4 CS-GTA-ML的HR

图5 小鼠注射1 g/L的CS-GTA-ML的组织病理观察结果
2.3 CS-GTA-ML的血凝抑制效价评估利用免疫试验验证CS-GTA-ML的免疫增强活性。首先根据图6的免疫方式和次数小鼠皮下免疫,并在免疫后7 d后开始采血进行检测。如图7所示,免疫后7 d,对照组与试验组无显著性差异(P>0.05);免疫14 d后,添加佐剂组疫苗免疫组小鼠血清HI效价均显著提高,其中CS-GTA-ML+H7N9-100 mg/L组HI效价略高于ISA206+H7N9组(P<0.05)。至首次免疫后6周,随着免疫时间的延长,CS-GTA-ML免疫组小鼠仍保持着较高的抗体水平。
定期监测小鼠的体质量变化,结果如图8所示,免疫42 d后不同质量浓度的CS-GTA-ML的H7N9疫苗组小鼠均生长良好,与PBS组和纯H7N9疫苗组相比较,小鼠体质量增加1.5 g左右,与ISA206+H7N9疫苗组小鼠体质量接近,各组之间无显著性差异(P>0.05)。
由图9可见,SPF鸡皮下免疫14 d后,CS-GTA-ML+H7N9-100 mg/L组HI效价仍显著高于H7N9组(P<0.001),且与ISA206+H7N9组HI效价无显著性差异(P>0.05)。但是,免疫28 d后,CS-GTA-ML+H7N9-100 mg/L组HI效价仍显著高于ISA206+H7N9组(P<0.05)。
2.4 细胞因子检测通过ELISA试剂盒对免疫后28 d采集的小鼠血清进行IL-2、IL-4、IL-6和IFN-γ检测。如图10所示,与单一的H7N9疫苗对比,添加佐剂(ISA206和CS-GTA-ML)后,免疫后小鼠血清中IL-2、IL-4、IL-6和IFN-γ均显著上调;与ISA206+H7N9组相比,CS-GTA-ML+H7N9-100 mg/L 组小鼠血清的IL-2(P<0.05)、IL-6(P<0.05)和IFN-γ(P<0.05)表达量有显著性升高,而IL-4的表达量无显著性差异(P>0.05)。
2.5 脾淋巴细胞中CD4+和CD8a+细胞亚群流式分析为了进一步研究CS-GTA-ML对淋巴细胞的作用机制,通过流式细胞分析不同免疫组对脾T淋巴细胞分化的影响。
皮下免疫不同疫苗组后28 d,通过流式细胞术检测不同疫苗免疫组小鼠脾细胞中CD3+CD4+及CD3+CD8a+的比例。如图11所示,试验组小鼠脾细胞中CD3+CD4+T细胞比例显著高于空白对照(PBS)组,且添加CS-GTA-ML+H7N9-100 mg/L或ISA206+H7N9的疫苗组免疫后,小鼠脾细胞中CD3+CD4+T细胞比例显著高于单纯H7N9抗原免疫组。另外,结合CD8a+/CD4+比值可以发现,CS-GTA-ML能显著提高CD8a+T细胞的比例(图11E)。

图6 小鼠免疫试验方案

图7 小鼠免疫后血清的HI抗体

图8 小鼠免疫后体质量变化

图9 SPF鸡免疫后28 d血清的HI抗体

图10 小鼠免疫后血清中IL-2(A)、IL-4(B)、IL-6(C)和IFN-γ(D)的质量浓度

图11 流式细胞仪检测免疫不同组别小鼠的脾CD4+、CD8a+T细胞的表达
3 讨论
免疫佐剂是配合抗原使用的无免疫原且增强抗原特异性免疫应答的新物质[24]。理想的免疫佐剂能在减少抗原用量及免疫次数的前提下产生高效免疫应答,便于生产和使用。传统的兽用油乳佐剂因代谢缓慢造成不良反应,因而亟需开发新型佐剂。有研究发现,生物可降解材料CS已被证实具有佐剂性能,不仅能够作为疫苗载体递送[25-26],还能作为免疫增强剂[27]。通常将CS溶解在盐酸溶液中,直链上的氨基吸附H+使其质子化,形成带正电荷的结构,便于通过电荷响应负载抗原。但其仅能在酸性环境中溶解的缺点限制了进一步的佐剂应用。
本研究通过温和的合成路线制备出CS-GTA-ML,并在不同pH环境下展现出良好的水溶性,通过体内外生物相容性试验发现其无毒、生物相容性好,为注射剂型的应用提供试验数据。配合灭活H7N9亚型流感病毒评估CS-GTA-ML的免疫增强性能,不同质量浓度CG-GTA-ML的血凝抑制效果不低于商品化的ISA206,且免疫42 d后仍有较高的血凝抑制作用,延长了免疫持续期。
CS刺激免疫效力有很多因素,如激活巨噬细胞、诱发研发性超敏反应和产生循环抗体、诱发杀伤性淋巴细胞(CD8+)、激发NK细胞及诱发细胞因子等。本研究首先通过对免疫后2周的血清进行细胞因子的检测,发现CS-GTA-ML诱导机体分泌高水平的Th1型(INF-γ和IL-2)和Th2型(IL-6)细胞因子,初步判断具有一定的体液和细胞双重免疫。T淋巴细胞的活化及分化影响免疫途径,其中CD4和CD8是两个重要的细胞表面指标。CD4+T细胞能够参与Th细胞TCR识别抗原的信号转导,在免疫反应过程通常发挥辅助机体产生体液免疫和细胞免疫应答的功能,CD8+T细胞则是重要的效应细胞,具有杀伤靶细胞的功能。同时,CD4+/CD8a+的比值同样可以说明免疫增强作用的大小。进一步探究对T淋巴细胞的分化,CS-GTA-ML刺激机体产生大量的CD4+T细胞,可能是MHC Ⅱ类分子通过溶酶体途径递呈进入淋巴细胞中,同时CD4+与CD8a+比值增加验证T淋巴细胞趋向于CD4的分化,诱导机体分泌大量的体液和细胞免疫反应的细胞因子,增强了机体免疫应答能力。
因此,推测带有正电荷的CS-GTA-ML静电结合H7N9灭活疫苗后通过皮下注射到机体后,利用CS的黏着性将疫苗带入到DC细胞中,并通过吗啉环的靶向溶酶体后,引起“质子海绵效应”,使得溶酶体内环境吸收大量的H+,导致溶酶体膜内外渗透压变化,使得溶酶体膜破碎,引发溶酶体逃逸能力,将H7N9抗原缓慢释放至细胞质中,持续刺激机体产生体液和细胞双重免疫。
