血清SAA、CRP及PCT对胎膜早破并发宫内感染的预测价值
2023-09-22吕冉冉孟德侠
吕冉冉 孟德侠
胎膜在临产前发生破裂,称为胎膜早破,它可诱发宫内窘迫、早产、脐带脱垂、胎儿感染等,也可导致孕产妇宫内感染、产褥感染、难产,增加羊水栓塞的概率,是当前威胁我国母婴健康的产科最常见并发症之一[1]。研究表明宫内感染与胎膜早破互为因果关系,胎膜早破并发宫内感染的发生率在30.0%左右,是导致母婴结局不良的主要危险因素之一,加强早期预测具有重要价值[2]。血清β-人绒毛膜促性腺激素(β-HCG)是预测宫内感染的重要指标,但是预测的特异性不强,容易出现误诊情况[3]。血清淀粉样蛋白A(SAA)、C反应蛋白(CRP)、降钙素原(PCT)是当前临床上的常见检测项目,都是感染性疾病标志物,在检测操作上也比较方便简单[4]。本文具体探讨与分析血清SAA、CRP及PCT对胎膜早破并发宫内感染的预测价值,以促进早期检出宫内感染。现报道如下:
1 资料与方法
1.1 一般资料 收集我院2020 年1 月-2022 年10 月收治的88 例胎膜早破产妇作为研究对象。研究得到了我院伦理委员会的批准。①纳入标准:单胎头位妊娠;年龄20~45 岁;孕周大于或等于35周;产妇自愿参与本次研究;临床资料完整且依从性好的产妇。②排除标准:合并有呼吸系统感染者;合并有HPV感染、HIV感染的产妇;不具备完整临床资料者;合并子痫前期、胎儿畸形等严重合并症的产妇;凝血功能障碍的产妇。在88 例产妇中,发生宫内感染20 例(宫内感染组),占比22.7%。宫内感染组产妇的年龄、妊娠周数、孕次、产次、体质指数等与非宫内感染组对比,差异均无统计学意义(P>0.05),具有可比性,见表1。
表1 两组产妇一般资料比较()
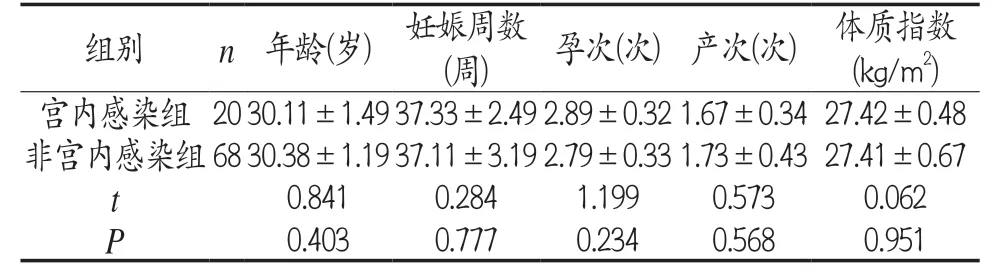
表1 两组产妇一般资料比较()
?
1.2 血清SAA、CRP及PCT检测 采集产妇的空腹外周静脉血5 mL左右,不抗凝,静置30 min后,以3000 rpm/min离心10 min,离心半径为10 cm,留取上层血清置于-20.0℃低温冰箱保存。采用酶联免疫法检测血清SAA、PCT含量,放射免疫法检测血清CRP含量(试剂盒分别购自罗氏诊断产品上海有限公司与上海碧云天生物技术有限公司),严格室间与室内质量控制。阳性标准:CRP大于9 mg/L,SAA大于10 mg/L,PCT大于0.5 μg/L。
1.3 宫内感染判定 对产妇外阴常规消毒,使用一次性无菌注射器抽取羊水约2 mL,然后进行病理检测。宫内感染判定标准:在光学显微镜的高倍镜下进行观察,中性粒细胞大于5个/高倍镜视野。
1.4 调查内容 调查所有产妇的一般资料、妊娠情况等,包括年龄、妊娠周数、孕次、产次、体质指数等因素。
1.5 统计学方法 采用SPSS 20.00 统计软件分析数据,计量资料采用t检验;计数数据采用χ2检验,相关性分析采用Spearman相关系数,行单因素分析后有统计学意义的相关因素纳入Logistic多因素分析,预测价值分析采用受试者工作特征(ROC)曲线分析,P<0.05 为差异有统计学意义。
2 结 果
2.1 两组产妇血清SAA、CRP、PCT含量比较 宫内感染组产妇的血清SAA、CRP、PCT含量与非宫内感染组对比有显著升高(P<0.05),见表2。
表2 两组产妇血清SAA、CRP、PCT含量比较()

表2 两组产妇血清SAA、CRP、PCT含量比较()
?
2.2 相关性分析 在88 例产妇中,Spearman相关性分析显示血清SAA、CRP、PCT含量与宫内感染存在正向相关性(P<0.05),见表3。

表3 胎膜早破产妇宫内感染发生与血清SAA、CRP、PCT的相关性(n=88)
2.3 影响因素分析 在88 例产妇中,以宫内感染作为因变量,以血清SAA、CRP、PCT含量作为自变量,Logistic多因素分析显示血清SAA、CRP、PCT含量都为导致宫内感染发生的主要独立危因素(P<0.05),见表4。

表4 胎膜早破产妇宫内感染发生的多因素分析(n=88)
2.4 预测价值分析 在88 例产妇中,ROC曲线分析显示血清SAA、CRP、PCT含量对胎膜早破并发宫内感染预测的曲线下面积分别为0.730、0.751、0.714、,联合检测的曲线下面积为0.872,见图1。
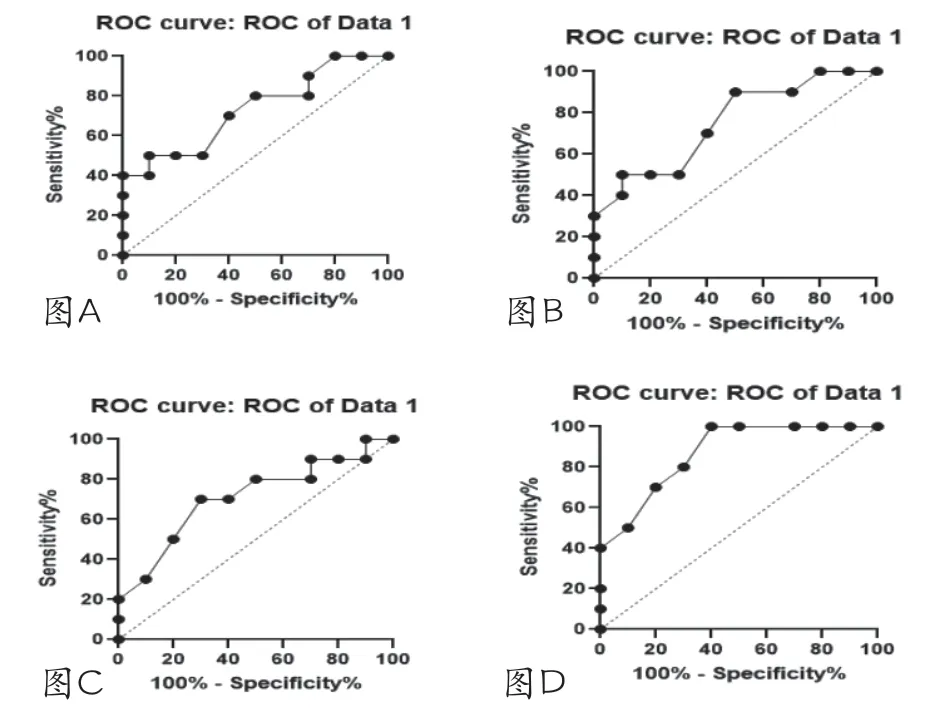
图1 血清SAA、CRP、PCT单独检测及联合检测对胎膜早破并发宫内感染的预测ROC曲线
3 讨 论
胎膜在妊娠末期往往会变得很薄,而为了适应不断增大的子宫,胎膜须依靠自身伸张能力才不至于发生破裂,直到胎儿娩出[5]。胎膜早破有着相当复杂的诱因及发生机制,当机体出现营养不良、感染、外伤、宫颈内口松弛、妊娠后期出现频繁性交、胎先露部高浮、羊膜腔内高压力、胎膜本身病变等不良情况时,胎膜就有发生破裂的高度危险[6]。胎膜早破发生后,细菌可逆行进入羊膜腔,形成急性绒毛膜炎,也就是宫内感染。部分胎膜早破并发宫内感染产妇在早期无明显临床症状,但是随着病情的进展,可增加上行感染风险,诱发胎儿宫内窘迫、新生儿感染、早产、流产、死产等,为此加强早期预测与诊断具有重要价值。
研究表明宫内感染伴随有炎症细胞因子浸润诱发的慢性非特异性炎症,可表现为炎症因子的大量释放[7]。本研究显示在88 例产妇中,发生宫内感染20 例(宫内感染组),占比22.7%;宫内感染组产妇的血清SAA、CRP、PCT含量与非宫内感染组对比有显著升高(P<0.05)。从机制上分析,血清CRP是目前临床应用较为广泛的炎性因子指标,主要由肝脏合成,在发生感染后4 h内可急剧升高,从而参与机体免疫抵抗反应调节,使局部胎膜细胞缺氧坏死,可作为反映早期组织炎症情况的重要指标之一[8]。SAA是一种急性时相蛋白,当宫内感染时SAA明显升高,可刺激胶原降解,直接抑制胶原合成,参与胎膜早破的发生,从而形成恶性循环。PCT是由甲状腺C细胞分泌的无激素活性降钙素前体物质,在健康人群中具有很好的分泌稳定性。当人体发生感染时,血清PCT水平显著上升,在12 h后达到峰值,能够反映全身炎性反应的活跃程度。因而宫内感染组血清SAA、CRP、PCT含量显著升高。本研究Spearsman分析显示血清SAA、CRP、PCT含量与胎膜早破并发宫内感染存在正向相关性(P<0.05);Logistic多因素分析显示血清SAA、CRP、PCT含量都为导致胎膜早破并发宫内感染的主要独立危险因素(P<0.05)。从机制上分析,感染是胎膜早破的主要原因,可导致母体胎盘结构被破坏,且宫内感染与胎膜早破互为因果关系。一旦产妇发生感染,血清SAA、CRP、PCT含量会显著增加,且基本受到机体免疫抑制状态的影响 ,三者水平会随着产妇宫内感染的严重程度而出现升高,为评价宫内感染严重程度的一个有效指标[9]。并且当产妇受到炎症刺激时,SAA、CRP、PCT的反应都极快,基本在12 h内可达到峰值,具有很好的诊断敏感性。
早期宫内感染无明显症状,检出的敏感性较低,容易延误最佳治疗时机。本研究ROC曲线分析显示血清SAA、CRP、PCT含量对胎膜早破并发宫内感染预测的曲线下面积分别为0.730、0.751、0.714,联合检测的曲线下面积为0.872,表明血清SAA、CRP、PCT对胎膜早破并发宫内感染都有很好的预测价值,联合检测的预测价值更好。从机制上分析,当产妇发生感染时导致胎膜受损,可造成产妇宫内发生缺氧,导致滋养细胞异常增生,从而诱发炎症因子的大量释放。且SAA、CRP、PCT表达水平增加能抑制胶原合成,促进胎膜细胞的凋亡,参与产妇的液体循环,导致胎膜早破的发生。而三者的联合检测能够避免单一指标检测的不足,从而取得更好的预测效果[10]。本次研究没有纳入健康产妇进行对比分析,多因素分析的资料也比较少,将在后续研究中探讨。
综上所述,胎膜早破并发宫内感染产妇多伴随有血清SAA、CRP、PCT的高表达,血清SAA、CRP、PCT对胎膜早破并发宫内感染都有很好的预测价值,联合检测的预测价值更好。
